Журнал «Медицина неотложных состояний» 6 (37) 2011
Вернуться к номеру
Гемодинамические варианты течения шока при тяжелом абдоминальном сепсисе
Авторы: Курсов С.В. Харьковский национальный медицинский университет
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Версия для печати
Изучали состояние гемодинамики в условиях первой манифестации септического шока у больных с признаками абдоминального сепсиса. Определено, что тяжелый абдоминальный сепсис ассоциирован с высокой вероятностью развития септического шока. На основании анализа результатов исследования центральной гемодинамики выделено два варианта течения шока при абдоминальном сепсисе: дистрибутивный и кардиогенный. В раннем госпитальном периоде в патогенезе септического шока чаще основным был дистрибутивный механизм. После операции в патогенезе септического шока преобладал кардиодепрессорный компонент. Оба варианта шока характеризовались снижением производительности сердца при снижении общего периферического сосудистого сопротивления.
Абдоминальный сепсис, септический шок, центральная гемодинамика.
Введение
Септический шок представляет собой одно из тяжелейших осложнений сепсиса, летальность при котором может достигать 60–80 % [3, 6, 8]. В клинической практике достаточно часто встречается абдоминальный сепсис. Абдоминальный сепсис является системной воспалительной реакцией организма в ответ на развитие начального пускового деструктивного процесса в органах брюшной полости и/или забрюшинного пространства и характеризуется совокупностью явлений эндотоксикоза и полиорганной недостаточности [1, 2, 6]. На современном этапе наблюдается увеличение количества больных с инфицированным панкреонекрозом, перфорациями желудочно-кишечного тракта, перитонитом разной этиологии — заболеваниями, при которых имеет место высокая частота развития сепсиса и высокая летальность [1–3]. Нередко причиной быстрой гибели больных с абдоминальным сепсисом становится септический шок. По механизму формирования синдрома малого сердечного выброса септический шок принято считать разновидностью дистрибутивного шока. То есть ведущим механизмом при септическом шоке является острая сосудистая недостаточность. Септический шок подразделяют также на «теплый», при котором наблюдается нормальный или повышенный сердечный выброс на фоне резкого снижения сосудистого тонуса, и «холодный» (или «холодная фаза» шока), при котором имеется угнетение сердечного выброса на фоне возрастающего сосудистого сопротивления. Так как течение абдоминального сепсиса обычно ассоциировано с активацией роста и распространением грамотрицательной микрофлоры, то «теплой фазы» обычно не наблюдается и шок сразу протекает по «холодному» типу [2, 5, 8]. Однако, проводя исследования центральной гемодинамики у больных с признаками абдоминального сепсиса, мы обнаружили, что эти традиционные представления не всегда подтверждаются. Кроме того, в связи с тем что при сепсисе достаточно быстро развиваются дистрофические процессы в сердечной мышце, шок может иметь характер кардиогенного, а не дистрибутивного. Цель данного исследования — изучение изменений центральной гемодинамики в условиях шока, возникшего на фоне абдоминального сепсиса.
Материалы и методы исследования
Работа выполнена на базе хирургических отделений и отделения интенсивной терапии Харьковской клинической больницы скорой и неотложной помощи. В период 2007–2010 гг. оказана помощь 244 пациентам с признаками абдоминального сепсиса. Из 244 больных выделено 37 пациентов с признаками тяжелого сепсиса (15,16 %). В состоянии септического шока в клинику поступило 7 больных (2,87 %). В послеоперационном периоде септический шок развился еще у 3 пациентов (4,1 %). Всего среди тех, кто имел оценку 4 балла по шкале SIRS, частота возникновения септического шока достигла 27,03 %. Причиной абдоминального сепсиса у этих больных была перфорация органов желудочно-кишечного тракта. Позже, в 2009–2011 гг., еще 20 случаев септического шока констатировано у другого контингента больных. В этих случаях шок развивался на фоне панкреонекроза. У всех больных изучены начальные расстройства гемодинамики при поступлении в отделение интенсивной терапии.
Центральную гемодинамику (ЦГД) изучали методом интегральной тетраполярной реографии, артериотензометрии и центральной флеботензометрии. По этическим принципам мероприятия по устранению шока начинали незамедлительно, поэтому данные о состоянии ЦГД в условиях шока на фоне еще отсутствующей гемодинамической коррекции количественно ограничены, но именно они приводятся в данной работе.
Результаты исследования и их обсуждение
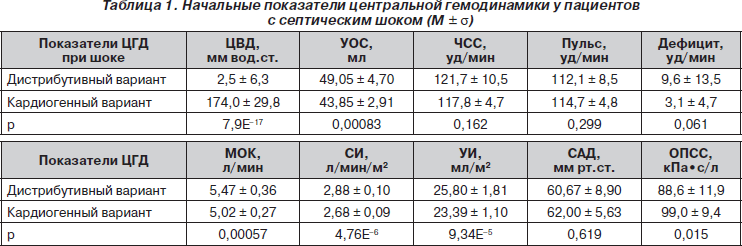
Если септический шок при перфорации полых органов имел место уже в момент поступления больных в клинику, то в большинстве случаев (6 из 7 — 85,71 %) он имел выраженный дистрибутивный характер. Начальная ведущая сердечная слабость констатирована только у 1 больного. У 3 больных, у которых шок развился после операции, он протекал по кардиогенному варианту. У больных с панкреонекрозами констатирована большая частота развития шока после операции. У них при формировании синдрома малого сердечного выброса в 16 случаях преобладала начальная сердечная слабость и только в 4 случаях — сосудистая недостаточность. Проведенных реографий при кардиогенном варианте — 20, при дистрибутивном — 10. Показатели ЦГД на высоте ее расстройств, при отсутствии активной жидкостной ресусцитации и инфузии симпатомиметиков приводятся в табл. 1.
Несомненное наличие 2 гемодинамических вариантов септического шока подтверждается у 2 групп больных отличительными показателями величины центрального венозного давления (ЦВД), которые в таблице вынесены на первый план. Состояние производительности сердца при кардиогенном варианте оказалось достоверно хуже, чем при первичной сосудистой недостаточности. Показатели ударного объема сердца (УОС), минутного объема кровообращения (МОК), сердечного индекса (СИ) и ударного индекса (УИ) в условиях дистрибутивного и кардиогенного вариантов септического шока это уверенно демонстрируют. Достоверная разница обнаружена при сравнении всех этих показателей. В то же время состояние системного сосудистого тонуса достоверно не отличалось. Не отличались достоверно показатели частоты сокращений сердца (ЧСС), частоты пульса и его дефицита.
Интересно, что ожидаемого резкого снижения показателя СИ, который наилучшим образом отражает состояние производительности сердца, до критических величин, составляющих 2,0–2,2 л/мин/м2, у больных с абдоминальным сепсисом не происходило. СИ колебался в пределах 2,5–2,9 л/мин/м2, которые многими авторами расцениваются как состояние компенсации или даже нормы. В частности, у пациентов с явлениями хронической сердечной недостаточности, которые не находятся в критических состояниях и могут проходить лечение в терапевтических отделениях в плановом порядке, в процессе исследования тем же методом тетраполярной реографии получают значения СИ в пределах 2,42 ± ± 0,04 л/мин/м2, а МОК — порядка 4,67 ± 0,13 л/мин. Нормальными же показателями производительности сердца в состоянии покоя в настоящее время считают СИ в пределах 3,5 ± 0,7 л/мин/м2, а УИ — в пределах 46 ± 8 мл/м2 [5, 7]. Однако у пациентов с абдоминальным сепсисом сравнительно незначительное снижение СИ сопровождалось серьезным снижением среднего артериального давления (САД), которое нельзя было расценить никак иначе, кроме как состояние шока. Наиболее серьезно у больных с шоком от нормальных значений отличались величины показателя УИ. Закономерно возникающая компенсаторная тахикардия, очевидно, может обеспечить нормальные величины МОК, характерные для нормальных метаболических потребностей, но не может обеспечить резко возрастающих метаболических запросов при критических состояниях. Резкого повышения периферического сосудистого сопротивления (ОПСС), которое считают характерным для «холодного» грамотрицательного шока, у больных обнаружено не было. ОПСС изменялось в пределах 75–100 кПа•с/л, что несколько ниже его нормальных значений.
При проведении корреляционного анализа обнаружена сильная связь между изменениями ЦВД и главного показателя производительности сердца СИ у больных с дистрибутивным вариантом шока. Коэффициент линейной корреляции Пирсона составил 0,77. То есть увеличение венозного возврата способствовало росту производительности сердца, тогда как связь СИ с УИ оказалась весьма слабой — 0,14. При кардиогенном варианте шока коэффициент линейной корреляции, вычисленный между показателями ЦВД и СИ, составил всего 0,02. Более тесной в этом случае оказалась связь между УИ и СИ, когда коэффициент Пирсона достигал 0,44. Нарастание тахикардии при обоих вариантах шока увеличению производительности сердца не способствовало.
Заключение
Немедленное исследование центральной гемодинамики в начале клинической манифестации шока при абдоминальном сепсисе позволяет четко выделить два варианта его течения. Синдром малого сердечного выброса при сепсисе может формироваться как по дистрибутивному, традиционно признанному механизму, так и по кардиогенному. Снижение производительности сердца при септическом шоке сопряжено и с наличием сосудистой недостаточности. Классических признаков наличия как гипердинамического, так и гиподинамического режима кровообращения у больных с абдоминальным сепсисом не обнаружено. На фоне снижения производительности сердца чаще наблюдается снижение периферического сосудистого сопротивления.
1. Гусак І.В. Сучасні погляди на проблему сепсису / І.В. Гусак // Шпитальна хірургія. — 2004. — № 4. — С. 59-62.
2. Бойко В.В. Абдоминальный сепсис: диагностика и лечение / В.В. Бойко, И.А. Криворучко, И.В. Гусак // Международный медицинский журнал. — 2002. — № 1–2. — С.102-111.
3. Гринев М.В. Септический шок / М.В.Гринев, Е.Ф. Багненко, Д.М. Кулибаба, М.И. Громов // Вестник хирургии им. И.И. Грекова. — 2004. — Т. 163, № 2. — С. 12-17.
4. Гемодинамика при хронической сердечной недостаточности / Н.Д. Татаркина, Л.Р. Казанова, А.Н. Шестернин [и др.]. // Pacific Medical Journal. — 2008. — № 3. — Р. 61-64.
5. Леон М. Как использовать норадреналин при сепсисе? / М. Леон, С. Мартин (M. Leone, C. Martin) // Біль, знеболювання і інтенсивна терапія. — 2006. — № 2. — С. 42-48.
6. Мальцева Л.А. Сепсис: этиология, эпидемиология, патогенез, диагностика, интенсивная терапия / Мальцева Л.А., Усенко Л.В., Мосенцев И.Ф. — Москва: МЕДпресс-информ, 2005. — 176 с.
7. Eachempati Soumitra R. Monitoring and Testing the Critical Care Patient [електронний ресурс] / S.R. Eachempati // The Merck Manual for Health Care Professionals.–Режим доступу: http://www.merckmanuals.com/professional/sec06/ch067/ch067b.html
8. Pinsky M. Septic Shock [електронний ресурс] / M.Pinsky // Medscape Reference. Drugs, Diseases & Procedures. — Режим доступу: http://emedicine.medscape.com/article/168402-overview