Журнал «Медицина неотложных состояний» 6 (37) 2011
Вернуться к номеру
Динамика сывороточных маркеров апоптоза при благоприятном прогнозе сочетанной травмы
Авторы: Киселева А.В.3, 5, Чурляев Ю.А.3, 4, Борщикова Т.И.3, 4, Епифанцева Н.Н.4, Радивилко А.С.2, Дербенева О.А.2, Григорьев Е.В.1, 2 1УРАМН НИИ комплексных проблем сердечно-сосудистых заболеваний СО РАМН, г. Кемерово 2ГОУ ВПО «Кемеровская государственная медицинская академия Росздрава» 3Филиал УРАМН НИИ общей реаниматологии им. В.А. Неговского РАМН, г. Новокузнецк 4ГОУ ДПО «Новокузнецкий ГИУВ Росздрава», г. Новокузнецк 5ФГУ «Новокузнецкий научно-практический центр медико-социальной экспертизы и реабилитации инвалидов ФМБА»
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Версия для печати
Цель исследования: определение динамики сывороточных маркеров апоптоза при благоприятном прогнозе сочетанной травмы. Материалы и методы: в исследование были включены 34 пострадавших с сочетанной травмой. Тяжесть пострадавших по шкале ISS — 35,0 ± 14,0 балла, что соответствует вероятности летального исхода по TRISS 9,5 %; по шкале APACHE II — 16,0 ± 6,0 балла. В сыворотке крови определяли sAPO-1/Fas (растворимый Fas-рецептор), sFas-L (растворимый Fas-лиганд), Bcl-2 и р53 методом иммуноферментного анализа. Результаты: у пациентов с сочетанной травмой в первые сутки определялся исходно высокий уровень sAPO-1/Fas (410,9 ± 89,7 пг/мл), который резко снижался на вторые сутки, оставаясь при этом достоверно выше контрольных значений. Уровень растворимого Fas-лиганда (Т-клеточная или NK-клеточная цитотоксичность) исходно почти в три раза превышал контрольные значения и с третьих суток повышался параллельно sAPO-1/Fas. Уровень Bcl-2 в сыворотке крови в первые сутки был достоверно выше, чем в контрольной группе, что составило 26,5 ± 6,3 пг/мл. На пятые сутки происходило значительное повышение концентрации Bcl-2 до 39,8 ± 8,8 нг/мл. Уровень р53 в первые сутки в сыворотке крови в три раза превышал контрольные значения, достигая 7,21 ± 3,39 ед/мл. На вторые и третьи сутки наблюдалась тенденция к снижению концентрации р53 до контрольных величин — 2,52 ± 1,03 ед/мл к третьим суткам. Заключение: динамика приведенных и анализированных показателей позволяет предполагать, что вследствие сочетанной травмы апоптоз развивается в клетках различных органов и тканей как по внешнему пути — через «рецепторы смерти», так и по внутреннему — через регуляцию проницаемости митохондриальных мембран.
Сочетанная травма, апоптоз, сывороточные маркеры.
Критические состояния, включая травму и сепсис, часто осложняются развитием полиорганной недостаточности и связаны с гибелью клеток паренхиматозных и непаренхиматозных тканей. Множество исследований посвящено роли апоптоза в развитии иммунной и органной дисфункции, наблюдаемой при сепсисе и шоке. Апоптотическим изменениям подвергаются нейтрофилы, макрофаги, дендритные клетки, а также различные популяции лимфоцитов, эндотелиальные и эпителиальные клетки. Клинические и экспериментальные наблюдения позволяют предположить, что «программированная гибель» клеток путем апоптоза может играть важную роль в механизмах полиорганной недостаточности (ПОН) у пациентов в критических состояниях [1–3]. В ранний период сочетанной травмы, осложненной шоком, апоптоз индуцируется в тимусе, селезенке, печени, легких и кишечнике, при этом процент фрагментированной ДНК в этих органах возрастает в соответствии с тяжестью травмы [3]. Исследование методом ISEL показало развитие апоптоза также в мозге, сердце и почках [4, 5]. В головном мозге после геморрагического шока наблюдалось нарастание апоптоза в течение первых суток после ишемии-реперфузии [6]. Ишемия кишечника после травмы и геморрагического шока приводит к дисфункции кишечного барьера и продукции-высвобождению биологически активных и повреждающих ткани факторов в мезентериальную лимфу, что, в свою очередь, вызывает острую легочную недостаточность и развитие системного воспалительного ответа. Предполагается, что повреждение легких при травме с геморрагическим шоком связано с апоптозом эндотелиальных и эпителиальных клеток легких. Есть мнение, что апоптоз в легких протекает по Fas-опосредованному механизму [2, 6, 7].
Цель исследования: определение динамики сывороточных маркеров апоптоза при благоприятном прогнозе сочетанной травмы.
Материалы и методы
В исследование были включены 34 пострадавших с сочетанной травмой. Исключены пострадавшие с превалированием тяжелой черепно-мозговой травмы (ЧМТ); сопутствующей тяжелой соматической патологией, известной на момент включения; умершие в первые сутки от необратимого шока. Исследование одобрено Этическим комитетом учреждений. Тяжесть пострадавших по шкале ISS — 35,0 ± 14,0 балла (Champion et al., 1991), что соответствует вероятности летального исхода по TRISS 9,5 %; по шкале APACHE II — 16,0 ± 6,0 балла. У всех больных регистрировался системный воспалительный ответ (по наличию клинических признаков системного воспаления: ССВО I — 45 %, ССВО II — 35 %, ССВО III — 20 %) (Bone еt al., 1991). В динамике оценивалась органная недостаточность по шкале SOFA: при поступлении 5,0 ± 3,0 балла. Отметим, что показатель SOFA на вторые сутки снижался до минимальных значений, что в совокупности с клиническими данными характеризует регресс полиорганной недостаточности и благоприятный прогноз сочетанной травмы.
В первые сутки пострадавшим были выполнены оперативные вмешательства (по клиническим, лабораторным и инструментальным показаниям) в объеме остановки кровотечения и иммобилизации переломов.
Интенсивная терапия:
1) нормализация объема циркулирующей крови путем целенаправленной инфузионно-трансфузионной терапии с достижением целевых значений среднего АД 80 мм рт.ст., венозной сатурации — не менее 65 % и уровня гематокрита — не менее 0,30;
2) респираторная поддержка у всех больных в объеме от масочной инсуффляции кислорода до перевода на искусственную вентиляцию легких в режиме контроля по давлению;
3) обезболивание опиатными агонистами;
4) нутритивная поддержка с исключением иммунных смесей из расчета 15–20 ккал/кг/сутки, преимущественно энтеральным путем после коррекции гемодинамики и метаболического ацидоза;
5) симптоматическая терапия.
Все пациенты переведены в профильные отделения и выписаны с улучшением. Контрольную группу составили 11 человек (8 мужчин, 3 женщины, средний возраст 35,8 ± 4,1 года), данные показателей сывороточных маркеров апоптоза которых были приняты за норму.
Венозная кровь забиралась при поступлении, далее на 2-е, 3-и, 5-е и 7-е сутки. Пробы крови центрифугировались, сыворотка сохранялась до проведения исследования при температуре –70 °С. В сыворотке определяли sAPO-1/Fas (растворимый Fas-рецептор, sFas), sFas-L (растворимый Fas-лиганд), Bcl-2 и р53 методом иммуноферментного анализа на планшетном фотометре Multiskan-EX (Labsystems, Финляндия) наборами фирмы Bender MedSystems (Австрия) в соответствии с инструкциями фирмы-производителя. Материал обработан статистически с помощью программы Statistica 7.0, данные приведены как средняя ± стандартное отклонение.
Результаты и обсуждение
Система Fas-L/Fas
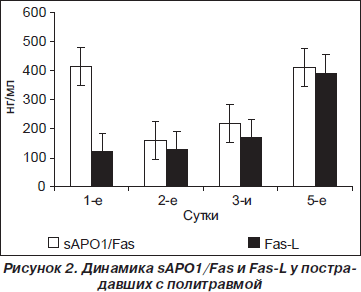
У пациентов с сочетанной травмой в первые сутки определялся исходно высокий уровень sAPO-1/Fas (410,9 ± 89,7 пг/мл), который резко снижался на вторые сутки, оставаясь при этом достоверно выше контрольных значений, составлявших для sAPO-1/Fas 108,0 ± ± 12,0 пг/мл (р < 0,01). Далее уровень sAPO-1/Fas увеличивался, достигая максимума на пятые сутки (419,5 ± ± 94,5 пг/мл) (рис. 1). К седьмым суткам происходило заметное снижение по сравнению с пятыми сутками, однако показатель оставался достоверно выше, чем в контрольной группе (р < 0,01).
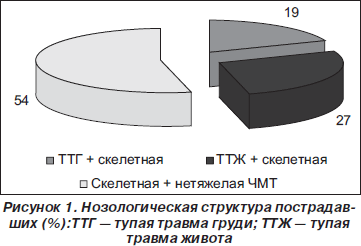
Уровень растворимого Fas-лиганда исходно почти в три раза превышал контрольные значения, составлявшие 48,0 ± 14,0 пг/мл, и с третьих суток повышался параллельно sAPO-1/Fas, также достигая максимума на пятые сутки, а на седьмые — снижаясь до исходных величин.
Система Fas-L/Fas является одним из наиболее значимых механизмов, регулирующих индукцию апоптоза. Fas-рецептор (CD95) — это белок на клеточной поверхности, наиболее изученный член семейства TNF-мембранных рецепторов. Fas экспрессируется в различных типах клеток, включая тимоциты, активированные В-клетки, Т-клетки, моноциты, макрофаги, нейтрофилы, а также в неиммунных клетках в легких и сердце [8, 9]. Fas также широко экспрессируется всеми клетками печени и играет центральную роль в различных заболеваниях печени [10]. Fas опосредует апоптоз в том случае, когда он связывается со специфическими белками. Естественный специфически связывающийся с Fas белок — его лиганд, или Fas-L массой 40 kDa, который является мембранным белком типа II и принадлежит семейству TNF. Fas-L доминирует на активированных Т-клетках и NK-клетках. Таким образом, Fas-L-опосредованная клеточная гибель связана с Т-клеточной или NK-клеточной цитотоксичностью, некоторыми видами патологического повреждения тканей и регуляцией лимфоцитарного гомеостаза. Молекула Fas-L может «отрезаться» от мембраны матриксной металлопротеиназой и переходить в растворимую форму sFas-L.
Fas-опосредованный апоптоз играет важную роль в воспалительном ответе. Растворимые формы sFas образуются в результате альтернативного сплайсинга мРНК [11].Механизмы регулирующего действия sFas в организме еще до конца не изучены. Предполагают, что растворимые формы ингибируют апоптоз, блокируя связывание мембранной формы Fas с Fas-L за счет взаимодействия в кровотоке [12, 13].
Сепсис, шок и травма ассоциированы с индукцией системного воспаления и последующей активацией лейкоцитов, приводящей к дисрегуляции и активации иммунных клеток и далее к повреждениям органов и развитию ПОН. В исследовании [14] было показано, что нейтрофилы способны индуцировать смерть клеток легочного эпителия через высвобождение sFas-L. Мы предполагаем, что в ответ на повышение Fas-L происходит выброс sFas, как защитный механизм от возможных аутоиммунных повреждений. В эксперименте было показано, что sFas проявляет цитотоксичность в культуре лимфоцитов, в то время как Fas-L частично блокирует этот эффект [12]. Снижение sFas и sFas-L на вторые сутки, возможно, связано с индукцией апоптоза и потерей лимфоцитов. Исследования состояния лимфоцитов в раннем посттравматическом периоде показывают резкое снижение содержания этих клеток уже в течение первых 24 часов после травмы. Соотношение Fas и Fas-L является одним из показателей, характеризующих критическое состояние. При повышенной экспрессии Fas-L и недостатке sFas обширный апоптоз в органах и тканях приводит к развитию полиорганной недостаточности, а при избытке sFas массовая гибель лимфоцитов может вызывать иммуносупрессию.
BCL-2 и р53
Уровень Bcl-2 в сыворотке крови в первые сутки был достоверно выше, чем в контрольной группе (7,11 ± ± 5,55 нг/мл; р < 0,01) и составлял 26,5 ± 6,3 нг/мл. На пятые сутки происходило значительное повышение концентрации Bcl-2 до 39,8 ± 8,8 нг/мл, однако к седьмым суткам уровень Bcl-2 снижался до 22,8 ± 4,3 нг/мл (рис. 2).
Ген Bcl-2 открывает новое семейство генов, причастных к регуляции апоптоза и повышению жизнеспособности клеток без воздействия на клеточную пролиферацию. Ген Bcl-2 выполняет уникальную среди онкогенов млекопитающих функцию в качестве негативного регулятора апоптоза. Основной функцией Bcl-2 и его антиапоптотических белков является сохранение целостности митохондрий, обеспечивая синтез АТФ и ингибируя высвобождение проапоптотических факторов, в частности цитохрома С, который активирует каспазный каскад, неминуемо ведущий к апоптозу (R.J. Youle, А. Strasser, 2008). Способность Bcl-2 образовывать на наружной митохондриальной мембране гетеродимеры с проапоптотическими белками семейства ингибирует прямую пермеабилизацию мембраны, тогда как способность ингибировать высвобождение Ca2+ из ЭПР препятствует транспорту Ca2+ в митохондрии, тем самым предотвращая открытие РТР (permeability transition pores — поры временной проницаемости).
Белок р53 является транскрипционным фактором, запускающим внутренний путь апоптоза. В здоровых клетках концентрация р53 поддерживается на низком уровне благодаря его короткому периоду полужизни и деградации в протеосомах [14, 15]. На ранних этапах изучения индукции р53 было установлено, что активность р53 появляется в ответ на повреждения ДНК. Условия для появления генетически измененных клеток возникают при самых разнообразных сбоях физиологических процессов. Описан целый ряд состояний, способных активировать р53. К ним относится состояние гипоксии и ишемии, состояние гипероксии, отсутствие или избыток некоторых цитокинов, действие окиси азота и многое другое. Все эти состояния вызывают характерные для каждого из них модификации как самого белка р53, так и систем, контролирующих его уровень и активность [15].
У пациентов с сочетанной травмой в первые сутки уровень р53 в сыворотке крови в три раза превышал контрольные значения, составлявшие 2,3 ± 0,4 ед/мл, и достигал 7,21 ± 3,39 ед/мл. На вторые и третьи сутки наблюдалась тенденция к снижению концентрации р53 до контрольных величин — 2,52 ± 1,03 ед/мл к третьим суткам, однако на пятые сутки определялся всплеск уровня р53 до 9,73 ± 5,01 ед/мл. Помимо регуляции транскрипции р53 может напрямую взаимодействовать с белками семейства Bcl-2. В семейство Bcl-2 белков входят как анти-, так и проапоптотические белки, которые содержат гомологичные последовательности внутри консервативного участка, известного как Bcl-2-гомологичные домены [16]. Возможно, увеличение уровня р53, индуцированное гипоксией, приводит к повышению концентрации антиапоптотического белка Bcl-2 [16].
Заключение
Динамика приведенных и анализированных показателей позволяет предполагать, что вследствие сочетанной травмы апоптоз развивается в клетках различных органов и тканей как по внешнему пути — через «рецепторы смерти», так и по внутреннему — через регуляцию проницаемости митохондриальных мембран.
1. Епифанцева Н.Н., Борщикова Т.И., Ситников П.Г., Чурляев Ю.А. и др. Сывороточные маркеры апоптоза при травматическом и ишемическом повреждении головного мозга // Общая реаниматология. — 2009. — № 6. — С. 54-60.
2. Голубев А.М., Москалева Е.Ю., Северин С.Е., Веснянко Т.П. Апоптоз при критических состояниях // Общая реаниматология. — 2006. — II (5–6). — С. 184-190.
3. Akazawa Y., Gores G.J. Death receptor-mediated liver injury // Semin. Liver. Dis. — 2007. — 27(4). — Р. 327-338.
4. Barlos D., Deitch E.A., Watkins A.C., Caputo F.J., Lu Q., Abungu B., Colorado I., Xu D.Z., Feinman R. Trauma-hemorrhagic shock-induced pulmonary epithelial and endothelial cell injury utilizes different programmed cell death signaling pathways // Am. J. Physiol. Lung. Cell. Mol. Physiol. — 2009. — 296(3). — L404-417.
5. Guan J., Jin D.D., Jin L.J., Lu Q. Apoptosis in organs of rats in early stage after polytrauma combined with shock // J. Trauma. — 2002. — 52(1). — 104-11.
6. Устьянцева И.М. Апоптоз и воспалительный ответ // Политравма. — 2007. — 1. — 74-80.
7. Konno R., Takano T., Sato S., Yajima A. Serum soluble fas level as a prognostic factor in patients with gynecological malignancies // Clin. Cancer. Res. — 2000. — 6(9). — 3576-3580.
8. Hao Z., Hampel, B., Yagita, H., Rajewsky, K. T cell-specific ablation of Fas leads to Fas ligand-mediated lymphocyte depletion and inflammatory pulmonary fibrosis // J. Exp. Med. — 2004. — 199. — 1355-1365.
9. Kalkan E., Eser O., Avunduk M.C., Coşar M., Fidan H., Kalkan S. Apoptosis and cerebral ischemic reperfusion injury developed after haemorrhagic shock: experimental study // Ulus. Trauma Acil. Cerrahi Derg. — 2006. — 12(4). — 263-267.
10. Krammer P.H. CD95 (APO-1/Fas)-mediated apoptosis: live and let die // Adv. Immunol. — 1999. — 71. — 163-210
11. Perl M., Chung C.S., Perl U., Lomas-Neira J., de Paepe M., Cioffi W.G., Ayala A. Fas-induced pulmonary apoptosis and inflammation during indirect acute lung injury // Am. J. Respir. Crit. Care Med. — 2007. — 176(6). — 591-601.
12. Serrao K.L., Fortenberry J.D., Owens M.L., Harris F.L., Brown L.A. Neutrophils induce apoptosis of lung epithelial cells via release of soluble Fas ligand // Am. J. Physiol. Lung Cell. Mol. Physiol. — 2001. — 280. — L298-L305.
13. Telegina E., Reshetnyak T., Moshnikova A., Proussakova O., Zhukova A., Kuznetsova A., Ivanov A., Paltsev M., Beletsky I. A possible role of Fas-ligand-mediated «reverse signaling» in pathogenesis of rheumatoid arthritis and systemic lupus erythematosus // Immunol. Lett. — 2009. — 29. — 122(1). — 12-17.
14. Yasuhara S., Asai A., Sahani N.D., Martyn J.A. Mitochondria, endoplasmic reticulum, and alternative pathways of cell death in critical illness // Crit. Care Med. — 2007. — 35 (Suppl. 9). — S488-95.
15. Чумаков П.М. Белок р53 и его универсальные функции в многоклеточном организме // Успехи биологической химии. — 2007. — 47. — 3-52.
16. Youle R.J., Strasser A. The Bcl-2 protein family: Opposing activities that mediate cell death // Nat. Rev. Mol. Cell. Biol. — 2008. — 9. — 47-59.
