Журнал «Медико-социальные проблемы семьи» 2 (том 18) 2013
Вернуться к номеру
Локальний протокол «Організація медичної допомоги недоношеним дітям при народженні»
Авторы: Левченко Л.А., Батман Ю.А., Лінчевський Г.Л., Головко О.К., Міміношвілі Т.В. - Донецький національний медичний університет ім. М. Горького, Центральна міська клінічна лікарня № 3, м. Донецьк
Рубрики: Анестезиология-реаниматология, Медицина неотложных состояний, Акушерство и гинекология, Педиатрия/Неонатология
Разделы: Медицинское образование
Версия для печати
У даній роботі зроблена спроба скласти локальний протокол із надання медичної допомоги недоношеним дітям при народженні. Акцент зроблений на змінах у первинній реанімації новонароджених згідно з гестаційним віком і тяжкістю стану дитини. Стан оксигенації новонародженого слід визначати за даними пульсоксиметрії. Вірогідним критерієм ефективності реанімації є зростання частоти серцевих скорочень. Запропонована змінена методика перев’язки пуповини. У ряді випадків рекомендовано починати респіраторну підтримку повітрям. Докладно розписані всі пункти теплового ланцюжка. Потрібно проводити реанімаційні заходи недоношеному новонародженому з низькою та екстремально низькою масою тіла при народженні шляхом загортання в поліетиленовий мішок так, щоб відкритою залишалась тільки голова. За необхідності для обігріву недоношеного можна використовувати екзотермічний матрац. Лікарський огляд новонародженого здійснюється відповідно до схеми. Профілактика та лікування гіпотермії включає рекомендації для створення нейтрального температурного середовища в інкубаторі. Наведена і тактика лікаря-неонатолога при виявленні гіпоглікемії у дитини. Надані методи оцінки дихальних розладів у недоношених новонароджених. Визначено поняття затримки дихання і апное, з подальшою тактикою лікування таких хворих дітей, включаючи штучну вентиляцію легенів. Детально розписана методика введення екзогенного сурфактанту з профілактичною та лікувальною метою. Рекомендована авторська методика введення препарату через додатковий бічний отвір в інтубаційній трубці. Практичні рекомендації із застосовування сурфактанту спрямовані на підвищення ефективності дії, що дозволить виключити як перинатальні ускладнення, так і технічні складнощі з уведення препарату.
В данной работе сделана попытка составить локальный протокол по оказанию медицинской помощи недоношенным детям при рождении. Акцент сделан на изменениях в первичной реанимации новорожденных согласно гестационному возрасту и тяжести состояния ребенка. Состояние оксигенации новорожденного следует определять по данным пульсоксиметрии. Достоверным критерием эффективности реанимации является увеличение частоты сердечных сокращений. Предложена измененная методика перевязки пуповины. В ряде случав рекомендовано начинать респираторную поддержку воздухом. Подробно расписаны все пункты тепловой цепочки. Необходимо проводить реанимационные мероприятия недоношенным новорожденным с низкой и экстремально низкой массой тела при рождении, предварительно завернув в полиэтиленовый мешок так, чтобы открытой оставалась только голова. При необходимости для обогрева недоношенного можно использовать экзотермический матрас. Врачебный осмотр новорожденного осуществляется согласно схеме. Профилактика и лечение гипотермии включает рекомендации для создания нейтральной температурной среды в инкубаторе. Приведена и тактика врача-неонатолога при выявлении гипогликемии у ребенка. Даны методы оценки дыхательных расстройств у недоношенных новорожденных. Определены понятия задержки дыхания и апноэ с последующей тактикой лечения таких больных детей, включая искусственную вентиляцию легких. Подробно расписана методика введения экзогенного сурфактанта с профилактической и лечебной целью. Рекомендована авторская методика введения препарата через дополнительное боковое отверстие в интубационной трубке. Практические рекомендации по применению сурфактанта направлены на повышение эффективности действия, что позволит исключить как перинатальные осложнения, так и технические сложности по введению препарата.
In this paper we attempt to make a local protocol for the provision of medical care to preterm infants at birth. Emphasis is made on changes in neonatal resuscitation according to gestational age and the severity of the child. The state of oxygenation of the newborn should be determined by pulse oximetry. The reliable criterion of the effectiveness of resuscitation is increased heart rate.We propose a modified technique of umbilical cord ligation. In some cases, the recommended starting respiratory air support. All the points of thermal chain had been decribed in detail. It is necessary to carry out resuscitation for premature newborns with low and extremely low birth weight, before this you have to wrap the child in a plastic bag so that only the head remained open. If necessary for heating of premature you can use exothermic mattress. Medical examination of the newborn is being carried out according to the scheme. Prevention and treatment of hypothermia include recommendations for the creation of a neutral thermal environment in the incubator. Tactics of neonatologist in detecting hypoglycemia in child is also given. Evaluation methods for respiratory disorders in premature infants are given. The definitions of the concepts of breath-holding and apnea with the follow tactics of treating such children, including artificial lung ventilation, are determined. The method of administration of exogenous surfactant with prophylactic and therapeutic purposes is described in detail. The author’s method of administration of the drug through the additional lateral hole in the endotracheal tube is recommended. The practical guidelines on the use of surfactant are directed on increase of efficiency of action, which will prevent both perinatal complications and the technical complexity for the introduction of the drug.
недоношені новонароджені, первинна реанімація, сурфактант.
недоношенные новорожденные, первичная реанимация, сурфактант.
premature newborns, primary resuscitation, surfactant.
Для України тема виходжування недоношених дітей дуже актуальна, бо щороку народжується близько 20 тисяч недоношених малюків, з них 3700 — з наднизькою масою тіла (менше 1500 грамів), у тому числі близько 1200 дітей з екстремально малою масою тіла (менше 1000 грамів) [1, 5, 14]. Згідно з Наказом № 179 МОЗ України, з 1 січня 2007 року в Україні реєструється кожен малюк, який народився починаючи з 22-го тижня вагітності і/або вагою від 500 г. Відповідно, процес виходжування таких новонароджених для лікарів-неонатологів став значно складнішим [2, 7–9]. Як зазначила головний спеціаліст із неонатології МОЗ України, професор Є.Є. Шунько, якість життя глибоконедоношених новонароджених вимагає впровадження сучасних світових стандартів інтенсивної терапії та виходжування дітей із дуже малою масою тіла [14]. Ці стандарти ґрунтуються на забезпеченні медичних установ сучасним обладнанням, високопрофесійними медичними кадрами, впровадженні клінічних протоколів на основі доказової медицини, безперервному навчанні лікарів і медичних сестер [4, 6].
Клінічний протокол — нормативний акт державного рівня, що розробляється на основі клінічної настанови з урахуванням можливостей системи охорони здоров’я. Покроково визначає процес надання медичної допомоги, обсяг та її результати при певному захворюванні, затверджується Міністерством охорони здоров’я [4, 7]. Сьогодні згідно з Наказом МОЗ України № 102/18 від 19.02.2009 заохочується створення локальних протоколів для вдосконалення медичної допомоги в регіонах. Локальний протокол медичної допомоги — це нормативний документ регіонального рівня, що спрямований на забезпечення надання безперервної, ефективної та економічно доцільної медичної допомоги при певних захворюваннях та інших патологічних станах відповідно до уніфікованих клінічних протоколів медичної допомоги, забезпечує координацію та впорядкування за часовим графіком технологій та методів надання медичної допомоги багато-міждисциплінарного змісту, регламентує реєстрацію медичної інформації і ведення клінічного аудиту; затверджується головним лікарем лікувально-профілактичного закладу.
Враховуючи сказане, пропонуємо вашій увазі локальний протокол з організації медичної допомоги недоношеним дітям при народженні.
1. Первинна реанімація в пологовій залі (дані Міжнародної конференції з серцево-легеневої реанімації і невідкладної кардіологічної допомоги, 2010 рік) [5, 7, 9].
1.1. Пологова зала
Адекватна реанімаційна допомога новонародженим дозволяє знизити їх смертність і/або захворюваність на 5–40 %.
Дитина, яка потребує медичної допомоги відразу після народження, визначається за такими ознаками:
— ціаноз;
— гестаційний вік (ГВ) менше 37 тижнів;
— відсутнє або неадекватне дихання;
— відсутній або значно знижений м’язовий тонус.
Перехід до наступного реанімаційного кроку після первинної оцінки стану новонародженого базується на результатах одномоментної оцінки 2 життєво важливих ознак: частоти серцевих скорочень (ЧСС < 100 уд/хв) і дихання (апное або термінальні дихальні рухи за типом гаспінгу).
Стан оксигенації новонародженого слід визначати за даними пульсоксиметрії, бо візуальна оцінка кольору шкіри є невірогідною. Треба пам’ятати, що пульсоксиметрія є допоміжним методом, який не може замінити клінічної оцінки стану новонародженого. Вірогідним критерієм ефективності реанімації є зростання ЧСС.
Недоношеного новонародженого з гестаційним віком < 28 тижнів не обсушувати, а відразу загорнути в поліетиленовий мішок так, щоб відкритою залишалась тільки голова. Початкову допомогу і всі реанімаційні заходи проводять під лампою променевого тепла, не витягуючи дитину з мішка. Для обігріву недоношеного можна використовувати екзотермічний матрац. Важливо не знімати мішок із дитини до моменту вимірювання температури тіла у відділенні інтенсивної терапії. Температура повітря в пологовій залі повинна бути не нижче ніж 26 °С.
Санація верхніх дихальних шляхів у новонародженого рекомендується у випадках явного утруднення самостійного дихання (дихальні розлади) або необхідності проводити штучну вентиляцію легень (ШВЛ).
Необхідність у додатковому призначені кисню визначається за данними пульсоксиметрії. Штучну вентиляцію легень недоношених новонароджених з гестаційним віком 32–36 тижнів виконують повітрям, а з гестаційним віком менше 32 тижнів — 30–90% киснем із послідовним титруванням концентрації кисню в дихальній суміші (у разі відсутності змішувача — також повітрям). Якщо проводилась ефективна вентиляція, а оксигенація (дані пульсоксиметрії) залишається недостатньою і ЧСС < 60 уд/хв, потрібно використовувати більш високу концентрацію кисню (інколи 100 %).
Співвідношення між частотою натискування на грудину та кількістю вентиляцій легень під час реанімації новонародженого залишається 3 : 1. Однак, якщо термінальний стан дитини пов’язаний із серцевими проблемами, то співвідношення між частотою компресії і вентиляцією може досягати 15 : 2.
Доза внутрішньовенного адреналіну залишається 0,1–0,3 мл/кг 0,01% розчину, а ендотрахеального — 0,5–1,0 мл/кг 0,01% розчину.
1.1.1. За умови терміну гестації 34–36 тижнів і задовільного стану дитини при народженні (табл. 1) акушерка викладає дитину на живіт матері та обсушує сухою і теплою пелюшкою голову та тулуб дитини, потім вкриває іншою сухою теплою пелюшкою. Після закінчення пульсації пуповини, але не пізніше 1 хв, замінивши стерильні рукавички, акушерка «зціджує» кров у напрямку до дитини, а потім перетискає та перетинає пуповину, вдягає шапочку і шкарпетки, перекладає дитину на груди матері та накриває спільно з нею.
1.1.2. Наприкінці 1-ї та 5-ї хвилини лікар-неонатолог здійснює оцінку стану дитини за шкалою Апгар (під час контакту «шкіра до шкіри»).
1.1.3. Спостереження за дитиною триває протягом перебування дитини в контакті «шкіра до шкіри» у пологовій кімнаті. Спостереження за дитиною здійснює лікар-неонатолог, а за його відсутності — лікар акушер-гінеколог, акушерка або медсестра. Спостерігають за кольором шкіри і слизових оболонок, характером і частотою дихання, частотою серцевих скорочень, руховою активністю кожні 15 хвилин протягом першої години, потім щонайменше кожні 30 хвилин протягом другої години.
1.1.4. Контакт «шкіра до шкіри» триває не менше 2 годин у разі стабільного клінічного стану дитини.
1.1.5. При виявленні пошукового і смоктального рефлексів (дитина відкриває рот, повертає голівку, проявляє підвищену рухову активність) акушерка допомагає здійснити перше прикладання дитини до грудей матері. Якщо дитина не виявляє ознак пошукового і смоктального рефлексів, необхідно здійснити прикладання дитини до грудей матері з метою колонізації флорою матері і стимуляції лактації.
1.1.6. Лікар-неонатолог надає матері інформацію про особливості спостереження за дитиною.
1.1.7. Через 30 хвилин після народження під час контакту «шкіра до шкіри» необхідно виміряти температуру тіла дитини електронним термометром в аксилярній ділянці та занести дані в карту розвитку новонародженого. Температуру тіла дитини слід контролювати щонайменше кожні 30 хвилин під час перебування в пологовій кімнаті, потім у динаміці кожні 4–6 годин у першу добу.
1.1.8. Під час проведення контакту «шкіра до шкіри» і після першого прикладання до грудей (але не пізніше першої години життя дитини) після відповідної обробки рук акушерка проводить новонародженому однократну профілактику офтальмії із застосуванням 0,5% еритроміцинової або 1% тетрациклінової мазі відповідно до інструкції про застосування.
1.1.9. У разі виявлення будь-яких патологічних ознак (табл. 1) огляд дитини проводиться лікарем-неонатологом негайно. Якщо адаптація дитини в умовах контакту «шкіра до шкіри» перебігає без ускладнень, повний лікарський огляд проводиться на теплому пеленальному столі під променевим теплом через дві години після народження.
1.1.10. Акушерка здійснює медичне спостереження за станом новонародженого протягом перебування дитини в пологовій залі.
1.1.11. Після 2 годин перебування дитини в пологовій залі акушерка вимірює та зважує дитину; одягає в повзунки, дитячу сорочечку, шапочку, шкарпетки, рукавички (можна використовувати чистий домашній одяг).
1.1.12. Дитина передається матері і переводиться до післяпологового відділення в контакті «шкіра до шкіри» або в кувезі, або в ліжечку з підігрівом.
Недоношеним новонародженим з гестаційним віком 32–33 тижні після надання реанімаційної допомоги питання про викладання на груди або живіт матері вирішується індивідуально в кожному випадку.
Медична допомога недоношеним новонародженим у пологовій кімнаті і операційній із гестаційним віком менше 32 тижнів надається згідно з протоколом первинної реанімації новонароджених.
2. Тепловий ланцюжок [3, 12, 20].
Потрібно дотримуватися 10 кроків теплового ланцюжка:
— тепла пологова кімната (t = 25–28 °С), одежу дитини своєчасно підготувати та підігріти;
— після народження негайно обсушити дитину попередньо підігрітими пелюшками;
— контакт «шкіра до шкіри»;
— грудне вигодовування починати якомога раніше;
— зважування та антропометрію дитини необхідно проводити після здійснення контакту «шкіра до шкіри»;
— правильно одягнути та загорнути дитину;
— транспортування в теплих умовах;
— реанімаційні заходи проводити в теплих умовах;
— всі медичні працівники і члени родини дитини повинні мати відповідну підготовку з принципів дотримання теплового ланцюжка.
Водночас догляд за дитиною з малою масою тіла при народженні потребує більш ретельного дотримання теплового режиму та частішого контролю температури тіла дитини.
3. Рутинні медичні втручання [7, 13].
3.1. Діти з масою тіла > 1500 грамів і терміном гестації > 32 тижні без ознак захворювання при народженні не потребують жодних діагностичних лабораторних обстежень за відсутності показань.
3.2. Визначення рівня глюкози крові проводиться обов’язково новонародженим із масою тіла при народженні 1500 г і менше в перші 4–6 годин однократно, а також дітям із клінічними ознаками гіпоглікемії. Повторне визначення рівня глюкози крові проводиться відповідно до клінічного стану дитини та результатів попереднього дослідження.
4. Лікарський догляд за новонародженою дитиною з малою масою тіла при народженні [3, 7, 11, 15].
4.1. Первинна лікарська оцінка стану новонародженої дитини з малою масою тіла при народженні:
1) первинна оцінка стану новонародженого з малою масою тіла при народженні (табл. 1) здійснюється лікарем-неонатологом відразу після народження дитини;
2) у разі виявлення будь-яких патологічних ознак первинний лікарський огляд дитини проводиться лікарем-неонатологом негайно.
4.2. Первинний лікарський огляд новонародженого з малою масою тіла при народженні у пологовій залі:
— у разі, якщо адаптація новонародженого з малою масою тіла при народженні в умовах контакту «шкіра до шкіри» перебігає без ускладнень, повний лікарський огляд проводиться на теплому пеленальному столі під променевим теплом через дві години після народження дитини перед переведенням у палату спільного перебування матері та дитини;
— перед оглядом дитини лікар здійснює миття рук та знезараження фонендоскопа. Фонендоскоп перед використанням треба зігріти. Результати огляду необхідно занести до карти розвитку новонародженого;
— лікар, який здійснив первинний лікарський огляд, записує результати огляду в медичній документації, інформує батьків про стан здоров’я дитини на момент огляду.
4.3. Лікарський огляд новонародженого здійснюється посистемно, не допускається переохолодження дитини (табл. 2).
4.4. Новонародженим із малою масою тіла при народженні необхідно визначати гестаційний вік за шкалою Балард з 12 до 36 годин життя.
Висновок
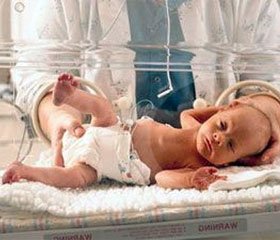
4.5. У разі фізіологічної адаптації новонародженого (рис. 1), що перебігає в умовах раннього необмеженого контакту матері та дитини, можливості раннього початку грудного вигодовування, відсутності вроджених вад розвитку або інших порушень у стані дитини, з урахуванням результатів лікарського огляду, дитину можна вважати здоровою на час огляду.
/154/154_1.jpg)
5. Оцінка ризиків та запобігання розвитку патологічних станів [10, 11, 16].
5.1. Дихальні розлади:
1) для визначення наявності дихальних розладів необхідно спостерігати за новонародженим в умовах контакту «шкіра до шкіри», інкубатора або під джерелом променевого тепла (щоб уникнути охолодження), оцінюючи частоту дихань, наявність експіраторного стогону, колір шкіри і слизових оболонок кожні 15 хвилин протягом першої години після народження і кожні 30 хвилин протягом другої години;
2) оцінювання за шкалою Довнеса або Сільвермана (табл. 3) проводять через 15 хвилин після народження дитини не рідше ніж кожні 3 години, а після отримання нульового результату (0 балів) — двічі протягом наступних 2 годин. У разі відсутності ознак дихального дистресу (0 балів) протягом 3 наступних годин оцінювання слід припинити, забезпечити спільне перебування та вигодовування дитини грудним молоком, ретельне спостереження за дитиною, консультування матері щодо догляду за дитиною;
3) у разі появи ознак дихальних розладів необхідно відразу оцінити дитину за шкалою Довнеса або Сільвермана (табл. 3) та класифікувати тяжкість дихального дистресу. У разі виявлення респіраторного дистрес-синдрому (РДС) помірного і тяжкого ступеня необхідно надати невідкладну медичну допомогу відповідно до сучасних вимог ведення дитини з розладами дихання та перевести дитину до неонатологічного відділення.
5.2. Профілактика та лікування гіпотермії [5, 7, 12]:
1) обов’язковою умовою для запобігання гіпотермії у новонароджених із малою масою тіла при народженні є постійний контроль за температурою в приміщенні (наявність кімнатного настінного термометра обов’язкова в кожній палаті);
2) у першу добу життя нормальною температурою тіла дитини є 36,5–37,5 °С. У наступні дні оптимальною є температура тіла в межах 36,8–37,2 °С. Слід уникати розвитку в дитини як гіпотермії, так і гіпертермії;
3) новонароджений із малою масою тіла при народженні потребує додаткового тепла й більш ретельного контролю температури тіла;
4) заходи збереження тепла включають використання теплих кімнат, методу «кенгуру», інкубаторів, ламп-обігрівачів, ліжок-грілок і матраців-грілок. Доцільно використовувати догляд за методом «мами-кенгуру»;
5) інкубатори слід використовувати тільки для хворих новонароджених або для новонароджених з дуже низькою масою тіла;
6) при використанні обігрівальних апаратів (інкубатори, столи з підігрівом, ліжечка з підігрівом та лампи променевого тепла) треба пам’ятати, що новонароджені при цьому повинні бути одягнені в дитячу сорочечку, шапочку, шкарпетки і повзунки і мати стабільний клінічний стан;
7) при виходжуванні новонароджених в інкубаторах необхідно контролювати температуру тіла дитини щонайменше кожні 4–6 годин і регулювати температуру всередині апаратів в межах 30–37 °С (табл. 4). У разі наявності сервоконтролю вважати обов’язковим його використання;
8) контроль температури тіла дитини рутинно проводиться щонайменше 4 рази на добу, у випадках нестабільної температури — частіше;
9) новонародженим з масою тіла ≤ 1000 грамів слід проводити контроль температури тіла кожні 3 години;
10) результати термометрії записуються до карти розвитку новонародженого;
11) у разі розвитку гіпотермії (температура тіла дитини < 36,5 °С) негайно розпочати заходи щодо зігрівання дитини:
— розпочати контакт «шкіра до шкіри». Не дозволяється користуватись грілками для обігрівання дитини;
— перевірити температуру у приміщенні. У разі низької температури в приміщенні обігріти його додатковими обігрівачами;
— перевірити рівень глюкози крові. У разі гіпоглікемії розпочати корекцію цього стану;
— продовжити грудне вигодовування дитини. У разі неможливості вигодовування груддю слід годувати дитину зцідженим грудним молоком за допомогою альтернативних методів;
— провести контрольне вимірювання температури тіла через 15–30 хвилин після проведених заходів. При отриманні результату менше 36,5 °С продовжити зігрівання дитини і вимірювання температури кожні 15–30 хвилин до стабілізації температури тіла дитини та отримання двох послідовних результатів вимірювання температури тіла дитини > 36,5 °С;
— у подальшому контролювати температуру тіла дитини слід щонайменше кожні 4–6 годин.
5.3. У разі розвитку тяжкої гіпотермії (температура тіла ≤ 35 °С):
— негайно розпочати заходи щодо зігрівання дитини (дивись вище);
— припинити ентеральне годування і почати внутрішньовенне введення 10% розчину глюкози із розрахунку фізіологічної потреби дитини;
— контролювати температуру тіла кожні 15 хвилин після проведених заходів до стабілізації температури тіла дитини та отримання двох послідовних результатів вимірювання температури тіла дитини > 36,5 °С;
— паралельно з заходами щодо зігрівання перевірити рівень глюкози в крові; у разі розвитку гіпоглікемії розпочати корекцію цього стану. У разі відсутності гіпоглікемії слід визначати рівень глюкози в крові щонайменше кожні 8 годин протягом 3 діб;
— розпочати ентеральне харчування після стабілізації стану дитини і досягнення температури тіла > 35 °С.
5.4. Профілактика і корекція гіпоглікемії [3, 7, 13].
Нормальним слід вважати рівень глюкози крові 2,6–5,5 ммоль/л. Для контролю за рівнем глюкози крові необхідна наявність в кожному закладі охорони здоров’я глюкотесту (глюкометра) з метою зниження ризику ускладнень інвазивних втручань.
1. Для профілактики розвитку гіпоглікемії годування дитини треба розпочати якомога раніше після народження і проводити його часто (не менше 8 разів на добу як удень, так і вночі).
2. У перші 2–4 години життя дитини відбувається фізіологічне зниження рівня глюкози в крові, тому контрольне вимірювання рівня глюкози треба проводити не раніше ніж через 4 години після народження і не раніше 30 хвилин після останнього годування. При появі симптомів гіпоглікемії, таких як судоми, апное, гіпотонія, погане смоктання, пригнічення або млявість, негайно визначити рівень глюкози крові та розпочати медичну допомогу відповідно до даного протоколу.
3. Контроль рівня глюкози крові дитині, яка знаходиться на грудному вигодовуванні та має задовільний стан, рутинно не проводиться.
4. Визначення рівня глюкози крові проводиться обов’язково новонародженим з масою тіла при народженні 1500 г і менше в перші 4–6 годин однократно, а також дітям з клінічними ознаками гіпоглікемії. Якщо вміст глюкози крові > 2,6 ммоль/л, подальші обстеження цим новонародженим слід проводити кожні 3 години до отримання 2 послідовних результатів рівня глюкози крові > 2,6 ммоль/л.
5. Рівень глюкози в крові рекомендується вимірювати глюкотестом. У разі отримання результату ≤ 2,6 ммоль/л необхідне лабораторне визначення рівня глюкози в крові.
6. У разі отримання результату рівня глюкози в крові < 2,6 ммоль/л, але >2,2 ммоль/л необхідно збільшити частоту годувань дитини, продовжити ретельне клінічне спостереження і провести контроль рівня глюкози в крові глюкотестом через 30 хвилин після годування з подальшим лабораторним підтвердженням рівня глюкози в крові.
7. Новонародженим, які мають при першому вимірюванні рівень глюкози ≤ 2,6 ммоль/л і клінічні прояви гіпоглікемії або ≤ 2,2 ммоль/л незалежно від наявності клінічних ознак гіпоглікемії, треба розпочати корекцію гіпоглікемії:
— негайно розпочати внутрішньовенне введення 10% розчину глюкози із розрахунку 2 мл/кг (200 мг/кг) струминно у периферичну вену протягом 5–10 хвилин, потім перевести на інфузію 10% розчину глюкози із швидкістю 6–8 мг/кг/хвилину та продовжити годування дитини;
— через 30 хвилин від початку корекції гіпоглікемії перевірити рівень глюкози. Якщо він > 2,6 ммоль/л, інфузію слід припинити та продовжити годування дитини. Контроль рівня глюкози проводити до отримання двох послідовних результатів рівня глюкози в крові більше 2,6 ммоль/л з інтервалом в 30 хвилин. Далі треба спостерігати за дитиною;
— якщо при повторному вимірюванні рівень глюкози залишається ≤ 2,2 ммоль/л або дитина має клінічні симптоми гіпоглікемії, повторити струминне введення 10% розчину глюкози із розрахунку 2 мл/кг (200 мг/кг) протягом 5–10 хвилин, потім знову перевести на інфузію 10% розчину глюкози із швидкістю 6–8 мг/кг/хвилину та обов’язково продовжити годування дитини. Повторне вимірювання рівня глюкози в крові провести через 30 хвилин.
5.5. Апное у новонародженої дитини з малою масою тіла при народженні.
Затримка дихання — це зупинка самостійного дихання тривалістю до 20 секунд. Апное — це зупинка самостійного дихання тривалістю понад 20 секунд [10, 13, 18, 20].
1. Недоношені новонароджені схильні до епізодів затримки дихання. Чим менші термін гестації і маса тіла дитини (< 32 тижнів гестації і < 1500 грамів), тим частіше виникають ці епізоди.
2. Рідкісні й короткочасні спонтанні періоди затримки дихання (тривалістю не більше 20 секунд та не більше 2 епізодів на добу) без брадикардії і ціанозу, які пов’язані з годуванням, смоктанням і руховою активністю дитини, не вважаються патологічними і не потребують лікування, але потребують ретельного спостереження. Лікар-неонатолог повинен обов’язково навчити матір заходів щодо виявлення цього стану і надання первинної допомоги дитині з затримкою дихання.
3. Виникнення більше ніж 2 епізодів апное на добу тривалістю понад 20 секунд або будь-якого апное з брадикардією та ціанозом є показанням для переведення в палату або відділення інтенсивної терапії новонароджених і початку інтенсивної терапії.
4. Допомога дитині при апное:
— якщо дитина перестала дихати, слід негайно провести тактильну стимуляцію вздовж спини дитини протягом 10 секунд. Якщо дитина після проведеної стимуляції не почала дихати, негайно розпочати штучну вентиляцію за допомогою мішка і маски;
— проконтролювати температуру тіла дитини. У разі виникнення гіпотермії негайно розпочати необхідні дії щодо корекції цього стану;
— проконтролювати рівень глюкози крові. У разі виникнення гіпоглікемії негайно розпочати необхідні дії щодо корекції цього стану;
— доцільно регулярно профілактично змінювати положення тіла дитини і ретельно слідкувати за нею;
— необхідно навчити матір спостерігати за дитиною та проводити початкові кроки допомоги (тактильна стимуляція) у разі апное.
6. Ендотрахеальне введення сурфактанту [2, 10, 17]:
Загальні вимоги до введення сурфактанту:
1. Препарат сурфактанту потрібно ввести недоношеному новонародженому якомога скоріше після визначення наявних показань;
2. Вводити сурфактант слід лише після стабілізації клінічного стану дитини (нормальна температура тіла, відсутність метаболічних порушень, відсутність брадикардії, артеріальної гіпотензії та ін.).
Показання до ендотрахеального введення сурфактанту [1, 2, 10, 12, 19]:
І. Профілактика респіраторного дистрес-синдрому (проводиться в перші 15–30 хвилин життя, до появи ознак респіраторних розладів):
— у недоношених дітей із гестаційним віком < 28 тижнів;
— у недоношених дітей із гестаційним віком 28–30 тижнів, якщо антенатальна профілактика глюкокортикоїдами не була проведена або проведена в неповному обсязі, високий ризик розвитку РДС (хронічна гіпоксія плода, у матері цукровий діабет, кровотеча в ІІІ триместрі вагітності, артеріальна гіпотензія, попередні випадки народження дітей із РДС, чоловіча стать плода);
— у новонароджених із ГВ > 30 тижнів, з підтвердженою об’єктивними методами незрілістю легенів (пінний тест Клеменса або співвідношення лецитин/сфінгомієлін в навколоплідних водах).
ІІ. Лікування РДС у новонароджених із клінічно підтвердженим діагнозом РДС, яким проводиться ШВЛ через ендотрахеальну трубку:
— рентгенологічні ознаки РДС;
— РаО2 < 50 мм рт.ст. або SрО2 < 88 % у новонародженого на ШВЛ з FiO2 > 30 %; МАР > 6–7 см водн.ст.;
— за неможливості визначити РаО2 або SрО2 лікування сурфактантом показане при клінічних ознаках дихального дистресу і необхідності проведення ШВЛ з FiO2 > 30 %;
— за наявності показань лікувальне введення може проводитися повторно.
III. Тяжкий перебіг внутрішньоутробної (або меконіальної, аспіраційної) пневмонії;
IV. Поєднана патологія: внутрішньоутробна пневмонія та РДС із респіраторними порушеннями тяжкого ступеня.
Розрізняють:
— раннє лікування — у перші 2 години після народження;
— пізнє лікування — у перші 8 годин, але не пізніше 24 годин життя.
Профілактичне введення передбачає два підходи:
— інтубація, введення сурфактанту, наступне проведення ШВЛ;
— інтубація, введення сурфактанту, екстубація з наступним проведенням СРАР через назальні канюлі або маску.
Раннє лікування вважається найбільш оптимальним. Раннє застосування сурфактанту знижує ризик синдромів витоку повітря, ризик смертності від РДС та розвиток бронхолегеневої дисплазії. Введення препарату після 24 год може поліпшувати газообмін, однак суттєво не впливає на результат лікування РДС, тому стандартно не рекомендується.
Протипоказання:
— нестабільність центральної та легеневої гемодинаміки;
— несумісна з життям вада (або вади) розвитку;
— значне порушення життєвих функцій і метаболізму (гіпотермія < 35 °С, брадикардія, артеріальна гіпотензія, метаболічний ацидоз (рН < 7,1 та ВЕ ≤ 15 ммоль/л);
— тяжке органічне ураження центральної нервової системи;
— невідповідний рівень медичної установи (відносне протипоказання);
— легенева кровотеча (відносне протипоказання);
— внутрішньошлуночкова кровотеча (ВШК) III ступеня тяжкості;
— гіперчутливість до компонентів препарату.
Необхідне обладнання:
— препарат сурфактанту, підготовлений і підігрітий (безпосередньо перед використанням флакон з емульсією сурфактанту зігрівають у руках протягом щонайменше 10 хвилин, уникаючи його струшування);
— шприці 2 мл, 5 мл;
— зонд діаметром 3,5 мм або 5 мм (не більше 2/3 діаметра інтубаційної трубки);
— перехідник інтубаційної трубки з боковим адаптером (при потребі);
— фонендоскоп;
— електричний аспіратор;
— катетер для проведення санації ендотрахеальної трубки.
Підготовка пацієнта, спостереження за дитиною [2, 4, 7, 10, 20]:
1. До моменту введення препарату дитині має бути проведена інтубація трахеї і ШВЛ через ендотрахеальну трубку. При цьому необхідно переконатися, що трубка правильно розташована над біфуркацією трахеї. Бажано провести контроль положення ендотрахеальної трубки за допомогою рентгенографії грудної клітки.
2. Індивідуально визначають дозу сурфактанту згідно з рекомендаціями виробника, враховуючи масу тіла дитини при народженні.
3. Важливо безперервно проводити контроль ЧСС, SрО2, артеріального тиску (АТ) під час введення сурфактанту і в наступні години. Через 15–30 хвилин після ендотрахеального уведення сурфактанту бажано визначити газовий склад крові для запобігання можливій гіпероксії та гіпокапнії.
4. Чітко дотримуватись умов стерильності.
5. Для виключення ВШК в недоношеної дитини потрібно сурфактант вводити дрібно (по 1/2 дози з інтервалом 20–30 хвилин).
Методика введення [2, 5, 10]
Існує два методи введення препаратів екзогенного сурфактанту:
— шприцом через зонд, який введено в інтубаційну трубку;
— через додатковий боковий отвір в інтубаційній трубці (Патент на корисну модель № 19748) [21].
1. Метод введення шприцом через зонд.
Проводиться вдвох, при цьому одна особа в стерильних рукавичках виконує дії зі стерильними зондами, катетерами, шприцами, а інша допомагає з утриманням нестерильного обладнання (від’єднує і приєднує дихальний контур, утримує і повертає голову дитини, змінює параметри ШВЛ при необхідності тощо).
1. Зонд вкоротити в асептичних умовах, щоб його довжина дорівнювала довжині інтубаційної трубки та злегка (на 0,2–0,5 см) виступала нижче її кінця. Для визначення потрібної довжини зазвичай використовують як взірець нову інтубаційну трубку того ж виробника, такого ж розміру.
2. Провести санацію ендотрахеальної трубки і продовжити ШВЛ із попередніми параметрами.
3. Набрати потрібну дозу препарату, зігрітого згідно з інструкцією (не збовтувати), в шприц або по 1/2 дози в два шприци, запобігаючи утворенню пухирців повітря, під’єднати зонд і заповнити його препаратом.
4. Забезпечити положення дитини під час уведення сурфактанту на спині з фіксацією голови по середній лінії.
5. Від’єднати інтубаційну трубку від апарата ШВЛ, увести в неї заздалегідь укорочений і наповнений сурфактантом зонд на повну глибину.
6. Увести половину дози препарату з максимально можливою швидкістю (не довше ніж за 30 секунд), увести слідом 1–2 мл повітря, щоб звільнити зонд від сурфактанту.
7. Витягнути зонд, одночасно повертаючи голову новонародженого на один бік на 30 секунд.
8. Відразу відновити апаратну ШВЛ або (якщо дитина не була на ШВЛ) ручну вентиляцію з попередніми параметрами протягом 30–60 секунд.
9. Через 30 секунд покласти дитину в положення на спині з фіксацією голови по середній лінії.
10. Після стабілізації стану новонародженого від’єднати інтубаційну трубку від апарата ШВЛ, повторно увести знов наповнений зонд в інтубаційну трубку, увести другу половину препарату сурфактанту і витягнути зонд.
11. Під’єднати інтубаційну трубку до апарата ШВЛ, відновити вентиляцію в попередньому режимі, одночасно повертаючи голову на протилежний бік на 30 секунд.
12. Забезпечити вихідне положення дитини, продовжуючи ШВЛ.
13. Провести аускультацію дихальних шумів.
14. Адаптувати параметри ШВЛ з урахуванням газів крові, SрО2, графічного моніторингу, екскурсії грудної клітки, даних аускультації. У першу чергу слід знижувати концентрацію кисню в дихальній суміші, потім — час вдиху та тиск на вдиху.
15. У процесі введення препарату контролювати загальний стан дитини, ЧСС, АТ, SрО2.
16. Провести контрольну рентгенографію грудної клітки.
17. Не проводити санацію трахеї протягом мінімум 2 годин.
18. Якщо проводилось профілактичне уведення препарату і в дитини немає тяжких дихальних розладів, ендотрахеальну трубку слід видалити і спостерігати за дитиною. При наявності дихальних розладів слід забезпечити СРАР або іншу дихальну підтримку.
2. Метод введення препарату за допомогою шприца через додатковий боковий отвір в інтубаційній трубці.
Суспензію/емульсію сурфактанту вводять в ендотрахеальну трубку через боковий отвір в інтубаційній трубці, який робить лікар-неонатолог шприцем. Це дозволяє вводити препарат у дихальні шляхи без використання катетерів, не перериваючи апаратної ШВЛ і не знижуючи тиск у дихальних шляхах, особливо в кінці видиху. Препарат вводять, натискаючи на поршень шприца в такт з кожним апаратним вдихом. Важливо, щоб прокол шприцем був близько до конектора, забезпечуючи вільне стікання препарату під дією сили тяжіння. Швидкість уведення препарату визначається толерантністю дитини, але не слід значно подовжувати термін уведення, оскільки чим швидше введений сурфактант, тим вища його ефективність.
При застосуванні методу введення препарату через додатковий боковий прокол інтубаційної трубки:
1. Покласти дитину на спину і ввести 1/2 дози сурфактанту.
2. Через 30–60 секунд після введення сурфактанту продовжити введення другої половини препарату.
3. Впродовж наступних 2 годин санацію ендотрахеальної трубки не проводити.
4. Від’єднати конектор і відрізати ту частину трубки, де був прокол, знову приєднати конектор і продовжити ШВЛ.
Контроль стану новонародженого [1, 3, 12]
Під час введення препарату слід контролювати стан дитини, колір шкіри, екскурсію грудної клітки, а також показники моніторів.
Введення препарату слід призупинити, якщо дитина стає збудженою, з’являються кашлеві поштовхи та відбувається викид сурфактанту в ендотрахеальну трубку, з’являється ціаноз шкіри і слизових оболонок, знижується або різко підвищується ЧСС, SрО2 знижується більше ніж на 15 % від вихідного рівня.
Транзиторне зниження SрО2 можна усунути, тимчасово підвищивши РІР апаратних вдихів на 3–5 см вод.ст.
Відсутність ефекту при використанні сурфактанту [2, 10, 17]:
— невідповідні параметри вентиляції;
— неадекватна інфузійна терапія;
— наявність пневмонії або сепсису;
— нестабільність гемодинаміки;
— легенева гіпертензія з право-лівим шунтуванням крові через фетальні комунікації;
— синдроми витоку повітря;
— тяжкі метаболічні розлади.
У такій ситуації, насамперед, поки перевіряється наявність або відсутність супутніх захворювань, треба збільшити FіО2 до 90–100 %, збільшити РІР і РЕЕР до появи помітних рухів грудної клітки.
Важливо адекватно синхронізувати дитину з ШВЛ. Якщо не вдається досягти цього шляхом використання седативних засобів і наркотичних анальгетиків, використовують міорелаксанти.
Ускладнення:
— обтурація інтубаційної трубки;
— легенева кровотеча (до засобів профілактики кровотечі належить підтримка тиску в кінці видиху не менше +4–5 см вод.ст. та +3 см водн.ст. у дітей з масою менше 1000 г);
— синдром витоку повітря;
— гіпероксія;
— гіпокапнія.
Профілактика цих ускладнень передбачає своєчасну зміну параметрів ШВЛ після ведення сурфактанту.
Практичні рекомендації щодо введення сурфактанту:
— ефективність дії препарату підвищується, якщо його вводити новонародженим після надання первинної реанімації і стабілізації стану дитини під контролем температури тіла, сатурації й артеріального тиску в умовах відділення інтенсивної терапії, що дозволить виключити як перинатальні ускладнення, так і технічні складності у введенні препарату;
— в умовах пологових зал, де відсутня можливість динамічного термоконтролю, введення ендотрахеального сурфактанту становить ризик для недоношеної дитини, особливо з екстремально низькою масою тіла при народженні;
— у недоношених новонароджених, які потребують реанімації, найчастіше неможливо виключити гіпотензію, на фоні якої введення препарату небажане;
— недоношені новонароджені, які потребують негайного введення сурфактанту, народжуються в стані тяжкої асфіксії, що вимагає в першу чергу проведення АВС-реанімації і тільки після стабілізації їх стану можливо ендотрахеальне введення сурфактанту;
— сурфактант за інструкцією рекомендовано вводити до першого механічного вдиху — неможливо проконтролювати правильність перебування ендотрахеальної трубки над біфуркацією трахеї, не виключений ризик введення лікарського препарату в шлунок;
— не аспірується вміст шлунка у новонародженого до введення сурфактанту, існує високий ризик аспірації легень;
— згідно з Наказом № 484 оптимальним терміном для введення сурфактанту з профілактичною метою є перші 15 хв життя дитини, а з лікувальної — відразу ж після встановлення діагнозу, що підтверджує доцільність введення препарату в умовах відділення інтенсивної терапії новонароджених.
1. Аряев Н.Л. Реалии и перспективы выхаживания детей с экстремально малой массой тела при рождении в мире и в Украине / Н.Л. Аряев, Н.В. Котова // Неонатологія, хірургія та перинатальна медицина. — 2011. — Т. 1, № 1. — С. 101-107.
2. Багатоцентрове дослідження порівняльної клінічної ефективності препаратів екзогенного сурфактанту «Неосурф» і «Куросурф» у лікуванні респіраторного дистрес-синдрому у недоношених новонароджених / Д.О. Добрянський, О.В. Новікова, З.В. Салабай [та ін.] // Современная педиатрия. — 2010. — № 2. — С. 164-169.
3. Базовая помощь новорожденному — международный опыт / [Под ред. Н.Н. Володина, Г.Т. Сухих]. — М.: ГЭОТАР-Медиа, 2008. — 208 с.
4. Гіпоксія плода та асфіксія новонародженого / [Т.К. Знаменська, В.І. Похилько, В.В. Подольський та ін.]. — Київ, 2011. — 451 с.
5. Добрянський Д.О. Початкова допомога глибоконедоношеним дітям після народження — сучасні пріоритети / Д. О. Добрянський // Неонатологія, хірургія та перинатальна медицина. — 2011. — Т. 1, № 1. — С. 108-112.
6. Моісеєнко Р.О. Аналіз захворюваності дітей першого року життя в Україні / Р.О. Моісеєнко // Перинатология и педиатрия. — 2010. — № 1 (41). — С. 6-9.
7. Наказ № 584 від 29.08.06 р. МОЗ України «Про затвердження протоколу медичного догляду за новонародженою дитиною з малою масою тіла при народженні». — К., 2006. — 41 с.
8. Наказ № 179 від 29.03.2006 р. МОЗ України «Про затвердження Інструкції з визначення критеріїв перинатального періоду, живонародженості, порядку реєстрації живонароджених і мертвонароджених». — К., 2006. — 26 с.
9. Наказ № 312 від 08.06.07 р. МОЗ України «Про затвердження клінічного протоколу з Первинної реанімації та після реанімаційної допомоги новонародженим». — К., 2007. — 53 с.
10. Наказ № 484 від 21.08.08 р. МОЗ України «Про затвердження клінічного протоколу надання допомоги новонародженій дитині з дихальними розладами». — К., 2008. — 57 с.
11. Підручник з реанімації новонароджених / [Американська Кардіологічна Асоціація, Американська Академія Педіатрії; під ред. Дж. Катвінкела]. — Львів: Галицька видавнича спілка, 2007. — 264 с.
12. Посібник з неонатології / Джон П. Клоерті, Ерік К. Ейхенвальд, Енн Р. Старк; пер. з англ. — [Шосте видання]. — К.: Фонд допомоги і розвитку дітям Чорнобиля; Вид-во «Фенікс», 2010. — 856 с.
13. Тимошенко В.Н. Недоношенные новорожденные дети/ В.Н. Тимошенко. — Ростов-н/Д: Феникс, 2007. — 184 с.
14. Шунько Є.Є. Впровадження концепції подальшого розвитку перинатальної допомоги в Україні / Є.Є. Шунько // Неонатологія, хірургія та перинатальна медицина. — 2011. — Т. 1, № 1. — С. 10-16.
15. Berger R. Perinatal brain injury/ R. Berger, Y. Garnier // J. Perinatal. Med. — 2000. — Vol. 28, № 4. — P. 261-285.
16. Ichani R. Respiratory distress in the newborn / R. Ichani // Child. Health. — 2004. — Vol. 33, № 2. — P. 82-84.
17. Interfacial properties of pulmonary surfactant layers / R. Wustneck, J. Perez-Gil, N. Wustneck [et al.] // Adv. Colloid Interface Sci. — 2005. — Vol. 117, № 1. — P. 33-58.
18. Lung protective strategies for premature infants / G. Moriette, L. Mayry, P. le Hudoux [et al.] // Arch. Pediatr. — 2005. — Vol. 12, № 5. — P. 573-578.
19. Mode of delivery and risk of respiratory diseases in newborns / E. Levine, V. Ghai, J. Barton [et al.] // Obstet. Gynecol. — 2001. — Vol. 97, № 3. — P. 439.
20. Pulmonary microvascular fracture in patient with acute respiratory distress syndrome / J.R. Hotchkiss, D.A. Simonson, D.J. Marek [et al.] // Crit. Care Med. — 2002. — Vol. 30, № 10. — P. 2368-2370.
21. Патент 19748 Україна, МПК А61М5/142.Спосіб ендотрахеального введення лікарських речовин/ Левченко Л.А., Мухіна Н.І., Подоляка В.Л. та ін.; заявник і патентовласник Донецький національний медичний університет. — № u200608629; заявл. 31.07.2006; опубл. 15.12.2006, Бюл. № 12.

/151/151.jpg)
/153/153.jpg)
/154/154_2.jpg)
/155/155.jpg)