Журнал «Медицина неотложных состояний» 7 (62) 2014
Вернуться к номеру
Особливості післяопераційного знеболювання та інтенсивної терапії у новонароджених з вадами розвитку шлунково-кишкового тракту
Авторы: Курочкін М.Ю., Чемерис Ю.О., Давидова А.Г. - Запорізький державний медичний університет
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Метою роботи було вивчення особливостей центральної гемодинаміки, транспорту кисню і деяких маркерів стресу у новонароджених із хірургічною патологією в післяопераційному періоді при комбінованому знеболюванні з використанням центральних нейроаксіальних блокад. Виявлено, що центральні нейроаксіальні анестезії у новонароджених хірургічного профілю, які застосовують шляхом одноразових введень бупівакаїну або наропіну до епідурального простору через каудальний доступ в інтра- і післяопераційному періодах, порівняно з традиційними методами знеболювання мають кращий аналгетичний ефект і перешкоджають розвитку післяопераційного стресу, сприяють стабільній гемодинаміці, збалансованому кисневому режиму, а також дозволяють значно зменшувати дози наркотичних анальгетиків, скорочувати строки перебування дітей на штучній вентиляції легенів та відновлювати моторно-евакуаторну функцію кишечника до 24 годин післяопераційного періоду.
Целью работы было изучение особенностей центральной гемодинамики, транспорта кислорода и некоторых маркеров стресса у новорожденных с хирургической патологией в послеоперационном периоде при комбинированном обезболивании с использованием центральных нейроаксиальных блокад. Выявлено, что центральные нейроаксиальные анестезии у новорожденных хирургического профиля, применяемые путем одноразового введения бупивакаина или наропина в эпидуральное пространство через каудальный доступ в интра- и послеоперационном периодах, имеют лучший анальгетический эффект по сравнению с традиционными методами обезболивания и препятствуют развитию послеоперационного стресса, способствуют стабильной гемодинамике, сбалансированному кислородному режиму, а также позволяют значительно уменьшать дозы наркотических анальгетиков, сокращать сроки пребывания детей на искусственной вентиляции легких и восстанавливать моторно-эвакуаторную функцию кишечника до 24 часов послеоперационного периода.
The objective of the work was to study the characteristics of central hemodynamics, oxygen transport, and some stress markers in neonates with surgical pathology in postoperative period in the combined anesthesia using central neuroaxial blockades. It was found that central neuraxial anesthesia in surgical neonates used by a single administration of bupivacaine or naropina into the epidural space through the caudal access in intra- and postoperative periods, have a better analgesic effect compared to traditional methods of pain relief and prevent the development of postoperative stress, contribute to stable hemodynamics, balanced oxygen regime, as well as also can significantly reduce the doses of narcotic analgesics, the time of mechanical ventilation in children and restore motor-evacuation function of the intestine up to 24 hours of the postoperative period.
новонароджені, гемодинаміка, транспорт кисню, післяопераційна аналгезія.
новорожденные, гемодинамика, транспорт кислорода, послеоперационная аналгезия.
neonates, hemodynamic, oxygen transport, postoperative anesthesia.
Статья опубликована на с. 114-117
Актуальність
У структурі вроджених вад розвитку частка патології шлунково-кишкового тракту становить від 21,7 до 25 % [3]. У 33 % випадків ці пороки розвитку проявляються вродженою кишковою непрохідністю [2]. Показник летальності в цій групі вад залишається високим, незважаючи на вдосконалення хірургічних методів лікування і реанімаційно-анестезіологічної допомоги [1]. Операція дозволяє провести радикальну корекцію вади розвитку в новонародженого, але не усуває відразу комплекс патофізіологічних змін, що пов’язані з основною патологією, і може призводити до порушень гомеостазу в післяопераційному періоді [5]. Головним завданням усіх анестезіологів, які працюють із новонародженими, немовлятами та дітьми старшого віку, є усунення болю незалежно від причини його виникнення. Для якісного знеболювання в новонароджених хірургічного профілю, переважно за кордоном, широко використовують каудально-епідуральну анестезію в комбінації з поверхневою загальною анестезією [7, 8]. Тому оптимізація інтра- та післяопераційного знеболювання й інтенсивної терапії може поліпшувати результати лікування в цієї категорії хворих. Загальноприйнятими критеріями оцінки ступеня тяжкості порушень гомеостазу у хворих високого ступеня ризику є показники гемодинаміки, транспорту кисню [4].
Мета роботи: вивчення особливостей центральної гемодинаміки, транспорту кисню і деяких маркерів стресу в новонароджених із хірургічною патологією в післяопераційному періоді при комбінованому знеболюванні з використанням центральних нейроаксіальних блокад.
Об’єкт та методи дослідження
Центральну гемодинаміку досліджували УЗ-допплером Aloka; кислотно-лужний стан — мікроелектродним методом за допомогою апарата Easy blood gas; показники кисневого статусу (індекс тканинної доставки кисню, індекс тканинного споживання кисню, показник кисневого режиму, ПКР) розраховували на основі даних серцевого індексу (СІ) і збагачення гемоглобіну киснем в артеріальній і венозній крові [4]; показник кисневого режиму — співвідношення індексу тканинної доставки кисню до тканинного споживання вважали напруженим, якщо він становив 2–3 ум.од., збалансованим — 3–3,5 ум.од., надлишковим — понад 3,5 ум.од. [6]; пульсоксиметрію і моніторинг артеріального тиску проводили на апараті «Ютасоксі-200». Центральний венозний тиск (ЦВТ) вимірювали апаратом Вальдмана. Дослідження гемодинаміки, транспорту кисню, рівня глюкози та кортизолу проведено у 38 новонароджених дітей із хірургічною патологією (атрезії стравоходу, діафрагмальні грижі, висока і низька кишкова непрохідність та ін.). До 1-ї групи увійшли 20 дітей, яким в інтраопераційному та післяопераційному періоді (протягом 3 діб) були застосовані центральні ней–роаксіальні блокади. Центральні нейроаксіальні блокади в післяопераційному періоді виконувались шляхом одноразового каудально-епідурального введення місцевого анестетика (0,2% бупівакаїну або наропіну) в об’ємі 1 мл/кг 1–2 рази на добу протягом 3 діб. Другу групу становили 18 новонароджених, яким була проведена багатокомпонентна загальна анестезія в інтраопераційному періоді, а післяопераційна аналгезія була забезпечена постійною інфузією фентанілу в дозі 5 мкг/кг/год протягом 2–3 діб. Дітям 1-ї групи післяопераційна аналгезія була також забезпечена інфузією фентанілу в аналогічній дозі, але після 1-ї доби доза значно зменшувалась — до 1–3 мкг/кг/год, надалі діти знеболювались за допомогою парацетамолу у вікових дозах (ректальні супозиторії або парентеральне введення). Передопераційна підготовка в більшості випадків тривала 1–2 доби до стабілізації і компенсації життєво важливих функцій. Хворим призначались антибіотики широкого спектра дії (напівсинтетичні пеніциліни з сульбактамами й аміноглікозиди) або глікопептиди (ванкоміцин з аміноглікозидами) у вікових дозах. Зміна антибіотиків проводилась за результатами бактеріо–логічного скринінгу й динаміки клініко-лабораторних показників. Діти знаходились у кувезах із постійною вологістю (60–70 %) і температурою повітря (31–32 °С); всі діти в післяопераційному періоді тривалий час перебували на штучній вентиляції легень (ШВЛ); фізіологічну потребу в калоріях немовлятам забезпечували призначенням часткового або повного парентерального харчування: глюкоза з розрахунку 13–15 г/кг/добу, амінокислоти (аміновен) із розрахунку 1–2 г/кг/добу; жирові емульсії (інтраліпід 15–20%) з розрахунку 0,5–3 г/кг/добу.
Ударний індекс (УІ), серцевий індекс, центральний венозний тиск і показники транспорту кисню, рівень кортизолу та глюкози в крові визначали в 4 етапи: при доставці хворого до відділення АІТ, відразу після операції, через 24 години після операції, через 3 доби після операції. Статистична обробка результатів проводилася за допомогою пакета прикладних програм (Statistica for Windows) із використанням критерію Стьюдента. Різницю вважали вірогідною при р < 0,05.
Результати дослідження
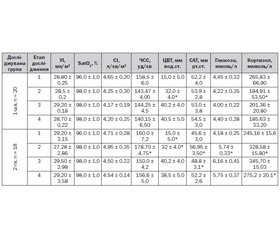
Згідно з даними, наведеними в табл. 1 і 2, гемодинамічні показники на першому етапі у немовлят 1-ї та 2-ї груп характеризувались як помірна гіпердинамія кровообігу: серцевий індекс 4,65–4,7 л/хв/м2, частота серцевих скорочень (ЧСС) 160 уд/хв, ударний індекс відповідав середньовіковим показникам. Слід відзначити субкомпенсований метаболічний ацидоз — рН 7,26–7,28, дефіцит основ становив 7–8 ммоль/л, сатурація венозної крові була нижчою за середньовікові показники приблизно на 27 %; індекс тканинного споживання кисню (ІСО2) був високим в обох групах і становив 381,89 і 451 мл/хв/м2 відповідно; підвищене тканинне споживання кисню було забезпечене досить високою доставкою кисню (ІДО2) за рахунок підвищеного СІ — 1100 і 1109 мл/хв/м2 відповідно; режим співвідношення доставки та споживання кисню — ПКР відповідав напруженому (2,87 та 2,45 ум.од. відповідно). Середній артеріальний тиск (САТ) становив 51,2 та 45,6 мм рт.ст. відповідно, а ЦВТ був незначно зниженим і становив 15 мм вод.ст., щогодинний діурез — близько 0,7 мл/кг/год; рівень кортизолу в крові становив у середньому 250 мкмоль/л, а рівень глюкози був 4,5 ммоль/л.
На 2-му етапі дослідження у хворих 1-ї групи порівняно з попереднім етапом не спостерігалось вірогідних змін СІ, УІ, ЧСС, САТ, невірогідно знизився СІ і ЧСС — на 9 %, вірогідно більше ніж у 2 рази підвищився ЦВТ — до 35 мм вод.ст., щогодинний діурез становив 1,7 мл/кг/год, що підтверджувало адекватність волемічної загрузки перед оперативним втручанням і під час нього; у хворих 2-ї групи зберігалась помірна гіпердинамія кровообігу за рахунок підвищення ЧСС на 12 %, САТ підвищився на 15,7 %. Показники кисневого транспорту на цьому етапі дослідження були такими: спостерігалась повна компенсація кислотно-лужного стану у хворих обох груп. При сатурації артеріальної крові 98–99 % венозна сатурація на цьому етапі вірогідно підвищувалась у 1-й групі на 18 % і в 2-й групі на 14 %; ІДО2 невірогідно знижувався на 11 % у хворих 1-ї групи, проте цей показник у хворих 2-ї групи вірогідно не змінювався; ІСО2 у хворих 1-ї і 2-ї груп на цьому етапі вірогідно знижувався — на 23 і 39 % відповідно, а ПКР відповідав збалансованому кисневому режиму — 3,29 ум.од. тільки у хворих 1-ї групи. У дітей 2-ї групи ПКР становив 3,88 ум.од. і відповідав надлишковому кисневому режиму в основному за рахунок збереження помірної гіпердинамії кровообігу. Стосовно маркерів стресу у хворих 1-ї групи на цьому етапі спостерігалось вірогідне зниження рівня кортизолу на 22 %, а рівень глюкози вірогідно не змінювався, що свідчило про якісну аналгезію на інтраопераційному етапі. У той же час у хворих 2-ї групи вірогідно зростав рівень кортизолу і глюкози порівняно з попереднім етапом на 34 і 37 % відповідно.
Третій етап характеризувався стабільністю гемодинамічних показників і транспорту кисню, збалансованого кисневого режиму у хворих 1-ї групи, гемодинамічні показники і маркери стресу вірогідно не змінювались порівняно з попереднім етапом. Характерним є відновлення стійкої перистальтики кишечника, відсутність стоків по шлунковому зонду. У дітей 2-ї групи вірогідно знизились показники САТ і ЧСС — на 15 %, ПКР був надлишковим — 3,65 ум.од., але близьким до збалансованого, маркери стресу вірогідно не змінювались. На 4-му етапі спостерігалась повна нормалізація гемодинаміки і кисневого режиму, вірогідне зниження маркерів стресу у хворих 2-ї групи і збалансований ПКР у дітей обох груп.
Висновки
1. Адекватна комплексна інтенсивна терапія, що включає ефективне волемічне навантаження і знеболювання в передопераційному і інтраопераційному періодах, сприяє повній нормалізації кислотно-лужного стану в ранньому післяопераційному періоді у новонароджених хірургічного профілю.
2. Центральні нейроаксіальні анестезії в новонароджених хірургічного профілю, що застосовують шляхом одноразових введень бупівакаїну або наропіну до епідурального простору через каудальний доступ в інтра- і післяопераційному періодах, сприяють стабільній гемодинаміці, збалансованому кисневому режиму й характеризуються мінімальними її коливаннями, дозволяють значно зменшувати дози наркотичних анальгетиків, скорочувати строки перебування дітей на ШВЛ та відновлювати моторно-евакуаторну функцію кишечника до 24 годин післяопераційного періоду.
3. Центральні нейроаксіальні блокади порівняно з традиційними методами знеболювання з використанням наркотичних анальгетиків у новонароджених хірургічного профілю мають кращий аналгетичний ефект і перешкоджають розвитку післяопераційного стресу, що підтверджується відсутністю зростання рівня кортизолу і глюкози в крові на всіх етапах дослідження.
1. Жученко Л.А. Профилактика врожденных пороков развития / Л.А. Жученко // Российский вестник акушера-гинеколога. — 2003. — № 1. — С. 64-69.
2. Кулаков В.И. Репродуктивное здоровье населения России / В.И. Кулаков // Гинекология. — 2007. — Т. 9, № 1. — С. 7-9.
3. Кулаков В.И. Хирургическая коррекция врожденных пороков развития плода и новорожденного / В.И. Кулаков // Журнал акушерства и женских болезней. — 2005. — Спецвыпуск. — С. 13-16.
4. Рябов Г.А. Гипоксия критических состояний / Г.А. Рябов. — М.: Медицина, 1988. — 288 с.
5. Степаненко С.М. Пути снижения летальности у новорожденных с пороками развития / С.М. Степаненко, В.А. Михельсон, И.Д. Беляева [та ін.] // Анест. и реан. — 2002. — № 1. — С. 58-61.
6. Шифрин Г.А. Методика системно-количественной оценки гомеостаза // Материалы конференции «Медицинская гомеостатика в анестезиологии и реаниматологии». — Запорожье, 1989. — С. 133-138.
7. Aprodu G.S. Caudal anesthesia in pediatric surgery / G.S. Aprodu, V. Munteanu, G. Filciu [et al.] // Rev. Med. Chir. Soc. Med. Nat. Iasi. — 2008. — Vol. 112. — P. 142-147.
8. Berde C.B. Anesthesia and analgesia during and after surgery in neonates / C.B. Berde, T. Jaksic, A.M. Lynn [et al.] // Clin. Therapeutics. — 2005. — Vol. 27, № 6. — P. 900-921.

/116/116.jpg)