Журнал «Почки» 3 (09) 2014
Вернуться к номеру
Гепаторенальний синдром
Авторы: Таран О.І. — Кафедра нефрології та нирково-замісної терапії НМАПО імені П.Л. Шупика
Рубрики: Нефрология
Разделы: Медицинское образование
Версия для печати
Статья опубликована на с. 64-68
Визначення поняття. Гепаторенальний синдром (ГРС) — гостре прогресуюче зниження ниркового кровотоку та швидкості клубочкової фільтрації (ШКФ) функціонального характеру, є формою ниркової недостатності, що розвивається на тлі гострої або хронічної (декомпенсованої) хвороби печінки за відсутності хвороби нирок.
Близько 120 років відомо про поєднання хвороб нирок та печінки. У 1932 році K. Helwig і C. Sсhutz ниркову недостатність, що розвинулась після операції на жовчних шляхах, описали як синдром «печінка — нирки».
Епідеміологія. ГРС однаково часто виникає в чоловіків і жінок віком 40–80 років. За епідеміологічними даними США частота ГРС становить 10 % серед усіх госпіталізованих хворих із цирозом печінки та асцитом. У цих пацієнтів щорічний ризик розвитку ГРС становить 8–20 %. Цей показник зростає до 40 % через 5 років. У пацієнтів із цирозом печінки та розвитком портальної гіпертензії ГРС може виникнути на першому році діагностованого ускладнення у 20 %, у 40 % — через 5 років.
Етіологія. ГРС частіше виникає як ускладнення хвороби печінки з вираженими порушеннями її функціонального стану. До таких хвороб у дорослих пацієнтів зараховуються:
— цироз печінки (частіше алкогольний) з асцитом та портальною гіпертензією, особливо на тлі діуретичної терапії та надмірного діурезу, або видалення великої кількості рідини при парацентезах (без введення альбуміну);
— цироз печінки, ускладнений кровотечею з варикозно розширених вен стравоходу або прямої кишки;
— 20–25 % випадків цирозу печінки, ускладненого спонтанним бактеріальним перитонітом;
— фульмінантна печінкова недостатність;
— гострі вірусні гепатити;
— гепатоцелюлярна карцинома;
— метастатичне ураження нирок;
— гемігепатоектомія;
— гостра жирова печінка вагітних.
У дітей у 50 % випадків основною причиною ГРС є гострий вірусний гепатит з печінковою недостатністю. Також ГРС у дитячому віці може розвинутись при атрезії жовчних шляхів, хворобі Вільсона — Коновалова, автоімунному гепатиті, злоякісних новоутвореннях, дитячому автосомно-рецесивному полікістозі нирок, дефіциті оуантитрипсину, прийомі парацетамолу.
Окрім надмірного діурезу та крововтрат, факторами розвитку ГРС можуть стати: тривала діарея (у т.ч. індукована медикаментами); нестримна блювота, зменшення венозного повернення крові при асциті.
Патогенез. ГРС розвивається в декілька етапів, які включають такі патологічні процеси, як вазоконстрикція виносних ниркових артеріол, шунтування крові з кіркової в мозкову речовину, зниження ниркового кровотоку та зниження ШКФ; вазодилатація судин органів черевної порожнини. Факторами, що призводять до змін судинного тонусу, є гемодинамічні порушення, системна вазодилатація та активація механізмів вазоконстрикції.
Розвиток портальної гіпертензії викликає розширення артерій черевної порожнини внаслідок надлишкової локальної продукції оксиду азоту та інших вазодилататорів. Після певного етапу компенсаторної реакції організму на вазодилатацію та викликаного нею зниження загального судинного спротиву у вигляді підвищення серцевого викиду та збільшення частоти серцевих скорочень настає період зниження серцевого викиду, обумовленого неадекватним посиленням активності ренін-ангіотензин-альдостеронової системи (РААС) і симпатичної нервової системи (СНС) та частоти серцевих скорочень. Існують декілька поглядів на ці процеси. Деякі дослідники вважають, що циркуляторна дисфункція обумовлена серцевою недостатністю, що розвивається внаслідок специфічної кардіоміопатії. Є думка, що порушення інотропної функції серця при ГРС має функціональну природу за рахунок зниження венозного повернення до серця, а порушення хронотропої функції — шляхом пригнічення бета-адренорецепторів. Гіпердинамічний тип кровообігу не в змозі довго підтримувати артеріальний тиск (АТ) на нормальному рівні. Його підвищення утримується за рахунок рефлекторної стимуляції РААС та СНС, але надлишкова продукція ангіотензину ІІ, норадреналіну, вазопресину та інших вазоконстрикторів не має адекватної дії на артерії черевної порожнини, що в результаті надлишкової секреції локальних вазодилататорів (глюкагон) стають резистентними до цих вазоконстрикторів.
Вазодилатація судин органів черевної порожнини у пацієнтів із цирозом печінки й портальною гіпертензією обумовлена як підвищенням вмісту вазодилататорів (оксид азоту, простациклін, глюкагон), так і зменшенням проникності калієвих каналів.
Утримання АТ на нормальному або субнормальному рівні досягається за рахунок вазоконстрикції позачеревних судин, таких як артерії нирок, м’язів, шкіри, головного мозку та ін. Значна ренальна вазоконстрикція призводить до зниження ниркової перфузії та ШКФ із наступним порушенням азотовидільної функції нирок. Ще одним механізмом формування ниркової недостатності є порушення балансу в нирковій продукції ендогенних вазоконстрикторів та вазодилататорів. При ГРС значно знижується виділення з сечею хворих таких вазодилататорів, як простагландин Е2, метаболіт простацикліну 6-простагландин F1a, калікреїн. У той же час ішемія нирок призводить до посилення секреції речовин, що посилюють судинні ефекти ангіотензину ІІ (вазопресин, ренін, ендотелін-1, аденозин, лейкотрієни, тромбоксан-2 тощо).
До факторів ризику розвитку ГРС зараховують гіпонатріємію (< 134 ммоль/д) і гіперренінемію (> 3,5 мг/мл/год), індекс резистентності кровотоку у внутрішньочасточкових артеріях понад 0,7 за даними допплерівського дослідження.
Морфологічних змін із боку нирок не виявляють. Функціональний характер ураження нирок підтверджує також відновлення їх функції після трансплантації печінки.
У разі розвитку ГРС спостерігається значне підвищення внутрішньопечінкового опору та посилення портальної гіпертензії. Ці процеси обумовлені гіперсекрецією вазоконстрикторів в умовах зниження печінкової продукції вазодилататорів. Тому при ГРС часто спостерігаються кровотечі з варикозно розширених вен стравоходу.
Класифікація ГРС (1996). Залежно від тяжкості клінічних проявів та прогнозу виділяють два типи ГРС.
І тип — гострий ГРС зі швидкопрогресуючим перебігом. Виникає у людей із гострою печінковою недостатністю та при алкогольному цирозі печінки. Діагностика стану базується на визначенні дворазового підвищення концентрації креатиніну сироватки крові або зниження ШКФ до рівня менше ніж 20 мл/хв. У чверті пацієнтів ГРС І типу виникає при спонтанному бактеріальному перитоніті, у випадках видалення великої кількості рідини при парацентезі без введення альбуміну (15 %), у разі шлунково-кишкової кровотечі (10 %). Прогноз серйозний, летальність протягом 2 тижнів досягає 80 %.
ІІ тип — ниркова недостатність розвивається повільно як наслідок рефрактерного асциту. Зниження функції нирок спостерігається протягом декількох місяців. Прогноз кращий, ніж при ГРС І типу (пацієнти живуть 3–6 місяців), але гірший, ніж у популяції хворих на цироз печінки з асцитом.
Ця класифікація є умовною й не має клінічного значення для вибору тактики консервативного лікування ГРС. Швидкість зростання рівня креатиніну є показником, що визначає прогноз виживання, але вона вкрай непостійна та не дає підстав для диференційованого підходу до терапії. Однак виділення типів ГРС має значення в трансплантології, оскільки дозволяє виділити кандидатів на термінову трансплантацію.
Клініка ГРС. ГРС розвивається у хворих на гостре та хронічне захворювання печінки, тому у хворих виявляються: асцит, жовтяниця, ознаки печінкової недостатності й енцефалопатія; виникають шлунково-кишкові кровотечі. Пацієнтів турбує слабкість, значна втомлюваність, спотворення смаку. Добовий діурез не перевищує 500 мл. При наявності асциту на передній поверхні черевної стінки виявляються пупкові кили, визначаються периферичні набряки. У разі огляду хворого можливе виявлення іктеричності склер, пальмарної еритеми, судинних зірочок, ксантелазм, деформації пальців рук та ніг за типом «барабанних паличок», нігтів — за типом «годинникових скелець». Печінка і селезінка збільшені. У чоловіків може з’явитись гінекомастія.
Діагностичні критерії ГРС. У 2005 році розроблені та опубліковані діагностичні критерії ГРС:
1) цироз печінки з асцитом;
2) рівень сироваткового креатиніну понад 133 ммоль/л (1,5 мг/дл);
3) відсутність збільшення ШКФ (досягнення рівня сироваткового креатиніну ≤ 133 ммоль/л) після як мінімум дводенної відміни сечогінних і введення альбуміну — доза, що рекомендується, — 1 г на 1 кг маси тіла на день (до максимальної дози 100 г/день);
4) відсутність шоку;
5) відсутність даних про використання нефротоксичних препаратів;
6) відсутність будь-яких паренхіматозних хвороб нирок, які проявляються протеїнурією, макрогематурією і/або відповідними УЗ-ознаками.
До сьогодні не існує специфічних діагностичних маркерів ГРС. Діагноз встановлюється при виключенні всіх можливих причин ниркової недостатності (пре-, пост- та ренального гострого ушкодження нирок) або псевдогепаторенального синдрому у пацієнтів із гострою або хронічною хворобою печінки.
У клінічній практиці до лабораторних критеріїв діагностики ГРС зараховують також зниження концентрації натрію в крові < 130 ммоль/л і сечі < 10 ммоль/л, зниження систолічного артеріального тиску; швидке зростання рівня загального білірубіну зі зниженням протромбінового індексу.
ГРС фактично є преренальним гострим ушкодженням нирок. У клінічній практиці для визначення функціональної ниркової недостатності орієнтуються на показники добового діурезу та кліренсу креатиніну. Одним із неінвазивних методів, який дозволяє прогнозувати розвиток ГРС у хворих на цироз печінки, є УЗ-допплерівське дослідження з визначенням показника опору артеріального русла нирок. Значно підвищений показник (індекс спротиву понад 0,9) може бути раннім діагностичним маркером ГРС у хворих на цироз печінки з асцитом і нормальним рівнем креатиніну сироватки крові. За допомогою УЗ-дослідження при ГРС можливе виключення обструкції сечовивідних шляхів і хвороб нирок. Якщо концентрація креатиніну висока, а рівень натрію в плазмі залишається в межах норми, то діагноз ГРС не виставляється.
Диференціальна діагностика. Хвороби печінки і жовчних шляхів за наявності жовтяниці або без неї можуть супроводжуватись вторинними нефропатіями, що ускладнює проведення диференціальної діагностики. При хронічних вірусних гепатитах В і С спостерігаються мембранозний гломерулонефрит (ГН), мезангіокапілярний ГН, IgA-нефропатія з розвитком гломерулосклерозу та хронічної ниркової недостатності. За умови хвороб гепатобіліарної системи може розвинутись дистальний або дистально-проксимальний нирковий канальцевий ацидоз, гострий канальцевий некроз. При обстеженні хворих, окрім характерних для кожної з нозологічних форм хвороби печінки клініко-лабораторних ознак, виявляють також зміни в показниках аналізів сечі та порушення структури нирок при гістологічному дослідженні, що не характерні для ГРС. Але біопсія нирок, як правило, не проводиться.
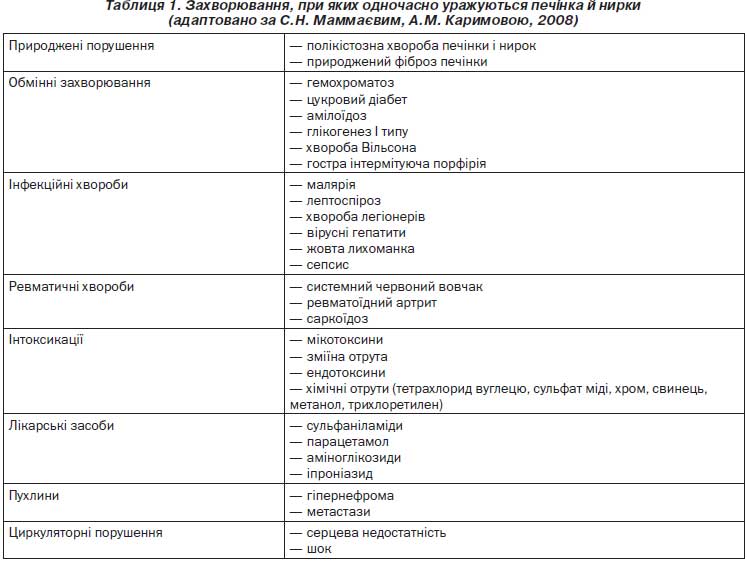
Псевдогепаторенальний синдром — одночасне ураження печінки і нирок при різних захворюваннях (табл. 1).
Лікування. Терапія ГРС становить великі труднощі і часто залишається малоефективною. Метою лікування є корекція гемодинамічних порушень із досягненням системної вазоконстрикції та ниркової вазодилатації.
У харчовому раціоні хворого обмежують кількість солі (до 2 г), зменшують вживання продуктів, що містять натрій та калій. Хворим відміняють нефротоксичні ліки та суттєво обмежують призначення сечогінних засобів. При ознаках печінкової енцефалопатії зменшують споживання білка та дотримуються рекомендацій щодо лікувального харчування при асциті та цирозі печінки.
Актуальним залишається лікування альбуміном. Одним із механізмів недостатнього діурезу й ниркової недостатності в пацієнтів із цирозом печінки є зниження онкотичного тиску крові внаслідок гіпоальбумінемії. Введення розчину альбуміну дозволяє попередити гіповолемію. Вводять його по 20–60 г/добу внутрішньовенно. Застосування альбуміну супроводжується збільшенням виживання хворих. З 2005 року альбумін застосовують тільки в комбінації з аналогами вазопресину (лізин-вазопресин, орніпресин, терліпресин) або в комбінації пероральним застосуванням мідодрину (aльфа-агоніста) з внутрішньовенним або підшкірним введенням октреотиду (синтетичний аналог соматостатину) протягом 1–3 тижнів. Частіше застосовують терліпресин (реместил) в/в по 0,5–2 мг кожні 4 години. Окреотид (сандостатин) призначають в/в по 25–50 мкг/год або п/ш по 250 мкг протягом 3 місяців. Вважається, що лікування найефективніше, особливо при ГРС І типу, там, де застосовується комбінація альбуміну та терліпресину, оскільки альбумін не тільки здатен підвищувати об’єм циркулюючої крові, а й має пряму вазоконстрикторну дію. Що стосується доз терліпресину, то вважається, що якщо пацієнт не відповів на прийом 12 мг/день, то подальше збільшення дози не має сенсу. Комбінована інфузія альбуміну і терліпресину нормалізує ниркову функцію у 34–44 % хворих на ГРС.
Ще одним препаратом вибору при лікуванні пацієнтів із ГРС є допамін (особливо при неможливості застосувати терліпресин) у дозі 2–3 мкг/кг/хв, але він має незначний клінічний ефект, незважаючи на його діуретичний, натрійуретичний ефекти, збільшення ниркового кровотоку та покращення клубочкової фільтрації. Після відміни препарату олігурія, як правило, відновлюється. Вплив допаміну на виживання хворих на ГРС не доведений.
Лікування хворих, які відповіли на терапію, повинно продовжуватись до тих пір, поки не нормалізується рівень креатиніну.
Для хворих з ІІ типом ГРС основною проблемою є рефрактерний асцит. Застосування комбінованої терапії альбуміном та вазоконстрикторами ефективне на час проведення лікування, але, як правило, припинення терапії призводить до зворотного розвитку ГРС. Альтернативою всім видам лікування при ГРС ІІ типу є трансплантація печінки.
Шунтуючі операції. Транс’югулярне внутрішньопечінкове портосистемне стентування (TIPS). Ефективний метод зниження портальної гіпертензії, нормалізації сироваткового альбуміну в пацієнтів із цирозом печінки і тяжкою азотемією. Імплантація TIPS протипоказана при тяжкій печінковій недостатності з енцефалопатією, при вираженому холестазі. Розроблений також метод перинеовенозного шунтування. Після цих операцій виживання пацієнтів становить 2–4 місяці.
Альбумінопосередкована гемофільтрація. Виявлений позитивний вплив на системну гемодинаміку і печінкову енцефалопатію. Як діалізат застосовується 20% альбумін, донорський (метод MARS) або виділений із плазми пацієнта (метод Prometheus). Зниження концентрації креатиніну найвірогідніше обумовлене впливом діалізу. Альтернативою альбуміновому діалізу може бути метод плазмафільтрації. Окрім продуктів азотистого обміну, з організми людини виводяться некон’югований білірубін, аміак та ліпофільні печінкові токсини. Виживання після першого і третього місяця терапії становило 41 і 34 % відповідно.
Гемодіаліз. У пацієнтів із цирозом печінки в стадії декомпенсації проведення гемодіалізу має високий ризик розвитку ускладнень, особливо у вигляді шлунково-кишкових кровотеч, гіпотонії та шоку.
Трансплантація печінки. Ефективний метод лікування ГРС, терапія вибору при цій патології. Гемодинамічні та нейрогуморальні зсуви, які асоціюються з ГРС, зникають протягом першого місяця після операції, у більшості хворих відновлюється екскреція натрію й води. П’ятирічне виживання становить 70 %. Майже у 60 % хворих спостерігається зворотний розвиток ГРС і відновлення функції нирок.
Профілактика. При ГРС профілактичні заходи мають дуже велике значення. Основні напрямки профілактики ГРС:
1. Уникати ятрогенного впливу на водний баланс хворого на цироз печінки з асцитом (неправильне видалення асцитичної рідини, надлишкове обмеження вживання рідини та погано контрольована діуретична терапія).
2. Проводити адекватне лікування печінкової енцефалопатії.
3. Попереджати виникнення інфекційних ускладнень у пацієнтів з цирозом печінки (призначення антибактеріальної терапії хворим, у яких була шлунково-кишкова кровотеча, пацієнтам зі спонтанним бактеріальним перитонітом).
4. Уникати призначення нефротоксичних ліків (нестероїдні протизапальні препарати, аміноглікозиди, діуретики, інгібітори АПФ, дипіридамол).
Таким чином, основною роллю всіх варіантів лікування є збільшення часу до трансплантації печінки. Лікування може також забезпечити зворотний розвиток ниркової недостатності та полегшення окремих симптомів, але повторення не виключається. Аналоги вазопресину, особливо терліпресин, є перспективною фармакологічною терапією, особливо в поєднанні з альбуміном у пацієнтів зі спонтанним бактеріальним перитонітом. Транс’югулярне внутрішньопечінкове портосистемне шунтування може забезпечити певний успіх у лікуванні пацієнтів із ГРС. Октреотид неефективний як монотерапія, але може бути використаний як додаткова терапія з іншими вазоактивними засобами. Агоністи дофаміну, антагоністи ендотеліну, натрійуретичні пептиди та інгібітори синтезу оксиду азоту також можуть бути ефективними для зворотного розвитку ГРС. Роль штучної печінки або трансплантації нирки потребує подальшої оцінки, перш ніж вони можуть бути рекомендовані регулярно.

1. Николаев А.Ю., Милованов Ю.С. Лечение почечной недостаточности. Руководство для врачей. — М.: МИА, 2011. — С. 37-30, 67-70.
2. Маммаев С.Н., Каримова А.М. Гепаторенальный синдром 1-го и 2-го типа: современное состояние проблемы // РЖГГХ. — 2008 — № 6. — С. 5-13.
3. Огурцов П.П., Гармаш И.В., Мазурчук Н.В. и др. Гепаторенальный синдром (перспективы лечения терлипрессином) // Клиническая фармакология и терапия. — 2005. — № 1. — С. 31-32.
4. Поликарпова Т.С., Мазурчук Н.В., Огурцов П.П. и др. Гепаторенальный синдром: критерии диагностики, подходы к терапии // Клиническая фармакология и терапия. — 2009. — № 18(4).
5. Шерлок Ш., Дули Дж. Заболевания печени и желчных путей. — М.: ГЭОТАР-Медиа, 2002.
6. Moreau R., Lebrec D. Acute kidney injury: new concepts. Hepatorenal syndrome: the rjole of vasopressors // Nephron Physiol. — 2008. — № 109(4). — 73-79.
7. Ruiz-del-Arbol L., Monescillo A., Arocena C. et al. Circulatory function and Hepatorenal syndromein cirrhosis // Hepatology. — 2005. — 42. — 439-447.