Журнал «Медицина неотложных состояний» 2 (65) 2015
Вернуться к номеру
Малообъемная ресусцитация препаратом Гекотон при лечении травматического шока
Авторы: Кобеляцкий Ю.Ю., Царев А.В., Машин А.М., Йовенко И.А., Муравская Л.И. — Кафедра анестезиологии и интенсивной терапии ГУ «Днепропетровская медицинская академия МЗ Украины»; КУ «Днепропетровская областная клиническая больница им. И.И. Мечникова»
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Статья посвящена использованию инфузионного препарата Гекотон («Юрия-Фарм», Украина) для малообъемной ресусцитации у пациентов с политравмой и травматическим шоком тяжелой степени.
Стаття присвячена використанню інфузійного препарату Гекотон («Юрія-Фарм», Україна) для малооб’ємної ресусцитації у пацієнтів із політравмою та травматичним шоком тяжкого ступеня.
The article deals with the use of infusion agent Gecoton («Yuria-Pharm», Ukraine) for low-volume resuscitation in patients with polytrauma and severe traumatic shock.
Гекотон, инфузионная терапия, политравма, травматический шок, интенсивная терапия.
Гекотон, інфузійна терапія, політравма, травматичний шок, інтенсивна терапія.
Gecoton, infusion therapy, polytrauma, traumatic shock, intensive therapy.
Статья опубликована на с. 77-81
Основной задачей интенсивной терапии травматического шока является проведение адекватной по составу, объему и скорости инфузионной терапии с целью восполнения дефицита объема циркулирующей крови (ОЦК). Это связано с тем, что эффективность механизмов, поддерживающих адекватную доставку кислорода к тканям в условиях сниженного содержания кислорода в крови, зависит в первую очередь от сохранения нормоволемии и сократительной способности сердца. Гиповолемия уменьшает компенсаторный эффект пониженной вязкости крови на венозный возврат и угнетенную функцию миокарда, препятствуя таким образом увеличению систолического объема, связанного с повышением венозного возврата [1, 2].
В связи с этим представляет интерес методика «малообъемной ресусцитации» (small-volume resuscitation), предназначенная для коррекции острой гиповолемии и включающая использование гиперосмолярных кристаллоидных растворов. Данная концепция подразумевает воздействие на микроциркуляцию и получение немедленного ответа в виде улучшения центральной гемодинамики у пациентов с тяжелым гиповолемическим шоком при объеме инфузионной терапии, равном всего 4 мл/кг.
Еще в 1944 г. впервые было предложено использовать гипертонический раствор натрия хлорида для лечения гиповолемического шока. В последующем I.T. Velasco и соавт. (1980) в эксперименте на собаках при моделировании тяжелого геморрагического шока продемонстрировали, что восполнение кровопотери изотоническими растворами кристаллоидов приводило к 100% летальности животных. Напротив, инфузия 7,5% раствора натрия хлорида в дозе 4 мл/кг обеспечивала эффективное повышение системного давления и восстановление сердечного выброса с 100% выживанием животных. В том же году J. De Felippe и соавт. опубликовали результаты клинического применения 7,5% раствора натрия хлорида в объеме 100–400 мл у 12 пациентов с тяжелым гиповолемическим шоком, рефрактерным к традиционным методам терапии. Авторы отметили повышение артериального давления и появление диуреза, при этом в данной группе 9 пациентов выжили [3]. Эти работы заложили основу вышеназванной концепции малообъемной ресусцитации как одного из методов экстренной начальной терапии гиповолемического шока, которая включает в себя быструю инфузию малого объема (4 мл/кг) 7,2–7,5% раствора натрия хлорида. Эффект связан с быстрой мобилизацией эндогенной жидкости по осмотическому градиенту во внутрисосудистое пространство [3]. Так, введение 100 мл 7,5% раствора натрия хлорида увеличивает внутрисосудистый объем на 270 мл [4]. Рекомендуемая доза 7,5% раствора натрия хлорида составляет 4 мл/кг массы тела, ее желательно ввести в течение 2–5 минут. Максимальный эффект наблюдается сразу после окончания инфузии и заключается в увеличении объема на 8–12 мл/кг. Другими положительными эффектами при введении гипертонического раствора натрия хлорида являются: снижение риска отека легких при уменьшении объема инфузии; увеличение сократимости миокарда за счет непосредственного снижения отека клеток; натрий-уретическое действие, заключающееся в снижении обратной резорбции натрия; коррекция внутричерепной гипертензии [4, 5].
Противопоказаниями к применению гипертонических растворов являются: дегидратация, почечная недостаточность, гиперосмолярность плазмы (более 300 мосм/л), гипернатриемия (более 150 ммоль/л), тяжелая сердечная недостаточность, некомпенсированный сахарный диабет [4]. Необходимо подчеркнуть, что инфузия 7–7,5% раствора натрия хлорида является безопасной. Напротив, инфузия в периферическую вену гипертонического раствора NaCl с концентрацией более 10 % приводила к выраженному гемолизу [3].
Необходимо отметить, что гемодинамический эффект инфузии гипертонического раствора натрия хлорида является кратковременным. Небольшая продолжительность гемодинамического эффекта, обусловленного резким повышением осмолярности плазмы, связана с быстрым уравновешиванием гипертонического раствора между внеклеточным и внутриклеточным секторами. В связи с этим было предложено комбинировать гипертонические кристаллоидные растворы с коллоидными, что обусловливает синергизм действия обоих компонентов (гиперосмолярного и онкотического), обеспечивая усиление гемодинамического эффекта, а также пролонгирование действия данного препарата. Совместное применение коллоидов и гиперосмолярных кристаллоидов эффективно нормализует центральную гемодинамику, восстанавливает микроциркуляцию и экстракцию кислорода без значимого увеличения осмолярности плазмы крови при гиповолемическом шоке, а также снижает внутричерепное давление у больных с отеком мозга травматического и нетравматического генеза. В целом в большинстве публикаций не зарегистрировано развитие тяжелой гипернатриемии после инфузии гипертонических растворов [4].
Необходимо подчеркнуть, что малообъемная ресусцитация предполагает возврат «одолженной» интерстициальной жидкости последующей инфузией изотонических кристаллоидных и/или коллоидных растворов, поскольку технология обеспечивает быстрое возмещение тяжелого дефицита ОЦК с целью стабилизации состояния и спасения жизни пациента с тяжелым травматическим шоком. В связи с этим нельзя повторять введение гипертонического раствора, а необходимо начать регидратацию с использованием стандартных плазмозаменителей.
Оригинальная идея совмещения гиперосмолярного кристаллоида и современного коллоида на основе низкомолекулярного гидроксиэтилкрахмала (ГЭК 130/0,4), преимущество которого было показано в целом ряде работ [6], была разработана корпорацией «Юрия-Фарм». Важной чертой препарата является реализация концепции сбалансированной по электролитному составу инфузионной среды [7]. Таким образом, Гекотон представляет собой многокомпонентный сбалансированный коллоидно-гиперосмолярный раствор. Основными действующими веществами препарата Гекотон являются: 5% ГЭК 130/0,4 (5,0 г), ксилитол (5,0 г), натрия лактат (1,5 г) и электролиты (NaCl — 0,8 г, KCl — 0,03 г, CaCl — 0,02 г, MgCl — 0,01 г).
Целью данного исследования стало изучение эффективности и безопасности применения отечественного сбалансированного коллоидно-гиперосмолярного раствора Гекотон («Юрия-Фарм», Украина) у пострадавших с политравмой в качестве малообъемной ресусцитации при лечении травматического шока тяжелой степени.
Материалы и методы исследования
Нами были обследованы 40 пациентов с диагнозом «политравма», которым оказывалась помощь в условиях реанимационного зала приемно-диагностического отделения и в последующем в отделении реанимации и интенсивной терапии политравмы КУ «Днепропетровская областная клиническая больница им. И.И. Мечникова». Все пациенты имели клиническую картину травматического шока III–IV степени. Возраст пациентов составлял от 25 до 60 лет. В исследование включались пациенты, имевшие систолическое артериальное давление (АДсист.) < 80 мм рт.ст. и эмпирически рассчитанную кровопотерю более 1500 мл. Пациенты были разделены на 2 группы: I — основную (n = 20), в которой в схему коррекции дефицита объема ОЦК с целью стабилизации показателей гемодинамики включали препарат Гекотон в дозе 5–7 мл/кг массы тела; II — контрольную (n = 20), в которой включали инфузию препарата рефортан (ГЭК 200/0,5) в дозе 5–7 мл/кг массы тела. Указанные группы были репрезентативными по основным клиническим и половозрастным характеристикам (табл. 1).
Для оценки эффективности предложенного метода оценивали показатели гемодинамики: систолическое артериальное давление, диастолическое артериальное давление (АДдиаст.), частоту сердечных сокращений (ЧСС).
Исследование проводилось на 4 этапах: исходно, через 15, 25, и 40 минут после окончания инфузии растворов Гекотон и рефортан. При этом важно подчеркнуть, что вазопрессорная поддержка в обеих группах подключалась только через 40 минут с момента инфузии препаратов, таким образом, не влияя на оценку параметров гемодинамики. Пациенты, которым требовалось более раннее подключение вазопрессорной поддержки, были исключены из исследования.
Также на этапах 24 и 48 часов после инфузии препарата оценивался суточный диурез, осмолярность плазмы крови, наличие побочных эффектов и использование вазопрессорной поддержки.
Все пациенты обеих групп исследования получали традиционный комплекс интенсивной терапии, cогласно принятому в клинике анестезиологии и интенсивной терапии КУ «ДОКБ им. И.И. Мечникова» локальному «Клиническому протоколу диагностических мероприятий и интенсивной терапии при политравме». Он включает в себя: обследование пациента по алгоритму ABCDE, проведение спиральной компьютерной томографии в качестве «золотого стандарта» обследования при политравме, УЗИ и рентгенографию, эмпирический расчет степени кровопотери, обеспечение венозного доступа путем пункции-катетеризации 2–3 периферических вен с использованием катетеров большого диаметра — не менее 1,4 мм (14–16–18 G). В случае невозможности периферического доступа и при наличии показаний — обеспечение центрального венозного доступа. Поддержание целевого систолического АД в диапазоне 80–110 мм рт.ст., среднего артериального давления (САД) — 60–80 мм рт.ст. — до надежной остановки кровотечения. При этом необходимо обратить внимание на недопустимость снижения САД < 40 мм рт.ст., что обусловливает развитие тяжелой гипоперфузии, приводящей к синдрому полиорганной недостаточности (СПОН) и необратимым фатальным последствиям. При высоком риске или продолжающемся кровотечении используется стратегия «допустимой гипотонии» — кратковременная гипотония (АД систолическое 80–90 мм рт.ст.) до обеспечения хирургического гемостаза.
Согласно локальному протоколу, не рекомендуется использование однократного измерения гематокрита (Ht) в качестве изолированного маркера кровотечения. Требуется измерение Ht в динамике и сопоставление его уровня с клинической картиной. Необходимо учитывать тот факт, что уровень гемоглобина в первые 1,0–1,5 часа с момента получения травмы не является информативным из-за централизации кровообращения и может находиться в пределах нормы либо нижней границы нормы.
Пациентам с травматическим шоком, который не корригируется введением 2 л кристаллоидов, рекомендуется ранняя эмпирическая гемотрансфузия, которая должна основываться не только на учете уровня гемоглобина (Hb), но и на физиологических параметрах каждого конкретного пациента, скорости и предполагаемом объеме продолжающегося кровотечения. При этом ее следует начинать при Hb < 100 г/л на фоне продолжающегося кровотечения. При отсутствии продолжающегося кровотечения гемотрансфузия должна быть начата при снижении уровня Hb < 70 г/л, а в случае сопутствующей тяжелой кардиальной патологии — при уровне Hb < 80 г/л. Целевое значение гематокрита — 0,30 л/л.
Нами использовалась стратегия максимально раннего применения свежезамороженной плазмы (СЗП) у пациентов с массивным кровотечением или выраженной коагулопатией (протромбиновое время или АЧТВ больше чем в 1,5 раза выше нормы). Начальная доза СЗП — 15 мл/кг, дополнительные дозы будут зависеть от мониторинга свертывания крови и количества других препаратов крови.
При массивной кровопотере соотношение СЗП и эритроцитной массы — 1 : 1.
Введение транексамовой кислоты в дозе 1 г внутривенно болюсно, затем 1 г в виде непрерывной внутривенной инфузии (перфузором) в течение > 8 часов.
Криопреципитат вводился в случае продолжающегося кровотечения, которое сопровождалось дефицитом уровня фибриногена менее 1,5–2,0 г/л. Концентрат протромбинового комплекса рекомендуется для экстренного прекращения действия витамин-К-зависимых пероральных антикоагулянтов либо в качестве альтернативы криопреципитату.
«Золотым стандартом» обезболивания при политравме является использование фентанила в виде как болюсного, так и непрерывного введения при помощи перфузора.
Основными критериями выведения больного из травматического шока является появление диуреза (целевое значение диуреза > 0,5 мл/кг/час), а также нормализация показателей кислотно-щелочного состояния (по уровню рН и дефицита оснований).
Статистическую обработку результатов исследования проводили с использованием методов биометрического анализа, реализованных в пакетах программ Excel-2003, Statistica 8.0.
Результаты исследования и их обсуждение
Как видно из табл. 1 и 2, в основной группе исследования (с применением препарата Гекотон) исходно преобладала более тяжелая категория пациентов с политравмой, с большей тяжестью повреждений и более высокой степенью кровопотери, что характеризовалось более выраженной степенью гипотензии. Артериальное давление в первой группе определялось на уровне 40/0 — 60/20 мм рт.ст., частота сердечных сокращений равнялась 130–140 уд. в 1 мин, что указывало на необходимость проведения экстренных противошоковых мероприятий, поскольку столь критически низкие показатели гемодинамики могли не позволить обеспечить стабилизацию состояния из-за высокой вероятности недостижения достаточной скорости инфузионной терапии для восполнения дефицита ОЦК и, как следствие, могли вызвать остановку кровообращения на фоне острой гиповолемии тяжелой степени.
Пациенты обеих групп из-за неадекватности внешнего дыхания исходно были интубированы и переведены на искусственную вентиляцию легких. В связи с нестабильностью гемодинамики всем пациентам первой группы и 17 пациентам второй группы проводилась вазопрессорная поддержка (табл. 1). В ряде случаев это было обусловлено не только тяжелой гиповолемией, но также тяжестью черепно-мозговой травмы и необходимостью поддержания оптимального церебрального перфузионного давления.
Анализ показателей гемодинамики в группе пациентов с применением препарата Гекотон продемонстрировал, что уже на 15-й минуте с момента инфузии препарата была отмечена тенденция к уменьшению частоты сердечных сокращений и повышению систолического и диастолического давления. На 40-й минуте исследования в первой группе достоверно снижалась частота сердечных сокращений. Аналогичная динамика была отмечена при исследовании показателей системного давления. Так, систолическое АД (p < 0,05) и диастолическое АД (p < 0,05) достоверно были выше на 40-й минуте исследования в сравнении с исходным значением, что свидетельствовало о высокой эффективности данного препарата в лечении острой кровопотери и обеспечении быстрой волемической ресусцитации (табл. 2).
По сравнению с основной во второй группе пациентов, несмотря на исходно более высокие показатели артериального давления (что было связано с меньшим объемом кровопотери), была отмечена только тенденция к повышению показателей системной гемодинамики и к уменьшению частоты сердечных сокращений.
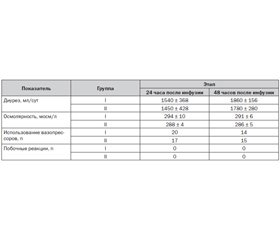
Уровень осмолярности плазмы крови достоверно не различался в обеих группах на этапах 24 и 48 часов исследования (табл. 3). Таким образом, гиперосмолярный препарат Гекотон не вызывал у пациентов существенных сдвигов осмолярности крови.
Диурез в группе с использованием препарата Гекотон оставался в пределах нормы на этапе 24 часов с момента его инфузии и имел тенденцию к увеличению через 48 часов (табл. 3), что в отсутствие в нашем исследовании случаев развития острого повреждения почек свидетельствовало о безопасности данной инфузионной среды.
Побочных эффектов после инфузии исследованных препаратов не было отмечено ни у одного из пациентов. Больные хорошо переносили введение препарата Гекотон, также нами было выявлено улучшение клинического течения травматической болезни.
Другой перспективной областью применения препарата Гекотон является коррекция внутричерепной гипертензии (ВЧГ) у пациентов с тяжелой черепно-мозговой травмой. Так, нами был использован Гекотон у пациента Р. (участник АТО) с диагнозом: огнестрельное проникающее пулевое ранение головы; огнестрельное ранение левого легкого, гемоторакс слева (состояние после резекции доли левого легкого, дренирования плевральной полости); многооскольчатый огнестрельный перелом костей правой голени; огнестрельное пулевое ранение позвоночника на уровне Th5 с повреждением спинного мозга (состояние после операции ламинэктомии, удаления гематомы и мозгового детрита). На 5-е сутки после получения ранения у пациента было отмечено развитие отрицательной неврологической симптоматики с углублением неврологического статуса до комы 1-й степени. По данным проведенной спиральной компьютерной томографии головного мозга, у пациента присутствовали признаки отека головного мозга со смещением срединных структур на 8 мм.
С целью коррекции ВЧГ однократно проведена инфузия препарата Гекотон в объеме 400 мл, через 30 минут отмечена положительная неврологическая симптоматика в виде улучшения неврологического статуса до уровня глубокого оглушения. В дальнейшем пациент был переведен из ОРИТ в ясном сознании в профильное отделение.
В заключение необходимо отметить, что эффективная коррекция волемического статуса при гиповолемии позволяет предотвратить неадекватную тканевую перфузию и снижение доставки кислорода к тканям. В тяжелых случаях гиповолемия приводит к развитию шока, а следовательно, к повреждению клеток, полиорганной недостаточности, смерти. Основная цель инфузионной терапии — обеспечение адекватной циркуляции с достаточным артериальным давлением и сердечным выбросом и тем самым тканевой перфузии и оксигенации. Волемическая терапия должна не только корригировать показатели системной гемодинамики, но и улучшать микроциркуляцию, перфузию и оксигенацию тканей. Таким образом, в экстренных ситуациях, когда необходимо использование небольшого объема инфузии с целью восполнения дефицита ОЦК и восстановления кровотока на уровне микроциркуляции, инфузионный препарат Гекотон позволяет эффективно и безопасно обеспечивать малообъемную ресусцитацию тяжелой гиповолемии у пациентов в состоянии травматического шока.
Выводы
1. Препарат Гекотон («Юрия-Фарм») является безопасным и эффективным плазмозаменителем комплексного действия для проведения малообъемной ресусцитации в комплексе противошоковых мероприятий у пациентов с политравмой, который позволяет в максимально короткие сроки ликвидировать состояние критической гиповолемии, обеспечивая стабилизацию гемодинамики и возможность восполнения дефицита ОЦК кристаллоидными и коллоидными инфузионными средами, предотвращая развитие необратимого шока, влияя таким образом на исход у пациентов с травматическим шоком III–IV степени.
2. Представляется интересным проведение дальнейшего изучения использования препарата Гекотон для коррекции внутричерепной гипертензии у пациентов нейрореанимационного профиля.
1. Марино П. Интенсивная терапия. — М.: Гэотар-Медиа, 2010. — 768 с.
2. Усенко Л.В., Шифрин Г.А. Интенсивная терапия при кровопотере. — К.: Здоров’я, 1995. — 235 с.
3. Краймейер У. Применение гипертонического раствора NaCl при геморрагическом шоке // Актуальные проблемы анестезиологии и реаниматологии. Освежающий курс лекций. — Архангельск; Тромсе, 1997. — С. 283–291.
4. Рыбицкий З. Интенсивное лечение взрослых пациентов. — Люблин: Makmed, 2012. — 643 с.
5. Хеламяэ Х. Воздействие инфузии гипертонического раствора NaCl на функцию сердца и метаболизм // Актуальные проблемы анестезиологии и реаниматологии. Освежающий курс лекций. — Архангельск; Тромсе, 1997. — С. 279–282.
6. Westphal M., James M.F.M., Kozek-Langenecker S. et al. Hydroxyethyl Starches. Different Products — Different Effects // Anaesthesiology. — 2009. — Vol. 111. — P. 187–202.
7. Wilkes N.J., Woolf R.L., Powanda M.C. et al. Hydroxyethyl starch in balanced electrolyte solution (Hextend®) — Pharmacokinetic and pharmacodynamic profiles in healthy volunteers // Anesth. Analg. — 2002. — Vol. 94. — P. 538–544.

/78/78.jpg)
/80/80.jpg)