Архив офтальмологии Украины Том 7, №1, 2019
Вернуться к номеру
Вплив вітреоретинальних втручань на клінічний перебіг діабетичної макулопатії у хворих на цукровий діабет 2-го типу
Авторы: Панченко Ю.О., Могілевський С.Ю.
Київська міська клінічна офтальмологічна лікарня «Центр мікрохірургії ока», м. Київ, Україна Медичний центр «ЛАЗЕР Плюс», м. Львів, Україна
Національна медична академія післядипломної освіти імені П.Л. Шупика МОЗ України, м. Київ, Україна
Рубрики: Офтальмология
Разделы: Справочник специалиста
Версия для печати
У статті наводяться результати впливу вітреоретинальних операцій та клінічний перебіг діабетичної макулопатії у хворих на цукровий діабет 2-го типу. Було вивчено ефективність вітректомії без пілінгу та з пілінгом внутрішньої пограничної мембрани (ВПМ) сітківки при лікуванні діабетичної макулопатії й діабетичного макулярного набряку (ДМН) через 1, 3 і 6 місяців після оперативного лікування. Установлено високу ефективність втручання через 1 і 3 місяці, що підтверджувалося резорбцією твердих ексудатів, мікрогеморагій і ДМН, а також статистично значущим зменшенням товщини сітківки в макулярній ділянці та зменшенням макулярного об’єму. Рецидив ДМН через 6 місяців становив 10,26 і 10,59 % у хворих без пілінгу ВПМ і з ним відповідно. Виконання пілінгу ВПМ не забезпечувало переваг у профілактиці рецидивів ДМН і при даному обсязі досліджень давало гірші функціональні результати.
В статье приводятся результаты влияния витреоретинальных операций на клиническое течение диабетической макулопатии у больных сахарным диабетом 2-го типа. Была изучена эффективность витрэктомии без пилинга и с пилингом внутренней пограничной мембраны (ВПМ) сетчатки в лечении диабетической макулопатии и диабетического макулярного отека (ДМО) через 1, 3 и 6 месяцев после оперативного лечения. Установлена высокая эффективность вмешательства через 1 и 3 месяца, что подтверждалось резорбцией твердых экссудатов, микрогеморрагий и ДМО, а также статистически значимым уменьшением толщины сетчатки в макулярной области и объема самой макулярной области. Рецидив ДМО через 6 месяцев составил 10,26 и 10,59 % у больных без пилинга ВПМ и с таковым соответственно. Выполнение пилинга ВПМ не обеспечивало преимуществ в профилактике рецидивов ДМО и при данном объеме исследований давало худшие функциональные результаты.
Background. Diabetic maculopathy is one of the main reasons of central vision loss in patients with diabetic retinopathy (DR) and type 2 diabetes mellitus (DM2T). The main symptom of diabetic maculopathy is diabetic macular edema (DME). DME develops as a result of increased permeability of the hemato-ophthalmic barrier due to dysfunction of the endothelium of retina vessels. Standard treatment for DME include pharmacological, laser photocoagulation, anti-VEGF and corticosteroid therapy. For treatment of more severe and resistant to pharmacological and laser treatments, as well as to anti-VEGF therapy, an alternative treatment approach is used, in particular endotracheal vitrectomy with retinal coagulation, tamponade of the reticulum, removal of the posterior hyaloid membrane and, if necessary, internal limiting membrane (ILM) peeling. The purpose of the research is to investigate the effects of various technologies of vitreoretinal surgery on the clinical picture of diabetic maculopathy in patients with DM2T. Materials and methods. The study included 163 patients (80 men, 49.1 %, and 83 women, 50.9 %) with moderate to severe non-proliferative diabetic retinopathy (NPDR) or proliferative diabetic retinopathy (PDR), and diabetic maculopathy. Duration of DM2T was from 1 year to 30 years. Ninety-eight patients had compensated DM2T, 39 — subcompensated and 26 — decompensated. The age of the patients ranged from 42 to 75 years, median age was 64.5 ± 4.2 years. These patients were divided into two groups of observation (78 patients and 85 patients). Both groups did not differ by gender, age and stage of DR (p > 0.05). The patients in the first group underwent a three-port closed subtotal vitrectomy 25+ on the Constellation Vision System (Alcon, USA) using standard technology. The patients in the second group during the vitrectomy additionally underwent ILM peeling in the macular region with a diameter of 2.5–3.5 mm. The observation period lasted 6 months. Results. After one month of follow-up, in the first group complete resorption of DME happened in 53 eyes (67.9 %), in the second group — in 70 eyes (82.3 %), thus statistically significant (p < 0.01). In 3 eyes (3.5 %) in the group where vitrectomy was performed with ILM peeling, at the first day after the operation there were the concentric narrowing of the visual field to 10–15 degrees and central relative scotoma. After 3 months of follow-up, in the first group total resorption of DME was in 63 eyes (80.8 %), in the second — in 70 eyes (82.3 %), i.e. statistically not significant (p > 0.05). After 6 months of follow-up, the resorption frequency of DME in the first and second groups was not statistically significantly and made 76.9 % and 75.3 %, respectively (p > 0.05); visual acuity in the second group reduced in 5 eyes (5.9 %) without recurrence of DMP and DME; the frequency of DME relapse in the first group was 10.3 %, in the second — 10.6 %, thus, not statistically significant (p < 0.05). In the group of vitrectomy along with ILM peeling in 10 eyes (11.8 %) there was concentric narrowing of the vision field to 5–10° mainly in nasal meridians and in 5 eyes (5.9 %) there were central and paracentral relative scotomas with no relapse of DMP and DME. Conclusions. Within 1 and 3 months observation periods, vitrectomy with and without ILM peeling is an effective method of DMP treatment, characterized with resorption of solid exudates, microhemorrhage and DME (60.7 % and 82.4 %; 80.8 % and 82.4 %, respectively), as well as statistically significant decrease in central macular thickness and the macular volume (p < 0.05). Relapse of DME after various technologies of the vitrectomy was observed in 6 months after the operation and made 10.3 % and 10.6 %, respectively, in groups without and with ILM peeling. ILM peeling did not provide benefits in terms of prevention of DME relapse and had worse functional results within the terms of research. ILM peeling with its diameter selection must be carried out, if medically required, taking into account both risks factors of this procedure and all well-known mechanisms of DMP and DME. Prospects for increasing the effectiveness of DMP and DME prevention are concentrated in the study of new fundamental mechanisms of their development.
діабетична макулопатія; цукровий діабет 2-го типу; вітректомія
диабетическая макулопатия; сахарный диабет 2-го типа; витрэктомия
diabetic maculopathy; diabetes mellitus type 2; vitrectomy
Вступ
Діабетична ретинопатія (ДР) — неспецифічне судинне ускладнення цукрового діабету (ЦД) як першого, так і другого типу (ЦД2), що нерідко призводить до слабкозорості і сліпоти. За даними ВООЗ, серед основних причин слабкозорості ДР становить 1 %, серед сліпоти — також 1 %. Серед основних причин сліпоти у світі у людей віком понад 50 років ДР становить 13 % [1]. Хворі на діабет мають у 25 разів більше шансів осліпнути, ніж решта населення [2]. До факторів ризику прогресування ДР дослідники відносять тривалість ЦД, гіперглікемію, порушення ліпідного обміну, артеріальну гіпертензію, діабетичну нефропатію, метаболічний синдром, вагітність, стать і вік пацієнта, недотримання дієти, низьку фізичну активність, а також виконану факоемульсифікацію катаракти [2–4, 13].
Однією з основних причин зниження центрального зору у хворих на ДР і ЦД2 є діабетична макулопатія (ДМП), що проявляється у вигляді макулярного набряку (ДМН), мікроаневризм, інтраретинальних мікросудинних аномалій (ІРМА), твердих ексудатів, ішемії й заднього відшарування склоподібного тіла в макулі [2]. Основним симптомом ДМП є діабетичний макулярний набряк. Багаторічними дослідженнями встановлено, що ризик розвитку ДМН вищий у хворих на ЦД2 [4, 9, 10]. Згідно з результатами міжнародного дослідження WESDR, у хворих на ЦД2 зі стажем захворювання до 5 років ДМН реєструють у 3 % випадків, при тривалості 20 років і більше — у 28 % випадків. Спостереження протягом 10 років показали, що ДМН був у кожного четвертого хворого на ЦД2, який отримував ін’єкції інсуліну, і у 13,9 % хворих, які отримували інші види цукрознижувальної терапії. Також було встановлено, що частота ДМН збільшується з прогресуванням ДР і може досягати 70 % при проліферативній діабетичній ретинопатії [2–6].
Ми раніше повідомляли про особливості розвитку ДМП і ДМН у хворих на ЦД2 [7].
Основними ланками патогенезу ДМП є набряк сітківки в ділянці жовтої плями в результаті збільшення проникності ретинальних судин і ретинальна ішемія в результаті капілярної й артеріальної неперфузії сітківки. Причина виникнення ДМН — підвищення проникності гематоофтальмічного бар’єра внаслідок дисфункції ендотелію судин сітківки при ЦД2. Має значення співвідношення гідростатичного онкотичного тиску між плазмою в середині капілярів і міжклітинними просторами сітківки.
Особливу роль у виникненні і ступені вираженості ДМН відіграють чинники зростання, що активують ангіогенез і призводять до розвитку типових патологічних змін при ДР і ДМП. Це гормон росту, інсуліноподібний фактор росту I, фактор росту фібробластів, трансформуючий фактор росту, фактор росту ендотелію судин (VEGF) і низка інших [5, 8–12].
Велику роль у виникненні ДМН відіграють зміни склоподібного тіла, зокрема задньої гіалоїдної мембрани (ЗГМ). Змінена ЗГМ перешкоджає метаболізму сітківки, викликає і підтримує набряк макули. Неповне самостійне відшарування склоподібного тіла також може утворювати тангенціальні макулярні тракції, що пояснює стійкість ДМН до лазеркоагуляції й інтравітреальних ін’єкцій кортикостероїдів й анти-VEGF-препаратів [6, 8–11].
Традиційними методами лікування ДМН є консервативний та лазерний методи, а також інтравітреальне введення анти-VEGF-препаратів і глюкокортикостероїдів.
На жаль, лазерні методи лікування ДМН найбільш ефективні лише на ранніх стадіях ДМН й обмежуються товщиною сітківки в зоні набряку [9–11].
Для лікування більш тяжких і стійких до консервативного й лазерного методів, а також анти-VEGF-терапії форм ДМН застосовують хірургічне лікування — вітректомію з ендолазеркоагуляцією сітчастої оболонки, тампонадою вітреальної порожнини, видаленням задньої гіалоїдної мембрани, за потреби — з пілінгом внутрішньої пограничної мембрани сітківки (ВПМ) [6, 10, 11]. Є дані про ефективність вітректомії з пілінгом ВПМ у комбінації з попередньо проведеною анти-VEGF-терапією [11].
Питання про доцільність видалення ВПМ, а також діаметр макулорексиса при ДМН без ознак тракції з боку склоподібного тіла залишається дискусійним [6, 16].
Мета дослідження: вивчити вплив різних варіантів вітреоретинальних утручань на клінічний перебіг діабетичної макулопатії у хворих на цукровий діабет 2-го типу.
Матеріали та методи
Під нашим спостереженням перебували 163 хворі (80 чоловіків, 49,1 %, та 83 жінки, 50,9 %) із ЦД2 та помірною або тяжкою непроліферативною діабетичною ретинопатією або проліферативною діабетичною ретинопатією та з діабетичною макулопатією. Тривалість ЦД2 — 1–30 років. У 98 хворих ЦД2 був компенсований, у 39 — субкомпенсований, у 26 — декомпенсований. Вік хворих — від 42 до 75 років, у середньому — 64,5 ± 4,2 року. Цих пацієнтів розподілили на дві групи спостереження (1-ша — 78 хворих, 2-га — 85 хворих). Обидві групи спостереження статистично значуще не відрізнялися за розподілом за статтю, віком та стадією ДР (p > 0,05).
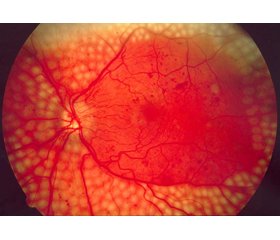
Усім хворим були проведені загальноприйняті офтальмологічні дослідження, що включали візометрію, статичну периметрію Humphrey, рефрактометрію, тонометрію, біомікроскопію, гоніоскопію, офтальмоскопію за допомогою асферичної лінзи Volk Super/Field (NC, США) і контактної тридзеркальної лінзи Гольдмана. Усім хворим виконували спектрально-доменну оптичну когерентну томографію (ОКТ) на приладі Optopoltechnology, SOCT, Copernicus REVO (протокол Retina3D, Retina Raster) і ОКТ в ангіорежимі (протокол Retina Angio, wide 6 x 6 mm). Також проводили дослідження очного дна на фундус-камері з його фотографуванням в 7 стандартних полях відповідно до модифікованої ETDRS системи клінічних ознак Airlie House. Флуоресцентну ангіографію (ФАГ) виконували за показаннями (у разі підозри на приховану неоваскуляризацію, що не було ідентифіковано офтальмо–скопічно й на фотографіях очного дна, а також у разі невідповідності зорових функцій офтальмоскопічним змінам у макулярній ділянці або даним ОКТ).
Рівень тяжкості ДР і ДМП встановлювали відповідно до Міжнародної клінічної шкали тяжкості діабетичної ретинопатії й діабетичної макулопатії Американської академії офтальмології (2002) [2]. Для аналізу знімків оптичної когерентної томографії макулярної ділянки сітківки при діабетичному макулярному набряку використовували вдосконалений алгоритм [15].
Показаннями для проведення закритої субтотальної вітректомії були прогресуюче зниження гостроти зору, зміни поля зору в центральних і парацентральних відділах, зміни якості зору на фоні непроліферативної діабетичної ретинопатії з рефрактерним макулярним набряком або макулярним набряком із наявністю тангенціальних тракцій, які з’явилися внаслідок неповного відшарування задньої гіалоїдної мембрани склоподібного тіла, а також проліферативної діабетичної ретинопатії з рефрактерним макулярним набряком, наявністю епіретинальних мембран та наявністю тангенціальних та осьових тракцій сітківки та загрозою тракційного відшарування сітківки, а також наявністю гемофтальму, преретинальних та субгілоїдальних крововиливів.
Пацієнтам першої групи виконували трипортову закриту субтотальну вітректомію 25+ на апараті Constellation Vision System (Alcon, США) за допомогою касети Constellation TOTALPLUS комбінований 7500СРМ, 25+ калібр (Alcon, США). Виконували порти троакарами 25 Ga на 10:00, 2:00, 7:00 або 5:00 годинах залежно від ока. У порт на 7:00 або 5:00 годинах установлювали іригаційну канюлю з подачею збалансованого розчину BSS. Виконували вітректомію центральних та периферичних шарів склоподібного тіла з попереднім введенням тріамциналону ацетоніду для чіткішої візуалізації структур, що видаляли. За допомогою екструзійної лінії проводили заднє відшарування склоподібного тіла, вітреотомом або вітреальними пінцетами видаляли задню гіалоїдну мембрану та епіретинальні мембрани, усували тангенціальні й осьові тракції сітківки. За допомогою склерокомпресії проводили вітректомію крайньої периферії сітківки. Ендолазерним зондом 25 Ga виконували ендолазеркоагуляцію з подальшою заміною рідини на стерильне повітря. У вітреальну порожнину вводили газоповітряну суміш 20 % С3F8. Видаляли троакари та герметизували порти.
Пацієнтам другої групи спостереження під час виконання вітректомії було додатково проведено пілінг внутрішньої пограничної мембрани у макулярній ділянці діаметром 2,5–3,5 мм із попереднім уведенням у вітреальну порожнину барвника Membran Blue для чіткої візуалізації мембрани.
Вивчали вплив вітректомії без макулопілінгу та з ним на клінічний перебіг ДМП та ДМН.
Термін спостереження — 6 місяців.
При проведенні аналізу для подання кількісних даних у таблицях наводилися середнє значення (M) і стандартне відхилення (± SD). Для якісних — наводився показник частоти (P, %) та стандартна помилка (± m). Наявність відмінностей середніх значень у двох вибірках оцінювали за допомогою критерію Стьюдента (у разі нормального закону розподілу) або критерію Вілкоксона (у разі відхилення закону розподілу від нормального). Для аналізу динаміки показників використано метод порівняння пов’язаних вибірок. Для порівняння якісних ознак застосовано точний критерій Фішера. Критичний рівень значущості прийняли рівним 0,05.
Результати та обговорення
Максимальна коригована гострота зору до операції в першій групі спостереження коливалась від 0,02 до 0,5 і в середньому становила 0,12 ± 0,08. На 28 очах (35,9 %) було визначено центральні та парацентральні відносні або абсолютні скотоми. Усі хворі мали різни прояви ДМП — мікроаневризми та мікрогеморагії у макулярний ділянці, ІРМА, відкладення твердих ексу–датів, а також ДМН різного ступеня прояву з кістозними порожнинами. Середня товщина сітківки коливалась від 300 до 823 мкм і в середньому становила 488,5 ± 55,0 мкм. Середній об’єм макулярної ділянки сітківки до оперативного втручання в першій групі спостереження становив 13,8 ± 1,7 мм3.
Максимальна коригована гострота зору до операції в другій групі спостереження коливалась від 0,05 до 0,4 і в середньому становила 0,15 ± 0,09. На 32 очах (37,6 %) було визначено центральні та парацентральні відносні або абсолютні скотоми. Усі хворі мали прояви ДМП і ДМН різного ступеня з кістозними порожнинами. Середня товщина сітківки коливалась від 312 до 825 мкм і в середньому становила 475,5 ± 54,0 мкм. Середній об’єм макулярної ділянки сітківки до оперативного втручання у другій групі спостереження становив 14,1 ± 1,9 мм3.
Оперативні втручання як у першій, так і другій групах спостереження були виконані в повному обсязі. Щодо інтраопераційних ускладнень відзначено мікрогеморагії після видалення ВПМ на 5 очах (6,4 %) і 6 очах (7,05 %) в 1-й і 2-й групі спостереження відповідно. Ці мікрогеморагії розсмокталися без додаткового лікування протягом перших двох діб після операції. На 2 очах (2,6 %) у першій групі спостереження і на 3 (3,5 %) у другій до моменту закінчення вітр–ектомії був частковий гемофтальм. Його поширення було блоковане тампонадою вітреальної порожнини ПФОС (DK-Line) і збільшенням параметрів іригації до 40,0 мм рт.ст. Після зупинки кровотечі ПФОС було виведено, параметри іригації нормалізовано до 25,0 мм рт.ст. У всіх випадках гемофтальм регресував без додаткового лікування протягом 2–3 діб після операції.
У ранньому післяопераційному періоді на 3 очах (3,8 %) у першій групі спостереження і на 5 (5,9 %) у другій розвинувся частковий гемофтальм. Було призначено додаткову одноразову парабульбарну ін’єкцію 64 ОД лідази. У всіх випадках гемофтальм розсмоктався. На 8 очах (10,3 %) і на 10 очах (11,8 %) в обох групах спостереження відповідно розвинувся післяопераційний іридоцикліт різного ступеня вираженості. Цим хворим були призначені парабульбарні ін’єкції глюкокортикостероїдів протягом 3–7 днів. Явища запальних ускладнень були купірувані. На 10 очах (12,8 %) в першій групі спостереження і на 12 (14,1 %) у другій розвинулася транзиторна гіпертензія. Цим пацієнтам була додатково призначено місцеве гіпотензивне лікування у вигляді інстиляцій тривалістю від 2 до 4 тижнів. Через 1 місяць після операції в усіх випадках транзиторна гіпертензія регресувала. З огляду на вищевикладене можна зробити висновок, що характер і частота операційних і ранніх післяопераційних ускладнень у двох групах спостереження не відрізнялися.
При обстеженні хворих першої групи спостереження через 1 місяць після операції було встановлено, що повна резорбція ДМН у першій групі відбулася на 53 очах (67,9 %), у другій групі — на 70 очах (82,4 %), тобто різниця статистично значуща (р = 0,04). На 3 очах (3,5 %) у групі, де вітректомію виконували з пілінгом ВПМ, у першу добу після операції відмічали концентричне звуження меж поля зору до 10–15 градусів, а також наявність центральної відносної скотоми. При обстеженні хворих першої групи спостереження через 3 місяці після операції було встановлено, що повна резорбція ДМН була на 63 очах (80,8 %), у другій — на 70 (82,4 %), тобто різниця статистично незначуща (р = 0,84). Через 6 місяців після вітректомії частота резорбції ДМН у першій та другій групах спостереження статистично значущо не відрізнялася та становила 76,9 та 75,3 % відповідно (р = 0,71).
У табл. 1 подана товщина сітківки у макулярній ділянці першої та другої груп спостереження до та через 1, 3, 6 місяців після оперативного лікування (Мсер ± SD).
Як видно з табл. 1, виконання вітректомії без видалення ВПМ (1-ша група) і з видаленням ВПМ (2-га група) дозволило зменшити товщину сітківки в макулярній ділянці через 1 і 3 місяці після операції (р < 0,05). Через 6 місяців після втручання як у першій, так і другій групах спостереження відзначено збільшення товщини сітківки, що було пов’язано з рецидивом макулярного набряку. Однак слід зазначити, що через 6 місяців товщина макулярної ділянки була статистично значуще меншою, ніж до операції.
У табл. 2 наведена динаміка об’єму макулярної ділянки в першій і другій групах спостереження до та через 1, 3, 6 місяців після оперативного лікування (Мсер ± SD).
Як видно з табл. 2, виконання вітректомії без видалення ВПМ (1-ша група) і з видаленням ВПМ (2-га група) дозволило зменшити об’єм макулярної ділянки сітківки через 1 і 3 місяці після операції (р < 0,05). Через 6 місяців після втручання як у першій, так і другій групах спостереження було відзначено збільшення об’єму макулярної ділянки сітківки, що також було пов’язано з рецидивом макулярного набряку. Макулярний об’єм сітчастої оболонки, як і товщина сітківки, був статистично значущо менший, ніж до операції.
У табл. 3 подана динаміка гостроти зору в першій і другій групах спостереження до та через 1, 3, 6 місяців після оперативного лікування.
Як видно з табл. 3, виконання вітректомії без видалення ВПМ (1-ша група) і з видаленням ВПМ (2-га група) дозволило в більшості випадків підвищити гостроту зору через 1, 3 і 6 місяців після операції. В обох групах спостереження через 1 місяць після втручання визначалися розшаровування дрібних твердих ексудатів, геморагій, а також максимальна резорбція ДМН. Варто відзначити, що через 6 місяців в обох групах спостереження збільшилась кількість пацієнтів зі зниженням гостроти зору. Це пов’язане, зокрема, із прогресуванням клінічних проявів ДМП і ДМН. Слід зазначити, що в 1-й групі, у якій пілінг ВПМ не проводили, гострота зору з максимальною корекцією коливалася через 6 місяців після операції від 0,1 до 0,8 і становила в середньому 0,55 ± 0,09. У другій групі, у якій проводили пілінг ВПМ, гострота зору з максимальною корекцією коливалася від 0,09 до 0,4, становила в середньому 0,3 ± 0,06 і була статистично нижчою, ніж в 1-й групі (р < 0,001).
Необхідно відзначити, що зниження гостроти зору через 6 місяців після втручання в другій групі спостереження було на 5 очах (5,9 %) без рецидиву ДМП і ДМН. За даного об’єму дослідження частота рецидиву ДМН у першій групі спостереження через 6 місяців становила 10,3 %, у другій — 10,6 %, тобто статистично значущо не відрізнялася (р = 0,80).
Також було встановлено, що в групі, у якій проводили вітректомію з пілінгом ВПМ, на 10 очах (11,8 %) відзначали концентричне звуження меж поля зору до 5–10° переважно у назальних меридіанах, а також наявність центральних і парацентральних відносних скотом на 5 очах (5,9 %), однак рецидивів ДМП і ДМН не було виявлено.
Таким чином, проведені нами дослідження показали, що виконання вітректомії у хворих із ДР і ЦД2 є досить ефективним методом лікування ДМП і ДМН. Максимальні функціональні результати лікування визначалися через 3 місяці після втручання. Через 6 місяців у 10 % випадків в обох групах спостереження відбулося прогресування ДМП із розвитком ДМН. Це, на нашу думку, було пов’язане, по-перше, із тим, що виконання вітректомії впливає лише на поодинокі, місцеві ланки патогенезу ДМП, по-друге, з тим, що хворі на ЦД2 практично завжди схильні до впливу як відомих факторів ризику розвитку ДМП і ДМН (гіперглікемія, дисліпідемія, артеріальна гіпертензія, нефропатії тощо), так і ще не вивчених.
Отримані нами дані про зниження гостроти зору і зміни поля зору після проведення вітректомії з пілінгом ВПМ на очах, коли втручання було виконано в повному обсязі, були відсутні операційні та післяопераційні ускладнення, а також рецидиви ДМН узгоджувались із даними літератури [2, 16, 17]. Загалом доцільність виконання пілінгу сітківки, показання для цього, розмір видаленої частини ВПМ як етап вітректомії для лікування ДМП і ДМН потребують ретельного вивчення. Видалення навіть невеликої (2–3,5 мм) частини ВПМ може призвести до необоротних процесів у сітчастій оболонці, яка і без цього знаходиться в стані хронічної ішемії і гіпоксії при ДР і ЦД2. Відомо, що одним із чотирьох елементів ВПМ є плазматична мембрана мюллерівських, а також інших гліальних клітин сітківки, найбільша товщина якої визначається саме в макулі. Клітини Мюллера є найбільшими клітинами сітківки; вони поширюються від зовнішньої до внутрішньої пограничної мембрани. Клітини Мюллера мають високу метаболічну активність, забезпечують поставку нейронам сітківки продуктів розпаду глікогену, виведення продуктів обміну нейронів, захищають нейрони від надлишкового вивільнення нейромедіаторів, здійснюють фагоцитоз продуктів розпаду при патологічних станах, синтез ретиноїдної кислоти з ретинолу, захист нейронів шляхом контролю гомеостазу іонів. Порушення функції клітин Мюллера лежить в основі багатьох захворювань сітківки. Гліальні клітини беруть участь у процесах регенерації сітківки при її пошкодженнях, у тому числі при ДР і ДМП [14]. З огляду на вищевикладене ми вважаємо, що пілінг ВПМ у хворих із ДР і ДМП повинен виконуватися у виняткових випадках і за суворими показаннями. Видалення навіть обмеженої ділянки ВПМ призводить до пошкодження відростків мюллерівских і інших гліальних клітин і, як наслідок, до порушення безлічі метаболічних процесів у всіх шарах сітчастої оболонки. Результатом цього є зниження зорових функцій в післяопераційному періоді без негативної динаміки на очному дні.
Висновки
1. Виконання вітректомії без пілінгу і з пілінгом ВПМ є ефективним методом лікування ДМП при терміні спостереження 1 і 3 місяці, що об’єктивується резорбцією твердих ексудатів, мікрогеморагій і ДМН (60,7 та 82,4 %, 80,8 та 82,4 % відповідно), а також статистично значущим зменшенням товщини сітківки в макулярній ділянці й об’єму макулярної ділянки (p < 0,05).
2. Рецидив ДМН після різних технологій вітректомії спостерігався через 6 місяців після операції, частота його була 10,3 і 10,6 % відповідно в групах, у яких пілінг ВПМ не проводили і проводили. Пілінг ВПМ не забезпечував переваг щодо профілактики рецидиву ДМН, але давав гірші функціональні результати при даному обсязі досліджень.
3. Пілінг ВПМ сітківки з вибором діаметра треба виконувати виключно з урахуванням як факторів ризику для цієї процедури, так і всіх відомих механізмів ДМП та ДМН.
4. Перспективи підвищення ефективності профілактики ДМП і ДМН ми бачимо у вивченні нових фундаментальних механізмів їх розвитку.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
1. Варивончик Д.В. Світові епідеміологічні характеристики поширеності порушень зору // Офтальмологія. — 2016. — 1(03).
2. Балашевича Л.И., Измайлова А.С. Диабетическая офтальмопатия. — СПб.: Человек, 2012. — 396 с.
3. Сидорова М.В. Діабетична ретинопатія. Патогенез, клініка, лікування. — К.: СМП «АВЕРС», 2006. — 156 с.
4. Danis R.P., Davis M.D. Diabetic retinopathy. Part I. Clinical aspect of diabetic retinopathy. 2. Proliferative diabetic retinopathy. — Totowa: Humana Press, 2008. — Р. 29-66.
5. Klein R., Klein B.E., Moss S.E., Cruickshanks K.J. The Wisconsin epidemiologic study of diabetic retinopathy. XV. The long-term incidence of macular edema // Ophthalmology. — 1995. — 102. — 7-16.
6. Файзрахманов Р.Р., Каланов М.Р., Зайнуллин Р.М. Витрэктомия в сочетании с пилингом внутренней пограничной мембраны при диабетическом макулярном отеке (обзор литературы) // Вестн. Оренбург. гос. унив. — 2015. — 12(187). — 257-259.
7. Могилевский С.Ю. Панченко Ю.А. Особенности диабетической макулопатии у больных сахарным диабетом 2 типа // Арх. офтальмол. Укр. — 2018. — 6. — 28-32.
8. Росненская И.В. Клинико-патогенетическое обоснование комбинированного лазерно-медикаментозного лечения макулярного диабетического отека: Автореф. дис… канд. мед. наук. — М., 2009. — 24 с.
9. Фабрикантов О.В., Гурко Т.С. Диабетическая макулопатия. Эпидемиология, патогенез, современные подходы к лечению (обзор лтературы) // Вестн. ТГУ. — 2014. — 19(12). — 744-56.
10. Величко П.Б. Диабетический макулярный отек // Науч. труды Мед. инст. ГТУ им. Г.Р. Державина. — Тамбов: Изд-во ТРРО «Бизнес-Наука-Общество», 2013. — 345-56.
11. Величко П.Б. Комплексное лечение диабетического макулярного отека // Вестн. ТГУ. — 2014. — 19(4). — 1097-1101.
12. Пасечникова Н.В. Диабетическая макулопатия. Современные аспекты патогенеза, клиники, диагностики, лечения. — К.: ООО «Карбон ЛТД». 2010. — 154 с.
13. Walker J., Рыков С.А., Сук С.А., Саксонов С.Г. Диабетическая ретинопатия. Просто о сложном. — К.: Бизнес-Логика, 2013. — 320 с.
14. Вит В.В. Строение зрительной системы человека. — Одесса: Астропринт, 2003. — 664 с.
15. Рыков С.А., Могилевский С.Ю., Пархоменко О.Г., Сук С.А. Усовершенствованный алгоритм анализа снимков оптической когерентной томографии макулярной области сетчатки при диабетическом макулярном отеке // Арх. офтальмол. Укр. — 2015. — 3. — 40-7.
16. Балашевич Л.И., Бойбородов Я.В., Гацу М.В. Эффективность закрытой витрэктомии с удалением внутренней пограничной мембраны сетчатки при лечении рефрактерного диффузного диабетического макулярного отека // Офтальмохирургия. — 2007. — 4. — 34-8.
17. Величко П.Б., Яблоков М.М., Козлов В.А. Анализ результатов хирургического лечения диабетического макулярного отека с эпиретинальным фиброзом после полной панретинальной лазеркоагуляции // Вестник ГТУ. — 2015. — 20(6). — 1659-61.

/80-1.jpg)
/81-1.jpg)