Журнал "Гастроэнтерология" Том 53, №3, 2019
Вернуться к номеру
Оптимізація лікування дуоденогастрального рефлюксу у хворих на хронічний гастрит
Авторы: Гуцаленко О.О.
Українська медична стоматологічна академія, м. Полтава, Україна
Рубрики: Гастроэнтерология
Разделы: Клинические исследования
Версия для печати
Актуальність. Відомі способи лікування дуоденогастрального рефлюксу із застосуванням прокінетика на тлі базисної терапії хронічного гастриту, як правило, мають низьку ефективність лікування. Мета дослідження: оцінити ефективність і безпеку комбінації метоклопраміду та сульпіриду (подвійного прокінетичного лікування) при дуоденогастральному рефлюксі в комплексному лікуванні хворих на хронічний гастрит. Матеріали та методи. Проведено ретроспективний аналіз результатів обстеження та лікування 30 хворих з дуоденогастральним рефлюксом і хронічним гастритом віком від 22 до 45 років. Лікування проводили згідно з Уніфікованим клінічним протоколом «Диспепсія» (Наказ МОЗ України № 600 від 03.08.2012 р.) та рекомендаціями Консенсусу Маастрихт ІІІ (2005) і Маастрихт ІV (2010). Базисну терапію хронічного гастриту поєднували з двома препаратами синергічної дії, а саме прокінетиком метоклопрамідом та препаратом з прокінетичними ознаками сульпіридом, за аналогічним принципом в режимі короткочасної ступінчастої терапії. Статистичну обробку результатів проводили згідно з алгоритмом аналізу якісних даних з використанням пакета програм MedCalc 2019. Аналізувалася частота прояву якісних бінарних змінних з розрахунком 95% довірчого інтервалу (ДІ). Для визначення впливу лікування на зміну частоти прояву клінічних синдромів застосовували критерій Мак-Немара для пов’язаних груп. Оцінка ризику побічної дії комбінації препаратів проводилася на підставі визначення рівня значимості 95% ДI для частки з урахуванням біномінального розподілу ознаки («наявність — відсутність ускладнення»). Сформульовані нульова і альтернативна статистичні гіпотези. Результати. Прояви диспептичного, абдомінального і астеновегетативного синдромів виявлені відповідно у 24 ((80,0 ± 7,3) %; 95% ДI 51,26–119,03 %), 13 ((43,00 ± 9,04) %; 95% ДI 23,07–74,10 %) і 18 хворих ((60,00 ± 8,94) %; 95% ДI 35,56–94,83 %). Через 20 днів подвійного прокінетичного лікування на тлі зникнення ендоскопічних ознак біліарного рефлюксу виявлені статистично значимі зміни частоти проявів диспептичного, абдомінального та астеновегетативного синдромів (відповідно двосторонні значення p < 0,0001; p = 0,0005 і p < 0,0001 за критерієм Мак-Немара). Синергізм дії метоклопраміду та сульпіриду як антагоністів дофамінових рецепторів та потенціювання їх прокінетичного впливу при лікуванні дуоденогастрального рефлюксу в комплексі з базисною терапією хронічного гастриту сприяє швидкому зникненню більшості клінічних проявів жовчного рефлюкс-синдрому, дозволяє досягти клінічного й ендоскопічного одужання та забезпечує стійку і тривалу ремісію. Переносимість комбінації препаратів у всіх хворих була доброю. Побічних ефектів не зареєстровано. Більше того, з вірогідністю 95 % доведено, що ризик побічної дії не перевищує 12 %. Висновки. Короткочасне призначення комбінації метоклопраміду і сульпіриду в режимі ступінчастої терапії є не лише ефективним, але й безпечним, що відповідає альтернативній статистичній гіпотезі.
Актуальность. Известные способы лечения дуоденогастрального рефлюкса с применением прокинетика в комплексе с базисной терапией хронического гастрита, как правило, имеют низкую эффективность лечения. Цель исследования: оценить эффективность и безопасность комбинации метоклопрамида и сульпирида (двойного прокинетического лечения) при дуоденогастральном рефлюксе в комплексном лечении больных хроническим гастритом. Материалы и методы. Проведен ретроспективный анализ результатов обследования и лечения 30 больных с дуоденогастральным рефлюксом и хроническим гастритом в возрасте от 22 до 45 лет. Лечение проводили согласно Унифицированному клиническому протоколу «Диспепсия» (приказ МЗ Украины № 600 от 03.08.2012 г.) и рекомендациям Консенсуса Маастрихт ІІІ (2005) и Маастрихт ІV (2010). Базисную терапию хронического гастрита сочетали с двумя препаратами синергического действия, а именно прокинетиком метоклопрамидом и препаратом с прокинетическими свойствами сульпиридом, по аналогичному принципу в режиме кратковременной ступенчатой терапии. Статистическую обработку результатов проводили согласно алгоритму анализа качественных данных с использованием пакета программ MedCalc 2019. Анализировалась частота проявления качественных бинарных переменных с расчетом 95% доверительного интервала (ДИ). Для определения влияния лечения на изменение частоты проявления клинических синдромов применяли критерий Мак-Немара для связанных групп. Оценка риска побочного действия комбинации препаратов проводилась на основании определения уровня значимости 95% ДИ для доли с учетом биноминального распределения признака («наличие — отсутствие осложнения»). Сформулированы нулевая и альтернативная статистические гипотезы. Результаты. Проявления диспептического, абдоминального и астеновегетативного синдромов обнаружены соответственно у 24 ((80,0 ± 7,3) %; 95% ДИ 51,26–119,03 %), 13 ((43,00 ± 9,04) %; 95% ДИ 23,07–74,10 %) и 18 больных ((60,00 ± 8,94) %; 95% ДИ 35,56–94,83 %). Через 20 дней лечения на фоне исчезновения эндоскопических признаков билиарного рефлюкса обнаружены статистически значимые изменения частоты проявлений диспептического, абдоминального и астеновегетативного синдромов (соответственно двусторонние значения p < 0,0001; p = 0,0005 и p < 0,0001 по критерию Мак-Немара). Синергизм действия метоклопрамида и сульпирида как антагонистов дофаминовых рецепторов и потенцирование их прокинетического влияния при лечении дуоденогастрального рефлюкса в комплексе с базисной терапией хронического гастрита способствует быстрому исчезновению большинства клинических проявлений желчного рефлюкс-синдрома, позволяет достичь клинического и эндоскопического выздоровления и обеспечивает стойкую и длительную ремиссию. Переносимость комбинации препаратов у всех больных была хорошей. Побочных эффектов не зарегистрировано. Более того, с вероятностью 95 % доказано, что риск побочного действия не превышает 12 %. Выводы. Кратковременное назначение комбинации метоклопрамида и сульпирида в режиме ступенчатой терапии является не только эффективным, но и безопасным, что соответствует альтернативной статистической гипотезе.
Background. The known methods of duodenogastric reflux treatment which include prokinetics administration against the background of chronic gastritis standard therapy, as a rule, have the low therapeutic efficacy. The aim of the research was to assess the efficacy and safety of metoclopramide and sulpiride combination (dual prokinetic treatment) for duodenogastric reflux in comprehensive treatment of patients with chronic gastritis. Materials and methods. The study is based on the retrospective analysis of the findings obtained while examining and managing 30 patients with duodenogastric reflux and chronic gastritis aged from 22 to 45 years. The patients received treatment in accordance with the Standardized Clinical Protocol of Primary Care “Dyspepsia”, approved by the Order of the Ministry of Health of Ukraine No. 600 of August 3, 2012, and recommended by Maastricht III (2005) and Maastricht IV (2010). The basic therapy for chronic gastritis was combined with two drugs of synergistic effect, namely, prokinetic metoclopramide and sulpiride with prokinetic properties by similar principle in the regimen of short-term step therapy. The statistical processing of data was carried out according to the algorithm for qualitative data analysis with MedCalc 2019 software package. The study includes the analysis of manifestation incidence of qualitative binary variables with calculation of 95% confidence interval. When determining the effect of dual prokinetic treatment on the change of clinical syndromes manifestation incidence, we used McNemar test for related groups. The study evaluated the risk of side effects of metoclopramide and eglonil combination on the basis of assessment the significance value 95% confidence interval, considering binominal distribution of a sign (presence or absence of complication). The study presented formulation of the null and alternative statistical hypotheses. Results. The manifestations of dyspeptic, abdominal and astheno-vegetative syndromes were detected in 24 ((80.0 ± 7.3) %; 95% CI 51.26–119.03 %), 13 ((43.00 ± 9.04) %; 95% CI 23.07–74.10 %) and 18 patients ((60.00 ± 8.94) %; 95% CI 35.56–94.83 %), respectively. After 20 days of dual prokinetic treatment, the statistically significant changes in the incidence of dyspeptic, abdominal and astheno-vegetative syndromes manifestations were observed in patients against the background of endoscopic signs of bile reflux elimination (bilateral values p < 0.0001; p = 0.0005 and p < 0.0001, respectively, according to the McNemar test). The synergism of metoclopramide and eglonil effect as dopamine receptor antagonists and prokinetic effect potentiation in combination with standard therapy contribute to the rapid elimination of the most clinical manifestations of the bile reflux syndrome, make it possible to achieve clinical and endoscopic recovery and ensure steady and long-term remission. The tolerability of drug combinations was good in all patients; they did not present with side effects. Moreover, the risk of side effects did not exceed 12 % with 95% probability. Conclusions. The short-term administration of metoclopramide and sulpiride combination in step therapy regimen is not only effective but also safe, which corresponds to the alternative statistical hypothesis.
дуоденогастральний рефлюкс; хронічний гастрит; подвійне прокінетичне лікування
дуоденогастральный рефлюкс; хронический гастрит; двойное прокинетическое лечение
duodenogastric reflux; chronic gastritis; dual prokinetic treatment
Вступ
Дуоденогастральний рефлюкс (ДГР), або жовчний рефлюкс-синдром, є важливою окремою клінічною проблемою. Під ДГР прийнято розуміти ретроградне закидання лужного вмісту дванадцятипалої кишки (ДПК) у порожнину шлунка та в анатомічно вище розміщені органи з наступним агресивним впливом через постійну травматизацію слизової оболонки шлунка (СОШ) та стравоходу компонентами рефлюксату [1–6].
Відомо, що ДГР будь-якого ступеня вираженості є важливим етіологічним чинником та патогенетичним ланцюгом у розвитку хронічного антрального гастриту, ступінь тяжкості якого безпосередньо залежить від ступеня ДГР [1, 5]. Це відкриває шлях для тривалого запалення СОШ та ДПК і можливого розвитку ерозивно-виразкових уражень та гастроканцерогенезу [1–3, 7]. Доведено, що під дією жовчних кислот і панкреатичного соку виникає стійка запальна реакція СОШ, що спричиняє виникнення рефлюкс-гастриту з наступним поетапним розвитком атрофії, появою метаплазії та дисплазії [1, 2, 4, 5, 7, 8].
За даними різних авторів, у 45–100 % випадків [3–5, 9] ДГР діагностується на фоні багатьох функціональних і органічних захворювань органів травлення (ОТ), перш за все гастродуоденальної зони, що накладає відбиток на клінічну симптоматику рефлюксу, значною мірою маскуючи її [1, 3, 4]. Слід зауважити, що лікарі нерідко недооцінюють значення ДГР в патогенезі захворювань ОТ [5]. Отже, ДГР досить часто залишається непоміченим клініцистами і оцінюється як такий, що не потребує додаткового лікування.
Тож актуальність розгляду даного синдрому диспепсії обумовлена перш за все значною його поширеністю (25–40 % усього населення), а у 2–5 % є причиною всіх звернень хворих до сімейних лікарів та суттєво впливає на якість життя цих хворих [5], що потребує своєчасної його діагностики й адекватного лікування.
Таким чином, актуальним постає питання розробки ефективних способів його лікування, які забезпечували б максимальний лікувальний ефект на тлі мінімальних побічних впливів. Відсутність клінічних рекомендацій при цій патології обумовлює велику кількість запитань щодо тактики ведення таких хворих.
Лікування ДГР являє собою складну задачу і включає призначення різних груп лікарських засобів (ЛЗ): прокінетиків [1–4, 9–11], антацидів [1, 3, 4, 10], інгібіторів протонної помпи [1–4], препаратів урсодезоксихолевої кислоти (УДХК), сорбентів [1, 3, 4] та цитопротекторів [1–4], ефективність яких досліджена по-різному, а загальноприйняті схеми лікування даної патології відсутні. За наявності ДГР засобами патогенетичної терапії та препаратами вибору є прокінетики [9–11], які підвищують тонус та стимулюють моторику шлунково-кишкового тракту (ШКТ), усувають антиперистальтику та прискорюють транзит харчового болюсу по ньому [11, 12]. Ефективність цих препаратів у відновленні моторики шлунка становить 70 % [4].
Незважаючи на наявність різних класів ЛЗ з потенційною прокінетичною дією, число препаратів, що реально можуть застосовуватися сьогодні у клінічній практиці для лікування хворих з ДГР, дуже обмежене. По суті, вони вичерпуються домперидоном (мотиліум), метоклопрамідом та ітоприду гідрохлоридом (ганатон, праймер, ітомед), які ефективні при порушенні моторики верхніх відділів ОТ. Останнім часом арсенал сучасних прокінетиків був суттєво переглянутий, внаслідок чого деякі ліки через кардіотоксичний ефект були вилучені з обігу клінічного застосування (цизаприд, тегасерод), а з 2015 р. внесені суттєві зміни стосовно призначення домперидону. Комітет з оцінки ризиків, пов’язаних з безпекою ЛЗ (Pharmacovigilance Risk Assessment Committee — PRAC EMA), рекомендував внести зміни в інструкцію щодо використання препаратів на основі домперидону на всій території Європейського Союзу, в тому числі використовувати ці ліки лише для полегшення симптомів нудоти і блювання. PRAC вважає, що зниження рекомендованої дози (до 10 мг тричі на добу per os) і тривалості лікування (не більше 1 тижня) є ключовим моментом у мінімізації ризиків використання цього ЛЗ. Крім того, проблема застосування препарату — низька біологічна доступність домперидону (близько 13–17 %), що певною мірою обумовлене екстенсивним метаболізмом у стінці кишечника [9]. Призначення ж метоклопраміду є обмеженим через розвиток побічних ефектів у 25–30 % випадків [3, 4, 11].
У доступній літературі відсутня доказова база стосовно застосування нового селективного прокінетика 2 покоління ітоприду гідрохлориду при ДГР. Ітоприд рекомендований до застосування при функціональній диспепсії (ФД), гастроезофагеальній рефлюксній хворобі (ГЕРХ), синдромі подразненого кишечника і гастропарезі різного генезу [11, 13]. Опубліковані у метааналізі 2017 р. дані порівняльної ефективності прокінетиків при лікуванні ФД показали, що метоклопрамід має кращу ефективність порівняно з ітопридом (OR (odds ratio — відношення шансів) 2,79; 95% довірчий інтервал (ДI) 1,29–6,21) [13]. Тож на сьогодні відсутні ґрунтовні дослідження та переконливі докази, що підтверджують ефективність застосування ітоприду при ДГР.
Відомо, що прокінетики є основою для лікування ФД, але систематичні огляди наводять суперечливі результати про їх ефективність та безпеку [13–17]. За останні два роки в доступній літературі наведені результати трьох систематичних оглядів та метааналізів рандомізованих клінічних досліджень (РКД) з вивчення порівняльної ефективності прокінетиків для лікування ФД [13–15].
У 2018 р. група канадських учених опублікувала результати пошуку систематичних оглядів 43 РКД, що включав Кокранівську бібліотеку, електронні бази даних MEDLINE, EMBASE та CINAHL за період з 1946 по вересень 2017 р. Із них у метааналіз включено 29 РКД у паралельних групах за участю 10 044 хворих, у яких порівнювали 6 прокінетиків з плацебо на предмет повної відсутності симптомів або поліпшення симптомів та балів симптомів у кінці лікування ФД [14]. У 10 РКД порівнювали різні прокінетики один з одним. Найбільш часто застосовувався домперидон по 10 мг тричі на добу (у 8 із 10 досліджень). У лютому 2019 р. ці ж автори опублікували систематичний огляд даних і метааналіз 38 РКД, в яких первинним результатом були відсутність або поліпшення диспептичних симптомів в кінці лікування ФД [15]. За результатами двох проведених метааналізів не було встановлено відмінностей між прокінетиками для поліпшення симптомів ФД [14, 15]. Переносимість усіх препаратів, окрім цизаприду, була доброю [15].
У 2017 р. групою корейських авторів опубліковані результати оцінки порівняльної ефективності прокінетиків при лікуванні ФД. До метааналізу 25 РКД ввійшли 4473 пацієнти з ФД, які отримували також 6 різних прокінетиків або плацебо [13]. Встановлено, що метоклопрамід, тримебутин, мосаприд і домперидон показали кращу терапевтичну ефективність для лікування ФД, ніж ітоприд або акотіамід. Незважаючи на побічні ефекти від прийому метоклопраміду або домперидону, автори роблять висновок, що для полегшення симптомів ФД може бути рекомендовано короткочасний прийом цих ЛЗ [13].
Про доцільність і безпеку короткочасного прийому прокінетиків для лікування ФД свідчать дані японських авторів ще у 2007 році [17]. Згідно з результатами метааналізу 27 РКД з оцінки ефективності 6 прокінетиків (метоклопрамід, домперидон, ітоприд, тримебутин, цизаприд і мосаприд), ці препарати при лікуванні ФД значно більш ефективні, ніж плацебо, при короткочасному їх прийомі. А доцільність і можливість тривалого їх застосування потребує подальшого вивчення [17].
До препаратів з вираженими прокінетичними властивостями також належить сульпірид, оскільки, як і метоклопрамід та домперидон, відноситься до специфічних антагоністів дофамінових рецепторів, які впливають на тонус і моторику ШКТ [12]. Препарати цієї групи призначають при ДГР, ФД, ГЕРХ, виразковій хворобі та інших захворюваннях ОТ. Якщо метоклопрамід є неселективним блокатором допаміну центральної та периферичної дії, то сульпірид є атиповим нейролептиком, похідним бензаміду з селективною блокадою центральних дофамінових рецепторів [12]. При прийомі всередину сульпірид діє також за рахунок блокади периферичних дофамінових рецепторів кровоносних судин і гладких м’язів ШКТ, що виявляється в нормалізації моторної активності шлунка, кишечника, жовчного міхура тощо [12]. Сульпірид належить до ЛЗ, що має широкий спектр терапевтичної активності та високий рівень безпеки [12, 18]. У комплексній терапії великої кількості хвороб ОТ використовується не лише анксіолітичний, соматотропний та анальгетичний ефект препарату, але і його прокінетичний вплив [12, 18, 19], протидиспептична дія [18]. Також добре відомий його загоюючий ефект у комплексному лікуванні ерозивно-виразкових уражень шлунка, ДПК, кишечника [18].
Отже, незважаючи на різноманітність ЛЗ з прокінетичною дією, можливості терапевтичної корекції порушень моторики ОТ й усунення ДГР на сьогодні є досить обмежені і включають використання лише метоклопраміду, сульпіриду та сучасного селективного прокінетика нової генерації ітоприду гідрохлориду у вигляді монотерапії або ж у комбінації з препаратами УДХК. Основними недоліками застосування ітоприду та УДХК є тривалий прийом цих препаратів (не менше 2 міс.) до досягнення позитивного терапевтичного ефекту [4, 11].
Відомі способи лікування ДГР із застосуванням прокінетика в комплексі з базисною терапією основного захворювання, як правило, послаблюють або усувають патологічний біліарний рефлюкс у шлунок і стравохід, проте мають низьку ефективність лікування. Саме тому і виникла необхідність оптимізації лікування ДГР у хворих на хронічний гастрит (ХГ). З цією метою запропоновано короткочасне застосування двох препаратів прокінетичної дії (подвійне прокінетичне лікування (ППЛ)), а саме комбінацію метоклопраміду та сульпіриду в комплексі з базисною терапією ХГ.
Мета дослідження: оцінити ефективність і безпеку комбінації метоклопраміду та сульпіриду при ДГР в комплексному лікуванні хворих на ХГ.
Завданням дослідження було розробити надійний спосіб лікування ДГР у хворих на ХГ з короткочасним призначенням ЛЗ із широким спектром дії, максимальним прокінетичним (за рахунок потенціювання синергічної дії двох медикаментів) та мінімальним побічним впливом (безпека короткочасного прийому прокінетиків), який дозволить усунути основний симптомокомплекс клінічних проявів жовчного рефлюкс-синдрому, досягти клінічного й ендоскопічного одужання та забезпечити підвищення ступеня ефективності його лікування. Первинною кінцевою точкою періоду лікування була повна відсутність або поліпшення симптомів у кінці лікування [14, 15, 20, 21].
Матеріали та методи
Наведене дослідження засноване на ретроспективному аналізі результатів обстеження та лікування 30 амбулаторних пацієнтів з ДГР та ХГ віком від 22 до 45 років ((28,6 ± 4,8) року), які звернулися за медичною допомогою з різними диспептичними розладами чи абдомінальним болем. Чоловіків було 9 (30 %), жінок — 21 (70 %).
Критеріями включення пацієнтів у дослідження були особи зрілого віку (від 22 до 45 років) з клінічними проявами диспептичного та/чи абдомінального синдромів різного ступеня вираженості на тлі ХГ з супутнім ДГР. Хворі віком понад 45 років не включалися у дослідження через високу ймовірність наявності супутньої (коморбідної) патології, що обмежує вибір терапії.
Із дослідження виключалися хворі з клінічними проявами ДГР за наявності «тривожних» симптомів; пацієнти до 20 років та літнього віку у зв’язку зі збільшенням ризику розвитку побічних ефектів при застосуванні метоклопраміду у дітей, підлітків та осіб літнього і старечого віку [22]. Групу виключення становили також пацієнти, яким проводилися оперативні втручання на органах черевної порожнини (зокрема, резекція шлунка, холецистектомія), тобто з так званим вторинним ДГР [6].
Усім пацієнтам проводилося обстеження згідно з діагностичним алгоритмом при недослідженій диспепсії. Діагностика захворювань ШКТ ґрунтувалася на ретельному анамнестичному та клінічному обстеженні хворих із застосуванням загальноклінічних, біохімічних, інструментальних (фіброезофагогастродуоденоскопія (ФЕГДС) з біопсією, рН-метрія, ультразвукове дослідження органів черевної порожнини, рентгенологічне дослідження шлунка та кишечника) і лабораторних досліджень (гістологічне дослідження біоптатів СОШ, інфікованості H.pylori швидким уреазним чи морфологічним методом). Діагноз ХГ верифіковано на підставі результатів морфологічного дослідження СОШ. Діагноз патологічного ДГР встановлювали згідно з критеріями J.K. Lin et al. (2003) при ФЕГДС, оскільки найбільш поширеним на сьогодні методом діагностики біліарного рефлюксу є ендоскопічний [1–5, 23].
Лікування хворих проводили згідно з Уніфікованим клінічним протоколом первинної медичної допомоги «Диспепсія», затвердженого Наказом МОЗ України № 600 від 03.08.2012 р. та рекомендаціями Консенсусу Маастрихт ІІІ (2005) і Маастрихт ІV (2010). На фоні дотримання дієтичних рекомендацій базисну терапію основного захворювання, що включала 10-денний курс трикомпонентної антигелікобактерної терапії, поєднували з двома препаратами синергічної дії, а саме прокінетиком метоклопрамідом та атиповим нейролептиком з прокінетичними властивостями сульпіридом, за аналогічним принципом в режимі короткочасної ступінчастої терапії [20, 21].
Для вирішення поставленого завдання запропоновано спосіб лікування ДГР у хворих на ХГ, який здійснювався таким чином: препарати спочатку призначають парентерально (внутрішньом’язово сульпірид по 2 мл (100 мг) на ніч 6 днів та паралельно метоклопрамід по 2 мл (10 мг) через 12 год — 5 днів) з подальшим переходом на прийом їх усередину протягом 14 днів (сульпірид по 1 капсулі (50 мг) двічі на добу і метоклопрамід по 1 таблетці (10 мг) три рази за 30 хв до прийому їжі). Загальна тривалість лікування — 20 днів. Саме існування двох лікарських форм цих прокінетиків (ін’єкційної і таблетованої) дозволяє проводити ступінчасту терапію, швидко і дієво коригуючи жовчний рефлюкс-синдром [20–21]. На завершення курсового лікування всім хворим проводилося контрольне ендоскопічне дослідження.
Оцінка ефективності ППЛ проводилася за такими критеріями: швидкість купірування больового синдрому; швидкість усунення основних клінічних проявів диспептичного синдрому за рахунок нормалізації моторики антродуоденальної зони (нудоти, блювання жовчю, відчуття переповнення шлунка, тяжкості у шлунку, дискомфорту в епігастрії, гіркоти у роті, відрижки, печії, здуття живота, зниження апетиту тощо); зникнення ендоскопічних ознак ДГР при контрольній ФЕГДС після проведеного курсового лікування.
Статистичну обробку отриманих результатів спостереження проводили згідно з алгоритмом статистичного аналізу даних, опису та надання якісних змінних [24–26] з використанням пакета програм MedCalc Software bvba, Ostend, Belgium, 1993–2019 [27].
У проведеному дослідженні аналізувалася частота прояву у хворих низки якісних показників (клінічних симптомів, синдромів та результати його лікування, ризик розвитку побічної дії від використання ППЛ), де змінна ознака має лише два значення — «так/ні», «є побічні ефекти/відсутні» тощо. Такі якісні дані, що аналізуються в медичних дослідженнях і мають лише два значення, називають бінарними або дихотомічними змінними [24, 25].
При описі якісних змінних бінарного типу для кожного значення вказували абсолютну величину, а також процентну частку ознаки у структурі всієї сукупності (точкова оцінка частоти прояву ознаки) з розрахунком інтервальної оцінки цієї величини — 95% довірчого інтервалу (95% ДІ, від англ. confidence interval) [24–27].
Для визначення впливу ППЛ на зміну частоти проявів основних клінічних синдромів на тлі зникнення ендоскопічних ознак біліарного рефлюксу застосовували непараметричний критерій Мак-Немара для пов’язаних (залежних) груп спостереження, у яких пацієнти виступають як власний контроль або в дослідженнях типу «до і після» [24–27].
Оцінка ризику побічної дії комбінації метоклопраміду та сульпіриду при лікуванні ДГР в комплексі з базисною терапією ХГ проводилася на підставі визначення рівня значимості 95% ДI для частки з урахуванням біномінального розподілу ознаки («наявність — відсутність ускладнення») [26].
Використання статистичного аналізу дало змогу підтвердити або відхилити прийняте рішення та сформулювати статистичні гіпотези. Для перевірки статистичних гіпотез сформульована нульова гіпотеза H0 [24–26]: запропонований спосіб лікування не є ефективним і безпечним.
Відповідно, альтернативною гіпотезою Ha, яка приймається у випадку відхилення нульової гіпотези, є така [24, 25]: запропонований спосіб лікування є ефективним і безпечним.
Для перевірки нульової гіпотези був використаний критерій Мак-Немара (для зв’язаних груп при описі результатів дослідження у парних спостереженнях — «до і після») [24, 25, 27].
Результати
Клінічно у хворих на ХГ з жовчним рефлюкс-синдромом відмічали три основні синдроми: прояви диспептичного синдрому (ДС) виявлені у 24 хворих ((80,0 ± 7,3) %; 95% ДI 51,26–119,03 %), абдомінального синдрому (АС) — у 13 осіб ((43,30 ± 9,04) %; 95% ДI 23,07–74,10 %), астеновегетативного синдрому (АвС) — у 18 осіб ((60,00 ± 8,94) %; 95% ДI 35,56–94,83 %).
Частота (%) розвитку основних клінічних симптомів при ДГР у хворих на ХГ наведена на рис. 1.
Проведена оцінка ефективності ППЛ при ДГР у комплексному лікуванні хворих на ХГ. Частота проявів основних клінічних синдромів у хворих оцінювалася до та після запропонованого способу лікування. Результати проведеного порівняння частот бінарних ознак у двох пов’язаних (залежних) групах спостереження (випадок парних спостережень) з використанням критерію Мак-Немара і точної вірогідності (біномінальний розподіл) подані у табл. 1 та на рис. 2.
При використанні нового способу лікування ДГР у хворих на ХГ у жодного пацієнта не виявлено побічного впливу ЛЗ. При розрахунках, які засновані на використанні нормального розподілу вибірки, це означає, що оцінка ризику побічної дії, як і 95% ДI, дорівнює нулю [26]. Але це суперечить здоровому глузду.
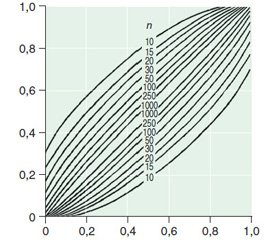
Саме тому проведені розрахунки 95% ДI для частки на підставі біномінального розподілу (рис. 3) [26], що дозволяє оцінити ризик побічного впливу ЛЗ. Для цього спочатку слід знайти на горизонтальній осі точку, яка відповідає вибірковій частці p (у даному випадку — нуль). Далі із цієї точки слід провести перпендикуляр до місць перетину з парою кривих, які відповідають числу об’єму вибірки. Вертикальні координати точок перетину і є межі 95% ДІ. У нашому випадку для n = 30 нижня межа ДІ — 0, а верхня — близько 0,12. Отже, з вірогідністю 95 % ми можемо стверджувати, що ризик розвитку побічної дії від використання ППЛ не перевищує 12 %.
Обговорення
Відомо, що одним із основних методів біостатистики при проведенні медичних досліджень є перевірка статистичних гіпотез [24, 25]. Для перевірки нульової гіпотези при порівнянні у вибірках, які пов’язані попарно (дослідження «до і після» лікування), використаний критерій Мак-Немара [24, 25, 27].
Аналіз ефективності запропонованого способу лікування проводили з урахуванням оцінки динаміки клінічних симптомів і синдромів та ендоскопічних змін в кінці лікування. Після призначення ППЛ в комплексі з базисною терапією ХГ у більшості пацієнтів на 2–3 день лікування відмічалися покращення самопочуття, апетиту, припинення блювання, зменшення гіркоти у роті, відрижки, нудоти, печії, а впродовж наступних декількох днів зменшення і дискомфорту, відчуття переповнення в шлунку та абдомінального болю, які до 5–7 дня суттєво зменшувалися і повністю зникали до 10–12 дня терапії. На завершення курсового 20-денного лікування клінічні прояви абдомінального синдрому повністю зникли у 97 % хворих, а симптоми диспептичного синдрому — відповідно у 93 % пацієнтів. Лише у трьох пацієнтів залишалися періодично виникаючі, незначні клінічні прояви жовчного рефлюкс-синдрому: у двох осіб спостерігалася відрижка повітрям, а в однієї — незначний дискомфорт в епігастрії. Інтенсивність проявів та частота розвитку залишкової симптоматики значно зменшилися. У кінці лікування у 90 % хворих ефект лікування оцінений як дуже хороший (повна відсутність симптомів), а у 10 % — як хороший (поліпшення симптомів).
Після проведеного лікування при контрольній ФЕГДС ендоскопічні ознаки ДГР та запальних змін СОШ (гіперемія, набряк СОШ, забарвлення вмісту шлунка у жовтий колір) повністю зникли в усіх хворих.
Відомо, що для визначення впливу лікування на зміну частоти прояву симптому чи синдрому застосовується непараметричний критерій Мак-Немара для пов’язаних вибірок (дослідження «до і після» лікування) [24, 25, 27]. Через 20 днів лікування ДГР у хворих на ХГ з використанням ППЛ виявлені статистично значимі зміни частоти проявів ДС, АС і АвС (відповідно двосторонні значення p < 0,0001; p = 0,0005 і p < 0,0001 за критерієм Мак-Немара). Це є свідченням того, що між цими двома пропорціями існує суттєва різниця [25, 27]. Проведений статистичний аналіз свідчить про ефективність запропонованого способу лікування ДГР у хворих на ХГ. Саме тому нульова статистична гіпотеза про відсутність клінічного ефекту ППЛ відкидається і приймається альтернативна гіпотеза [24, 25]: запропонований спосіб лікування є ефективним.
Швидке усунення основного симптомокомплексу клінічних проявів ДГР пов’язане з фармакологічними властивостями метоклопраміду і сульпіриду, оскільки останні є представниками однієї групи сучасних прокінетиків (антагоністів дофамінових рецепторів). Відомо, що центральним антидофаміновим ефектом сульпіриду вважають дію на дофамінергічні рецептори ОТ, зокрема, на пілоричну частину шлунка — він сприяє підвищенню тонусу пілоричного сфінктера, посилює і синхронізує (нормалізує) гастропілородуоденальну моторику, що спричиняє спорожнення шлунка та перешкоджає рефлюксу жовчі у шлунок [12].
Метоклопрамід уже більше 40 років використовувався в гастроентерології і набув почесного звання «робоча конячка прокінетиків». Він блокує центральні та периферичні D2-рецептори, стимулює вивільнення ацетилхоліну з постгангліонарних нервових закінчень, а також є агоністом 5-HT4- і антагоністом 5-HT3-рецепторів. Завдяки цим механізмам реалізуються прокінетичні ефекти препарату, переважно на рівні проксимальних відділів ОТ. Метоклопрамід знижує рухову активність стравоходу, підвищує тонус нижнього стравохідного сфінктера, поліпшує евакуацію їжі зі шлунка за рахунок підвищення тонусу його тіла та зростання фазової активності антрального відділу. Одночасно з цим розслаблюються верхні відділи тонкої кишки, запобігаючи розвитку ДГР та блюванню, прискорюється транзит по тонкій кишці [11].
На сьогодні через побічні ефекти використання метоклопраміду є обмеженим. Вираженість побічних ефектів за тривалого застосування перевищує позитивні прокінетичні й антиеметичні дії метоклопраміду та обмежує тривалість його прийому [11]. У 2017 році опубліковані дані про розвиток пізньої дискінезії, що пов’язано із кумулятивним впливом препарату в результаті тривалого його використання (більше 90 днів) [28].
Про доцільність і безпеку короткочасного призначення метоклопраміду як прокінетика при ФД свідчать результати метааналізу 27 клінічних досліджень (за період з 1951 по 2005 р.) японських авторів ще у 2007 році [17] та 25 РКД групи корейських авторів в 2017 р. [13].
На нашу думку, саме за рахунок їх синергічної дії як антагоністів дофамінових рецепторів і досягається потенціювання прокінетичного впливу. Саме це і забезпечує більш потужний вплив на зникнення симптомів ДГР та позитивно впливає на перебіг хвороби, оскільки дозволяє швидко та дієво усунути основні клінічні прояви жовчного рефлюкс-синдрому, сприяє стійкій і тривалій ремісії. Ефективність лікування ДГР підтверджена не лише суб’єктивними, а й ендоскопічними дослідженнями.
Отже, короткочасне призначення комбінації метоклопраміду та сульпіриду (ППЛ) в режимі ступінчастої терапії дозволяє прискорити редукцію основних клінічних проявів жовчного рефлюкс-синдрому, досягти клінічного й ендоскопічного одужання і, відповідно, суттєво скоротити потребу у тривалій терапії іншими ЛЗ.
У 2016–2017 рр. в літературі з’явилися публікації про можливість застосування ППЛ, зокрема призначення комбінації метоклопраміду та еритроміцину в інтенсивній терапії, за наявності затримки випорожнення шлунка при критичних захворюваннях [29, 30].
Переносимість застосування комбінації цих ЛЗ у всіх хворих була хорошою. Побічних ефектів ППЛ у пацієнтів не зареєстровано. На нашу думку, зменшення тривалості застосування метоклопраміду є ключовим моментом у мінімізації ризиків використання цього препарату у складі ППЛ, що узгоджується з результатами опублікованих метааналізів про доцільність та безпеку короткочасного призначення прокінетиків [13, 17]. З вірогідністю 95 % ми можемо стверджувати, що ризик розвитку побічної дії від використання ППЛ не перевищує 12 %.
Висновки
1. При лікуванні ДГР у хворих на ХГ короткочасне призначення комбінації метоклопраміду та сульпіриду в режимі ступінчастої терапії підвищує ефективність лікування: сприяє швидкому зникненню більшості клінічних проявів та ендоскопічних ознак жовчного рефлюкс-синдрому, що дозволяє істотно покращити загальний стан пацієнтів і поліпшити якість їх життя.
2. Синергізм дії сульпіриду та метоклопраміду при лікуванні ДГР та потенціювання їх прокінетичного впливу забезпечує більш потужний вплив на нормалізацію гастропілородуоденальної моторики, що дозволяє швидко та дієво усунути основний симптомокомплекс клінічних проявів жовчного рефлюкс-синдрому, досягти клінічного й ендоскопічного одужання, сприяє стійкій і тривалій ремісії.
3. Запропонований спосіб лікування є не лише ефективним, але й безпечним: з вірогідністю 95 % можна стверджувати, що ризик побічної дії ППЛ не перевищує 12 %.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів при підготовці даної статті.
1. Мазуренко Н.Н. Дуоденогастральный рефлюкс у детей: современный взгляд на проблему. Вестник ВГМУ. 2018. Т. 17, № 1. С. 23-33. doi.org/10.22263/2312-4156.2018.1.23.
2. Тельных Ю.В., Абгаджава Э.З., Коньков М.Ю. Билиарный рефлюкс-гастрит: этиология, патогенез и современные принципы терапии. Клин. мед. 2016. № 94(6). С. 454-457. DOI: 10.18821/0023-2149-2016-94-6-454-457 PMID: 30289664.
3. Галиев Ш.З., Амиров Н.Б. Дуоденогастральный рефлюкс как причина развития рефлюкс-гастрита. Вестник современной клин. медицины. 2015. Т. 8, вып. 2. С. 50-61. DOI: 10.20969/VSKM.2015.8(2).50-61.
4. Звягинцева Т.Д., Чернобай А.И. Дуоденогастральный рефлюкс в практике врача-гастроэнтеролога: очевидные опасности и скрытая угроза. Здоров’я України ХХІ сторіччя. 2012. Тематичний номер. № 1(23). С. 11.
5. Михайлусов С.В., Барт Б.Я., Михайлусова М.П., Николаева С.А. Дуоденогастральный рефлюкс (особенности клинического течения). Гастроэнтерология. Гепатология. Спецвыпуск. 2018. № 5. С. 28-34.
6. Mabrut J.Y., Collard J.M., Baulieux J. Le reflux biliaire duodéno-gastrique et gastro-œsophagien. Duodenogastric and gastroesophageal bile reflux. Journal de Chirurgie. 2006. Vol. 143, № 6. Р. 355-365. doi.org/10.1016/S0021-7697(06)73717-6.
7. Tatsugami М., Ito М., Tanaka S., Yoshihara M., Matsui H., Haruma K. et al. Bile acid promotes intestinal metaplasia and gastric carcinogenesis. Cancer Epidemiol. Biomarkers Prev. 2012. Vol. 21, № 11. Р. 2101-2107. DOI: 10.1158/1055-9965.EPI-12-0730. PMID: 23010643.
8. Matsuhisa Т., Arakawa Т., Watanabe Т., Tokutomi Т., Sakurai К., Okamura S. et al. Relation between bile acid reflux into the stomach and the risk of atrophic gastritis and intestinal metaplasia: a multicenter study of 2283 cases. Dig. Endosc. 2013. Vol. 25, № 5. Р. 519-525. DOI: 10.1111/den.12030. PMID: 23363381.
9. Кушниренко И.В., Майкова Т.В., Сиротенко И.А. Нарушения моторно-эвакуаторной функции желудка. Современные методы их коррекции при хроническом гастродуодените. Обзор и собственные исследования. Новости медицины и фармации. Гастроентерологія. 2011. № 382. С. 13-17.
10. Anderson S., Wilkinson-Prescriber М. Dyspepsia: recommended investigations and treatment. 2010. Vol. 21, № 18. P. 31-42. Wiley Online Library. URL: https://onlinelibrary.wiley.com/doi/abs/10.1002/psb.667. doi.org/10.1002/psb.667.
11. Бабак О.Я., Можина Т.Л. Прокінетичні препарати (від метоклопраміду до ітоприду) у клінічній практиці. Сучасна гастроентерологія. 2008. № 5(43). С. 4-11.
12. Губергриц Н.Б. Хроническая абдоминальная боль. Билиарная боль. Донецк: Лебедь, 2006. С. 68-72.
13. Yang Y.J., Bang C.S., Baik G.H. et al. Prokinetics for the treatment of functional dyspepsia: Bayesian network meta-analysis. BMC Gastroenterol. 2017. Vol. 17, № 1(83). Р. 2101-2107. DOI: 10.1186/s12876-017-0639-0 PMID: 28651565 PMCID: PMC5485548. URL: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5485548/.
14. Pittayanon R., Yuan Y., Bollegala N.P., Khanna R., Leontiadis G.I., Moayyedi P. Prokinetics for functional dyspepsia. Cochrane Database Syst. Rev. 2018. Oct 18. 10. CD009431. DOI:10.1002/14651858.CD009431.pub3. PMID: 30335201.
15. Pittayanon R., Yuan Y., Bollegala N.P. et al. Prokinetics for Functional Dyspepsia: A Systematic Review and Meta-Analysis of Randomized Control. Trials. Am. J. Gastroenterol. 2019. Vol. 114, № 2. P. 233-243. DOI: 10.1038/s41395-018-0258-6. PMID: 30337705.
16. Jan Tack, Karen Van den Houte, Florencia Carbone. The Unfulfilled Promise of Prokinetics for Functional Dyspepsia/Postprandial Distress Syndrome. The American Journal of Gastroenterology. 2019. Vol. 114, № 2. P. 204-206. DOI: 10.14309/ajg.0000000000000072. PMID: 30730856.
17. Hiyama T., Yoshihara М., Matsuo К. et al. Meta-analysis of the effects of prokinetic agents in patients with functional dyspepsia. J. Gastroenterol. Hepatol. 2007. Vol. 22, № 3. P. 304-310. DOI: 10.1111/j.1440-1746.2006.04493.x. PMID: 17295758.
18. Колюцкая Е.В. Роль сульпирида в лечении соматоформных расстройств. Медицинский совет. eLIBRARY ID: 30486852. 2017. № 17. Р. 20-24. https://elibrary.ru/item.asp?id=30486852. doi.org/10.21518/2079-701X-2017-17-20-24. URL: https://www.med-sovet.pro/jour/article/view/2143?locale=ru_RU.
19. Гуцаленко О.О., Катеренчук І.П., Сало Л.М. та ін. Терапевтична ефективність застосування еглонілу в комплексному лікуванні хворих з поєднаною патологією шлунково-кишкового тракту та психосоматичними розладами. Гастроентерологія: міжвідомчий збірник. Дніпропетровськ, 2005. Вип. 36. С. 617-622.
20. Спосіб лікування дуоденогастрального рефлюксу у хворих на хронічний гастрит: пат. 110408 України на корисну модель: МПК А61К 31/40 (2006.01), А61К 31/166 (2006.01), А61Р 1/04 (2006.01). Гуцаленко О.О.; заявник і власник патенту ВДНЗУ «Укр. мед. стомат. акад.»; заявл. 28.03.2016.; опубл. 10.10.2016, Бюл. № 19.
21. Гуцаленко О.О. Спосіб лікування дуоденогастрального рефлюксу у хворих на хронічний гастрит. Перелік наукової (науково-технічної) продукції, призначеної для впровадження досягнень медичної науки у сферу охорони здоров’я. 2018. Вип. 4. Реєстр. № 53/4/17. С. 58-60.
22. Haunton V., Boovalingam P., Lo N. Managing upper gastrointestinal disorders in older people. Prescriber. 2010. Wiley Online Library. URL: https://onlinelibrary.wiley.com/doi/abs/10.1002/psb.620. doi.org/10.1002/psb.620.
23. Lin J.K., Hu P.J., Li C.J. et al. A study of diagnosis of primary biliary reflux gastritis. Zhonghua Nei Ke Za Zhi. 2003. Vol. 42, № 2. P. 81-83. PMID: 12783700.
24. Реброва О.Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ Statistica. Москва: МедиаСфера, 2006. С. 134-184.
25. Гур’янов В.Г., Лях Ю.Є., Парій В.Д., Короткий О.В., Чалий О.В., Чалий К.О. та ін. Посібник з біостатистики. Аналіз результатів медичних досліджень у пакеті EZR (R-statistics): навч. посіб. Київ: Вістка, 2018. 208 с. С. 42-56, 73-80.
26. Стентон Гланц. Медико-биологическая статистика/пер. с англ. Ю.А. Данилова. Москва: Практика, 1998. С. 214-216.
27. MedCalc Statistical Software version 18.11.6 (MedCalc Software bvba, Ostend, Belgium; URL: https://www.medcalc.org; 2019).
28. Kaplan S., Staffa J.A., Dal Pan G.J. Duration of therapy with metoclopramide: a prescription claims data study. PDS. 2007. Vol. 16, № 8. P. 878-881. Wiley Online Library. URL: https://onlinelibrary.wiley.com/doi/abs/10.1002/pds.1397; doi.org/10.1002/pds.1397.
29. Taylor S.J., Allan K., McWilliam H., Manara A., Brown J., Greenwood R. et al. A randomised controlled feasibility and proof-of-concept trial in delayed gastric emptying when metoclopramide fails: We should revisit nasointestinal feeding versus dual prokinetic treatment. Achieving goal nutrition in critical illness and delayed gastric emptying: Trial of nasointestinal feeding versus nasogastric feeding plus prokinetics. Clinical nutrition ESPEN, 2016. Elsevier. Vol. 14. Р. 1-8. doi.org/10.1016/j.clnesp.2016.04.020.
30. Afshin Gholipour Baradari, Mohammad Reza Khajavi, Abolfazl Firouzian, Abbas Alipour, Hojatallah Daneshpour, Yunes Panahi et al. Effects of combined prokinetic administration on gastric emptying in critically ill patients. Arab. Journal of Gastroenterology. 2017. Vol. 18, № 1. Р. 30-34. doi.org/10.1016/j.ajg.2017.01.007.

/14-1.jpg)
/15-1.jpg)