Газета «Новости медицины и фармации» №5 (757), 2021
Вернуться к номеру
Клініко-патогенетичне значення ясенної мікробіоти при ревматоїдному артриті
Авторы: Синяченко О.В. , Єрмолаєва М.В., Гавілей Д.О., Лівенцова К.В., Верзілов С.М.
Донецький національний медичний університет, м. Лиман, Україна
Рубрики: Ревматология
Разделы: Клинические исследования
Версия для печати
Вступ
Поширеність ревматоїдного артриту (РА) серед населення земної кулі становить близько 1 %, а серед окремих популяцій людей сягає 5–7 % [1, 2]. При цьому показники занижені, оскільки не враховуються ранні (доманіфестні) форми захворювання [3].
Поки не вдалося довести зв’язок розвитку РА з тим або іншим конкретним етіологічним чинником, однак останні дані все більше змушують задуматися про роль мікробіому (мікробіоти) в даному процесі, у якому порожнина рота є одним із основних біотопів (зон рясного заселення мікроорганізмами) [4]. Було показано, що при РА вірогідно підвищується число випадків коморбідної інфекційної патології [5], а мікробіом може впливати на доклінічну фазу РА шляхом відхилень у складі мікрофлори (дисбіоз), діючи як мішень для дисрегуляції імунної системи організму [6]. У зв’язку з цим хворі на РА вимагають бактеріологічного дослідження порожнини рота, хоча можна виділити 600 видів бактерій, багато з яких не мають ніякого етіопатогенетичного значення [7].
Тригерними чинниками щодо розвитку РА можуть бути інфекції, пов’язані з протеєм і мікоплазмою [8], актиноміцети, кампілобактери, порфіромони, стрептококи та фузобактерії, але їх роль у генезі РА вивчена недостатньо [9–11]. Серед мікроорганізмів порожнини рота на найбільшу увагу заслуговують ясенні порфіромони, що здатні викликати дисрегуляцію місцевої імунної відповіді з подальшою стимуляцією дисбіозу [12, 13]. Проведена серія робіт із вивчення експресії ДНК бактерій пародонту в суглобовому лікворі пацієнтів з РА [14, 15]. Середня кількість виявлених видів ДНК бактерій у сироватці крові становила 6, а в синовії — 14, при цьому відзначені патогенетичні зв’язки саме з порфіромонами, хоча ці дані вимагають уточнення. Висунута гіпотеза, згідно з якою системна імунна відповідь при РА може бути недостатньою для запобігання поширенню окремих мікроорганізмів з порожнини рота, але це питання поки не вивчено [16].
Мета дослідження: визначити якісний і кількісний склад мікробіоти порожнини рота при РА, оцінити роль окремих бактерій у патогенетичних побудовах захворювання.
Матеріали та методи
Робота виконувалась відповідно до етичних норм, викладених в декларації Гельсінської медичної асамблеї, а пацієнти дали свою інформовану згоду на дослідження, затверджену комісією з біоетики Донецького національного медичного університету.
Обстежений 121 хворий на РА віком 18–76 років (в середньому 48,60 ± 1,12 року), серед яких було 19,0 % чоловіків і 81,0 % жінок. Тривалість РА від першої маніфестації захворювання становила 2–30 років (в середньому 9,8 ± 0,7 року). Серопозитивність РА за ревматоїдним фактором (RF) у крові становила 81,0 %, а за антитілами до цитрулінового циклічного пептиду (аССР) — 75,2 %. Частоту загальної активності захворювання (AAG) І, ІІ і ІІІ ступеня констатовано у 13,2, 44,6 і 42,2 % хворих відповідно, а співвідношення I, II, III і IV стадій (ARC) патологічного процесу становило 1 : 5 : 5 : 3. Пародонтит І, ІІ і ІІІ ступеня тяжкості відзначено в 35,4, 36,7 та 27,9 % випадків відповідно.
Системний остеопороз діагностовано у 77,7 % від числа обстежених пацієнтів, індекс активності артриту (DAS) становив 4,9 ± 0,1 відн.од., індекс прогресування артриту (PAI) — 1,90 ± 0,21 відн.од., індекс Лансбурі — 150,30 ± 6,08 бала, індекс тяжкості перебігу хвороби (SAI) — 94,70 ± 2,07 відн.од., остеопорозний рентгенологічний показник Барнетта — Нордіна (BNI) — 41,70 ± 0,45 × 102 відн.од., денситометричний мінеральної щільності кістки (BMD) — 1,70 ± 0,06 SD, рівень в крові RF — 14,70 ± 1,97 мОд/мл, aCCP — 26,10 ± 1,17 Од/мл, С-реактивного протеїну (СRP) — 16,70 ± 0,75 мг/л, фібриногену (FG) — 8,40 ± 0,36 г/л, інтерлейкіну 1b (IL-1b) — 12,30 ± 0,60 пг/мл, туморонекротичного фактора a (TNF-a) — 57,70 ± 4,33 пг/мл. Тяжкість перебігу патології пародонту, ясен і зубів за індексом Рассела становила 3,190 ± 0,302 бала, індексом Рамферда — 3,150 ± 0,211 бала, індексом Сільнесса — Лое — 1,450 ± 0,102 бала і потреби в лікуванні пародонту — 2,900 ± 1,138 бала, а їх усереднений показник характеризував інтегральний індекс тяжкості пародонтиту (SPII), що дорівнював 3,010 ± 0,380 бала.
При дослідженні мікробіому слизової оболонки ясен у контексті аеробної (факультативно-анаеробної) і анаеробної флори використовували тіогліколеве живильне середовище з додаванням агару «Діфко», крові та дріжджового гідролізату, застосовували набори «Мікро-Ла-Тест», «СТРЕПТОтест 16», «АНАЕРОтест 23», «НЕФЕРМтест 24». Імуноферментним методом (рідер «PR2100 Sanofi diagnostic pasteur», Франція) досліджували вміст у крови аССР і прозапальних цитокінів (IL-1b і TNF-a), а рівні в сироватці крові RF, СRP і FG — за допомогою аналізатора «Olympus-AU-640» (Японія). Як конт–роль були вивчені лабораторні показники 30 практично здорових людей (11 чоловіків і 19 жінок) віком від 18 до 62 років (в середньому 36,50 ± 0,41 року).
Всім хворим виконували рентгенологічне дослідження зубів, міжзубних альвеолярних перегородок (внутрішньоротова прицільна рентгеноортопантографія) та суглобів («Multix-Compact-Siеmens», Німеччина), ультразвукове опорно-рухового апарату («Envisor-Philips», Нідерланди) та двохенергетичну рентгенівську остеоденситометрію («QDR-4500-Delphi-Hologic», США). Оцінювали периферичний метакарпальний індекс Барнетта — Нордіна (BNI) та індекс мінеральної щільності кістки (BMD).
Статистична обробка результатів досліджень проведена за допомогою комп’ютерних програм Microsoft Excel і Statistica-Stat-Soft (США). Аналізували середні значення показників (M), їх стандартні похибки (SE) й відхилення (SD), коефіцієнти параметричної кореляції Пірсона (r) та непараметричної Кендалла (t), критерії дисперсії (D), однорідності дисперсії Брауна — Форсайта (BF), багатофакторного аналізу Вілкоксона — Рао (WR) та відмінностей Стьюдента (t), а такоже вірогідность статистичних показників (р).
Результати
Вегетацію аеробів виявлено на яснах у 96,7 % хворих на РА, а анаеробів — у 91,7 %. Середній ступінь мікробного пейзажу (бакчисло) становив 3,840 ± 0,154 од., причому аеробів — 2,400 ± 0,109 од., а анаеробів — 1,450 ± 0,078 од. За даними багатофакторного дисперсійного аналізу Вілкоксона — Рао, на інтегральне дзеркало ясенної мікробіоти при РА впливають вік хворих (WR = 8,63, p < 0,001), показник AAG (WR = 5,88, p < 0,001) і серопозитивність захворювання за аССР (WR = 3,39, p = 0,004).
Як бачимо на рис. 1, серед аеробів частота обсіменіння порожнини рота стрептококами становила 52,1 %, коринебактеріями — 37,2 %, стафілококами — 29,8 %, аерококами і нейсеріями — 16,5 %, кандидами — 15,7 %, ентерококами — 13,9 %, ємелами — 13,2 %, фекальним лугоутворювачем та кишковою паличкою — 9,9 %, моракселами та псевдомонами — 8,3 %, протеєм — 6,6 %. Щодо окремих анаеробів: актиноміцети констатовані в 32,2 %, біфідобактерії — в 24,0 %, пептострептококи — в 23,1 %, бактероїди та сарцини — в 14,1 %, пропіонібактерії — в 10,7 %, еубактерії та фузобактерії — в 8,3 %, клостридії — в 7,4 %, мегасфери — в 2,5 %.
Існують дисперсійні зв’язки з наявністю системного остеопорозу обсіменіння ясен хворих на РА аерококами (D = 5,87, p = 0,007), фекальним лугоутворювачем (D = 5,35, p = 0,022) і еубактеріями (D = 4,34, p = 0,039), з позасуглобовими ознаками захворювання — наявністю ентерококів (D = 7,19, p = 0,008), нейсерій (D = 4,61, p = 0,034), фузобактерій (D = 4,55, p = 0,035) і мегасфер (D = 6,36, p = 0,013), із серопозитивністю за аССР — ентерококів (D = 7,54, p = 0,006) і кишкової палички (D = 4,48, p = 0,036).
Наявність коморбідного пародонтиту чинить вірогідний вплив на характер мікробного пейзажу ротової порожнини у хворих на РА, причому це стосується як аеробів (WR = 8,15, p < 0,001), так і анаеробів (WR = 3,87, p = 0,004), про що свідчить багатофакторний аналіз Вілкоксона — Рао. Однофакторний дисперсійний аналіз демонструє зв’язок з пародонтитом наявності вегетацій на яснах фекального лугоутворювача (D = 7,40, p = 0,008), коринебактерій (D = 4,62, p = 0,034), кишкової палички (D = 7,49, p = 0,008), мораксел (D = 5,99, p = 0,016), протея (D = 4,65, p = 0,033), псевдомонів (D = 5,99, p = 0,016), стрептококів (D = 19,80, p < 0,001), клостридій (D = 5,31, p = 0,023), пропіонібактерій (D = 4,80, p = 0,030) і бактероїдів (D = 11,33, p = 0,001).
На рис. 2 подана залежність від ясенної мікробіоти інтегрального параметра SPII. Встановлений зв’язок із вегетаціями стрептокока (D = 4,45, p = 0,001), мораксел (D = 4,06, p = 0,002), сарцинів (D = 3,08, p = 0,010) й еубактерій (D = 2,90, p = 0,014). Необхідно відзначити, що мали місце прямі дисперсійно-кореляційні зв’язки SPII з мікробним числом аеробів (D = 2,73, p = 0,019; r = +0,323, p = 0,004), але не анаеробів.
Обговорення
За даними аналізу однорідності дисперсії Брауна — Форсайта, аероби в порожнині рота впливають на показники AAG (BF = 3,80, p = 0,025) і RF (BF = 1,76, p = 0,026), як свідчить кореляційний аналіз Пірсона, існують різноспрямовані взаємозв’язки ясенного мікробного числа з параметрами SAI (r = 0,287, p = 0,026) і остеопорозного BNI (r = –0,333, p = 0,009). Рівень анаеробів впливає на параметри AAG (BF = 4,50, p = 0,013), індекс Лансбурі (BF = 2,40, p = 0,002), BMD (BF = 5,00, p = 0,008) і IL-1b (BF = 3,17, p = 0,001), при цьому прямі кореляційні зв’язки стосуються AAG (r = +0,414, p = 0,001), SAI (r = +0,292, p = 0,024), BMD (r = +0,317, p = 0,014), aCCP (r = +0,256, p = 0,049) і FG (r = +0,344, p = 0,007), а обернений — BNI (r = –0,300, p = 0,020). Слід зазначити, що у пацієнтів з РА частота пародонтиту приблизно в 2–4 рази вища, ніж у популяції [17], а його перебіг більш агресивний [18]. Чинником ризику запалення пародонту є також експериментальний артрит на моделях у тварин [19]. Необхідно відзначити і обернений зв’язок обох захворювань, коли пародонтит сприяє виникненню і прогресуванню РА [20].
На сьогодні розвивається так звана концепція пародонт-асоційованого РА, якою намагаються пояснити причинну роль патобіонтів пародонту в ініціюванні суглобової патології [21, 22]. Вже доведений факт, що пародонтит посилює несприятливий перебіг РА через додаткову продукцію прозапальних ферментів своїми патогенами, які цитрулюють білки [23, 24]. РА і пародонтит пов’язані з загальними імунозапальними реакціями дисбалансу патогенетичних побудов обох захворювань [25, 26]. Вони мають схожу остеоклазію, алельні гени та спільний дисбаланс стану цитокінової мережі [27–29].
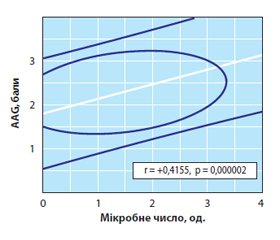
Треба підкреслити, що наявність анаеробів у яснах хворих на РА з коморбідним пародонтитом не відрізняється збільшенням середніх показників AAG та BMD. На рис. 3 і 4 знайшли своє відображення прямі кореляції AAG й BMD з числом ясенних анаеробів. Після статистичної обробки отриманих результатів дослідження (варіаційний, дисперсійний і кореляційний аналіз) встановлено, що мікробне число анаеробів при пародонтиті у хворих РА в яснах ≥ 3 (≥ M + 2SD хворих) відображає високий ступінь активності основного захворювання (рівень прогнозування пропонованого результату моделі становить 86,7 %). На рис. 5 подані тривимірні гістограми інтегральних параметрів тяжкості перебігу суглобового синдрому при РА (DAS + PAI + SAI) з наявністю в порожнині рота аеробів та анаеробів. Виявилося, що ці дві групи між собою не відрізняються.
Встановлений вірогідний вплив вегетацій у яснах пептострептококів на показник DAS (D = 2,92, p = 0,037), нейсерій і клостридій — на SAI (відповідно D = 1,78, p = 0,031 і D = 2,03, p = 0,011), мораксел — на аССР (D = 1,68, p = 0,003). Ми відібрали ті показники ясенної мікробіоти, рівень яких одночасно мав вірогідні прямі зв’язки з параметрами перебігу РА за критерієм однорідності дисперсії Брауна — Форсайта й непараметричної кореляції Кендалла. До таких належав зв’язок AAG і RF c протеєм (відповідно BF = 8,84, p = 0,001; t = +0,175, p = 0,005 і BF = 2,08; t = +0,157, p = 0,011), ARS з ентеро–коками (BF = 2,11, p = 0,007; t = +0,135, p = 0,028), BNI з аерококами (BF = 3,24, p = 0,043; t = +0,159, p = 0,010), CRP з псевдомонами (BF = 2,38, p = 0,005; t = +0,150, p = 0,015) та еубактеріями (BF = 2,53, p = 0,003; t = +0,196, p = 0,002).
За даними літератури, 80–90 % від числа хворих на РА в пародонтальних каналах мають вегетації хоча б однієї з наступних бактерій: порфіромонів, актиноміцетів, преводел, пептострептококів і кампілобактерів [16]. Встановлено, що в таких пацієнтів збільшується частота постійного носійства в порожнині рота преводел і селеномонів [19]. При цьому доведено підвищення параметрів антибактеріальних антитіл у синовіальній рідині [14]. Існує гіпотеза, згідно з якою механізм резорбції кістки при пародонтиті лежить в основі прогресування суглобових ерозій у хворих на РА [30].
Рентгеносонографічні ознаки суглобової патології та періартикулярні прояви РА не були пов’язані з наявністю в порожнині рота актиноміцетів, бактероїдів, біфідобактерій, ємел, кишкової палички, коринебактерій, мораксел, нейсерій, пептострептококів, протея, псевдомонів, стафілококів, стрептококів, фекального лугоутворювача та ентерококів. За даними дисперсійно-кореляційного аналізу, патогенетичний зв’язок із сарцинами стосувався розвитку асептичного остеонекрозу (D = 7,04, p = 0,009; t = +0,236, p < 0,001), тендовагінітів (D = 4,08, p = 0,046; t = +0,182, p = 0,003) і периферичної нейропатії (D = 3,98, p = 0,048; t = +0,206, p = 0,001), з еубактеріями — інтраартикулярних тіл Штайді (D = 7,23, p = 0,008; t = +0,238, p < 0,001), кіст Бейкера (D = 5,91, p = 0,017; t = +0,218, p < 0,001), тендовагінітів (D = 4,27, p = 0,041; t = +0,186, p = 0,003) і ентезопатій (D = 7,09, p = 0,009; t = +0,237, p < 0,001). Крім того, формування остеоузур виявилося залежним від вегетацій кандид (D = 5,01, p = 0,027; t = +0,201, p = 0,001), асептичного остеонекрозу — мегасфер (D = 30,77, p < 0,001; t = +0,453, p < 0,001), тіл Штайді — пропіонібактерій (D = 14,57, p < 0,001; t = +0,330, p < 0,001), тендовагінітів — аерококів (D = 4,21, p = 0,042; t = +0,181, p = 0,004), моно- і поліневритів — клостридій (D = 6,32, p = 0,013; t = +0,126, p = 0,040). Підкреслимо, що з характером мікробіоти порожнини рота не був пов’язаний розвиток епіфізарного остеопорозу, остеокістозу, лігаментозу, артрокальцинатів, змін рогів менісків, а також депозиції в порожнині суглобів хондральних тіл і тіл Гоффа.
Висновки
Вегетація асоціацій аеробів на яснах виявлена у 97 % від числа хворих, анаеробних бактерій — у 927 %, число яких тісно пов’язане з клінічними, лабораторними та рентгеносонографічними ознаками РА, при цьому на інтегральний пейзаж ясенної мікробіоти діє тяжкість перебігу коморбідного хронічного генералізованого пародонтиту, що впливає на наявність у порожнині рота мораксел, сарцинів, стрептококів та еубактерій, причому кількість анаеробів відображає ступінь активності РА і мінеральну щільність кістки, а в патогенетичних побудовах окремих ознак захворювання беруть участь аерококи, кандиди, клостридії, мегасфери, пропіонібактерії, сарцини, фузобактерії й еубактерії.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів. Автори не отримували від окремих осіб і організацій фінансової підтримки дослідження, гонорарів та інших форм винагороди.
Інформація про внесок кожного спів–автора: Синяченко О.В. — дизайн, концепція дослідження і написання тексту; Єрмолаєва М.В. — статистична обробка матеріалу, виконання ілюстрацій; Гавілей Д.О. — стоматологічне обстеження хворих; Лівенцова К.В. — ревматологічне обстеження хворих; Верзілов С.М. — аналіз даних літератури за проблемою.
Список литературы
Список літератури знаходиться в редакції

/14_m.jpg)
/15_m.jpg)