Международный неврологический журнал Том 19, №6, 2023
Вернуться к номеру
Вплив вираженості поліневропатії на нервову провідність та больовий синдром у пацієнтів із цукровим діабетом типу 2
Авторы: Сабовчик А.Я. (1, 2), Орос М.М. (1)
(1) — ДВНЗ «Ужгородський національний університет», медичний факультет, м. Ужгород, Україна
(2) — КНП «Закарпатська обласна клінічна лікарня ім. А. Новака» ЗОР, м. Ужгород, Україна
Рубрики: Неврология
Разделы: Клинические исследования
Версия для печати
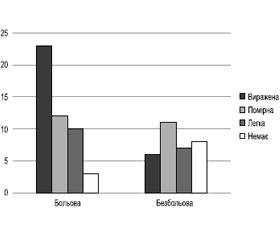
Актуальність. Стаття присвячена дослідженню зв’язку між показниками нервової провідності та вираженістю поліневропатії у пацієнтів з цукровим діабетом типу 2. Вивчено вплив рівня вираженості поліневропатії на нервову провідність, а також розглянуто вплив інсулінотерапії на ці показники. Мета: визначити вплив вираженості поліневропатії та потреби в додатковому введенні інсуліну у пацієнтів із цукровим діабетом типу 2 на показники нервової провідності та розвиток больового синдрому. Матеріали та методи. Обстежено 80 пацієнтів з цукровим діабетом типу 2, серед них 49 чоловіків та 31 жінка. Усім досліджуваним пацієнтам проведено загальноклінічні та біохімічні лабораторні дослідження для оцінки кровотворної системи, печінки, нирок, жирового та вуглеводного обміну. За рівнем С-пептиду визначалась потреба в інсулінотерапії. Для верифікації діагнозу діабетичної поліневропатії оцінювали скарги, дані клінічного огляду та інструментального обстеження. Бралися до уваги основні показники нервової провідності при визначенні поліневритичних розладів, а саме: рeroneal motor nerve conduction velocity (PMNCV), sensory nerve action potential (SNAP) литкового нерва, sensory nerve conduction velocity (SNCV) литкового нерва. Результати. Було виявлено залежність показників нервової провідності від ступеня вираженості поліневропатії, показник моторної провідності PMNCV був найнижчим у групі із вираженою поліневропатією. Також була встановлена залежність рівня сенсорних показників SNAP та SNCP від вираженості поліневропатії, швидкість нервової провідності зменшується при більшій її вираженості. Встановлено вплив вираженості поліневропатії на больову чи безбольову форму. Серед пацієнтів із вираженою поліневропатією частіше спостерігалася больова форма. Не було встановлено взаємозв’язку між впливом потреби в інсулінотерапії на больову чи безбольову форму поліневропатії. Висновки. Показники нервової провідності залежать від ступеня вираженості поліневропатії. Наявність та вираженість больового синдрому прямо залежить від вираженості поліневропатії. Потреба у додатковому введенні інсуліну впливає на сенсорні показники, проте не має впливу на розвиток больової форми поліневропатії.
Background. The article examines the relationship between nerve conduction indicators and polyneuropathy severity in patients with type 2 diabetes. The influence of polyneuropathy severity on nerve conduction was studied, as well as the effect of insulin therapy on these indicators. Objective: to determine the influence of polyneuropathy severity and the need for additional insulin administration in patients with type 2 diabetes on nerve conduction indicators and the development of pain syndrome. Materials and methods. Eighty patients with type 2 diabetes were examined, 49 men and 31 women. All of them underwent general clinical and biochemical laboratory tests to evaluate the hematopoietic system, li-ver, kidneys, fat and carbohydrate metabolism. The need for insulin therapy was assessed by the C-peptide level. To verify the diagnosis of diabetic polyneuropathy, complaints, clinical and instrumental examination data were evaluated. The main indicators of nerve conduction were taken into account when determining polyneuritis disorders, namely: рeroneal motor nerve conduction velocity, sensory nerve action potential of the sural nerve, sensory nerve conduction velocity of the sural nerve. Results. A dependence of nerve conduction on polyneuropathy severity was revealed, рeroneal motor nerve conduction velocity was the lowest in the group with severe polyneuropathy. A correlation was also found between the levels of sensory indicators (sensory nerve action potential and sensory nerve conduction velocity) and polyneuropathy severity, nerve conduction velocity decreases with an increase in the latter. The influence of polyneuropathy severity on the painful or painless form has been found. Among patients with severe polyneuropathy, the painful form was observed more often. No relationship was found between the need for insulin therapy and the painful or painless form of polyneuropathy. Conclusions. Indicators of nerve conduction depend on polyneuropathy severity. The presence and severity of pain syndrome directly depends on polyneuropathy severity. The need for additional insulin administration affects sensory indicators but has no effect on the development of the painful form of polyneuropathy.
цукровий діабет; діабетична поліневропатія; нервова провідність; інсулінозалежність
diabetes; diabetic polyneuropathy; nerve conduction; insulin dependence