Журнал «Почки» Том 13, №1, 2024
Вернуться к номеру
Гіпергомоцистеїнемія — ризик-фактор судинних ускладнень у хворих на хронічну хворобу нирок
Авторы: Палієнко І.А. (1), Карпенко О.В. (1), Красюк І.В. (1), Кравчук А.Д. (2), Миколаєнко Ю.В. (2), Руденко О.А. (1)
(1) - Національний медичний університет імені О.О. Богомольця, м. Київ, Україна
(2) - КНП «Київський міський центр нефрології та діалізу», м. Київ, Україна
Рубрики: Нефрология
Разделы: Справочник специалиста
Версия для печати
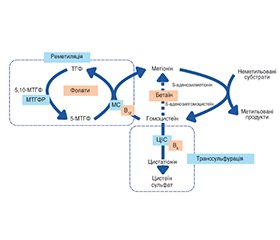
Гіпергомоцистеїнемія вважається фактором ризику багатьох захворювань, включно із судинним тромбозом. У пацієнтів з хронічною хворобою нирок часто виникають судинні ускладнення у вигляді артеріальних або венозних тромбозів, а врахування рівня гомоцистеїну в крові як предиктора тромбофілії є важливим. Причинами гіпергомоцистеїнемії можуть бути як генетичні мутації, так і дефіцит ферментів метаболізму гомоцистеїну, а також дефіцит фолієвої кислоти, вітаміну В12 і, меншою мірою, дефіцит вітаміну В6, який впливає на метаболізм метіоніну. З огляду на роль гіпергомоцистеїнемії як предиктора серцево-судинних подій у хворих із захворюваннями нирок, на нашу думку, мультифакторність підвищення гомоцистеїну потребує подальшого дослідження окремих ланок його патогенезу при хронічній хворобі нирок та розробки цілеспрямованих терапевтичних втручань.
Hyperhomocysteinemia is considered a risk factor for many diseases, including thrombosis. Patients with chronic kidney disease often have vascular complications in the form of arterial or venous thrombosis, and it is important to consider the blood homocysteine level as a predictor of thrombophilia. The causes of hyperhomocysteinemia can be both genetic mutations and deficiency of homocysteine metabolism enzymes, as well as deficiency of folic acid, vitamin B12 and, to a lesser extent, deficiency of vitamin B6, which affects methionine metabolism. Given the role of hyperhomocysteinemia as a predictor of cardiovascular events in patients with kidney diseases, in our opinion, the multifactorial nature of increased homocysteine requires further research into some links of its pathogenesis in chronic kidney disease and the development of targeted therapeutic interventions.
гомоцистеїн, хронічна хвороба нирок, гіпергомоцистеїнемія, тромбоз
homocysteine; chronic kidney disease; hyperhomocysteinemia; thrombosis
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- González-Lamuño D, Arrieta-Blanco FJ, Fuentes ED, et al. Hyperhomocysteinemia in Adult Patients: A Treatable Metabolic Condition. Nutrients. 2023 Dec 30;16(1):135. doi: 10.3390/nu16010135.
- Habib SS, Al-Khlaiwi T, Almushawah A, Alsomali A, Habib SA. Homocysteine as a predictor and prognostic marker of atherosclerotic cardiovascular disease: a systematic review and meta-analysis. Eur Rev Med Pharmacol Sci. 2023 Sep;27(18):8598-8608. doi: 10.26355/eurrev_202309_33784.
- Muzaffar R, Khan MA, Mushtaq MH, et al. Hyperhomocysteinemia as an Independent Risk Factor for Coronary Heart Disease. Comparison with Conventional Risk Factors. Braz J Biol. 2021 Sep 6;83:e249104. doi: 10.1590/1519-6984.249104.
- Zaric BL, Obradovic M, Bajic V, Haidara MA, Jovanovic M, Isenovic ER. Homocysteine and Hyperhomocysteinaemia. Curr Med Chem. 2019;26(16):2948-2961. doi: 10.2174/0929867325666180313105949.
- Esse R, Barroso M, Tavares de Almeida I, Castro R. The Contribution of Homocysteine Metabolism Disruption to Endothelial Dysfunction: State-of-the-Art. Int J Mol Sci. 2019 Feb 17;20(4):867. doi: 10.3390/ijms20040867.
- Paradkar MU, Padate B, Shah SAV, Vora H, Ashavaid TF. Association of Genetic Variants with Hyperhomocysteinemia in Indian Patients with Thrombosis. Indian J Clin Biochem. 2020 Oct;35(4):465-473. doi: 10.1007/s12291-019-00846-9.
- Domi E, Hoxha M, Hoxha B, Zappacosta B. The Interaction between Arachidonic Acid Metabolism and Homocysteine. Endocr Metab Immune Disord Drug Targets. 2021;21(7):1232-1241. doi: 10.2174/1871530320999200904130504.
- Al-Shabrawey M, Elmarakby A, Samra Y, et al. Hyperhomocysteinemia dysregulates plasma levels of polyunsaturated fatty acids-derived eicosanoids. Life Res (Auckl). 2022 Apr;5(2):14. doi: 10.53388/2022-0106-103.
- Chen W, Feng J, Ji P, Liu Y, Wan H, Zhang J. Association of hyperhomocysteinemia and chronic kidney disease in the general population: a systematic review and meta-analysis. BMC Nephrol. 2023 Aug 23;24(1):247. doi: 10.1186/s12882-023-03295-y.
- Bhalla AK, Bhargava V, Meena P, Bhoiyar A, Yadav A, Rana DS. Bilateral Acute Renal Infarction Secondary to Methylene Tetrahydrofolate Reductase A1298C and PAI-1 Mutation. Indian J Nephrol. 2020 Sep-Oct;30(5):326-328. doi: 10.4103/ijn.IJN_65_20.
- ALSolami AA, Almalki AA, Alhedyan SY, et al. Plasma Homocysteine Levels and Cardiovascular Events in Patients With End-Stage Renal Disease: A Systematic Review. Cureus. 2023 Jun 13;15(6):e40357. doi: 10.7759/cureus.40357.
- Schiavi C, Marri L, Negrini S. Arterial thrombosis triggered by methotrexate-induced hyperhomocysteinemia in a systemic lupus erythematosus patient with antiphospholipid antibodies. Thromb J. 2023 Nov 3;21(1):113. doi: 10.1186/s12959-023-00557-5.