Архив офтальмологии Украины Том 12, №2, 2024
Вернуться к номеру
Ефективність нових двохетапних методів хірургічного і лазерного лікування первинної відкритокутової глаукоми в поєднанні з катарактою
Авторы: Могілевський С.Ю. (1, 2), Романюк А.В. (1, 2)
(1) - Національний університет охорони здоров’я України імені П.Л. Шупика, м. Київ, Україна
(2) - Офтальмологічний центр «Новий Зір», м. Київ, Україна
Рубрики: Офтальмология
Разделы: Клинические исследования
Версия для печати
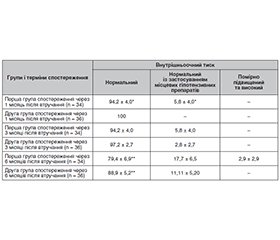
Актуальність. Зниження внутрішньоочного тиску є єдиним доведеним методом сповільнення прогресування глаукомної оптиконейропатії. Успішно проведене консервативне лікування або хірургічне втручання не гарантує збереження полів зору протягом усього життя. Незважаючи на сучасні досягнення консервативного лікування первинної відкритокутової глаукоми (ПВКГ), близько 5,3 % пацієнтів все ще потребують хірургічного або комбінованого втручання. Досі не існує консенсусу щодо підходів до лікування пацієнтів з глаукомою в поєднанні з катарактою. Мета: дослідити ефективність нових двохетапних методів хірургічного і лазерного лікування первинної відкритокутової глаукоми в поєднанні з катарактою. Матеріали та методи. Всього було залучено в дослідження 70 пацієнтів (70 очей) з первинною відкритокутовою глаукомою I–IV стадій та ускладненою катарактою, які становили 2 групи спостереження. Усім пацієнтам проведене двохетапне лікування — мікроімпульсна транссклеральна циклофотокоагуляція (МІ-ТСЦФК) та факоемульсифікація катаракти з імплантацією гнучкої монофокальної інтраокулярної лінзи (ІОЛ). Першу групу (n = 34) становили пацієнти, яким була виконана факоемульсифікація катаракти з імплантацією ІОЛ першим етапом та через 1 місяць МІ-ТСЦФК другим етапом. Другу групу (n = 36) — пацієнти, яким була виконана МІ-ТСЦФК першим етапом та через 1 місяць факоемульсифікація катаракти з імплантацією ІОЛ. Ці групи статистично не відрізнялися за віком, статтю, вихідним рівнем внутрішньоочного тиску (ВОТ) та стадією ПВКГ. Первинним критерієм успіху двохетапного методу була нормалізація ВОТ з використанням антиглаукомних препаратів або без нього за відсутності необхідності проведення повторних лазерних, а також фістулізуючих втручань через 1, 3 та 6 місяців. Вторинним та кінцевим критерієм успіху була стабілізація або розширення полів зору при оцінці після другого етапу через 1, 3 та 6 місяців. Результати. Середній рівень внутрішньоочного тиску з використанням місцевих антигіпертензивних препаратів перед початком втручання в першій групі становив 27,5 ± 1,3 мм рт.ст., в другій групі — 27,0 ± 1,1 мм рт.ст. Через 1 місяць після другого етапу у пацієнтів першої групи ВОТ був нормалізований на 94,2 % очей та ще на 5,8 % очей із застосуванням місцевих гіпотензивних препаратів, у другій групі на 100 % очей ВОТ був нормальним без застосування гіпотензивних препаратів (p < 0,05). Через 3 та 6 місяців кращі гіпотензивні результати були у другій групі спостереження, але це було статистично незначимо. Межі поля зору були збережені на доопераційному рівні або розширилися у пацієнтів першої та другої груп через 1 місяць після втручання на 91,2 та 97,2 % очей відповідно, через 3 місяці — на 91,2 та 97,2 % очей відповідно, через 6 місяців — на 88,2 та 94,4 % очей відповідно. У другій групі отримані кращі функціональні результати на всіх термінах, але статистично це було незначимо. Висновки. Проведені дослідження встановили високу ефективність та безпечність нових двохетапних методів хірургічного і лазерного лікування ПВКГ в поєднанні з катарактою у термін спостереження 6 місяців. Була встановлена тенденція до більшої ефективності методу, коли першим етапом виконувалася МІ-ТСЦФК, а другим — факоемульсифікація катаракти з імплантацією ІОЛ. Характер та частота операційних і післяопераційних ускладнень в обох групах не відрізнялися.
Background. Lowering the intraocular pressure (IOP) is the only proven method to slow the progression of glaucomatous optic neuropathy. Successful conservative treatment or surgery do not guarantee the preservation of visual fields throughout life. Despite the current advances in conservative treatment of primary open-angle glaucoma, about 5.3 % of patients still require surgical or combined treatment. There is no consensus yet on approaches to the treatment of patients with glaucoma and cataract. The objective was to evaluate the effectiveness of new two-stage methods for surgical and laser treatment of patients with primary open-angle glaucoma associated with cataract. Materials and methods. Seventy patients (70 eyes) with primary open-angle glaucoma stages I–IV complicated by cataract were included in this study. There were two observation groups. All patients received a two-stage treatment — micropulse transscleral cyclophotocoagulation (MP-TSCPC) and phacoemulsification with a monofocal intraocular lens (IOL) implantation. The first group (n = 34) included participants who underwent phacoemulsification with IOL implantation (stage 1) one month prior to MP-TSCPC (stage 2). The second group (n = 36) consisted of patients who underwent MP-TSCPC (stage 1) and phacoemulsification with IOL implantation a month after (stage 2). These groups did not statistically differ in terms of age, gender, baseline IOP, and stage of primary open-angle glaucoma. The primary outcome measure was the normalization of IOP with or without the use of antiglaucoma medications and without a need for further laser and incisional procedures in 1, 3 and 6 months. The secondary outcome was stabilization or expansion of visual fields when evaluating 1, 3, and 6 months after stage 2. Results. The average IOP level with antihypertensive medications before the treatment in group 1 was 27.5 ± 1.3 mmHg, in group 2 — 27.0 ± 1.1 mmHg. One month after the treatment, patients of group 1 had normal IOP in 94.2 % of eyes and in 5.8 % of eyes with local antihypertensive medications; in group 2, IOP was normal in 100 % of eyes without antiglaucoma medications (p < 0.05). In 3 and 6 months, better hypotensive results were in group 2, but outcomes were not statistically significant. The visual fields were preserved at the preoperative level or expanded in patients from groups 1 and 2 one month after the treatment in 91.2 and 97.2 % of the eyes, respectively, 3 months after — in 91.2 and 97.2 %, 6 months after — in 88.2 and 94.4 % of the eyes, respectively. In group 2, better functional results were obtained at all time points, but it was not statistically significant. Conclusions. The studies have established a high efficacy and safety of new two-stage methods for surgical and laser treatment of patients with primary open-angle glaucoma and cataract with a follow-up period of 6 months. There was a tendency to greater efficacy of the method, where MP-TSCPC as stage 1 was followed by phacoemulsification with IOL implantation as stage 2. The nature and frequency of surgical and postoperative complications in both groups did not differ.
первинна відкритокутова глаукома; катаракта; двохетапне лікування; мікроімпульсна транссклеральна циклофотокоагуляція
primary open-angle glaucoma; cataract; two-stage treatment; micropulse transscleral cyclophotocoagulation
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Tham YC, Li X, Wong TY, Quigley HA, Aung T, Cheng CY. Global prevalence of glaucoma and projections of glaucoma burden through 2040: a systematic review and meta-analysis. Ophthalmology. 2014;121:2081-2090. doi: 10.1016/j.ophtha.2014.05.013.
- Quigley HA, Broman AT. The number of people with glaucoma worldwide in 2010 and 2020. Br J Ophthalmol. 2006 Mar;90(3):262-7. doi: 10.1136/bjo.2005.081224.
- Kapetanakis VV, Chan MP, Foster PJ, Cook DG, Owen CG, Rudnicka AR. Global variations and time trends in the prevalence of primary open angle glaucoma (POAG): a systematic review and meta-–analysis. Br J Ophthalmol. 2016 Jan;100(1):86-93. doi: 10.1136/bjophthalmol-2015-307223.
- Аліфанова Т.А., Гладченко Ю.Ю., Чуйко О.Л. Інвалідність внаслідок патології органу зору в Україні. Філатовські читання: мат. наук-практ. конф. офтальмол. з міжнар, участю, присв. 75-річчю заснування Інституту ім. В.П. Філатова, 26–27 травня 2011 р. Тези доп. Одеса, 2011. С. 340.
- The Advanced Glaucoma Intervention Study (AGIS): 7. The relationship between control of intraocular pressure and visual field deterioration. The AGIS Investigators. Am J Ophthalmol. 2000 Oct;130(4):429-40. doi: 10.1016/s0002-9394(00)00538-9.
- Nouri Mahdavi K, Hoffman D, Coleman AL, et al. Predictive factors for glaucomatous visual field progression in the Advanced Glaucoma Intervention Study. Ophthalmology. 2004 Sep;111(9):1627-35. doi: 10.1016/j.ophtha.2004.02.017.
- Canadian Glaucoma Study Group. Canadian Glaucoma Study: 1. Study design, baseline characteristics, and preliminary analyses. Can J Ophthalmol. 2006 Oct;41(5):566-75. doi: 10.1139/i06-057.
- Hattenhauer MG, Johnson DH, Ing HH et al. The probability of blindness from open-angle glaucoma. Ophthalmology. 1998;105:2099-2104.
- Сердюк А.В., Могілевський С.Ю. Прогресування глаукомної оптичної нейропатії після різних видів антиглаукоматозних операцій. Вісник проблем біології і медицини. 2019. 4. 2(154). 195-9.
- Могілевський С.Ю., Сердюк А.В., Зябліцев С.В. Маркери апоптозу та прогресування глаукомної оптичної нейропатії після хірургічного лікування первинної відкритокутової глаукоми. Архів офтальмології України. 2020. 8 (2). 29-34.
- Lee SJ, Lee SA, Lee S et al. Risk factors for undergoing surgery in patients with newly diagnosed open-angle glaucoma. Sci Rep. 2022 Apr 5;12(1):5661. doi: 10.1038/s41598-022-09832-3.
- Nam GE, Han K, Ha SG et al. Relationship between socioeconomic and lifestyle factors and cataracts in Koreans: the Korea National Health and Nutrition Examination Survey 2008-2011. Eye (Lond). 2015 Jul;29(7):913-20. doi: 10.1038/eye.2015.66.
- Flaxman SR, Bourne RR, Resnikoff S et al. Global cau–ses of blindness and distance vision impairment 1990–2020: a systematic review and meta-analysis. Lancet Glob Health. 2017 Dec;5(12):e1221-e1234. doi: 10.1016/S2214-109X(17)30393-5.
- Yu-Chi L, Mark W, Terry K, et al. Lancet. 2017 Aug 5;390(10094):600-612. doi: 10.1016/S0140-6736(17)30544-5.
- Fea AM, Hengerer F, Lavia C, Au L. Glaucoma quality of life. J Ophthalmol. 2017;2017:4257151. doi: 10.1155/2017/4257151.
- Skalicky SE, Martin KR, Fenwick E, Crowston JG, Goldberg I, McCluskey P. Cataract and quality of life in patients with glaucoma. Clin Exp Ophthalmol. 2015 May-Jun;43(4):335-41. doi: 10.1111/ceo.12454.
- Musch DC, Gillespie BW, Niziol LM, et al. Cataract extraction in the collaborative initial glaucoma treatment study: incidence, risk factors, and the effect of cataract progression and extraction on clinical and quality-of-life outcomes. Arch Ophthalmol. 2006 Dec;124(12):1694-700. doi: 10.1001/archopht.124.12.1694.
- Arimura S, Iwasaki K, Gozawa M, Takamura Y, Inatani M. Trabeculectomy followed by phacoemulsification versus trabeculectomy alone: The Collaborative Bleb-Related Infection Incidence and Treatment Study. PLoS One. 2019 Oct 24;14(10):e0223439. doi: 10.1371/journal.pone.0223439.
- Jung JL, Isida-Llerandi CG, Lazcano-Gomez G, SooHoo JR, Kahook MY. Intraocular pressure control after trabeculectomy, phacotrabeculectomy and phacoemulsification in a hispanic population. J Curr Glaucoma Pract. 2014 May-Aug;8(2):67-74. doi: 10.5005/jp-journals-10008-1164.
- Li X, Liu Y, Li Y, Wang M. Effects of modified trabeculectomy combined with phacoemulsification and intraocular lens implantation on intraocular pressure and complications in patients with primary open angle glaucoma. International Journal of Clinical and Experimental Medicine. 2019;12(2):1778-1784.
- Mansberger SL, Gordon MO, Jampel H et al. Ocular Hypertension Treatment Study Group. Reduction in intraocular pressure after cataract extraction: the Ocular Hypertension Treatment Study. Ophthalmology. 2012 Sep;119(9):1826-31. doi: 10.1016/j.ophtha.2012.02.050.
- Mathalone N, Hyams M, Neiman S. Long-term intraocular pressure control after clear corneal phacoemulsification in glaucoma patients. J Cataract Refract Surg. 2005 Mar;31(3):479-83. doi: 10.1016/j.jcrs.2004.06.046.
- Daas A, Sherman T, Danieliute L et al. Phacoemulsification combined with micropulse cyclodiode laser in glaucoma patients: efficacy and safety. Eye (Lond). 2022 Nov;36(11):2188-2191. doi: 10.1038/s41433-021-01826-1.
- Al Habash Ahmed, Otaif Wael. Surgical Outcome of Combined MicroPulse Transscleral Laser Therapy with Phaco Emulsification in Patients with Cataract and Glaucoma. The Open Ophthalmo–logy Journal. 2022;16. doi: 10.2174/18743641-v16-e2209260.