Международный эндокринологический журнал 3 (35) 2011
Вернуться к номеру
Метформин: безопасность применения у пациентов с заболеваниями сердца
Авторы: Khurana R., Malik I.S., Department of Cardiology, Mary Stanford Wing, St Mary’s Hospital Campus, Imperial College Healthcare NHS Trust, London, UK
Рубрики: Эндокринология
Версия для печати
Метформин относится к группе бигуанидов. Он повышает чувствительность тканей к инсулину и снижает уровень сахара в крови. Имеются опасения, что прием метформина может приводить к развитию лактат-ацидоза у пациентов, которым выполняют диагностические процедуры, требующие введения йодосодержащих контрастных веществ, и у пациентов, имеющих почечную или сердечную недостаточность. В многочисленных исследованиях был выполнен обзор данных, на которых базируются подобные опасения, в результате чего был сделан вывод, что метформин редко является причиной лактат-ацидоза. Общепринятое мнение о том, что всем пациентам необходимо прекращать прием метформина за 48 ч до и в течение 48 ч после выполнения вмешательств с введением контрастных веществ, представляется нелогичным, лишенным какой-либо доказательной базы и не соответствует принципам приемлемой клинической практики. У пациентов с сердечной недостаточностью данное заболевание может предрасполагать к развитию лактат-ацидоза, при этом назначение метформина приводит скорее к улучшению наблюдаемых исходов, нежели к увеличению возможных рисков.
Метформин, лактат-ацидоз, риск.
Метформин, препарат из группы бигуанидов, повышает чувствительность тканей к инсулину, угнетает протекание глюконеогенеза в печени и, как следствие этого, понижает уровень сахара в крови. Он может быть назначен в комбинации с любым другим пероральным противодиабетическим средством и с инсулином. Для него характерен малый период полувыведения — около 6 ч; 90 % препарата выводится почками в течение 24 ч. При применении метформина существуют те же опасения, что и при использовании его бигуанидного предшественника — фенформина: у последнего была обнаружена сильная взаимосвязь с развитием лактат-ацидоза, в связи с чем в 1978 г. он был запрещен для клинического применения [1].
Среди врачей сформировалось мнение, что метформин вызывает лактат-ацидоз у пациентов с диабетом или почечной дисфункцией. Поэтому возможность его применения у пациентов с сердечными заболеваниями во время внутривенного или внутриартериального введения контрастных веществ, а также у пациентов с сердечной недостаточностью является спорной. Во многих протоколах катетеризации сердца оговорено, что метформин должен быть отменен за 48 ч до и в течение 48 ч после любого планового диагностического или лечебного вмешательства. У пациентов, которые не прекратили прием метформина, вмешательство часто выполняют с отсрочкой, что ухудшает ожидаемые от него результаты.
Метформин не обладает нефротоксичным действием и не взаимодействует с йодосодержащими контрастными веществами. Рекомендации по отмене этого препарата основаны на существовании теоретического риска развития лактат-ацидоза у пациентов, предрасположенных к острому нарушению функции почек, после введения контрастных веществ. В этом случае возможно накопление метформина, который может повысить концентрацию молочной кислоты в плазме крови. Однако насколько верифицирована эта концепция?
Риски, связанные с прекращением приема метформина
Наличие гипергликемии само по себе может быть вредным во время выполнения достаточно тонких коронарных и каротидных вмешательств [2, 3]. В дополнение к этому не были проведены специальные исследования, направленные на оценку долговременных эффектов «гипергликемии отдачи» у пациентов после временного прекращения приема метформина. Однако нужно отметить, что последствия прекращения приема метформина сроком на 1–2 недели были изучены в рамках Diabetes Prevention Program (Программа профилактики диабета), в которой 3234 пациента с нарушенной толерантностью к глюкозе были случайно распределены к приему плацебо, метформина или модификации стиля жизни; период наблюдения составил в среднем 2,8 года [4, 5]. Было выяснено, что в этот период времени вероятность развития диабета (определяемого по нарушению перорального теста толерантности к глюкозе) увеличивалась на 50 % в группе с метформином по сравнению с плацебо-группой, хотя различия и не достигали статистической значимости (p = 0,098).
Риски, связанные с продолжением приема метформина
Лактат-ацидоз у пациентов без сахарного диабета развивается при наличии инфекций, рака, печеночной и почечной недостаточности и при отсутствии коррекции этих заболеваний всегда ведет к летальному исходу. Факторы риска развития лактат-ацидоза во многом являются сходными и независимыми от диабетического статуса. Факторы риска, предрасполагающие к развитию лактат-ацидоза:
— возраст > 80 лет;
— тканевая гипоксия;
— снижение сердечного выброса;
— дыхательная недостаточность;
— печеночная недостаточность;
— почечная недостаточность;
— сепсис;
— хирургическое вмешательство;
— интоксикация этанолом;
— диабетический кетоацидоз;
— голодание/пониженное питание;
— синдром укороченной тонкой кишки (еюноилеальный анастомоз, резекция тонкой кишки);
— антиретровирусная терапия;
— высокие дозы (намеренное завышение дозы) метформина > 2 г/день.
Метформин был разрешен к применению в США в мае 1995 г., и в течение последующих 12 месяцев в Управление по надзору за качеством пищевых продуктов и лекарственных средств (Food and Drug Administration (FDA)) поступили сообщения о развитии лактат-ацидоза у 66 пациентов, получавших метформин. У 47 пациентов диагноз был установлен на основе повышения концентрации лактата в плазме крови (> 5 ммоль/л), в соответствии с принятыми критериями диагностики лактат-ацидоза [6]. Из них у 43 пациентов присутствовал один или больше фактор риска развития лактат-ацидоза: у 30 наблюдались заболевания сердца (18 страдало от сердечной недостаточности), у 13 присутствовала почечная недостаточность (причем 2 пациентам выполняли гемодиализ). У 3 пациентов наблюдалась хроническая обструктивная болезнь легких, 8 пациентов были в возрасте старше 80 лет. Лишь у 4 из 47 пациентов не было обнаружено видимых факторов риска развития лактат-ацидоза на момент начала терапии метформином; все они выздоровели от лактат-ацидоза. После получения этих данных связь между приемом метформина и лактат-ацидозом вызвала значительные противоречия, основываясь главным образом на единичных сообщениях, с частотой, оцениваемой в настоящее время как 2–5 случаев на 100 000 пациенто-лет [7].
Частота развития лактат-ацидоза у пациентов с сахарным диабетом 2-го типа была одинаковой среди пациентов, принимавших и не принимавших метформин, после исключения факторов риска, связанных с развитием лактат-ацидоза [8]. Смертность среди пациентов с лактат-ацидозом, приписываемым приему метформина, составляет примерно 40 % и связана, по-видимому, с сердечной недостаточностью. Создается впечатление, что в большинстве случаев метформин не был изначальной причиной лактат-ацидоза, но мог вносить вклад в увеличение его тяжести. Этио-логия лактат-ацидоза является достаточно сложной и, как полагают, связана со сдвигом внутриклеточного окислительно-восстановительного потенциала с аэробного на анаэробный механизм, что приводит к внутриклеточной продукции лактата [9].
Было выполнено интересное ретроспективное исследование, в рамках которого попытались ответить на вопрос, учитывались ли при назначении метформина опубликованные в литературе противопоказания и соблюдались ли требуемые меры предосторожности [10]. Было обнаружено, что врачи (предположительно осведомленные о потенциальной способности метформина вызывать лактат-ацидоз) редко точно следовали инструкциям и назначали метформин пациентам с заболеваниями, которые потенциально могли повлечь за собой развитие лактат-ацидоза. Несмотря на этот «минус», случаи лактат-ацидоза отмечены не были. В другом аналогичном исследовании, выполненном в Шотландии и включавшем 1847 пациентов, принимавших метформин, назначение препарата шло вразрез с инструкциями у 24,5 % пациентов, но, несмотря на это, лактат-ацидоз в течение 30 месяцев наблюдения развился только у 1 пациента, который умер от сердечной недостаточности.
Метформин и сердечная недостаточность
Диабет является частым сопутствующим заболеванием у пациентов с сердечной недостаточностью и обусловливает более плохой прогноз [12]. Метформин «противопоказан» при сердечной недостаточности в связи с наличием теоретического риска развития лактат-ацидоза, несмотря на то, что соответствующие длительные исследования выполнены не были. С другой стороны, в литературе, посвященной сердечной недостаточности, накоплено значительное количество данных, подтверждающих безопасность метформина. Результаты больших ретроспективных анализов регистров свидетельствуют о том, что, как это ни парадоксально, метформин является единственным противодиабетическим средством, который снижает заболеваемость (снижение частоты повторных госпитализаций по поводу сердечной недостаточности) и смертность у пациентов с сердечной недостаточностью, включая пожилых пациентов [13, 14]. Более того, ни одного случая лактат-ацидоза в этих исследованиях отмечено не было.
Был предложен механизм, который мог бы объ-яснить наблюдаемые улучшения. В модели сердечной недостаточности у мышей было показано, что кардиопротективные свойства метформина не зависят от его гипогликемических эффектов и опосредованы активацией АМФ-активируемой протеинкиназы [15].
Недавно было предпринято пилотное исследование, чтобы оценить возможность проведения крупного рандомизированного контролируемого исследования с конечными точками, направленными на оценку безопасности назначения метформина при сердечной недостаточности. Рандомизационный план предусматривал назначение либо метформина в дозе 1500 мг/день, либо сравнимого плацебо в течение 6 месяцев. В результате в исследование не удалось набрать пациентов, поскольку все 58 пациентов, проходивших скрининг, были исключены из исследования. Основные причины исключения из исследования сводились к использованию инсулина, наличию уровня гликозилированного гемоглобина < 7 % и приему высоких доз метформина. Пилотное исследование было прервано, а шансы на проведение крупного исследования стали почти безнадежными.
Много вопросов возникает также в отношении правомочности «противопоказаний» к назначению метформина у пациентов с диабетической кардиомиопатией, основанных на устаревших и неподтвержденных опасениях относительно способности данного препарата вызывать лактат-ацидоз [17, 18].
Данные о безопасности
Чтобы снизить напряженность вокруг безопасности метформина, фармацевтическая компания Bristol-Myers Squibb (Нью-Йорк, США) инициировала проведение большого исследования COSMIC (the Comparative Outcomes Study of Metformin Intervention versus Conventional approach — Сравнительное исследование безопасности метформина и других противодиабетических средств) длительностью 1 год, в рамках которого сравнили лечение метформином и «обычную терапию» другими противодиабетическими средствами. В результате не было обнаружено различий в безопасности между 7227 пациентами, принимавшими метформин, и 1505 пациентами, принимавшими «обычную терапию». Ни в одной из групп не развился лактат-ацидоз [19].
В двух больших, независимых от фармацевтических компаний клинических исследованиях были получены очень впечатляющие доказательства безопасности и эффективности метформина. Во-первых, в рамках крупного исследования UKPDS (UK Prospective Diabetes Study — Проспективное исследование диабета в Великобритании) субпопуляция из 753 пациентов с избыточным весом была рандомизирована либо к лечению традиционным методом, включающим только лишь диету (n = 342), либо к интенсивному гликемическому контролю с помощью метформина (n = 411). Метформин продемонстрировал большую эффективность в отношении снижения частоты развития связанных с диабетом конечных точек, включая макрососудистые осложнения, без негативного влияния на безопасность как в данной рандомизированной когорте, так и во всей популяции исследования UKPDS (n = 4075) в течение медианы времени наблюдения 10,7 года [20]. Следует отметить, что метформин приводит также к снижению массы тела, что оказывает положительное влияние на сердечно-сосудистые риски у пациентов с диабетом и ожирением [21]. Безопасность и эффективность метформина была подтверждена Diabetes Prevention Program (Программа профилактики диабета) (n = 2155) [5], в рамках которой было показано, что данный препарат снижает риск развития сахарного диабета на 31 % по сравнению с плацебо.
Не так давно были опубликованы результаты метаанализа Cochrane, в котором была изучена частота фатальных и нефатальных случаев лактат-ацидоза при использовании метформина по сравнению с плацебо и другими видами сахароснижающей терапии у пациентов с сахарным диабетом 2-го типа [8]. В обобщенных данных из 206 сравнительных и когортных исследований не было обнаружено случаев фатального или нефатального лактат-ацидоза в расчете на 47 846 пациенто-лет в группе с метформином и 38 221 пациенто-год в группе без метформина. Исследователи пришли к выводу, что данные проспективных сравнительных исследований и наблюдательных когортных исследований не подтверждают тот факт, что назначение метформина связано с повышением риска развития лактат-ацидоза.
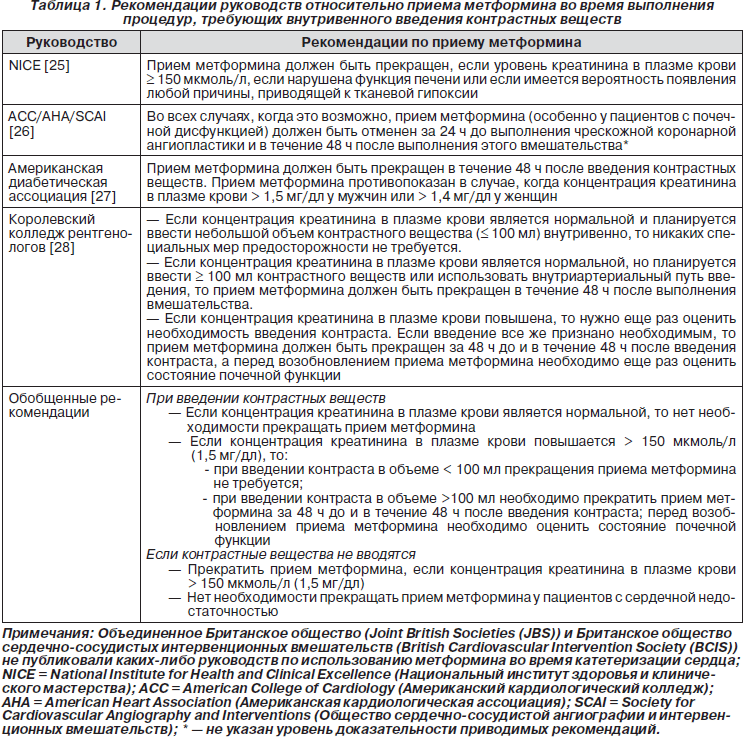
Несмотря на результаты контролируемых исследований, анализов регистров и метаанализов, представления о риске развития метформин-обусловленного лактат-ацидоза прочно вошли в нашу жизнь благодаря отдельным опубликованным сообщениям и типичным указаниям в руководствах, выпущенных крупными профессиональными ассоциациями (табл. 1).
В одном из недавно завершенных обзоров подобных отдельных сообщений было показано, что подавляющее большинство метформин-ассоциированных случаев лактат-ацидоза (особенно фатальных) было связано скорее с наличием сопутствующих заболеваний или с тем, что пациенты с сахарным диабетом склонны к развитию серьезных медицинских осложнений, которые могут приводить к развитию лактатацидоза, нежели с приемом самого метформина [22]. Еще в одном обзоре, посвященном анализу всех случаев лактат-ацидоза, развившихся после внутривенного введения контраста, указывалось на наличие у пациентов плохой функции почек или других противопоказаний для применения метформина [23]. Отсутствие у этих пациентов корреляции между содержанием лактата и метформина в плазме крови также указывало на «невиновность» метформина [24]. У подобных пациентов нужно еще раз тщательно взвесить необходимость введения контраста и в случае принятия положительного решения использовать режим агрессивной гидратации организма, чтобы минимизировать риск развития контраст-индуцированной нефропатии.
Выводы
При анализе большого клинического опыта применения метформина было выяснено, что реальное количество подтвержденных случаев метформин-ассоциированного лактат-ацидоза было весьма небольшим. Причинная связь является слабой и своим появлением обязана случаям завышения дозы метформина. У пациентов с сердечной недостаточностью данное заболевание может предрасполагать к развитию лактат-ацидоза, при этом назначение метформина приводит скорее к улучшению наблюдаемых исходов, нежели к увеличению возможных рисков. Кумуляция метформина в случаях почечной недостаточности может увеличивать риск развития лактат-ацидоза в группах пациентов с высоким риском — например, у пожилых пациентов и тех, которые получают высокие дозы метформина ≥ 2 г/день. Риск развития лактат-ацидоза вследствие приема метформина у пациентов, которым выполняют катетеризацию сердца, не был определен; опубликованные исследования или данные из регистров на эту тему отсутствуют. Общепринятое мнение о том, что всем пациентам необходимо прекращать прием метформина за 48 ч до и в течение 48 ч после выполнения вмешательств с контрастированием, представляется нелогичным, лишенным какой-либо доказательной базы и не соответствует принципам приемлемой клинической практики. Даже у пациентов с нарушением почечной функции причинная связь между приемом метформина и развитием лактат-ацидоза является слабой. В связи со всем вышеперечисленным при назначении метформина предлагается использовать прагматический подход.
Финансовая поддержка: Совет по биомедицинским исследованиям (Biomedical Research Council (BRC)).
Конфликт интересов: не заявлен.
Заказчик и рецензирование: статья не заказывалась; внешнее рецензирование не выполнялось.
Перевод А.В. Савустьяненко
Оригинал статьи опубликован в Postgrad. Med. J. — 2010. — 86. — 371-373
1. Dembo A.J., Marliss E.B., Halperin M.L. Insulin therapy in phenformin-associated lactic acidosis; a case report, biochemical considerations and review of the literature // Diabetes. — 1975. — 24. — 28e35.
2. Willfort-Ehringer A., Ahmadi R., Gessl A. et al. Neointimal proliferation within carotid stents is more pronounced in diabetic patients with initial poor glycaemic state // Diabetologia. — 2004. — 47. — 400e6.
3. Timmer J.R., Ottervanger J.P., de Boer M.J. et al. Hyperglycemia is an important predictor of impaired coronary flow before reperfusion therapy in ST-segment elevation myocardial infarction // J. Am. Coll. Cardiol. — 2005. — 45. — 999e1002.
4. Diabetes Prevention Program Research Group. Effects of withdrawal from metformin on the development of diabetes in the diabetes prevention program // Diabetes Care. — 2003. — 26. — 977e80.
5. Knowler W.C, Barrett-Connor E., Fowler S.E. et al. Reduction in the incidence of type 2 diabetes with lifestyle intervention or metformin // N. Engl. J. Med. — 2002. — 346. — 393e403.
6. Misbin R.I., Green L., Stadel B.V. et al. Lactic acidosis in patients with diabetes treated with metformin // N. Engl. J. Med. — 1998. — 338. — 265e6.
7. Brown J.B., Pedula K., Barzilay J. et al. Lactic acidosis rates in type 2 diabetes // Diabetes Care. — 1998. — 21. — 1659e63.
8. Salpeter S., Greyber E., Pasternak G. et al. Risk of fatal and nonfatal lactic acidosis with metformin use in type 2 diabetes mellitus // Cochrane Database Syst. Rev. — 2006. — 1. — CD002967.
9. Kreisberg R.A., Wood B.C. Drug and chemical-induced metabolic acidosis // Clin. Endocrinol. Metab. — 1983. — 12. — 391e411.
10. Calabrese A.T., Coley K.C., DaPos S.V. et al. Evaluation of prescribing practices: risk of lactic acidosis with metformin therapy // Arch. Intern. Med. — 2002. — 162. — 434e7.
11. Emslie-Smith A.M., Boyle D.I., Evans J.M. et al. Contraindications to metformin therapy in patients with type 2 diabetes — apopulation-based study of adherence to prescribing guidelines // Diabet. Med. — 2001. — 18. — 483e8.
12. Tang W.H. Glycemic control and treatment patterns in patients with heart failure // Curr. Cardiol. Rep. — 2007. — 9. — 242e7.
13. Eurich D.T., McAlister F.A., Blackburn D.F. et al. Benefits and harms of antidiabetic agents in patients with diabetes and heart failure: systematic review // BMJ. — 2007. — 33. — 497.
14. Masoudi F.A., Inzucchi S.E., Wang Y. et al. Thiazolidine-diones, metformin, and outcomes in older patients with diabetes and heart failure: an observational study // Circulation. — 2005. — 111. — 583e90.
15. Gundewar S., Calvert J.W., Jha S. et al. Activation of AMP-activated protein kinase by metformin improves left ventricular function and survival in heart failure // Circ. Res. — 2009. — 104. — 403e11.
16. Eurich D.T., Tsuyuki R.T., Majumdar S.R. et al. Metformin treatment in diabetes and heart failure: when academic equipoise meets clinical reality // Trials. — 2009. — 10. — 12.
17. Tahrani A.A., Varughese G.I., Scarpello J.H. et al. Metformin, heart failure, and lactic acidosis: is metformin absolutely contraindicated? // BMJ. — 2007. — 335. — 508e12.
18. McCormack J., Johns K., Tildesley H. Metformin’s contraindications should be contraindicated // CMAJ. — 2005. — 173. — 502e4.
19. Cryer D.R., Nicholas S.P., Henry D.H. et al. Comparative outcomes study of metformin intervention versus conventional approach the COSMIC Approach Study // Diabetes Care. — 2005. — 28. — 539e43.
20. UK Prospective Diabetes Study (UKPDS) Group. Effect of intensive bloodglucose control with metformin on complications in overweight patients with type 2 diabetes (UKPDS 34) // Lancet. — 1998. — 352. — 854e65.
21. Golay A. Metformin and body weight // Int. J. Obes. (Lond.). — 2008. — 32. — 61e72.
22. Stades A.M., Heikens J.T., Erkelens D.W. et al. Metformin and lactic acidosis: cause or coincidence? A review of case reports // J. Intern. Med. — 2004. — 255. — 179e87.
23. McCartney M.M., Gilbert F.J., Murchison L.E. et al. Metformin and contrast media: a dangerous combination? // Clin. Radiol. — 1999. — 54. — 29e33.
24. Lalau J.D., Race J.M. Lactic acidosis in metformin-treated patients. Prognostic value of arterial lactate levels and plasma metformin concentrations // Drug Saf. — 1999. — 20. — 377e84.
25. National Institute for Health and Clinical Excellence. Quick reference guided the management of type 2 diabetes, 2008. Available at http://www.nice.org.uk/Guidance/CG66/ (accessed 23 July 2009).
26. Smith S.C. Jr, Feldman T.E., Hirshfeld J.W. Jr et al. ACC/AHA/SCAI 2005 guideline update for percutaneous coronary intervention: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (ACC/AHA/SCAI Writing Committee to Update 2001 Guidelines for Percutaneous Coronary Intervention) // Circulation. — 2006. — 113. — e166e286.
27. American Diabetes Association. Standards of medical care in diabetes — 2009 // Diabetes Care. — 2009. — 32(Suppl. 1). — S13e61.
28. Thomsen H.S., Morcos S.K. Contrast media and metformin: guidelines to diminish the risk of lactic acidosis in non-insulin-dependent diabetics after administration of contrast media. ESUR Contrast Media Safety Committee // Eur. Radiol. — 1999. — 9. — 738e40.