Международный эндокринологический журнал 6 (38) 2011
Вернуться к номеру
Актовегін: нові можливості в лікуванні діабетичної поліневропатії
Авторы: Власенко М.В., Семенюк І.В., Кривов’яз Ю.О., Вінницький національний медичний університет ім. М.І. Пирогова, Вінницький обласний клінічний ендокринологічний диспансер
Рубрики: Эндокринология
Версия для печати
З огляду на те що близько 275 млн людей у світі хворіють на цукровий діабет (ЦД), можна говорити про значимість даної епідемії, яка вимагає підвищеної уваги. Погано контрольований ЦД є основною причиною смертності в більшості розвинутих країн світу і впливає на розвиток таких ускладнень, як діабетична невропатія, ниркова недостатність, сліпота й макросудинні ускладнення. У першу чергу хронічна гіперглікемія є причиною розвитку мікросудинних уражень, до яких відносимо невропатію, нефропатію й ретинопатію.
За визначеням ВООЗ, діабетична поліневропатія (ДПН) — захворювання, що характеризується прогресуючою втратою нервових волокон, яка призводить до втрати чутливості й розвитку виразок стопи. В американському проспективному дослідженні, яке тривало 25 років і в якому проводилося спостереження за 4400 пацієнтами із ЦД 2-го типу, ДПН була виявлена в 7,5 % хворих при встановленні діагнозу ЦД, а в 50 % — протягом усього періоду спостереження. Європейське дослідження за участю 3250 хворих із 31 центру в 16 країнах довело, що поширеність поліневропатії становила 28 % при встановленні діагнозу ЦД. Більшою мірою ДПН корелює з тривалістю діабету й рівнем глікемії.
ДПН у деяких випадках є першим клінічним проявом ЦД. За даними когортного дослідження Monica/KORA Augsburg, поширеність дистальної симетричної невропатії в контрольній групі становила 8,9 %, у групі порушення толерантності до вуглеводів — 13,0 %, а при ЦД 2-го типу — 27,6 %.
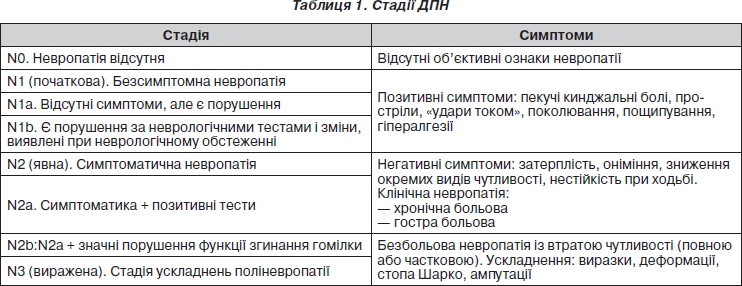
Клініцистам у своїй практиці при встановленні діагнозу ДПН слід спиратися на такі критерії: наявність симптомів дисфункції нерва, зміни швидкості поширення збудження по нервових волокнах, зміни за даними кількісних сенсорних або автономних тестів. Неврологічне обстеження пацієнтів включає оцінку різних видів чутливості — больової, тактильної, вібраційної, відчуття тиску, температурної, пропріоцептивної. Для оцінки зміни тактильної чутливості використовують ватні палички або вату, відчуття тиску — монофіламент 10 г, больової чутливості — голку з притупленим кінцем, температурну чутливість визначали за різницею у відчутті тепла й холоду, вібраційну — із використанням камертона 128 Гц. Для оцінки порушення моторної функції досліджують ахіллів або колінний рефлекс. Виявлені порушення оцінюють у балах із використанням спеціальних опитувальників і шкал, таких як шкала неврологічних симптомів і загальна шкала симптомів. На основі проведеного опитування й обстеження встановлюють стадію захворювання.
Щоб усвідомити характер лікування ДПН, необхідно знати патогенез цього ускладнення. Згідно з сучасними уявленнями, основну роль у розвитку ДПН відіграє хронічна гіперглікемія. Саме вона запускає метаболічні й судинні порушення. Відбувається активація поліолового шляху метаболізму глюкози, що призводить до підвищення осмолярності міжклітинного простору й набряку нервової тканини: посилення окисного стресу викликає пряму цитотоксичну дію на нервові волокна. Велике значення має зниження активності Na+/К+-АТФази, порушення обміну ліпідів, утворення автоімунних комплексів (антитіла до інсуліну), пригнічення факторів росту нервів.
Останніми роками значний прорив у пошуку шляхів впливу на патологічні зміни при ДПН був досягнутий завдяки розкриттю ролі гіперглікемії в розвитку окисного стресу й розумінню послідовності ланцюжків вільнорадикального окислення.
З’явився цілий ряд препаратів, які впливають на патогенетичні механізми ДПН. Ще в 1998 р. FDA США було висунуто ряд вимог до препаратів, що застосовувалися при лікуванні ДПН, а саме: вплив на патогенетичні механізми, зменшення симптомів невропатії, покращення функції нерва, зменшення ризику втрати нервових волокон і відсутність значних побічних ефектів.
Усім цим вимогам відповідає препарат Актовегін (Actovegin). Він покращує транспорт кисню і глюкози в клітини, що необхідно при ЦД, коли у тканинах формується енергетична недостатність. Актовегін є сильним антигіпоксичним препаратом, що покращує гемодинаміку й енергопродукцію. Завдяки наявності у складі гліколіпідів Актовегін викликає активацію переносників глюкози, не впливаючи на рецептори інсуліну в клітинах. Таким чином, із патофізіологічної точки зору Актовегін, що справляє антигіпоксичний й антиоксидантний ефект, може застосовуватися при неврологічних захворюваннях, таких як гіпоксія, ішемія й оксидантний стрес. Актовегін має показання до застосування при ДПН. Клінічна ефективність Актовегіну при ДПН була доведена в багатьох контрольованих дослідженнях. Лікування Актовегіном сприяло зниженню рівня малонового діальдегіду в плазмі й мембранах еритроцитів. Актовегін справляє антиоксидантний ефект, впливаючи на патогенетичні механізми розвитку ДПН. Після лікування Актовегіном відзначено вірогідне покращення показників капілярного кровотоку, що позначилося на реологічних властивостях крові й стані проникності стінки капіляра. Рекомендована схема застосування Актовегіну при ДПН та ангіопатіях на основі отриманих результатів: 1000–2000 мг/добу внутрішньовенно краплинно упродовж 10–20 діб, надалі 200–400 мг 3 рази на добу перорально протягом 2–3 місяців.
Усі ці досягнення стали умовою внесення ДПН до переліку показань до застосування Актовегіну. Форми випуску Актовегіну різні: 2 мл (80 мг), 5 мл (200 мг), 10 мл (400 мг), 250 мл 10% розчину із декстрозою (1000 мг), 250 мл 10% розчину з 0,9% NaCl (1000 мг), таблетки по 200 мг, 20% гель, 5% крем.
Між показниками постпрандіальної глікемії, серцево-судинним ризиком і клінічними наслідками в людей із нормальною толерантністю до глюкози, порушеною толерантністю до глюкози й цукровим діабетом існує тісний взаємозв’язок, також відзначено зв’язок між постпрандіальною гіперглікемією і оксидантним стресом, запаленням, ендотеліальною дисфункцією — факторами, що визнані маркерами серцево-судинних захворювань. Доведено, що постпрандіальна гіперглікемія може бути пов’язана з розвитком ретинопатії, когнітивними порушеннями в людей похилого віку з ЦД 2-го типу. Контроль глікемії натще необхідний, однак недостатній для досягнення оптимального глікемічного контролю. Стабілізація показників постпрандіальної глюкози плазми має важливе значення для досягнення цільових показників глікозильованого гемоглобіну (HbAlc).
Враховуючи вищевказане, Міжнародна діабетична федерація (IDF) опублікувала у 2007 р. керівництво з контролю постпрандіальної глікемії [1], що описує взаємозв’язок між постпрандіальним рівнем глікемії й розвитком ускладнень ЦД. Керівництво визначає цільові параметри постпрандіальної глікемії — 7,8 ммоль/л (140 мг%) (рівень доказовості 2++).
Метою нашого дослідження була оцінка ефективності й безпечності препарату Актовегін на декстрозі (виробництва компанії Nycomed) у лікуванні дорослих із ЦД 1-го і 2-го типу.
Матеріали і методи
Актовегін — депротеїнізований гемодериват із телячої крові, що відноситься до фармакологічної групи ангіопротекторів і коректорів мікроциркуляції, антигіпоксантів й антиоксидантів, регенерантів і репарантів.
Актовегін має широкий спектр призначень. Препарат є антиоксидантом, активує метаболізм глюкози й кисню. Він викликає збільшення утилізації і споживання кисню (підвищує стійкість до гіпоксії), підвищує енергетичний метаболізм і споживання глюкози тканинами. Сумарний ефект цих процесів полягає в посиленні енергетичного стану клітини, особливо за умов гіпоксії й ішемії. Продуктами цих метаболічних процесів є такі амінокислоти — глутамат та аспартат. Ці метаболічні процеси перебігають за участю ряду ферментів, наприклад піруватдегідрогенази (утворення ацетилкоензиму А).
Інозитол фосфат, полісахариди здатні регулювати деякі інсулінозалежні ферменти. Актовегін активує піруватдегідрогеназу й тим самим збільшує утилізацію глюкози. Препарат також стимулює споживання кисню. Це призводить до стабілізації плазматичних мембран клітин при ішемії і зниження утворення лактатів. Актовегін не тільки підвищує внутрішньоклітинний рівень глюкози, але й покращує окисний метаболізм, завдяки чому поліпшується енергетичне забезпечення клітин, про що свідчить збільшення концентрації безпосередніх переносників вільної енергії, таких як АТФ, АДФ і фосфокреатинін. Доведено, що Актовегін викликає вказані ефекти і при периферичних (артеріальних і венозних) порушеннях кровообігу, й наслідках цих порушень (артеріальна ангіопатія, виразкові ураження нижніх кінцівок). Доведено, що Актовегін активно прискорює загоєння ран різного походження (трофічні ураження, опіки, порушення мікроциркуляції). При цьому покращуються не тільки морфологічні, але й біохімічні параметри грануляції. У більшості пацієнтів, які отримують Актовегін, дія препарату починає проявлятися через 30 хвилин (10–30 хвилин) після парентерального або перорального застосування, максимальна дія — у середньому через 3 години (2–6 годин).
З огляду на вищезазначене рівень цукру в крові після введення Актовегіну на декстрозі не повинен підвищуватися. Однак в інструкції до препарату зазначено, що для хворих на ЦД слід ураховувати концентрацію глюкози в інфузійному розчині з декстрозою.
Інфузія препарату Актовегін на декстрозі має свої переваги перед розчином NaCl: глюкоза — кращий транспортер речовини й несе енергетичний матеріал для клітини.
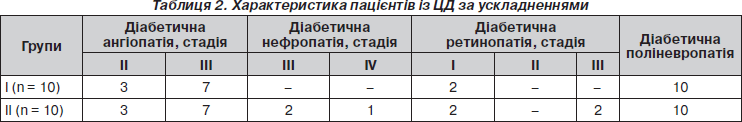
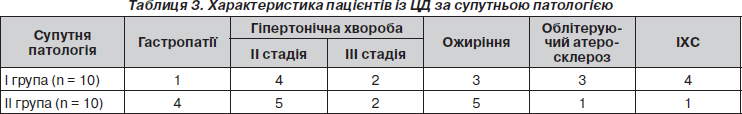
Клінічне дослідження проводилося на базі Вінницького обласного ендокринологічного диспансеру в умовах денного стаціонару. У ньому взяли участь 20 пацієнтів із ЦД, переважно 2-го типу, лише один хворий був із ЦД 1-го типу. Пацієнти були розподілені на 2 групи: І група отримувала Актовегін на фізіологічному розчині, а ІІ група — Актовегін на декстрозі. Середній вік пацієнтів І групи — 59,4 ± ± 0,8 року, а ІІ — 55,4 ± 1,2 року. Тривалість хвороби — 8,2 та 9,5 року відповідно для кожної групи. 9 хворих у І групі мали середній ступінь тяжкості перебігу ЦД, 1 — тяжкий перебіг, у ІІ групі — відповідно 7 і 3. Серед ускладнень ЦД у пацієнтів, які взяли участь у дослідженні, установили різного ступеня діабетичну ангіопатію ніг, нефропатію, ретинопатію, поліневропатію (табл. 2, 3), що й визначало ступінь тяжкості ЦД.
Як видно з табл. 2, 3, групи обстежених були майже рівноцінними за ускладненнями та супутньою патологією. У ІІ групу, яка отримувала Актовегін на декстрозі, ввійшли 4 хворі з патологією шлунково-кишкового тракту, що могло впливати на всмоктування та обмін вуглеводів, а в І групу, яка отримувала Актовегін на фізіологічному розчині, увійшли більше хворих на облітеруючий атеросклероз та ІХС. Усім цим хворим був призначений препарат Актовегін 250 мл в 10% р-ні 1 раз на добу в/в краплинно протягом 10 діб, надалі 200 мг 3 рази на добу перорально, до 3 місяців.
Для оцінки терапевтичної ефективності та переносимості препарату Актовегін проводили об’єктивне обстеження пацієнтів, вимірювання артеріального тиску (АТ), загальний аналіз крові, загальний аналіз сечі, визначали добову протеїнурію, мікроальбумінурію, швидкість клубочкової фільтрації, проводили біохімічні дослідження крові, визначали рівень глюкози крові натще та через 2 години після сніданку та введення препарату, середньодобовий показник глюкози, проводили допплерографію судин ніг, ЕКГ, визначали ахіллів рефлекс, аналізували заповнені анкети.
Критеріями ефективності лікування були зменшення та зникнення симптомів поліневропатії, покращення загального стану, стабілізація показників глікемії крові (табл. 4).
Пацієнти отримували індивідуальну терапію: інсулін та глюкофаж, глюкованс або комбінацію сульфаніламідів із метформіном. Переносимість препарату оцінювали на основі симптомів, суб’єктивних відчуттів пацієнта й об’єктивних даних, отриманих у процесі лікування. Враховували динаміку лабораторних показників, а також частоту та характер побічних реакцій, що виникли.
Результати дослідження та їх обговорення
За результатами аналізу отриманих об’єктивних показників можна стверджувати, що групи були рівноцінними. У пацієнтів І та ІІ груп АТ становив 134/85,5 ± 1,09/0,6 мм рт.ст. та 131,4/87,8 ± 1,0/0,4 мм рт.ст. при частоті серцевих скорочень 77,6 ± 1,2 уд/хв та 81,4 ± 0,4 уд/хв відповідно, що вказувало на коректність антигіпертензивної терапії. Середній показник індексу маси тіла — 30,6 ± 0,3 та 30,8 ± 0,2 при середній масі тіла 85,1 ± 1,7 кг та 90,6 ± 1,3 кг відповідно по групах.
Біохімічні дослідження крові довели, що в усіх пацієнтів такі показники, як уміст загального білка, креатиніну, сечовини, білірубіну, рівні a-амілази, АлАТ і АсАТ, холестерину, тригліцеридів, K, Na, до лікування та після нього були в межах фізіологічної норми. Загальні аналізи крові та сечі також відповідали референтним значенням.
Після проведеного лікування в пацієнтів із мікроальбумінурією був позитивний результат — відсутність цього симптому. Скарги та небажані відчуття в ногах у всіх хворих після курсу Актовегіну зникали.
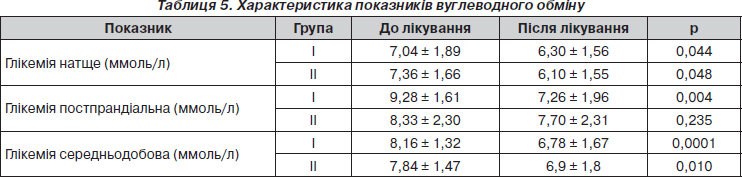
Основний показник, який детально вивчався, — глікемія крові. Усі хворі до лікування були в стані декомпенсації: HbA1c у хворих І групи — 9,1 ± 0,5 %, а у хворих ІІ групи — 8,7 ± 0,4 %. Глікемія натще в пацієнтів І групи — 7,04 ммоль/л, у хворих ІІ групи — 7,36 ммоль/л, постпрандіальний рівень глюкози був відповідно 9,28 та 8,33 ммоль/л (табл. 5).
Результати, отримані нами на фоні визначення тактики та підбору дози гіпоглікемічної терапії, засвідчили необхідність збільшення дози чи інсуліну, чи таблетованих препаратів. Збільшення добової дози інсуліну у хворих обох груп було майже однаковим та в основному за рахунок інсуліну тривалої дії. Це вказує на відсутність необхідності збільшувати дозу інсуліну короткої дії при введенні препарату Актовегін на декстрозі. Зміна тактики та доз таблетованих препаратів (групи метформіну та сульфаніламідних препаратів) здійснювалася відповідно до рівня глікемій та зовсім не залежала від форми препарату Актовегіну.
Слід відзначити, що, враховуючи інсуліноподібну дію Актовегіну, гіпоглікемічні реакції та симптоми не відзначені ні в групі введення Актовегіну на фізіологічному розчині, ні в групі пацієнтів, яким вводили Актовегін на декстрозі.
Після проведеного курсу лікування Актовегіном, підбору гіпоглікемічної терапії на фоні стабільної гіпотензивної терапії та дієтотерапії в пацієнтів отримали позитивну динаміку. Ефективність використання препарату Актовегін на декстрозі в пацієнтів із ЦД оцінювали за такими показниками: самопочуття пацієнтів, показники допплерографії судин нижніх кінцівок, час скорочення ахіллового сухожилка, рівень глюкози після введення препарату та середньодобовий показник глікемії.
Показники глікемії натще до лікування в пацієнтів обох груп вірогідно не відрізнялися (p = 0,63), після проведеного лікування рівень глюкози в крові натще вірогідно змінився (табл. 5) — відповідно 6,30 ± 1,56 ммоль/л і 6,10 ± 1,55 ммоль/л. При цьому після лікування ці показники в обох групах вірогідно не відрізнялися (p = 0,77). Аналіз постпрандіальної глікемії після введення Актовегіну засвідчив, що в І групі до та після лікування рівень показника вірогідно знизився, а в ІІ групі зниження мало місце, але не було вірогідним (8,33 ± 2,30 ммоль/л і 7,70 ± 2,31 ммоль/л, p = 0,235). Однак, порівнюючи постпрандіальну глікемію у пацієнтів І та ІІ груп (7,26 ± 1,96 ммоль/л та 7,70 ± 2,31 ммоль/л) після курсу Актовегіну, слід відзначити невірогідну різницю (p = 0,652). Подібний характер має аналіз середньодобової глікемії. Так, після курсу лікування пацієнтів в умовах денного стаціонару в обох групах глікемія вірогідно змінилася (табл. 5) і не відрізнялася між групами (p = 0,879).
Пацієнти обох груп відзначали позитивну динаміку після курсу лікування — зменшення або зниження болю в ногах у нічний час, задоволення загальним станом. За даними допплерографії та рефлексометрії зміни були позитивні, але не досягали статистично значимої різниці. Висока ефективність лікування відзначена у 2 пацієнтів І та ІІ груп, помірна ефективність лікування — у 7 й 8 пацієнтів відповідно. В одному випадку в І групі ефективність терапії оцінена як низька, хоча рівень глікемії позитивно змінився.
На фоні лікування в жодній групі не відзначено побічних реакцій. Призначення Актовегіну на декстрозі пацієнтам із ЦД не викликало негативних змін біохімічних показників крові та стану пацієнтів.
Переносимість препарату Актовегін на декстрозі в пацієнтів із ЦД оцінена нами як добра.
Висновки
1. Результати досліджень продемонстрували ефективність, безпечність та добру переносимість препарату Актовегін на декстрозі в пацієнтів із ЦД.
2. При застосуванні Актовегіну на декстрозі в пацієнтів із ЦД слід контролювати рівень глюкози у крові через 2 години після введення та, при необхідності, корегувати дозу цукрознижуючої терапії.
3. Як правило, не було потреби в корекції глікемії після введення Актовегіну на декстрозі, до неї вдавалися з метою досягнення цільових рівнів компенса-ції ЦД.
1. IDF Guideline for the Management of Postmeal Glucose 2007. www.idf.org
2. Майров А.Ю. Комментарии к руководству международной диабетической федерации по контролю постпрандиальной гликемии // Сахарный диабет. — 2008. — № 2. — С. 1-2.
3. Тронько Н.Д. Государственная комплексная программа «Сахарный диабет» // Доктор. — 2003. — № 5. — С. 9-12.
4. International Consensus for Wound healing and treatments for people with diabetic foot ulcers // Diabet. Metab. Res. Rew. — 2007. — Vol. 20 (Suppl. 1). — Р. 78-79.
5. Loredo R.A., Garcia G., Chhaya S. Medical imaging of the diabetic foot // Clin. Podiatr. Med. Surg. — 2007. — № 3. — Р. 397-424.