Международный эндокринологический журнал 6 (38) 2011
Вернуться к номеру
Симпозиум «Несахарный диабет: эпидемиология, диагностика, клиническая симптоматика, лечение»
Авторы: Панькив В.И., Украинский научно-практический центр эндокринной хирургии, трансплантации эндокринных органов и тканей МЗ Украины
Рубрики: Эндокринология
Версия для печати
Проводит: Донецкий национальный медицинский университет имени М. Горького.
Рекомендован: эндокринологам, семейным врачам, терапевтам.
Определение
Несахарный диабет (НСД) (лат. diabetes insipidus) — тяжелое заболевание, имеющее в своей основе дефект синтеза, секреции или действия аргинин-вазопрессина (АВП), что приводит к потере способности почек реабсорбировать воду и концентрировать мочу и проявляется выраженной жаждой и экскрецией большого количества разведенной мочи. Гормон АВП является самым важным регулятором водно-электролитного обмена в организме человека. Его функция заключается в поддержании осмотического гомеостаза и объема циркулирующей жидкости. АВП синтезируется в телах нейронов, образующих супраоптическое и паравентрикулярное ядра гипоталамуса, он связывается с белком-носителем нейрофизином. Комплекс «АВП — нейрофизин» в виде гранул транспортируется к терминальным расширениям аксонов нейрогипофиза и срединного возвышения, где накапливается и секретируется в кровь. После попадания в кровь АВП связывается с вазопрессиновыми рецепторами 2-го типа (V2) на базальной мембране клеток собирательных канальцев почек, активация которых приводит к каскаду и встраиванию белка «водной поры» аквапорина-2 на поверхность апикальной мембраны, а аквапорина-3 и -4 — на поверхность базальной мембраны клеток собирательных канальцев, что повышает проницаемость клеток для воды и обеспечивает ее реабсорбцию из просвета канальцев обратно в кровяное русло, уменьшает диурез.
Эпидемиология
Распространенность НСД в популяции составляет от 0,004 до 0,01 %. Отмечается мировая тенденция к росту распространенности НСД, в частности за счет его центральной формы, что связывают с повышением числа оперативных вмешательств, проводимых на головном мозге, а также количества черепно-мозговых травм, при которых случаи развития НСД составляют до 30 %. Считается, что НСД одинаково часто страдают как женщины, так и мужчины. Пик заболеваемости приходится на вторую-третью декады жизни.
Патогенез и клиническая симптоматика
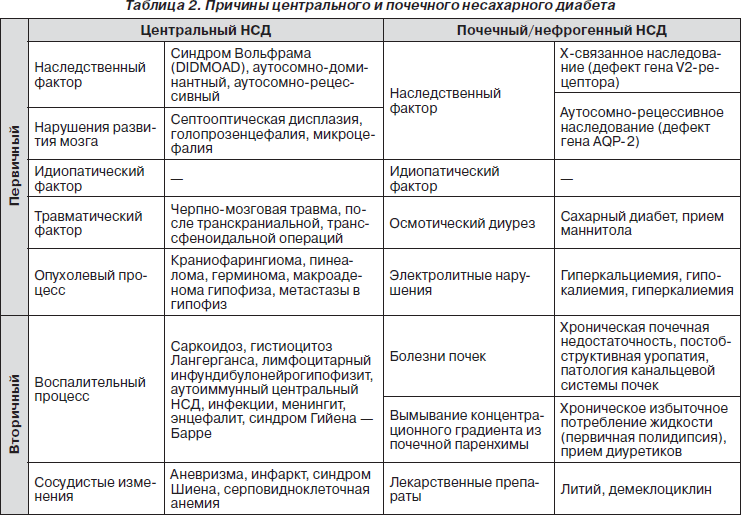
Выделяют несколько различающихся по патогенезу типов НСД, которые представлены в табл. 1.
При НСД, за исключением первичной полидипсии (ПП), абсолютная (отсутствие/снижение гормона в крови) или относительная (резистентность к действию гормона) недостаточность АВП проявляется снижением реабсорбции воды в почках и выделением большого количества неконцентрированной мочи, что приводит к дегидратации (дефициту внутриклеточной и внутрисосудистой жидкости), развитию гиперосмоляльности плазмы, активации осморецепторов гипоталамуса и возникновению жажды.
Основные симптомы НСД:
— жажда (полидипсия; количество выпиваемой жидкости колеблется от 3 до 20 л);
— обильное, учащенное мочеиспускание (поли-урия), ночное мочеиспускание (никтурия);
— общая дегидратация (сухость кожи и слизистых оболочек, уменьшение слюно- и потоотделения; при неадекватности восполнения потерь жидкости наступает резко выраженная дегидратация, проявляющаяся общей слабостью, головными болями, тошнотой, рвотой, лихорадкой, судорогами, тахикардией, сгущением крови, коллаптоидными состояниями или психомоторными возбуждениями);
— желудочно-кишечные проявления (постоянная перегрузка водой приводит к растяжению желудка, снижению секреторной функции желудочно-кишечного тракта, запорам).
При ПП не выявляется какого-либо дефицита секреции или действия АВП. Причинами заболевания, как правило, служат снижение порога чувствительности центра жажды, когда пациент чувствует жажду при совершенно нормальной или даже сниженной концентрации электролитов/осмоляльности крови, а также избыточный прием жидкости вследствие компульсивного (маниакального) желания пить, что может наблюдаться при манифестации различных психических заболеваний. Объем циркулирующей жидкости в организме у таких пациентов повышен, поэтому для клинической картины ПП не характерно наличие симптомов дегидратации — напротив, пациенты могут предъявлять жалобы на потливость или слюнотечение. Разведение крови проявляется снижением уровней электролитов/осмоляльности, что приводит к физиологическому блоку синтеза и секреции АВП и, таким образом, к водному диурезу, целью которого является выведение лишней воды, поступившей в организм.
Дифференциальная диагностика
В клинической практике, как правило, приходится проводить дифференциальную диагностику между тремя основными типами НСД: центральным НСД, почечным НСД и ПП, разделение которых крайне важно для назначения патогенетического лечения, предупреждения потенциально опасных побочных эффектов неправомерно назначенного лечения и для дальнейшего направленного поиска причин заболевания (табл. 2).
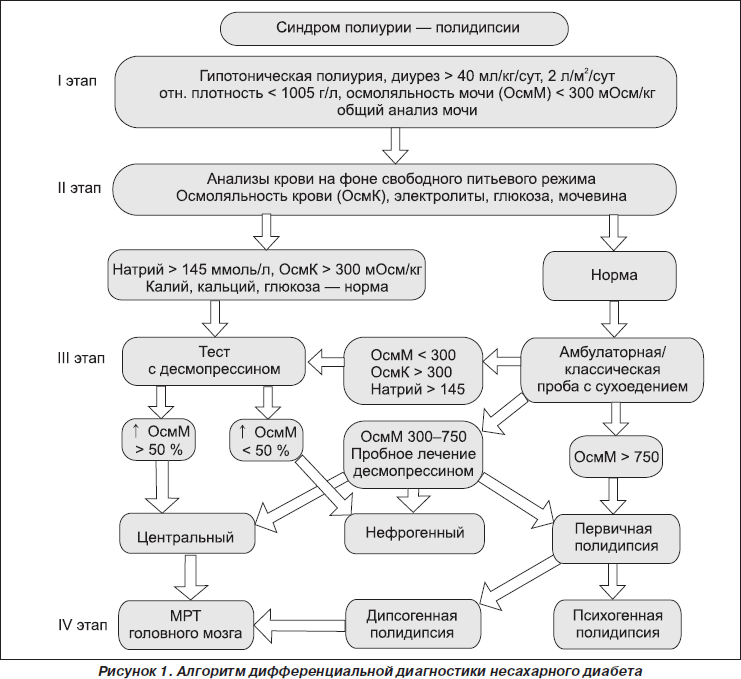
Дифференциальная диагностика НСД базируется на четырех основных этапах: на первом подтверждается гипотоническая полиурия у пациентов с синдромом полиурии — полидипсии, на втором исключаются наиболее распространенные причины нефрогенного НСД (сахарный диабет, гиперкальциемия, гиперкалиемия, гипокалиемия, хроническая почечная недостаточность, мочевая инфекция и др.), на третьем проводятся проба с сухоедением и тест с десмопрессином для исключения первичной полидипсии и нефрогенного НСД соответственно, на четвертом ведется активный поиск причин, например при подтверждении центрального НСД осуществляется МРТ-исследование головного мозга (рис. 1).
Измерение осмотической концентрации крови и мочи при проведении дифференциальной диагностики НСД имеет первостепенное значение, так как именно этот показатель влияет на секрецию АВП через осморецепторы гипоталамуса и является косвенным показателем действия гормона на V2-рецепто- ры почек. В норме осмоляльность крови составляет 280–300 мОсм/кг, ночной или максимально концентрированной порции мочи — 600–1200 мОсм/кг. Определение относительной плотности мочи менее специфично для НСД и имеет некоторые ограничения, такие как невозможность измерения этого показателя в крови, выраженная зависимость результата от присутствия клеточных и неклеточных элементов (клеток крови, эпителия, бактерий и др.) и ошибки диагностики. Применение относительной плотности мочи для диагностики НСД сопряжено с гипердиагностикой заболевания у более чем 15 % пациентов и неправомерным назначением десмопрессина.
Осмотическая концентрация может измеряться специальным прибором — осмометром — по снижению точки замерзания жидкости или рассчитываться по формуле из показателей биохимического анализа, которая имеет следующий вид:
Осмоляльность = 2 ´ [Na (ммоль/л) + + К (ммоль/л)] + глюкоза (ммоль/л) + мочевина (ммоль/л) + 0,03 ´ общий белок (г/л).
История лечения центрального НД берет свое начало с 1912 г., с первого применения при этом заболевании вытяжки задней доли гипофиза. В 1954 г. американский биохимик Vincent du Vigneaud описал структуру и синтезировал АВП, годом позже за эти успехи ему была присуждена Нобелевская премия. Препараты синтетического АВП обладали теми же недостатками, что и эндогенный АВП: очень низкой эффективностью и малой продолжительностью действия, частыми побочными явлениями при интраназальном применении. Переломным моментом стало появление в 1974 г. десмопрессина — синтетического аналога природного АВП, специфического агониста V2-рецепторов, лишенного сосудосуживающей активности и обладающего более выраженным и продолжительным антидиуретическим эффектом. Более 30 лет в заместительной терапии центрального НСД применялся десмопрессин в каплях для интраназального введения (адиуретин). В настоящее время имеются две формы десмопрессина: таблетки минирин (Ferring, Швеция) и интраназальные спреи.
При центральном НСД назначается терапия десмопрессином в начальной дозе 0,1 мг 2–3 раза в сутки внутрь за 30–40 минут до или через 2 часа после еды либо 10 мкг 2 раза в сутки интраназально. Как было показано при обследовании пациентов, получающих постоянную терапию десмопрессином, средние суточные дозы препарата для лечения центрального НСД варьируют от 0,1 до 1,6 мг внутрь и от 10 до 40 мкг интраназально, что обусловлено индивидуальной чувствительностью к препарату и особенностями кишечного и назального всасывания. Потребность в препарате зачастую не коррелирует с объемом выпиваемой/выделяемой жидкости без лечения, индексом массы тела или полом пациента. Однако отмечено, что наименьшая потребность в препарате — 0,1–0,2 мг/сут — характерна для пациентов с центральным НСД послеоперационного и травматического генеза, а самая высокая потребность —до 1,2–2,4 мг/сут в 5–6 приемов — для некоторых пациентов с идиопатическим вариантом центрального НСД.
При использовании препарата внутрь натощак антидиуретическая активность наступает в течение 1 часа и длится от 7 до 12 часов. Интраназальное применение характеризуется более быстрым началом действия — через 15–30 минут. Прием препарата внутрь с пищей снижает его биодоступность и, следовательно, выраженность и продолжительность действия, поэтому при невозможности приема натощак (что нередко бывает при кратности назначения более 2 раз в сутки в середине дня) возможен прием под язык до полного рассасывания. Разжевывание или другое измельчение таблетки не снижает эффективности препарата. При простудных или аллергических заболеваниях, сопровождающихся отеком слизистой носа и невозможностью интраназального применения десмопрессина, распыление препарата в полость рта в дозах, превышающих интраназальные в 1,5–2 раза, может помочь компенсировать симптомы полиурии — полидипсии. В случае необходимости смены одной формы десмопрессина на другую можно воспользоваться следующим ориентировочным пересчетом дозы: клиническая эффективность 0,2 мг таблетированного десмопрессина равна таковой у 10 мкг интраназального. На практике таблетированная форма более удобна при небольшой (до 0,4 мг/сут) потребности пациента в препарате, так как таблетки выпускаются в двух различных дозировках (0,1 и 0,2 мг) и при необходимости легко делятся на части. Интраназальная форма бывает практически незаменима у пациентов с высокой потребностью в препарате (более 40 мкг/сут), которые составляют примерно 10–15 % от всех пациентов с центральным НСД.
Основная цель лечения десмопрессином — подбор минимально эффективной дозы препарата для купирования избыточной жажды и полиурии. Не следует ставить целью лечения обязательное повышение относительной плотности мочи, особенно в каждой из проб анализа мочи по Зимницкому, поскольку при этих анализах не у всех пациентов с центральным НСД на фоне клинической компенсации заболевания достигаются нормальные показатели концентрационной функции почек (с учетом физиологической вариабельности концентрации мочи в течение дня, пожилого возраста, сопутствующей патологии почек и др.). При лечении десмопрессином необходимо инструктировать пациентов о правилах питьевого режима — рекомендовать им пить только при жажде, избегать приема избыточных объемов жидкости.
Залог успеха лечения центрального НСД заключается в адекватной чувствительности центра жажды, нарушения которого могут сопутствовать и осложнять течение НСД.
При изменении функционального состояния центра жажды в сторону снижения порога чувствительности (при гипердипсии) пациенты предрас-положены к развитию такого осложнения терапии десмопрессином, как водная интоксикация, являющаяся потенциальным жизнеугрожающим состоянием. Таким пациентам рекомендуется периодически пропускать приемы препарата для выделения задержанного избытка жидкости или принимать жидкость фиксированно.
Состояние адипсии при центральном НСД может проявляться чередованием эпизодов гипо- и гипернатриемии. Ведение таких пациентов осуществляется при фиксированном ежедневном объеме потребления жидкости или с рекомендациями приема жидкости в объеме выделенной мочи.
Пациентам с нарушением ощущения жажды требуется особый динамический контроль состояния с ежемесячным, а в некоторых случаях и более частым, определением осмоляльности и концентрации натрия крови.
Особого внимания требует лечение центрального НСД после нейрохирургических вмешательств или черепно-мозговых травм, поскольку до 75 % случаев заболевания имеют транзиторное, а 3–5 % — трехфазное течение (I фаза — 5–7 дней — центральный НСД; II фаза — 7–10 дней — синдром неадекватной секреции АВП; III фаза — постоянный центральный НСД). После операции на головном мозге или черепно-мозговой травмы лечение десмопрессином назначается при наличии симптомов НСД (полидипсии, полиурии, гипернатриемии, гиперосмоляльности крови) в дозе 0,05–0,1 мг 2–3 раза в сутки. Каждые 1–3 дня оценивается необходимость приема препарата: пропускается очередная доза, кон-тролируется возобновление симптомов НСД. Через 3–4 недели назначается постоянная терапия в подобранной дозе. Такой подход позволяет избежать возможных осложнений лечения, связанных с транзиторным или трехфазным течением центрального НСД, которые проявляются водной интоксикацией (гипонатриемией, повышением артериального давления, отеками, слабостью, снижением уровня сознания вплоть до комы). Учитывая высокую вероятность ремиссии послеоперационного центрального НСД, которая обычно приходится на 3–6-й месяц после операции, при выписке из стационара пациента целесообразно инструктировать о симптомах водной интоксикации и мерах по ее предотвращению и лечению (рекомендовать снижение дозы/отмену десмопрессина, в тяжелых случаях — применение фуросемида).
Каких-либо контролированных исследований по применению десмопрессина у беременных женщин не проводилось. В настоящее время известно о более чем 150 случаях использования десмопрессина у беременных без вреда для женщины и плода. Десмопрессин для матери в терапевтических дозах трансплацентарный барьер не проходит. Репродуктивные исследования на крысах и кроликах изменений у плода на фоне приема препарата не выявили. Поэтому при наступлении беременности у пациентки с центральным НСД лечение препаратом продолжают в необходимых дозах, которые практически не нуждаются в коррекции. НСД при беременности нередко выделяют как отдельный тип НСД — гестагенный (табл. 1). Диагностика и лечение гестагенного НСД не отличаются от таковых при центральном НСД. Причиной заболевания служит разрушение эндогенного вазопрессина активными ферментами плаценты — вазопрессиназами. Уровень вазопрессина в крови пациентов снижен. Полиурия начинается обычно в III триместре, а после родов спонтанно исчезает. Полиурия не реагирует на экзогенный вазопрессин, но поддается лечению десмопрессином.
Лечение почечного НСД при первичной форме заболевания проводится с помощью тиазидных диуретиков и нестероидных противовоспалительных средств (НПВС). Данное лечение не является патогенетическим, но позволяет уменьшить объем суточной мочи и жажду у большинства пациентов. К сожалению, применение этих препаратов не так эффективно, как терапия десмопрессином при центральном НСД, и объем диуреза редко снижается более чем на 50 % от его первоначальных значений. Много вопросов вызывает также безопасность такой терапии, поскольку и тиазидные диуретики, и препараты группы НПВС при продолжительной терапии обладают рядом серьезных побочных эффектов. Применяются гидрохлортиазид в дозах 25–50 мг/сут, ибупрофен — 600–800 мг/сут, индометацин — 25–75 мг/сут. При приобретенном нефрогенном НСД в обязательном порядке проводится лечение сопутствующего заболевания (гиперпаратиреоза, гипокалиемии и др.).
Лечение частичных/легких форм НСД (с объемом выделяемой мочи менее 4 л в сутки) может проводиться без медикаментозной терапии — назначением потребления достаточных количеств жидкости для удовлетворения жажды.
Лечение первичной полидипсии. При психогенной полидипсии в части случаев происходит «выздоровление» после объяснения пациенту причины его заболевания или наглядной демонстрации концентрации мочи при ограничении приема жидкости в ходе дифференциальной диагностики. У некоторых пациентов эффективным бывает назначение карбамазепина в дозе 200–400 мг/сут — облегчение жажды может наблюдаться не сразу, а развиваться постепенно в течение месяца, при отсутствии положительного влияния препарата более 1–2 месяцев продолжение его приема не рекомендовано. Одним из подходов к лечению ПП может являться применение десмопрессина в прерывистом режиме, т.е. с обязательным пропуском очередной дозы (от ежедневного до нескольких раз в неделю). Это позволяет сократить объем выделяемой мочи и нивелировать проявления жажды. Но необходимо заметить, что такая терапия подойдет только тем пациентам с ПП, которые могут испытывать чувство насыщения жидкостью, у других пациентов неминуемым будет развитие водной интоксикации на фоне приема десмопрессина. В некоторых случаях могут оказаться неэффективными как психотерапия, так и применение психотропных препаратов.
1. Эндокринология / Под ред. проф. П.Н. Боднара. — Винница: НОВА КНИГА, 2007. — 344 с.
2. Дзеранова Л.К., Пигарова Е.А. Минирин в лечении несахарного диабета // Русский медицинский журнал: Эндокринология. — 2005. — Т. 13, № 28(252). — С. 1961-1965.
3. Дзеранова Л.К., Пигарова Е.А. Несахарный диабет // Эндокринология: Национальное руководство / Под ред. И.И. Дедова, Г.А. Мельниченко. — М.: ГЭОТАР-Медиа, 2008. — С. 673-677.
4. Дзеранова Л.К., Пигарова Е.А. Центральный несахарный диабет: современные аспекты диагностики и лечения // Лечащий врач. — 2006. — № 10. — С. 42-47.
5. Мельниченко Г.А., Петеркова В.А., Фофанова О.В. Диагностика и лечение несахарного диабета: Метод. рекомендации. — М., 2003. — 26 с.
6. Пигарова Е.А., Дзеранова Л.К., Рожинская Л.Я. Клинический случай центрального несахарного диабета, осложненного патологией центра жажды // Ожирение и метаболизм. — 2008. — № 3(16). — С. 28-31.
7. Disorders of water metabolism following transsphenoidal pituitary surgery: a single institution’s experience / J.R. Adams et al. // Pituitary. — 2006. — Vol. 9, № 2. — P. 93-99.
8. Ball S.G., Baylis P.H. Vasopressin, diabetes, and syndrome of inappropriate antidiuresis // Endocrinology, 5th ed. / Ed. by L.J. DeGroot and J.L. Jameson. — Philadelphia: Saunders, 2006. — P. 1324-367.
9. Baylis P.H. Posterior pituitary // Comprehensive Endocrinology, Revised Series / Ed. by Hiroo. — Imura Raven Press; 2 Sub. еdition, 1994. — P. 41-85.
10. Bichet D.G. Chapter 7: The posterior pituitary // The pituitary 2nd ed. / Ed. by S. Melmed. — Wiley-Blackwell, 2002. — 747 p.
11. Fenton R.A., Moeller H.B. Recent discoveries in vasopressinregulated aquaporin-2 trafficking // Progress in Brain Research. — Amsterdam; New York: B.V. Elsevier, 2008. — Vol. 170. — P. 571-579.
12. Current perspective on the pathogenesis of central diabetes insipidus / S. Ghirardello et al. // J. Pediatr. Endocrinol. Metab. — 2005. — Vol. 18, № 7. — P. 631-645.
13. Goodfriend T.L., Friedman A.L., Shenker Y. Chapter 133: Hormonal regulation of electrolyte and water metabolism // Endocrinology, 5th ed. / Ed. by L.J. DeGroot and J.L. Jameson. — Philadelphia: Saunders, 2006. — P. 1324-1367.
14. Loh J.A., Verbalis J.G. Diabetes insipidus as a complication after pituitary surgery // Nat. Clin. Pract. Endocrinol. Metab. — 2007. — Vol. 3, № 6. — P. 489-494.
15. Robertson G.L. Disorders of Neurohypophysis // Harrison’s Principles of Internal Medicine / Еd. by E. Braunwald, A.S. Fauci, D.L. Kasper, S.L. Hauser, D.L. Longo, and J.L. Jameson. — New York: McGraw-Hill, 2005. — P. 2097-2101.