Международный эндокринологический журнал 7 (39) 2011
Вернуться к номеру
Симпозиум «Гиперальдостеронизм: определение, этиология, классификация, клинические признаки и синдромы, диагностика, лечение»
Авторы: Панькив В.И. Украинский НПЦ эндокринной хирургии, трансплантации эндокринных органов и тканей МЗ Украины
Рубрики: Эндокринология
Версия для печати
Проводит: Донецкий национальный медицинский университет им. М. Горького.
Рекомендован: эндокринологам, терапевтам, семейным врачам.
Гиперальдостеронизм — это синдром, обусловленный гиперсекрецией главного надпочечникового минералокортикоида — альдостерона.
Первичный гиперальдостеронизм — клинический синдром, развивающийся в результате избыточной продукции альдостерона корой надпочечников и проявляющийся артериальной гипертензией (АГ) в сочетании с гипокалиемией.
Псевдогиперальдостеронизм — группа заболеваний, характеризующихся АГ с гипокалиемическим алкалозом и низкой, нестимулируемой активностью ренина плазмы. Они сходны с классическим гиперальдостеронизмом, но отличаются от него низким уровнем альдостерона в плазме крови.
Вторичный гиперальдостеронизм — повышенная продукция альдостерона корой надпочечников, вызываемая стимулами, исходящими не из надпочечников; имитирует первичную форму болезни. Причиной служат АГ и состояния, сопровождающиеся отеками (например, сердечная недостаточность, цирроз печени с асцитом, нефротический синдром).
Эпидемиология
Распространенность гиперальдостеронизма составляет до 25 % среди больных АГ, причем гипокалиемия (т.е. «классический» первичный гиперальдостеронизм) имеется лишь у 41 % обследованных.
Первичный гиперальдостеронизм обычно встречается в возрасте 30–40 лет, у женщин чаще, чем у мужчин (соотношение 3 : 1). Для одной из форм первичного гиперальдостеронизма — глюкокортикоидзависимого гиперальдостеронизма характерно начало в подростковом или юношеском возрасте.
Наследственные формы псевдогиперальдостеронизма (синдром Лиддла) развиваются у детей дошкольного возраста.
Возраст дебюта и распространенность вторичного гиперальдостеронизма определяются фоновым заболеванием.
Классификация
Гиперальдостеронизм подразделяют:
на первичный гиперальдостеронизм:
— одиночная альдостеронпродуцирующая аденома надпочечника (альдостерома, синдром Конна) (65 % случаев);
— идиопатический гиперальдостеронизм, обусловленный двусторонней диффузной мелкоузелковой гиперплазией коры надпочечников (30–40 %);
— односторонняя надпочечниковая гиперплазия;
— глюкокортикоидзависимый гиперальдостеронизм — редкое семейное заболевание, обусловленное дефектом гена 18-гидроксилазы (1–3 %);
— альдостеронпродуцирующая карцинома (0,7–1,2 %);
— псевдогиперальдостеронизм:
— псевдогиперальдостеронизм 1-го типа (избыток альтернативных минералокортикоидов):
– болезнь и синдром Иценко — Кушинга, эктопический АКТГ-синдром;
– кортикостеронсекретирующая аденома или карцинома; персистирование фетальной зоны коры надпочечников; врожденная гиперплазия надпочечников (дефицит 11b-гидроксилазы, 17a-гидроксилазы и 18-оl-дегидрогеназы);
— псевдогиперальдостеронизм 2-го типа (нарушение метаболизма минералокортикоидов или их связывания с рецепторами):
– врожденная или ятрогенная недостаточность 11b-гидроксистероиддегидрогеназы и/или 5b-стероид-редуктазы;
– резистентность к глюкокортикоидным средствам (ГКС): (дефект глюкокортикоидных рецепторов с избыточной секрецией адренокортикотропного гормона (АКТГ) и дезоксикортикостерона);
— псевдогиперальдостеронизм 3-го типа (тубулопатии):
– синдром Гительмана (гипокалиемический метаболический алкалоз, гипермагниурия и гипомагниемия, сниженная экскреция кальция); синдром Лиддла (редкое наследственное заболевание с клинической картиной гиперальдостеронизма, но чрезвычайно низким уровнем альдостерона в крови; в основе лежит повышенная реабсорбция натрия в дистальных канальцах вследствие мутации гена b-субъединицы амилоридчувствительного натриевого канала);
вторичный гиперальдостеронизм:
— стимуляция ренин-ангиотензин-альдостероновой системы (РААС):
– органический вторичный гиперальдостеронизм, сочетающийся с АГ (стеноз почечных артерий, ренинпродуцирующая опухоль почки — ренинома);
– функциональный вторичный гиперальдостеронизм без АГ (гипонатриемия, гиповолемия, синдром Барттера (повышение экскреции калия с мочой, гипокалиемический алкалоз, гиперренинемия, гиперальдостеронизм, метаболический алкалоз, нормальное или пониженное АД);
— относительный вторичный гиперальдостеронизм, развивающийся в результате нарушения метаболизма альдостерона (почечная, сердечная недостаточность, цирроз печени, нефротический синдром).
Этиология и патогенез
Альдостерон — основной и самый активный минералокортикоидный гормон, секретируемый клубочковой зоной коры надпочечников.
Альдостерон выполняет четыре важные биологические функции:
— повышает реабсорбцию натрия в почечных канальцах;
— увеличивает экскрецию калия;
— увеличивает секрецию протонов водорода;
— оказывает ингибиторный эффект на юкстагломерулярный аппарат почек, тем самым снижая секрецию ренина.
Первичный гиперальдостеронизм
Повышение реабсорбции натрия в почечных канальцах сопровождается увеличением его уровня в крови. Задержка натрия способствует задержке жидкости. Кроме того, повышенная концентрация натрия увеличивает чувствительность гладкомышечных клеток артериол к вазоактивным веществам, в т.ч. к ангиотензину II, катехоламинам и простагландинам. Все это наряду с избыточным потреблением соли способствует стойкому повышению артериального давления (АД), особенно диастолического. Задержка натрия в крови способствует развитию гиперволемии, подавляющей выработку ренина и ангиотензина II, что и наблюдается у больных первичным гиперальдостеронизмом. В связи с подавлением активности РААС при первичном гиперальдостеронизме наблюдается парадоксальное снижение концентрации альдостерона в крови в ответ на ортостаз.
Установлено, что примерно в 60 % случаев первичный гиперальдостеронизм обусловлен аденомой коры надпочечников, которая, как правило, бывает односторонней, размером не более 3 см (нечувствительна к ангиотензину II и не зависит от секреции АКТГ).
Вторая по частоте форма первичного гиперальдостеронизма — идиопатический гиперальдостеронизм встречается в 30–40 % случаев. Само название «идиопатический» говорит о том, что этиология гиперальдостеронизма неясна. Существует мнение, что идиопатический гиперальдостеронизм является заключительной стадией эволюции низкорениновой эссенциальной АГ. Развитие идиопатического альдостеронизма связано с двусторонней мелко- или крупноузелковой гиперплазией коры надпочечников. В клубочковой зоне гиперплазированных надпочечников секретируется избыточное количество альдостерона, что приводит к развитию АГ, гипокалиемии и снижению уровня ренина плазмы. Принципиальным отличием идиопатического гиперальдостеронизма является сохраненная чувствительность гиперплазированной клубочковой зоны к стимулирующему влиянию ангиотензина II. В данном случае образование альдостерона контролируется АКТГ.
Редкая форма первичного гиперальдостеронизма — гиперальдостеронизм, сочетающийся с двусторонней мелкоузелковой гиперплазией коры надпочечников; при этом прием ГКС приводит к снижению АД и нормализации обмена калия. При глюкокортикоидзависимом гиперальдостеронизме образуется дефектный фермент в результате неравного кроссинговера генов 11b-гидроксилазы и альдостеронсинтетазы. В норме ген, кодирующий альдостеронсинтетазу, экспрессируется только в клубочковой зоне, и только в этой зоне синтезируется альдостерон. В результате мутации пучковая зона, главным регулятором функции которой является АКТГ, приобретает способность синтезировать альдостерон, а также большое количество 18-оксикортизола и 18-гидроксикортизола.
Злокачественная опухоль коры надпочечников крайне редко является причиной первичного альдостеронизма.
Псевдогиперальдостеронизм
В основе патогенеза псевдогиперальдостеронизма лежат врожденный дефицит/дефект фермента 11b-ги-дроксистероиддегидрогеназы, врожденный дефицит Р450с11, некоторые наследственные болезни. Синдром Лиддла является аутосомно-доминантным заболеванием. В его основе лежит мутация гена, кодирующего b- и/или g-части амилоридчувствительных натриевых канальцев почек. Это приводит к торможению синтеза ангиотензина I, его переходу в ангиотензин II и снижению секреции альдостерона.
Вторичный гиперальдостеронизм
При вторичном гиперальдостеронизме усиление секреции альдостерона обусловлено вненадпочечниковыми факторами (например, повышением активности ренина плазмы — АРП). Главное звено патогенеза вторичного гиперальдостеронизма — усиление секреции ренина клетками юкстагломерулярного аппарата почек. К наиболее частым причинам усиления секреции ренина относятся:
— потеря натрия (ограничение хлорида натрия в диете, прием диуретиков, понос, сольтеряющие нефропатии);
— уменьшение объема циркулирующей крови (ОЦК) (при кровопотере, дегидратации) или перераспределение внеклеточной жидкости со снижением объема крови в крупных сосудах при отечных синдромах (нефротический синдром, цирроз печени с асцитом, застойная сердечная недостаточность);
— нормальная беременность (возможны очень высокие уровни АРП и альдостерона, особенно во II и в III триместрах);
— чрезмерное потребление калия (непосредственная стимуляция секреции альдостерона);
— в редких случаях — спонтанная гиперсекреция ренина (при синдроме Барттера или ренинсекретирующих опухолях).
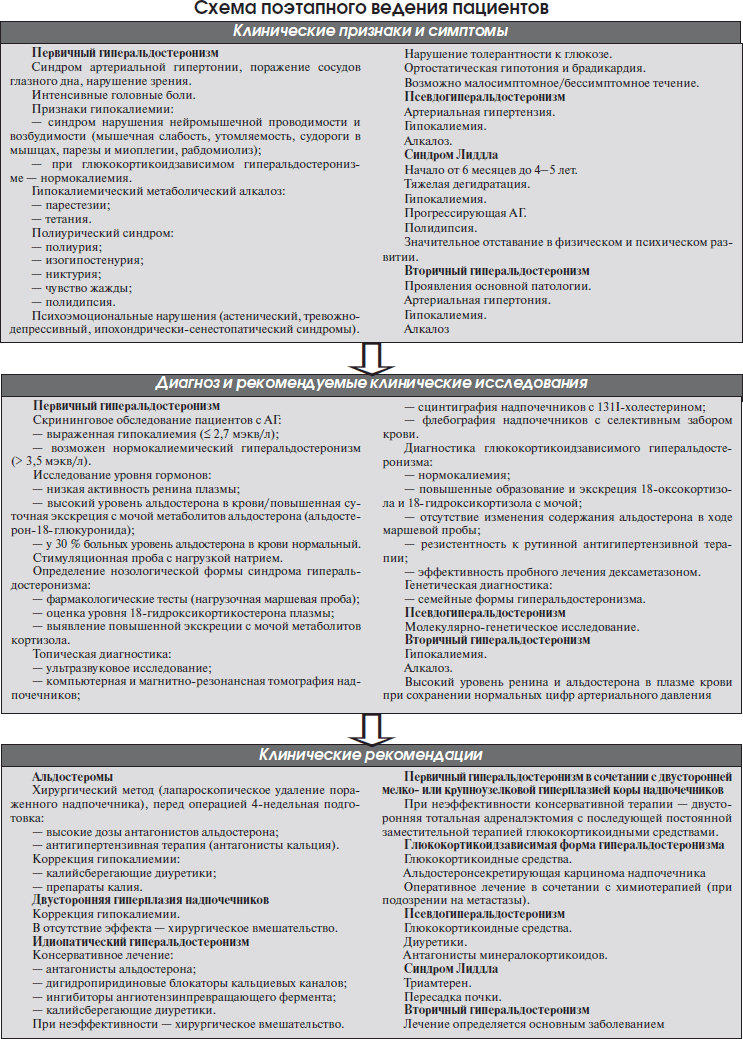
Клинические признаки и симптомы
Первичный гиперальдостеронизм
Основные клинические проявления первичного гиперальдостеронизма включают:
— синдром АГ — практически у 100 % больных первичным гиперальдостеронизмом (постоянно повышенное АД, особенно диастолическое, или кризовый характер АГ; как следствие, развивается выраженная гипертрофия левого желудочка с соответствующими изменениями на ЭКГ). У 50 % больных наблюдают поражение сосудов глазного дна, у 20 % — нарушение функции зрения;
— интенсивные головные боли как при повышении АД, так и в результате гипергидратации головного мозга;
— признаки гипокалиемии обычно проявляются синдромом нарушения нейромышечной проводимости и возбудимости. При этом развиваются мышечная слабость, утомляемость, судороги в мышцах, в тяжелых случаях — парезы и миоплегии. Степень выраженности мышечной слабости различна — от умеренной усталости и быстрой утомляемости до псевдопаралитических состояний. Слабость мышц может быть распространенной либо охватывать определенные группы мышц, чаще нижних конечностей. Самым тяжелым проявлением гипокалиемической и нейротрофической миопатии служит рабдомиолиз. При глюкокортикоидзависимом гиперальдостеронизме, напротив, отмечают нормокалиемию;
— гипокалиемический метаболический алкалоз может проявляться парестезиями и иногда тетанией;
— полиурический синдром обусловлен изменением функции почечных канальцев в условиях гипокалиемии; в результате развиваются полиурия, изогипостенурия, никтурия, возникает чувство жажды и полидипсия;
— возможны психоэмоциональные нарушения (обычно включающие астенический, тревожно-депрессивный и ипохондрически-сенестопатический синдромы). В их основе лежит водно-электролитный дисбаланс;
— нарушение толерантности к глюкозе — примерно у 50 % больных первичным гиперальдостеронизмом (вследствие нарушения секреции инсулина b-клетками поджелудочной железы в условиях гипокалиемии);
— возможны ортостатическая гипотония и брадикардия.
Указанные признаки не всегда присутствуют одно-временно; нередко наблюдается малосимптомное или даже бессимптомное течение заболевания.
Остальные виды гиперальдостеронизма встречаются чрезвычайно редко. Их особенности приведены ниже.
Вторичный гиперальдостеронизм
При вторичном гиперальдостеронизме ведущими клиническими симптомами будут проявления основной патологии, а не гиперальдостеронизма. Иногда возможны АГ, гипокалиемия, алкалоз.
Псевдогиперальдостеронизм
Псевдогиперальдостеронизм обычно сопровождается артериальной гипертензией, гипокалиемией, алкалозом.
Для синдрома Лиддла характерно раннее начало (в возрасте от 6 месяцев до 4–5 лет) с тяжелой дегидратацией, гипокалиемией, прогрессирующей АГ, полидипсией и значительным отставанием ребенка в физическом и психическом развитии.
Диагноз и рекомендуемые клинические исследования
Первичный гиперальдостеронизм
В диагностике синдрома гиперальдостеронизма следует выделять три этапа.
Первый этап — скрининговое обследование пациентов с АГ для исключения первичного гиперальдостеронизма. При этом необходимо как минимум дважды определять уровень калия в крови у всех пациентов с АГ.
Для гиперальдостеронизма характерна выраженная гипокалиемия (< 2,7 мэкв/л), не связанная с приемом гипотензивных лекарственных средств (ЛС). Однако возможен и нормокалиемический гиперальдостеронизм (уровень калия > 3,5 мэкв/л).
Второй этап — диагностика синдрома первичного гиперальдостеронизма включает исследование уровня гормонов: АРП и альдостерона в крови или метаболитов альдостерона в суточной моче (альдостерон-18-глюкуронида).
При первичном гиперальдостеронизме обнаруживают:
— низкую АРП. Однако нередко низкая активность ренина может быть обусловлена приемом диуретиков и вазодилататоров, которые стимулируют секрецию ренина. Кроме того, низкий уровень ренина отмечают у 25 % больных гипертонической болезнью и пожилых;
— высокий уровень альдостерона в крови или повышенную суточную экскрецию с мочой метаболитов альдостерона (альдостерон-18-глюкуронида). Однако у 30 % больных первичным гиперальдостеронизмом уровень альдостерона в крови нормальный. Следует помнить, что уровень альдостерона в крови и моче снижается при старении, а также при гиперволемии, гипокалиемии или повышенном потреблении натрия.
При сомнительных результатах исследований целесообразно провести стимуляционную пробу с нагрузкой натрием, основанную на увеличении ОЦК. Пациент при этом находится в горизонтальном положении. Введение 2 л изотонического раствора хлорида натрия со скоростью 500 мл/ч в норме приводит к снижению уровня альдостерона не менее чем на 50 % от исходного. Уровень альдостерона в плазме выше 5–10 нг/дл (или 138–276 пкмоль/л) свидетельствует об автономности секреции альдостерона, т.е. о первичном гиперальдостеронизме.
Третий этап — определение нозологической формы синдрома гиперальдостеронизма — включает:
— проведение фармакологических тестов, например нагрузочной маршевой пробы, при которой сравнивают уровни альдостерона, ренина и калия крови после ночного покоя и после 4-часовой ходьбы (для дифференциальной диагностики опухолевого и идиопатического генеза гиперальдостеронизма). При альдостероме, т.е. опухолевом происхождении гиперальдостеронизма, содержание альдостерона и АРП в крови после нагрузки будет ниже, чем до нагрузки. При идиопатическом гиперальдостеронизме концентрация альдостерона в указанные периоды почти не изменится. У здоровых людей в ответ на нагрузку отмечается повышение АРП и уровня альдостерона;
— оценку уровня 18-гидроксикортикостерона плазмы. Повышение уровня 18-гидроксикортикостерона является надежным признаком первичного гиперальдостеронизма. При идиопатическом гиперальдостеронизме уровень 18-гидроксикортикостерона в норме или незначительно повышен;
— выявление повышенной экскреции с мочой метаболитов кортизола (18-оксикортизола и 18-гидроксикортизола), характерное для первичного гиперальдостеронизма.
Топическая диагностика позволяет установить локализацию и характеристики опухолей надпочечников, выявить гиперплазию надпочечников:
— ультразвуковое исследование (УЗИ). Это самый доступный и безопасный метод топической диагностики. Его чувствительность составляет 92 %, а при проведении интраоперационного УЗИ — более 96 %;
— КТ и МРТ надпочечников. Чувствительность КТ при диагностике альдостеронпродуцирующих аденом составляет 62 %, тогда как чувствительность МРТ достигает 100 %;
— сцинтиграфия надпочечников с 131I-холестерином. Чувствительность радиоизотопной сцинтиграфии надпочечников с 131I-6-бета-йодметил-19-норхолестерином (NP-59) сопоставима с чувствительностью КТ и МРТ и составляет около 90 %. Но специфичность этого метода, в т.ч. при диагностике односторонней мелко- и крупноузловой гиперплазии, приближается к 100 %. Асимметричное накопление радиоизотопа в ткани обоих надпочечников позволяет идентифицировать альдостеронсекретирующую аденому. При идиопатическом гиперальдостеронизме после введения NP-59 отмечается умеренное его поглощение обоими надпочечниками через 72–120 ч. Радиоизотопная сцинтиграфия позволяет установить локализацию различных опухолей надпочечников при аденоме диаметром от 0,5 см, а также выявить диффузную либо диффузно-узловую гиперплазию обоих надпочечников при идиопатическом гиперальдостеронизме. Однако нужно учесть, что обязательна предварительная блокада щитовидной железы, т.к. NP-59 содержит радиоактивный йод;
— флебография надпочечников с селективным забором крови для исследования градиента концентрации альдостерона и ренина плазмы на разных уровнях венозного русла. Это высокоточный, но инвазивный и сложный метод дифференциальной диагностики при первичном гиперальдостеронизме.
Диагностика глюкокортикоидзависимого гиперальдостеронизма основывается:
— на выявлении нормокалиемии;
— обнаружении повышенного образования и экскреции 18-оксокортизола и 18-гидроксикортизола с мочой;
— отсутствии изменения содержания альдостерона в ходе маршевой пробы;
— резистентности к рутинной антигипертензивной терапии;
— результатах пробного лечения дексаметазоном (2 мг внутрь 1 р/сут в течение 4 недель) или преднизолоном (5 мг внутрь 2 р/сут в течение 4–6 недель). Эффективность терапии (исчезновение симптомов гиперальдостеронизма через 3–4 недели) указывает на глюкокортикоидзависимый гиперальдостеронизм.
Установить диагноз семейных форм гиперальдостеронизма возможно только с помощью генетической диагностики:
— семейная форма первичного гиперальдостеронизма 1-го типа (глюкокортикоидзависимый первичный гиперальдостеронизм). Наследование по аутосомно-доминантному типу. Химерическое удвоение гена как следствие неравного перекреста между геном lip-гидроксилазы (CYP11B1) и геном альдостеронсинтазы (CYP11B2);
— семейная форма первичного гиперальдостеронизма 2-го типа. Отсутствует полиморфизм гена рецептора 1-го типа к ангиотензину II, гена МЭН-1, гена альдостеронсинтетазы (GYP11B2), супрессорного гена р53 или супрессорного гена р16.
Вторичный гиперальдостеронизм
Синдром вторичного гиперальдостеронизма сопровождается гипокалиемией, алкалозом, высоким уровнем ренина и альдостерона в плазме крови при сохранении нормальных цифр АД. Такой синдром встречается при заболеваниях почек (нефрит, цистиноз, синдром Барттера, тубулопатии, характеризующиеся потерей кальция или магния, почечный канальцевый ацидоз).
Псевдогиперальдостеронизм
Наиболее точно диагноз отдельных форм псевдогиперальдостеронизма устанавливается с помощью молекулярно-генетического исследования путем обнаружения типичных мутаций или при установлении характерной аминокислотной последовательности измененных белков.
Дифференциальная диагностика
Дифференциальная диагностика проводится между различными формами первичного и вторичного гиперальдостеронизма, а также псевдогиперальдостеронизма (см. выше).
Первичный гиперальдостеронизм
Оперативное лечение
Основным методом лечения больных с альдостеромами является хирургический. В настоящее время все шире применяется проведение лапароскопического удаления пораженного надпочечника. Перед операцией необходима 4-недельная подготовка, включающая высокие дозы антагонистов альдостерона (спиронолактона). Такая терапия позволяет снизить АД, нормализовать содержание калия в организме и функцию РААС. При недостаточном снижении АД на фоне антагонистов альдостерона проводят подбор антигипертензивной терапии с использованием ЛС практически всех групп. Считают, что наиболее патогенетически обосновано назначение антагонистов кальция, которые блокируют стимулирующее действие ангиотензина II на синтез альдостерона благодаря блокаде входа кальция в клетку. Также для коррекции гипокалиемии используют калийсберегающие диуретики (триамтерен, амилорид), возможно назначение препаратов калия.
При подозрении на двустороннюю гиперплазию надпочечников хирургическое вмешательство показано только в тех случаях, когда выраженную и сопровождающуюся клиническими симптомами гипокалиемию не удается купировать медикаментозно с помощью спиронолактона, триамтерена или амилорида. Предоперационная подготовка также направлена на устранение эффектов избытка альдостерона.
При первичном гиперальдостеронизме в сочетании с двусторонней мелко- или крупноузелковой гиперплазией коры надпочечников показана медикаментозная терапия. При ее неэффективности проводят двустороннюю тотальную адреналэктомию с последующей постоянной заместительной терапией ГКС.
При идиопатическом гиперальдостеронизме методом выбора является консервативное лечение. Для коррекции АД, устранения гипокалиемии рекомендуют антагонисты альдостерона, дигидропиридиновые блокаторы кальциевых каналов, ингибиторы АПФ, калийсберегающие диуретики. Лишь при неэффективности медикаментозной терапии рекомендуется прибегать к хирургическому вмешательству.
При альдостеронсекретирующей карциноме надпочечника показано оперативное лечение в сочетании с химиотерапией (при подозрении на метастазы).
Предоперационная подготовка
В рамках предоперационной подготовки больным первичным гиперальдостеронизмом назначают:
— аминоглутетимид 250 мг 2–3 р/сут (в 8–9 ч и в 16–18 ч); при необходимости возможно увеличение дозы на 250 мг/сут каждую неделю до максимально переносимой дозы, но не более 1000–1500 мг/сут, 4 нед. (лечение проводят под контролем АД, клинического анализа крови, гормонов щитовидной железы, уровня кортизола в суточной моче не реже чем 1 раз в 10–14 сут.) или
— спиронолактон внутрь 50–100 мг 2–4 р/сут, 2 нед. (после достижения эффекта возможно снижение дозы до 50 мг 2–4 р/сут, в такой дозе ЛС принимают еще 2 нед.). В случае развития побочных эффектов спиронолактона возможна комбинированная терапия меньшими дозами спиронолактона и калийсберегающими диуретиками:
— спиронолактон внутрь 25–50 мг 2 р/сут, 4 нед. + + амилорид внутрь 5–20 мг 1 р/сут, 4 нед. или триамтерен внутрь 50–100 мг 1–2 р/сут, 4 нед. При сохранении повышенного АД на фоне приема спиронолактона и аминоглютетимида к лечению добавляют антигипертензивные ЛС, прежде всего блокаторы кальциевых каналов: амлодипин внутрь 5–10 мг 1–2 р/сут, 4 нед., или верапамил внутрь 40–80 мг 3–4 р/сут, 4 нед., или дилтиазем внутрь 60–180 мг 1–2 р/сут, 4 нед., или нифедипин внутрь 10–20 мг 2–4 р/сут, 4 нед., или фелодипин внутрь 5–10 мг 1–2 р/сут, 4 нед. Каптоприл внутрь 12,5–25 мг 3 р/сут, 4 нед., или периндоприл внутрь 2–8 мг 1 р/сут, 4 нед., или рамиприл внутрь 1,25–5 мг 1 р/сут, 4 нед., или трандолаприл внутрь 0,5–4 мг 1 р/сут, 4 нед., или фозиноприл внутрь 10–20 мг 1 р/сут, 4 нед., или хинаприл внутрь 2,5–40 мг 1 р/сут, 4 нед., или эналаприл внутрь 2,5–10 мг 2 р/сут, 4 нед.
В случае недостаточной стабилизации АД возможно добавление антигипертензивных ЛС других классов (целесообразно ведение больного совместно с кардиологом).
Терапия в послеоперационном периоде
Заместительная терапия в послеоперационном периоде включает: гидрокортизон в/м 25–50 мг каждые 4–6 ч, 2–3 сут., с постепенным снижением дозы в течение нескольких дней до полной отмены ЛС при отсутствии признаков надпочечниковой недостаточности.
Постоянная терапия в отсутствие необходимости или при невозможности оперативного лечения
Для постоянного лечения идиопатического гиперальдостеронизма и при невозможности оперативного лечения аденомы или карциномы надпочечника назначают:
— аминоглутетимид 250 мг 2–3 р/сут (в 8–9 ч и в 16–18 ч); при необходимости возможно увеличение дозы на 250 мг/сут каждую неделю до максимально переносимой дозы, но не более 1000–2500 мг/сут, постоянно (лечение проводят под контролем АД, клинического анализа крови, гормонов щитовидной железы, уровня кортизола в суточной моче не реже чем 1 раз в 10–14 сут.) или
— спиронолактон внутрь 50 мг 2 р/сут, постоянно (лечение проводят под контролем уровня калия в крови каждые 2 нед.; целесообразно назначение минимальных эффективных доз ЛС). Для профилактики побочных эффектов спиронолактона возможна комбинированная терапия меньшими дозами спиронолактона и калийсберегающими диуретиками:
— спиронолактон внутрь 25–50 мг 1–2 р/сут, постоянно (лечение проводят под контролем уровня калия в крови каждые 2 нед.) + амилорид внутрь 5–20 мг 1 р/сут, постоянно, или триамтерен внутрь 50–100 мг 1–2 р/сут, постоянно. При выраженной гипокалиемии к терапии добавляют препараты калия: калия хлорид внутрь 40–100 мэкв/сут (в пересчете на калий), до нормализации уровня калия (уровень калия в крови определяют каждые 2–3 сут.), или калия цитрат/калия бикарбонат внутрь 40–100 мэкв/сут (в пересчете на калий), до нормализации уровня калия (уровень калия в крови определяют каждые 2–3 сут.).
После нормализации уровня калия в крови дозу калия снижают: калия хлорид внутрь 16–24 мэкв/сут (в пересчете на калий), длительно, под контролем уровня калия в крови, или калия цитрат/калия бикарбонат внутрь 16–24 мэкв/сут (в пересчете на калий), длительно, под контролем уровня калия в крови.
Терапия ГКС глюкокортикоидзависимой формы гиперальдостеронизма
Глюкокортикоидзависимая форма гиперальдостеронизма не требует оперативного вмешательства. Лечение таких больных дексаметазоном уже через 3–4 недели полностью нормализует АД и устраняет гормональные и метаболические нарушения (гипокалиемию, гиперальдостеронизм, гипоренинемию). Подбирают такую минимальную дозу ГКС, при приеме которой показатели АД остаются в нормальных пределах: дексаметазон внутрь 2 мг 1 р/сут, постоянно, или преднизолон внутрь 5 мг 2 р/сут, постоянно.
Псевдогиперальдостеронизм
Для лечения псевдогиперальдостеронизма используются небольшие дозы дексаметазона, которые устраняют все симптомы гиперминералокортицизма. Прием амилорида или спиронолактона также корригирует электролитные нарушения и гипертонию.
ЛС выбора при лечении больных с синдромом Лиддла является триамтерен: внутрь 50–100 мг 1–2 р/сут, постоянно.
Однако единственным радикальным методом лечения больных с синдромом Лиддла на сегодняшний день является пересадка почки.
Вторичный гиперальдостеронизм
Лечение вторичного гиперальдостеронизма определяется в каждом случае конкретным заболеванием (лечение хронической сердечной недостаточности, компенсация цирроза печени и т.д.).
Оценка эффективности лечения
Критериями эффективности лечения считают нормализацию уровня АД, концентрации калия в крови, результатов нагрузочных проб (например, маршевой), достижение соответствующего возрасту уровня ренина, альдостерона, отсутствие признаков рецидива опухоли по данным методов топической диагностики.
Осложнения и побочные эффекты лечения
Передозировка ЛС, блокирующих биосинтез стероидов в надпочечниках, может приводить к развитию надпочечниковой недостаточности.
Ошибки и необоснованные назначения
Применение антагонистов альдостерона уменьшает тяжесть клинических проявлений гиперальдостеронизма, однако их действие сохраняется лишь в период лечения и спустя непродолжительное время после него.
К сожалению, высокие дозы ЛС вызывают антиандрогенный эффект (импотенцию и гинекомастию у мужчин, снижение либидо, мастопатию, нарушение менструального цикла у женщин). Для снижения побочного действия спиронолактона можно применять небольшие дозы ЛС в сочетании с калийсберегающими диуретиками. Передозировка спиронолактона чревата не только быстрым проявлением побочных эффектов, но и гиперкалие- мией.
Прогноз
Хирургическое лечение позволяет добиться выздоровления в 50–60 % наблюдений при верифицированной альдостеронпродуцирующей аденоме надпочечника.
При гиперальдостеронизме, обусловленном одиночной аденомой на фоне диффузной или диффузно-узловой гиперплазии коры надпочечника, полного выздоровления добиться, как правило, не удается. Для достижения и поддержания ремиссии в таких случаях требуется практически постоянная терапия спиронолактоном, а у ряда больных — и ингибиторами стероидогенеза.
Аналогичная терапия требуется больным, оперированным (односторонняя адреналэктомия) по поводу гиперальдостеронизма, обусловленного двусторонней диффузной или диффузно-узловой гиперплазией коры.
1. Эндокринология / Под ред. проф. П.Н. Боднара. — Винница: Нова книга, 2007. — 344 с.
2. Балаболкин М.И., Клебанова Е.М., Креминская В.М. Дифференциальная диагностика и лечение эндокринных заболеваний: Руководство. — М.: Медицина, 2002. — С. 653-668.
3. Борнстейн С.Р., Стратакис К.А., Крусос Дж.П. Опухоли коры надпочечников: современные представления об этиологии, патогенезе, диагностике и лечении // Международный журнал медицинской практики. — 2000. — № 11. — C. 30-43.
4. Бочков Н.П., Захаров А.Ф., Иванов В.И. Медицинская генетика. — М., 1984.
5. Гарагезова А.Р., Калинин А.П., Лукьянчиков B.C. Диагностика и лечение минералкортицизма // Клин. мед. — 2000. — № 11. — С. 4-8.
6. Гарагезова А.Р., Калинин А.П., Лукьянчиков B.C. Классификация, этиология и патогенез синдрома минералкортицизма // Клин. мед. — 2000. — № 10. — С. 4-7.
7. Дедов И.И., Балаболкин М.И., Марова Е.М. и др. Болезни органов эндокринной системы: Руководство для врачей / Под ред. акад. РАМН И.И. Дедова. — М.: Медицина, 2000. — С. 353-358.
8. Калинин А.П., Тишенина Р.С, Богатырев О.П. и др. Клинико-биохимические тесты в изучении отдаленных результатов хирургического лечения первичного гиперальдостеронизма и феохромоцитомы. — М.: МОНИКИ, 2000.
9. Павленко А.К., Фадеев В.В., Мельниченко Г.А. Диагностика первичного гиперальдостеронизма // Проблемы эндокринологии. — 2001. — T. 47(2). — C. 15-25.
10. Щетинин В.В., Майстренко Н.А., Егиев В.Н. Новообразования надпочечников / Под ред. В.Д. Федорова. — М.: Мед. практика, 2002.