Международный эндокринологический журнал 6 (54) 2013
Вернуться к номеру
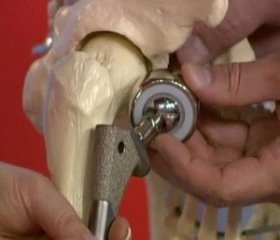
Особливості лікування переломів шийки стегнової кістки у пацієнтів в умовах селенодефіцитного регіону
Авторы: Васюк В.Л., Ковальчук П.Є., Тулюлюк С.В. - Кафедра травматології, ортопедії та нейрохірургії,
Буковинський державний медичний університет, м. Чернівці
Рубрики: Эндокринология
Разделы: Медицинские форумы
Версия для печати
Серед безлічі мінералів селен посідає особливе місце як найбільш суперечливий мікроелемент. Він має дуже вузький діапазон між есенціальною дозою і токсичною. Незамінність елементу було встановлено лише 1957 року.
У 1973 р. було відкрито глутатіонпероксидазу — специфічний селенопротеїн, і лише через тридцять років — інші селенопротеїни. Тоді прийшло розуміння ролі селену в харчуванні та здоров’ї. Це можна вважати справжньою селеновою революцією, яка породила безліч гіпотез і стимулювала нові дослідження й практичне застосування його в медицині.
Фізіологічна добова потреба в селені становить 70 мкг для дорослих чоловіків та 55 мкг для жінок. Під час вагітності та лактації потрібен більш високий рівень — до 200 мкг (табл. 1).
/91/91.jpg)
Сьогодні заслуговує на увагу припущення стосовно того, що дефіцит селену є одним із чинників розвитку та прогресування тиреопатій. Практично всі континентальні держави, до яких належить і Україна, є селенодефіцитними. Особливо мало Sе в ґрунтах і рослинах Вінницької, Волинської, Київської, Луганської, Одеської, Полтавської, Тернопільської, Хмельницької, Чернівецької, Харківської, Чернігівської, Сумської областей і в Криму.
Щитоподібна залоза (ЩЗ) має особливо високу потребу в селені й належить до органів із найвищим рівнем цього елементу на 1 г тканини. Селен, як і йод, є необхідним для нормальної тиреоїдної функції, тиреоїдного гомеостазу.
Встановлено, що всі три дейодинази, що конвертують Т4 у Т3, вміщують селеноцистеїн. Це демонструє, наскільки продукція активного тиреоїдного гормону залежить від селенстатусу. Селеновмісні йодтироксиндейодинази (Ds) присутні в більшості тканин і забезпечують механізм регуляції активації тиреоїдних гормонів. Гормони ЩЗ стимулюють як формування кісткової тканини, так і її резорбцію.
Проблема загоєння переломів кісток є однією з актуальних в травматології. Одним з підходів до її вирішення є вивчення факторів, що впливають на остеогенез.
Мета дослідження — оприлюднити результати аналізу оперативного лікування переломів шийки стегнової кістки в пацієнтів за умов проживання в селенодифіцитному регіоні.
Матеріал та методи дослідження. В основу даного дослідження покладено аналіз результатів хірургічного лікування 28 пацієнтів, які з 2011 по 2012 рік знаходилися на лікуванні в травматологічному відділенні для дорослих ЛШМД м. Чернівці, де їм був проведений остеосинтез шийки стегнової кістки. 28 (100 %) пацієнтів із верифікованим в анамнезі гіпотиреозом та ймовірним вторинним остеопорозом.
З метою діагностики вторинного остеопорозу всім пацієнтам була проведена рентгенівська денситометрія (DEXA). На підставі даних денситометрії у 27 (96,4 %) хворих мінеральна щільність кісткової тканини в шийці стегнової кістки й поперекових хребцях (L1L4) відповідала остеопорозу, а в 1 (3,6 %) — остеопенії. Нормальна пікова кісткова маса (Ткритерій) в одиницях стандартних відхилень (SD) у пацієнтів з остеопорозом була < –2,5 SD, в пацієнтів з остеопенією — у межах від –1 до –2,5 SD.
Відповідно до класифікації Garden переломів I типу відзначено 3 (10,7 %), II типу — 2 (7,1 %), III типу — 16 (57,1 %), IV типу — 7 (24,9 %). Таким чином, більшість (82 %) становили пацієнти з переломами III і IV типів, що супроводжуються розладами кровообігу в головці стегнової кістки і є прогностично несприятливими.
Остеосинтез виконувався фіксаторами: трьома канюльованими спонгіозними гвинтами діаметром 6,5 мм — у 16 (57,1 %) пацієнтів, динамічним стегновим гвинтом (DHS) — у 5 (17,8 %) пацієнтів, трьома неканюльованими спонгіозними гвинтами діаметром 6,5 мм — у 2 (7,1 %) пацієнтів, трилопатевим цвяхом з діафізарною накладкою — 4 (14,2 %) пацієнтів та без діафізарної накладки — 1 (3,5 %) пацієнт.
У групах обстежених хворих 3 (10,7 %) осіб були прооперовані в термін до 24 годин після отримання травми, 13 (46,4 %) осіб прооперовані на 2гу — 5ту добу, 11 (39,2 %) пацієнтам операція проведена на 6–12ту добу і 1 (3,5 %) хворому операція виконана в термін понад 12 діб. Мінімальний час від моменту отримання травми до операції становив 21 годину, максимальний — 16 діб, середній ліжкодень до операції становив 5,86 ± 1,63 дня.
Результати дослідження та їх обговорення. Результати остеосинтезу в терміни від 1 до 1,5 року нами вивчені у 28 (100 %) пацієнтів. Зрощення перелому без ускладнень відмічено в 16 (57,1 %) оперованих хворих. У 12 прооперованих остеосинтез був проведений трьома спонгіозними канюльованими гвинтами — 75 % від числа пацієнтів, у яких застосовувався даний фіксатор; при використанні DHS переломи зрослися в 2 осіб (40 %), при використанні великих спонгіозних гвинтів консолідація наступила у 2 (100 %) пацієнтів. У пацієнтів, яким остеосинтез був зроблений трилопатевим цвяхом із діафизарною накладкою й без неї, зрощення не спостерігалося. Середні строки зрощення в пацієнтів віком до 50 років були 24,6 ± 1,8 тижня, 51–60 років — 25,3 ± 1,8 тижня, 60–77 років — 25,1 ± 2,5 тижня. Ускладнення виявлено в 12 хворих (42,9 %). Незрощення з остеолізом головки відзначені в 4 (25 %) пацієнтів, з них в 1 остеосинтез був виконаний канюльованими гвинтами, у 2 — трилопатевим цвяхом із діафізарною накладкою, в 1 — трилопатевим цвяхом. Асептичні некрози з розвитком тяжкого посттравматичного артрозу спостерігалися в 4 (14,2 %) пацієнтів, з них у 3 пацієнтів остеосинтез був виконаний DHS, а в 1 (67,5 %) — канюльованими гвинтами.
Висновок. Основною причиною переломів шийки стегнової кістки в пацієнтів за умов проживання в селенодефіцитному регіоні є вторинний остеопороз. Без адекватної медикаментозної терапії остеопороз може погіршити результати хірургічного лікування та сповільнювати терміни консолідації.