Международный эндокринологический журнал 2 (58) 2014
Вернуться к номеру
Клинический случай сочетанного течения диффузного токсического зоба и аутоиммунной офтальмопатии
Авторы: Марциник Е.Н., Чурсинова Т.В. — ГУ «Днепропетровская медицинская академия» МЗ Украины, кафедра факультетской терапии и эндокринологии; Сердюк В.Н. — КУ «Днепропетровская областная клиническая офтальмологическая больница»; Пастарус Л.Н., Крайняк Т.Л. — КУ «Днепропетровская городская клиническая больница № 9» ДОС», отделение эндокринологии
Рубрики: Семейная медицина/Терапия, Эндокринология, Офтальмология
Разделы: Справочник специалиста
Версия для печати
В статье представлен опыт лечения пациентки, страдающей диффузным токсическим зобом в сочетании с аутоиммунной офтальмопатией, по поводу чего пациентка принимала тиреостатики, β-блокаторы, системные глюкокортикоиды. На фоне отмены глюкокортикоидов наблюдалось резкое обострение симптомов офтальмопатии, которая приобрела злокачественное течение. Ввиду высокой активности офтальмопатии, отсутствия эффекта от пульс-терапии системными глюкокортикоидами пациентке было выполнено хирургическое вмешательство — транспальпебральная декомпрессия орбиты.
У статті наведено досвід лікування пацієнтки, яка страждає від дифузного токсичного зоба поєднано з автоімунною офтальмопатією, з приводу чого пацієнтка приймала тиреостатики, β-блокатори, системні глюкокортикоїди. На тлі скасування глюкокортикоїдів спостерігалося різке загострення симптомів офтальмопатії, що набула злоякісного перебігу. Зважаючи на високу активність офтальмопатії, відсутність ефекту від пульс-терапії системними глюкокортикоїдами, пацієнтці було виконано хірургічне втручання — транспальпебральна декомпресія орбіти.
The article presents the experience of treating a patient with diffuse toxic goiter in conjunction with autoimmune ophthalmopathy, about what the patient took thyrostatic drugs, β-blockers, systemic glucocorticoids. On the background of glucocorticoids withdrawal there has been detected an acute exacerbation of the symptoms of ophthalmopathy, which acquired malignant course. Due to the high activity of ophthalmopathy, the lack of effect of pulse therapy with systemic glucocorticoids, patient underwent surgery — transpalpebral orbital decompression.
Статья опубликована на с. 60-64
Диффузный токсический зоб (ДТЗ) является аутоиммунным заболеванием, которое развивается вследствие выработки антител к рецептору тиреотропного гормона (ТТГ), сопровождается диффузным увеличением щитовидной железы (ЩЖ) и развитием синдрома тиреотоксикоза [3, 7, 10]. Среди всех случаев диагностики синдрома тиреотоксикоза на долю ДТЗ приходится 80–85 % случаев. Данное заболевание встречается среди всех возрастных групп, однако пик заболеваемости приходится на возрастную группу 30–40 лет. ДТЗ чаще встречается в женской популяции, соотношение больных женского и мужского пола составляет 5 : 1 [3, 8]. В клинической практике часто наблюдается сочетание ДТЗ с патологией, имеющей аутоиммунный генез, такой как аутоиммунная офтальмопатия, претибиальная микседема, акропатия [6, 8].
Аутоиммунная офтальмопатия — аутоиммунное заболевание, сопровождающееся поражением мягких тканей и мышц орбиты, приводящее к экзофтальму и комплексу глазных симптомов. В патологический процесс вовлекаются экстраокулярные мышцы и ретробульбарная жировая клетчатка, при этом наблюдаются воспалительная инфильтрация и отек тканей. Фибробласты тканей орбиты под влиянием цитокинов увеличивают продукцию гликозаминогликанов, накопление которых способствует отеку мягких тканей орбиты [4, 5, 9]. Увеличение объема глазодвигательных мышц и ретробульбарной клетчатки приводит к увеличению внутриглазного давления, проптозу глазных яблок, сдавлению диска зрительного нерва, а также задних коротких и длинных цилиарных артерий [2, 10, 11].
Клиническая картина офтальмопатии вариабельна и зависит от избирательного поражения мягких тканей орбиты (мышечной или жировой ткани). Выявлено, что у больных с офтальмопатией моложе 40 лет в большей степени поражается ретробульбарная жировая клетчатка, что приводит к увеличению объема ретробульбарного пространства и проптозу глазных яблок. У больных старше 70 лет в процесс вовлекаются преимущественно экстраокулярные мышцы, что сопровождается ограничением подвижности глазных яблок [1, 3].
Больная И., 42 лет, 28.09.2009 поступила в отделение эндокринологии городской клинической больницы № 9 г. Днепропетровска с жалобами на сердцебиение, дрожь в конечностях, одышку при умеренной физической нагрузке, снижение массы тела на 5 кг с августа 2009 г., отечность век, рези и чувство давления в области глазных яблок, снижение работоспособности, эмоциональную лабильность.
Из анамнеза: считает себя больной с августа 2009 г., в поликлинике по месту жительства выявлен синдром тиреотоксикоза, в связи с которым была направлена на стационарное лечение в отделение эндокринологии с диагнозом «впервые выявленный тиреотоксикоз, средней тяжести, декомпенсированный».
Из перенесенных заболеваний отмечает хронический гайморит с 1996 г., курение как фактор риска развития офтальмопатии отсутствует.
При первичной госпитализации (28.09.2009): состояние больной средней тяжести. Рост — 160 см, вес — 54 кг, ИМТ — 21 кг/м2. Отмечается эмоциональная неустойчивость, плаксивость. Кожные покровы повышенной влажности. При пальпации ЩЖ диффузно увеличена, безболезненная, эластичной консистенции, свободно смещается при глотании. Обращал на себя внимание умеренный двусторонний экзофтальм, более выраженный справа, инъекция сосудов склер, периорбитальный отек с обеих сторон, D > S. Положительные симптомы Краузе, Дальримпля, Грефе, Кохера. Подвижность глазных яблок не ограничена. Симптом Мари положительный. При аускультации сердца тоны громкие, тахикардия — 115 уд/мин, АД — 130/60 мм рт.ст. Периферических отеков нет. При обследовании органов дыхания, мочевыделения, желудочно-кишечного тракта патологии не выявлено.
Данные обследования
Клинический анализ крови (от 29.09.2009): гемоглобин — 132 г/л, эритроциты — 4,1 • 1012/л, лейкоциты — 4,7 • 109/л, СОЭ — 12 мм/час, нарушений лейкоцитарной формулы не выявлено.
Биохимический анализ крови (от 29.09.2009): билирубин общий — 10 мкмоль/л, АЛТ — 20 ЕД/л, АСТ — 26 ЕД/л, креатинин — 54 мкмоль/л, холестерин — 3,2 ммоль/л.
Гликемия — 5,3 ммоль/л.
Исследование функции ЩЖ (от 29.09.2009): св. Т4 — 47,4 пмоль/л (норма 9–28 пмоль/л), св. Т3 — 14,5 пмоль/л (норма 3,8–7,7 пмоль/л), ТТГ — < 0,05 мМЕ/л (норма 0,35–5,5 мМЕ/л), антитела к ТПО — 30,5 МЕ/мл (норма < 30 МЕ/мл).
Общий анализ мочи без патологии.
Ультразвуковое исследование (УЗИ) ЩЖ: железа расположена в типичном месте, увеличена за счет обеих долей, суммарный объем — 21 см3, капсула уплотнена. Эхогенность ткани значительно снижена. Эхоструктура диффузно неоднородна за счет чередования участков повышенной и пониженной эхогенности, имеют место мелкие фиброзные включения. Дополнительные образования не выявлены. Регионарные шейные лимфоузлы не визуализируются.
УЗИ орбит: ретробульбарная клетчатка повышенной эхогенности, переднезадний размер (ПЗР) ретробульбарной клетчатки справа — 18,5 мм, слева — 17 мм, диаметр наружных прямых мышц — 6 мм.
Электрокардиография (ЭКГ) (от 29.09.2009): ритм сердца синусовый, правильный, частота сердечных сокращений (ЧСС) — 112 уд/мин. Электрическая ось сердца не отклонена. Увеличение амплитуды зубца Т в отведениях II–III, V2–V6.
Клинический диагноз: диффузный токсический зоб I степени (ВОЗ, 2000), средней тяжести, декомпенсированный. Аутоиммунная офтальмопатия, 3-й класс, активная фаза.
Больной назначена терапия: тирозол 10 мг 3 раза в сутки, анаприлин 20 мг 4 раза в сутки, преднизолон 30 мг в сутки, диакарб 250 мг через день, калипоз 1 табл. 2 раза в сутки, глицин по 1 табл. 3 раза в сутки.
На фоне проводимой терапии состояние пациентки с положительной динамикой, уменьшилась выраженность симптомов тиреотоксикоза, таких как сердцебиение, тремор конечностей, масса тела увеличилась на 3 кг, исчезла одышка.
При объективном исследовании: симптом Мари слабоположительный. При аускультации сердца сохраняется правильный ритм, ЧСС в состоянии покоя в диапазоне 64–70 уд/мин. Также уменьшились симптомы офтальмопатии, исчезли рези в глазах, несколько уменьшился экзофтальм, сократилась отечность век. Пациентка выписана из стационара 12.10.2009 под наблюдение участкового эндокринолога, окулиста. При выписке из стационара больной был рекомендован прием препаратов: тирозол 30 мг в сутки, через 4 недели от начала приема снижение дозы до 20 мг в сутки, последующая коррекция дозы тирозола на амбулаторном этапе под контролем клинических симптомов, уровня ТТГ; анаприлин 60 мг в сутки; преднизолон 30 мг в сутки, через 4 недели от начала приема препарата снижение дозы на 5 мг в неделю.
После выписки из стационара больная И. наблюдалась у участкового эндокринолога, окулиста, выполняла рекомендации, данные в период стационарного лечения. В начале декабря, после завершения запланированного курса глюкокортикоидов, резко усилились симптомы офтальмопатии, в связи с чем 07.12.2009 больная была госпитализирована в Днепропетровскую областную клиническую офтальмологическую больницу (ДОКОБ). При поступлении предъявляла жалобы на резкое выстояние глазных яблок, больше справа, снижение зрения, более выраженное со стороны правого глаза.
Офтальмологическое обследование
Правый глаз: резко выстоит из глазной щели, подвижность глазного яблока отсутствует, выраженный красный хемоз конъюнктивы. Конъюнктива глазного яблока резко гиперемирована, отечная с элементами некроза, выражен симптом «креста». Роговица сухая, эрозированная, инфильтрированная в глубоких слоях. Передняя камера средней глубины, влага прозрачная. Зрачок диаметром 2 мм. Глубже лежащие среды не дифференцируются.
Левый глаз: умеренно выстоит из глазной щели, подвижность ограничена. На роговице у лимба на 6 часах точечные серые инфильтраты. Передняя камера средней глубины. Диск зрительного нерва с четкими границами, бледен.
Острота зрения: правого глаза — 0,04, коррекция зрения не улучшает, левого глаза — 0,9–1.
Периметрия: правый глаз: верх 30°, внутренний отдел 35–40°, темпоральный 65°; левый глаз: верх 50°, внутренний отдел 50°, темпоральный 75°.
Клинический диагноз: злокачественная эндокринная офтальмопатия обоих глаз, активная фаза, ксероз роговицы правого глаза, атрофия зрительного нерва, краевой кератит левого глаза.
Больная получала терапию: инстилляции антисептиков, корнерегеля, солкосерила. На фоне проводимой терапии состояние больной без положительной динамики, выстояние глазных яблок в прежнем размере, сохраняется красный хемоз конъюнктивы, в области правого глаза хемоз конъюнктивы и ксероз роговицы более выражены в сравнении с левым глазом.
14.12.2009 больная И. выписана из Днепропетровской областной клинической офтальмологической больницы с рекомендациями проводить пульс-терапию преднизолоном в условиях отделения эндокринологии, куда поступила 15.12.2009 с диагнозом: диффузный токсический зоб I степени (ВОЗ, 2000), средней тяжести, медикаментозно компенсированный. Злокачественная аутоиммунная офтальмопатия обоих глаз, активная фаза, ксероз роговицы правого глаза, атрофия зрительного нерва, краевой кератит левого глаза.
При поступлении сохраняются жалобы на значительное увеличение глазных яблок, в большей степени правого, невозможность закрывать веки, чувство давления в области глазных яблок.
Состояние больной тяжелое, обусловлено аутоиммунной офтальмопатией, при этом симптомы тиреотоксикоза клинически не выражены. Рост — 160 см, вес — 57 кг, ИМТ — 22,3 кг/м2. При пальпации щитовидная железа диффузно увеличена, безболезненная, эластичной консистенции, свободно смещается при глотании. Симптом Мари отрицательный. Тоны сердца приглушены, ритм правильный, ЧСС — 74 уд/мин, АД — 120/70 мм рт.ст. Также не выявлено патологии со стороны органов дыхания, мочевыделения, желудочно-кишечного тракта.
Осмотр глазных яблок: злокачественный экзофтальм обоих глазных яблок, более выражен справа. Периорбитальные отеки с обеих сторон. Верхнее веко прикрывает правую глазную щель на 1/3, левую — на 2/3. Подвижность правого глазного яблока отсутствует, выраженный хемоз конъюнктивы — резкая гиперемия, отек конъюнктивы с элементами некроза. Подвижность левого глазного яблока ограничена, явления хемоза выражены в меньшей степени в сравнении с правым глазным яблоком.
Данные обследования
Общий и биохимический анализы крови, анализ мочи без патологии.
ЭГК (от 16.12.2009): ритм синусовый, правильный, ЧСС — 72 уд/мин. Электрическая ось сердца не отклонена.
Исследование функции ЩЖ (от 16.12.2009): св. Т4 — 7,4 пмоль/л, св. Т3 — 2,21 пмоль/л, ТТГ — 12,87 мМЕ/л. Полученные данные свидетельствовали о полной компенсации тиреотоксикоза и достижении медикаментозного транзиторного гипотиреоза.
Магнитно-резонансная томография орбит (от 17.12.2009). Произведены Т1-, Т2-взвешенные аксиальные, коронарные, сагиттальные томограммы орбит. На полученных томограммах определяется увеличение в объеме внутренних, верхних и нижних прямых мышц глазного яблока с двух сторон, отек периорбитальных тканей. Заключение: МР-картина двустороннего экзофтальма (рис. 1, 2).
Проводилась пульс-терапия метилпреднизолоном в дозе 1000 мг внутривенно-капельно через день 5 введений, суммарная доза составила 5000 мг. На фоне проведения пульс-терапии глюкокортикоидами отмечалось увеличение АД до 150/90 мм рт.ст., по поводу чего были назначены энап 10 мг 2 раза в сутки, верошпирон 50 мг в сутки утром. Также пациентка получала тиреостатическую терапию в режиме «блокируй и замещай» с использованием тирозола в дозе 10 мг в сутки в комбинации с L-тироксином в дозе 12,5 мкг в сутки, анаприлин 20 мг 3 раза в сутки, калипоз 1 табл. 2 раза в сутки, пантасан 40 мг 2 раза в сутки, инстилляции корнерегеля, окомистина.
В результате проведенной терапии в состоянии больной наблюдалась незначительная положительная динамика, уменьшились гиперемия и отек конъюнктивы, а также периорбитальные отеки. Однако сохранялись резкий экзофтальм, более выраженный справа, ограничение подвижности глазных яблок, явления хемоза.
Учитывая наличие у пациентки злокачественного течения офтальмопатии, которая сопровождается атрофией зрительного нерва, отсутствие значительного эффекта от проводимой консервативной терапии, а также на основании выводов консилиума с участием эндокринологов и офтальмологов было принято решение о необходимости проведения хирургического вмешательства — декомпрессии орбиты в условиях ДОКОБ. При выписке пациентке был рекомендован прием метилпреднизолона в дозе 48 мг в сутки, продолжить прием назначенных ранее медикаментов, включая тиреостатики в комбинации с L-тироксином, бета-блокаторы, верошпирон, ингибиторы АПФ, ингибиторы протонной помпы, глазные капли, ускоряющие процессы регенерации, местные антисептики.
В условиях ДОКОБ офтальмологами было принято решение о выполнении транспальпебральной декомпрессии орбиты правого глаза, которая является малотравматичным хирургическим вмешательством, выполняемым пациентам с аутоиммунной офтальмопатией с целью эвакуации орбитальной жировой клетчатки [2].
Протокол операции
Операционное поле обработано кутасептом. Анестезия: раствор лидокаина 2% 1,5 мл ретробульбарно. Разрез кожи выполнен по верхненаружному (с 9 до 12 часов на правом глазу) и нижневнутреннему краю орбиты (с 3 до 6 часов на правом глазу). В раны введены ранорасширители. Вскрыта теноновая капсула, ретробульбарная клетчатка частично иссечена на всем протяжении прямых мышц, сосуды коагулированы. Резекция ретробульбарной клетчатки произведена до приобретения физиологического положения глазного яблока в орбите. Наложены швы на кожу, нейлон 6/0, асептическая повязка.
В послеоперационном периоде для профилактики инфекционных осложнений пациентке вводили цефтриаксон внутримышечно по 1 г 2 раза в сутки, а также тобрадекс по 2 капли 3 раза в сутки в оба глаза, эритромициновая глазная мазь на ночь.
Результаты экзофтальмометрии ОД: до операции — 32 мм, после операции — 25 мм. Острота зрения ОД: до операции — 0,04, после операции — 0,08.
Таким образом, в результате проведенной декомпрессии орбиты правого глаза наблюдалось уменьшение экзофтальма (7 мм по данным экзофтальмометрии), повышение остроты зрения, послеоперационный период протекал без осложнений.
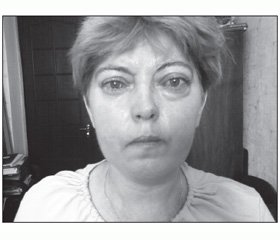
После выписки из стационара пациентка наблюдалась эндокринологом, окулистом, продолжала прием метилпреднизолона, тирозола, L-тироксина. Дозировка метилпреднизолона составляла 48 мг в сутки (0,8 мг/кг) в течение 3 месяцев, затем доза постепенно снижалась на 4 мг в 20 дней до поддерживающей — 4 мг в сутки. Длительность приема метилпреднизолона после оперативного вмешательства составила 1 год. За весь период наблюдения пациентки имела место положительная динамика со стороны органа зрения, постепенный регресс экзофтальма, более выраженный со стороны правого глазного яблока, улучшение остроты зрения, уменьшение косметического дефекта (рис. 3, 4).
Эутиреоидное состояние пациентки поддерживалось при помощи комбинации тирозола в поддерживающей дозе 10 мг/сутки и L-тироксина в дозе 12,5 мкг/сутки.
Дальнейшее наблюдение за состоянием орбит на фоне приема глюкокортикоидов осуществлялось при помощи ультразвукового исследования.
УЗИ орбит (23.03.2010) через 2 месяца после оперативного вмешательства: ретробульбарная клетчатка неоднородная, повышенной эхогенности. ПЗР справа — 20 мм, слева — 23 мм. Диаметр экстраорбитальных мышц с обеих сторон по 5,5 мм, структура не изменена. Определяется умеренное ограничение подвижности глазных яблок.
УЗИ орбит (06.09.2010): сохраняется неоднородность, повышенная эхогенность ретробульбарной клетчатки. ПЗР без динамики — справа 20 мм, слева 23 мм. Наблюдается уменьшение диаметра экстраорбитальных мышц справа до 3,8 мм, слева — до 4 мм, увеличение смещаемости глазных яблок.
УЗИ орбит (10.01.2011): ретробульбарная клетчатка справа однородной структуры, обычной эхогенности с единичными мелкими фиброзными включениями, слева — неоднородной структуры, обычной эхогенности с множеством фиброзных включений. Некоторое уменьшение ПЗР справа до 19,7 мм, слева — до 22,7 мм. Продолжает уменьшаться диаметр экстраорбитальных мышц, который составил слева 3,7 мм, справа — 3,5 мм. Смещаемость правого глазного яблока незначительно ограничена, левого — в полном объеме.
УЗИ орбит (11.04.2011) проведено при полной отмене глюкокортикоидов: ретробульбарная клетчатка неоднородная за счет мелких фиброзных включений, обычной эхогенности. ПЗР ретробульбарной клетчатки справа — 17,5 мм, слева — 19,2 мм. Экстраорбитальные мышцы не изменены, их диаметр справа — 3,5 мм, слева — 3,7 мм. Определяется незначительное ограничение смещаемости правого глазного яблока.
Таким образом, резкое обострение симптомов офтальмопатии у курируемой больной могло быть связано с отменой глюкокортикоидной терапии или же являлось проявлением активной фазы офтальмопатии. Компенсация тиреотоксикоза не оказала существенного влияния на течение офтальмопатии. Злокачественное течение офтальмопатии, высокая активность процесса, а также недостаточная эффективность проводимой глюкокортикоидной терапии потребовали более агрессивного метода лечения — хирургической декомпрессии орбиты. Хирургами-офтальмологами успешно проведена транспальпебральная декомпрессия орбиты, в результате которой наблюдалась положительная динамика в отношении проптоза глазных яблок, улучшились острота зрения и качество жизни пациентки. Однако проведенное оперативное вмешательство не позволило избежать дальнейшей длительной глюкокортикоидной терапии.
Учитывая данные клинического наблюдения, следует подчеркнуть необходимость тщательного контроля состояния орбит в период снижения дозы и отмены глюкокортикоидной терапии у пациентов с аутоиммунной офтальмопатией. Также следует учитывать особенности естественного течения офтальмопатии, выделять активную стадию офтальмопатии, когда происходит манифестация или утяжеление симптомов заболевания.
1. Бровкина А.Ф. Эндокринная офтальмопатия. — М.: ГЭОТАР-Медицина, 2005. — 174 с.
2. Бровкина А.Ф., Аубакирова А.С. Внутренняя декомпрессия орбиты при некомпенсированном отечном экзофтальме // Вестник офтальмологии. — 2006. — № 3. — С. 3–6.
3. Балаболкин М.И., Клебанова Е.М., Креминская В.М. Фундаментальная и клиническая тиреоидология: руководство. — М.: Медицина, 2007. — 816 с.
4. Балаболкин М.И., Клебанова Е.М., Креминская В.М. Дифференциальная диагностика и лечение эндокринных заболеваний. — М.: Медицинское информационное агентство, 2008. — 725 с.
5. Глазанова Т.В., Бубнова Л.Н., Трунин Е.М. Продукция некоторых цитокинов у больных с аутоиммунными заболеваниями щитовидной железы // Проблемы эндокринологии. — 2005. — № 3. — С. 29–32.
6. Паньків В.І. Практична тиреоїдологія (монографія). — Донецьк: Заславський О.Ю., 2011. — 224 с.
7. Фадеев В.В., Мельниченко Г.А. Болезнь Грейвса // Русский медицинский журнал. — 2005. — № 6. — С. 253–256.
8. Bahn R.S. Graves’ ophthalmopathy // N. Engl. J. Med. — 2010. — Vol. 8. — P. 726–738.
9. Davies T., Marians R., Latif R. The TSH receptor reveals itself // J. Clin. Invest. — 2002. — Vol. 14. — P. 110–161.
10. Krassas E.K., Wiersinga W.M. Thyroid eye disease: current concepts and the EUGOGO perspective // Thyroid international. — 2005. — Vol. 4. — P. 3–18.
11. Wiersinga W.M., Prummel M.F. Pathogenesis of Graves’ ophthalmopathy — current understanding // J. Clin. Endocrinol. Metab. — 2001. — Vol. 86. — P. 501–503.
12. Wiersinga W.M., Bartalena L. Epidemiology and prevention of Graves’ ophthalmopathy // Thyroid. — 2002. — Vol. 12. — P. 855–860.

/62/62.jpg)
/63/63.jpg)