Международный эндокринологический журнал 3 (59) 2014
Вернуться к номеру
Атипичные формы течения аутоиммунных заболеваний щитовидной железы как проявление аутоиммунного синдрома перекреста (overlap-синдрома)
Авторы: Генделека Г.Ф. - Одесский национальный медицинский университет
Рубрики: Эндокринология
Разделы: Справочник специалиста
Версия для печати
Аутоиммунные заболевания щитовидной железы являются относительно частой патологией. В основе патогенеза всех аутоиммунных болезней лежат нарушения иммунной толерантности у генетически предрасположенных лиц, которые приводят к развитию аутоиммунного процесса, направленного против щитовидной железы. Нередко встречаются заболевания щитовидной железы, которые характеризуются комбинацией клинических проявлений, свойственных нескольким заболеваниям этого органа. В данном случае речь идет о так называемом синдроме перекреста (overlap-синдроме). Автор приводит два клинических случая атипичного течения аутоиммунных заболеваний щитовидной железы как проявления аутоиммунного синдрома перекреста (overlap-синдрома) с детальным анализом.
Автоімунні захворювання щитоподібної залози є відносно частою патологією. В основі патогенезу всіх автоімунних хвороб лежать порушення імунної толерантності в генетично схильних осіб, що призводять до розвитку автоімунного процесу, спрямованого проти щитоподібної залози. Нерідко зустрічаються захворювання щитоподібної залози, що характеризуються комбінацією клінічних проявів, властивих декільком захворюванням цього органа. У даному випадку йдеться про так званий синдром перехрещення (overlap-синдром). Автор наводить два клінічних випадки атипового перебігу автоімунних захворювань щитоподібної залози як прояву автоімунного синдрому перехрещення (overlap-синдрому) з детальним аналізом.
Autoimmune thyroid disorders are relatively frequent pathology. The pathogenesis of all autoimmune diseases is based on disorders of the immune tolerance in genetically predisposed individuals, which lead to the development of autoimmune process directed against the thyroid gland. Often there are thyroid disorders, which are characterized by a combination of clinical manifestations common to several diseases of this organ. In this case we are talking about the so-called overlap syndrome. The author cites two clinical cases of atypical course of autoimmune thyroid disease as a manifestation of autoimmune overlap syndrome with a detailed analysis.
синдром перекреста, аутоиммунные заболевания щитовидной железы, атипичные формы течения.
синдром перехрещення, автоімунні захворювання щитоподібної залози, атипові форми перебігу.
overlap syndrome, autoimmune thyroid diseases, atypical forms of course.
Статья опубликована на с. 103-107
В настоящее время структура болезней человека существенно изменилась. Ушли в прошлое многие инфекционные заболевания, уносившие жизни сотен тысяч людей, а на их место пришли болезни цивилизованного общества: ишемическая болезнь сердца, сахарный диабет, ожирение, атеросклероз и другие. Среди последних особое место занимают аутоиммунные заболевания (АИЗ). За последние годы достигнут несомненный прогресс в понимании механизмов аутоиммунных заболеваний, разработаны стандарты их диагностики, а также современные методы лечения. Однако ряд вопросов остается неясным, что делает эту проблему актуальной для практикующих врачей различных специальностей.
Аутоиммунные заболевания щитовидной железы (ЩЖ) являются наиболее частыми аутоиммунными заболеваниями. Их распространенность среди населения достигает 10 %, при этом женщины болеют значительно чаще, чем мужчины. Основными нозологическими формами являются: аутоиммунный тиреоидит (АИТ), а также иммуногенный тиреотоксикоз. Последний получил название диффузного токсического зоба (ДТЗ). Редкими формами АИЗ ЩЖ являются бессимптомный тиреоидит, ятрогенные формы тиреопатий, а также послеродовой тиреоидит.
В патогенезе многих АИЗ ЩЖ определенную роль играют генетические факторы, что подтверждается частотой встречаемости этих болезней в некоторых семьях и высокой конкордантностью у монозиготных близнецов. Изучение наследственности АИЗ ЩЖ в эксперименте и клинических исследованиях позволило сделать вывод о полигенной природе этой патологии, обусловленной несколькими независимыми генами.
Для многих АИЗ ЩЖ установлена взаимосвязь между гаплотипами ІІ класса главного комплекса гистосовместимости (HLA) — DR3, DR4, DR5 и DQ и возникновением болезней. Данные носят неоднозначный характер. Установлена роль как генетических факторов, так и факторов окружающей среды. К последним относят курение и избыточное поступление йода, оба этих фактора ассоциируются с увеличением частоты встречаемости АИТ.
ДТЗ и АИТ — хорошо известные аутоиммунные заболевания ЩЖ. Классическими признаками ДТЗ являются тиреотоксикоз и повышенный уровень антител к рецепторам тиреотропного гормона (ТТГ), а при АИТ — к тиреоидной пероксидазе (ТПО). Кроме этих болезней, группа включает широкий круг заболеваний с различной клинической картиной.
Классификация аутоиммунных заболеваний ЩЖ (по Davies/Amino)
Тип 1. Эутиреоидная форма АИТ
1А с зобом
1В без зоба
Тип 2. Гипотиреоидная форма АИТ
2А с зобом — классический АИТ
2В без зоба — идиопатическая микседема (или атрофический АИТ)
Тип 3. ДТЗ (болезнь Грейвса)
3А — тиреотоксическая форма ДТЗ
3В — эутиреоидная форма ДТЗ
3С — гипотиреоидная форма ДТЗ
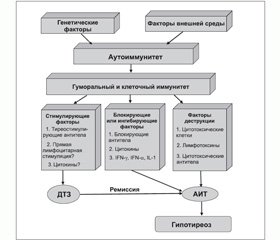
Патогенетически в основе этих болезней лежит нарушение иммунологической толерантности. При генетической предрасположенности под влиянием до сих пор окончательно не установленных факторов окружающей среды происходит активация клеточных и гуморальных аутоиммунных механизмов, направленных против ЩЖ и сходных антигенных структур экстратиреоидных тканей (соединительная, жировая и мышечная ткани, ретробульбарная клетчатка). Это приводит как к деструктивным, так и к функциональным изменениям — стимуляции функции ЩЖ или ее блокированию. В клинической практике положение осложняется тем, что эти отдельные механизмы могут распространяться друг на друга (хашитоксикоз), сменять друг друга (переход тиреотоксикоза при ДТЗ в гипотиреоз при АИТ) или поддерживать равновесие — эутиреоидное состояние (рис. 1).
Вниманию читателей представлены два случая из клинической практики. На основании данных случаев и их анализа можно продемонстрировать важные клинические аспекты аутоиммунных заболеваний ЩЖ. Поскольку диагноз аутоиммунного заболевания ЩЖ в значительной степени базируется на определении антител к тканям ЩЖ, необходимо коснуться их роли в этом процессе.
Антитела к ткани щитовидной железы
Решающее значение в диагностике аутоиммунных заболеваний ЩЖ играют два типа антител: антитела к рецептору ТТГ и к ТПО.
Антитела к тиреоидной пероксидазе (ранее носили название «микросомальные антитела») обнаруживаются при АИТ в 85 % случаев. Биологическое значение антител к ТПО спорно, возможно, они принимают участие в комплемент-опосредованной и/или антителозависимой клеточной цитотоксичности.
Антитела к рецептору ТТГ: речь идет об иммуноглобулинах G (IgG), которые направлены против рецепторов ТТГ. Они могут быть стимулирующими и блокирующими. В случае стимуляции они при связывании с рецепторами активируют секрецию тиреоидных гормонов — Т3 и Т4.
Кроме стимулирующих антител, имеются многочисленные нестимулирующие и блокирующие рецепторы ТТГ. Стимулирующие и блокирующие антитела можно определить только с помощью биологических методов, т.е. функциональных. Такие методы в настоящее время используются только с научно-исследовательской целью. В клинической практике применяют так называемые радиоиммунологические методы определения, которые не позволяют дифференцировать стимулирующие антитела от блокирующих. О характере обнаруженных антител к рецепторам ТТГ позволяет судить анализ клинических данных и лабораторных параметров функции ЩЖ.
Случай 1
Больная Н., 1973 г.р. Анамнез: поступила в отделение в феврале 1999 г. с признаками тиреотоксикоза (св. Т4 — 57 пмоль/л). Отмечалось диффузное увеличение ЩЖ (зоб ІІ ст.). Без определения TRAK тогда был выставлен диагноз ДТЗ, и до ноября 1999 г. пациентка получала адекватную тиреостатическую терапию тиамазолом (начальная доза 30 мг/сут). После отмены тиреостатика клинически сохранялся эутиреоз. Через некоторое время при отсутствии контроля в середине 2005 года установлены проявления субклинического гипотиреоза и обнаружены аутоантитела к ТПО в титре 1 : 500 ЕД. Поставлен диагноз АИТ. Назначено лечение L-тироксином — 50 мкг/сут. В дальнейшем в связи с беременностью больная находилась под тщательным контролем эндокринолога. Доза L-тироксина увеличена до 100 мкг/сут. После рождения здорового сына в 2005 году уровень ТТГ составлял 0,06 МЕ/мл и L-тироксин отменили. В дальнейшем из-за рецидива гипотиреоза возобновлен прием L-тироксина в дозе 50 мкг/сут.
Объективно: состояние удовлетворительное. Рост 170 см. Вес 69 кг. АД 130/85 мм рт.ст., ЧСС 80 в 1 мин, кожа обычной влажности. Глазные симптомы отсутствуют. ЩЖ не пальпируется. Рефлексы одинаковы с обеих сторон.
Лабораторные данные (сентябрь 2006 г.): ТТГ — 13 МЕ/л, свободный Т4 — 12 пмоль/л, свободный Т3 — 3,0 пмоль/л, антитела к ТПО — 3600 Ед/л, антитела к рецепторам ТТГ — 5,6 МЕ/л.
Диагноз: ДТЗ (дебют с тиреотоксикоза). В процессе болезни развился латентный гипотиреоз в результате трансформации (перетекания) в АИТ.
Течение и лечение: после повышения дозы L-тироксина до 75 мг/сут достигнуто состояние эутиреоза. В дальнейшем в связи с развитием ремиссии L-тироксин отменен. В 2008 г. при последнем контроле — клинически состояние эутиреоза. Содержание ТТГ — 0,8 МЕ/л.
Обсуждение. Три болезни у одной пациентки: ДТЗ — дебют с тиреотоксикоза, АИТ и эутиреоидная форма ДТЗ. Имеет ли место трансформация (переход) АИТ в ДТЗ?
Тиреотоксическая форма ДТЗ через длительный промежуток времени (10–15 лет), как правило, может трансформироваться в гипотиреоз [9, 11, 12]. При этом патогенез данного явления может быть мультифакториальным. С одной стороны, описан деструктивный фокальный или диффузный тиреоидит (трансформация в классическую форму АИТ), с другой — доминирование блокирующих антител к рецептору ТТГ [12] (рис. 1).
У представленной пациентки речь идет об особом течении тиреотоксической формы ДТЗ после латентного периода — 6 лет и его перехода в АИТ (антитела к ТПО — 3600 Ед/л) с развитием латентного гипотиреоза. В дальнейшем у больной наблюдалась спонтанная ремиссия. Через 10 лет после начала заболевания отмечено развитие эутиреоидной формы ДТЗ, при этом уровень ТТГ находился в пределах нижней границы нормы. Примечательно то, что в начале развития ДТЗ не обнаруживались TRAK и его трудно было дифференцировать с чистым АИТ с хашитоксикозом.
В целом потребность в высоких дозах тиреостатиков в течение 9 месяцев и дальнейшее выявление TRAK свидетельствовали о ДТЗ. Недостаточно ясен механизм развития гипотиреоидной формы ДТЗ во второй фазе заболевания. Резюмируя вышеизложенное, можно сказать, что у этой пациентки, вероятно, тиреотоксическая форма ДТЗ после латентного периода (6 лет) трансформировалась в АИТ, а последний через 4 года опять перешел в эутиреоидную форму ДТЗ.
Случай 2
Больная С., 59 лет. Жалобы и анамнез: в течение нескольких лет беспокоят сухость кожи, слабость, запоры. В последнее время состояние ухудшилось: появились зябкость, сонливость, повысилась масса тела (на 6 кг). Отмечает отсутствие потливости при физической нагрузке. Обратилась к участковому врачу, который направил на консультацию к эндокринологу.
Объективно: рост 167 см, масса тела 68 кг. Пульс — 60 в 1 мин, ритмичный, удовлетворительных свойств. АД 160/90 мм рт.ст. Кожа сухая, шелушится. ЩЖ не пальпируется. Сухожильные рефлексы снижены. Глазные симптомы отсутствуют.
Лабораторно-инструментальные данные: ТТГ — 55 Ед/л, свободный Т4 — 4 нмоль/л, свободный Т3 — 0,8 нмоль/л, антитела к рецепторам ТТГ — 10 Ед/л, антитела к ТПО — 40 Ед/л.
Диагноз: аутоиммунный тиреоидит с исходом в гипотиреоз.
Течение заболевания и лечение: назначено лечение L-тироксином 50 мкг/сут. Месяц спустя доза препарата увеличена до 75 мкг/сут. Показатели функции ЩЖ через 2 месяца: ТТГ — 30 Ед/л, свободный Т4 — 5,4 нмоль/л, свободный Т3 — 3,0 нмоль/л. В связи с сохранением состояния декомпенсации доза L-тироксина увеличена до 100 мкг/сут. Через 1,5 месяца при определении ТТГ и тиреоидных гормонов выявлен латентный тиреотоксикоз: ТТГ — 0,08 Ед/л, свободный Т4 — 25 нмоль/л, свободный Т3 — 6,0 нмоль/л. Доза L-тироксина уменьшена до 75 мкг/сут. Спустя два месяца сохранились проявления субклинического тиреотоксикоза (ТТГ — 0,15 МЕ/л), в связи с чем в дальнейшем дозу L-тироксина понизили до 50 мкг/сут, а затем — до 25 мкг/сут. В общей сложности через 8 месяцев после заместительной терапии достигнут эутиреоз. За это время масса тела уменьшилась на 5 кг.
Обсуждение. Дифференциальная диагностика в данном случае должна проводиться между классической формой АИТ с исходом в гипотиреоз и так называемой гипотиреоидной формой ДТЗ. АИТ достаточно хорошо известен врачам-эндокринологам. В основе его патогенеза лежит преимущественно деструктивный аутоиммунный процесс. Под влиянием неустановленных факторов окружающей среды у генетически детерминированных лиц (гаплотипы НLA-DR3/DR5) происходит активизация клеточных и гуморальных иммунных механизмов, направленных против ткани ЩЖ и сходных антигенных структур экстратиреоидных тканей. Признаком этого аутоиммунного процесса, т.е. повреждения паренхимы ЩЖ, является повышение титра антител к ТПО. Эти антитела встречаются в 95 % случаев АИТ и являются диагностически значимыми [10]. Широкому кругу врачей-специалистов мало или почти ничего неизвестно о существовании и роли нестимулирующих или блокирующих антител к рецептору ТТГ, которые были описаны еще в конце 1950-х годов. Они могут участвовать в развитии гипотиреоза при АИТ и их выявляют в 10–20 % случаев.
Блокирующие антитела играют роль в развитии так называемой гипотиреоидной формы ДТЗ. У пациентов с этой формой болезни обнаруживают как стимулирующие, так и блокирующие антитела [9], исходя из гипотезы баланса. У данной пациентки имеется манифестный гипотиреоз, который ввиду высокого титра антител к рецептору ТТГ возник в связи с аутоиммунным процессом в ЩЖ. Титр антител к ТПО не был увеличен. Дифференциальную диагностику следует проводить между АИТ с исходом в гипотиреоз и так называемой гипотиреоидной формой ДТЗ. Поскольку у 5 % пациентов с АИТ антитела к ТПО не выявлены, то их отсутствие при лабораторных исследованиях не исключает абсолютно АИТ. Высокий титр антител к рецептору ТТГ, напротив, свидетельствует о ДТЗ. В данном случае имеется дисбаланс между стимулирующими и блокирующими антителами. Для верификации диагноза важно было бы определение блокирующих антител с помощью биологических методов, однако, к сожалению, таких методов в распоряжении врачей в настоящее время не имеется. Выявление блокирующих антител в общем не имеет значения для лечения, так как, несмотря на это, в данном случае необходима заместительная терапия L-тироксином.
Таким образом, вышеприведенные случаи из практики характеризуются комбинацией клинических проявлений, свойственных нескольким заболеваниям ЩЖ. При этом оба заболевания в одном органе существуют одновременно. Однако в клинической практике, как правило, доминирует одна болезнь (Фисфален М.-Э., Де Грут Л., 2003; Генделека Г.Ф., 2010). В первом случае клинические проявления одной болезни у одного и того же больного сменяют друг друга на протяжении длительного периода наблюдения, т.е. одно заболевание трансформируется в другое. Речь идет о так называемом синдроме перекреста (overlap-синдроме). Несмотря на то, что проявления общих болезней могут наблюдаться одновременно, обычно симптоматика одного заболевания превалирует над симптоматикой другого. Аутоиммунный синдром перекреста ЩЖ — нередкая, хотя и недостаточно изученная патология этого органа и terra incognita как для исследователей, так и для практикующих врачей.
1. Генделека Г.Ф. Аутоиммунный синдром перекреста (overlap-синдром) при заболеваниях щитовидной железы // Междунар. эндокрин. журнал. — 2010. — № 2. — C. 117–128.
2. Зефирова Г.С. Заболевания щитовидной железы. — М.: Арт-Бизнес-Центр, 1999. — 215 с.
3. Данилова Л.И., Демидчик Е.П., Демидчик Ю.Е. и др. Заболевания щитовидной железы // Клиническая эндокринология: Руководство для врачей / Под ред. Е.А. Холодовой. — М.: ООО «МИА», 2011. — С. 51–134.
4. Вольпе Р. Аутоиммунные заболевания щитовидной железы // Болезни щитовидной железы: Пер. с англ. — М., 2000. — С. 140–178.
5. Фисфален М.-Э., Де Грут Л. Болезнь Грейвса и аутоиммунный тиреоидит // Молекулярная эндокринология / Пер. с англ.; под ред. Б.Д. Вайнтрауба. — M.: Mедицина, 2003. — С. 313–362.
6. Davis T.F. Newer Aspects of Graves’ disease // Baillieres Clin. Endocrinol. Metab. — 1997. — Vol. 11. — Р. 431–501.
7. Davis T.F. Editorial: Autoimmune thyroid disease in many styles and colors // J. Clin. Endocrinol. Metabol. — 1998. — Vol. 83. — Р. 3391–3393.
8. Hedey A., Young R., Jones S., Alexander W. Antithyroid drugs in the treatment of hyperthyroidism of Graves’ disease: long-term follow-up of 434 patients // Clin. Endocrinol. — 1989. — Vol. 31. — Р. 209–218.
9. Hirota Y., Tamai H., Hayashi Y. et al. Thyroid function and histology in forty-five patients with hyperthyroid Graves’ disease in clinical remission more than ten years after thionamide drug treatment // J. Clin. Endocrinol. Metabol. — 1986. — Vol. 62. — Р. 165.
10. Eber O., Langsteger W. Clinical aspects of autoimmune thyroid diseases // Acta Med. Austriaca. — 1994. — Vol. 24. — Р. 1–7.
11. Tamai H., Hirota Y., Kasagi K. et al. The mechanism of spontaneous hypothyroidism in patients with Graves’ disease after antithyroid drug treatment // J. Clin. Endocrinol. Metabol. — 1987. — Vol. 64. — Р. 718–722.
12. Wood L., Ingbar S. Hypothyroidism as a late sequela in patient with Graves’ disease treated with antithyroid agents // J. Clin. Invest. — 1979. — Vol. 64. — Р. 1429–1436.

/104/104.jpg)