Международный эндокринологический журнал 4 (60) 2014
Вернуться к номеру
Вплив гіпотиреозу на окремі ланки метаболізму, структури і функції серця за умов інсулінорезистентності
Авторы: Юзвенко Т.Ю. - Український науково-практичний центр ендокринної хірургії, трансплантації ендокринних органів і тканин МОЗ України, м. Київ
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
У статті наведені результати дослідження впливу зниженої тиреоїдної функції на тлі інсулінорезистентності на окремі ланки метаболізму, структури і функції серця. Встановлено, що при порушеннях функції щитоподібної залози основною нозологічною формою ураження міокарда у пацієнток без супутньої серцево-судинної патології є розвиток метаболічної ендокринної кардіоміопатії. Особливістю ураження серця є відсутність розвитку кардіосклеротичних, міокардитичних та ішемічних процесів при гіпотиреозі. Встановлено нечітку клінічну симптоматику з боку серця як при явному, так і при субклінічному гіпотиреозі. Особливостями клінічних, інструментальних і лабораторних змін у пацієнток зі зниженою функцією щитоподібної залози є тенденція до підвищення систолічного артеріального тиску, відсутність значущої дисліпідемії, дисглікемії, кардіоцитолізу і гепатоцитолізу. Нестача гормонів щитоподібної залози асоціюється з підвищенням гетерогенності процесів реполяризації міокарда: субклінічний гіпотиреоз супроводжується порушенням процесів реполяризації і розвитком електричної гетерогенності міокарда шлуночків, а при явному гіпотиреозі зміни більшою мірою пов’язані з порушенням гомогенності проведення електричного імпульсу по передсердях.
В статье представлены результаты исследования влияния сниженной тиреоидной функции на фоне инсулинорезистентности на отдельные звенья метаболизма, структуры и функции сердца. Установлено, что при нарушениях функции щитовидной железы основной нозологической формой поражения миокарда у пациенток без сопутствующей сердечно-сосудистой патологии является развитие метаболической эндокринной кардиомиопатии. Особенностью поражения сердца является отсутствие развития кардиосклеротических, миокардитических и ишемических процессов при гипотиреозе. Установлена нечеткая клиническая симптоматика со стороны сердца как при явном, так и при субклиническом гипотиреозе. Особенностями клинических, инструментальных и лабораторных изменений у пациенток со сниженной функцией щитовидной железы являются тенденция к повышению систолического артериального давления, отсутствие значимой дислипидемии, дисгликемии, кардиоцитолиза и гепатоцитолиза. Недостаток гормонов щитовидной железы ассоциируется с повышением гетерогенности процессов реполяризации миокарда: субклинический гипотиреоз сопровождается нарушением процессов реполяризации и развитием электрической гетерогенности миокарда желудочков, а при явном гипотиреозе изменения в большей степени связаны с нарушением гомогенности проведения электрического импульса по предсердиям.
The article presents research findings of reduced thyroid function impact on the background of insulin resistance on the specific links of metabolism, structure and function of the heart. It is found that in thyroid dysfunction, the main nosological form of myocardial lesion in female patients without concomitant cardiovascular disease is the development of metabolic endocrine cardiomyopathy. Feature of cardiac lesion is the absence of cardiosclerotic, myocardial and ischemic processes in hypothyroidism. Obscure clinical symptoms of the heart both in apparent and subclinical hypothyroidism are detected. Features of clinical, instrumental and laboratory changes in female patients with impaired thyroid function are a trend to systolic blood pressure increase, the absence of significant dyslipidemia, dysglycemia, and cardiocytolysis and hepatocytolysis. Thyroid hormone deficiency is associated with increased myocardial repolarization heterogeneity: subclinical hypothyroidism is accompanied by violation of repolarization processes and the development of electrical heterogeneity of ventricular myocardium, and in the apparent hypothyroidism changes are more linked with the violation of the homogeneity of the electrical impulse to the atria.
гіпотиреоз, інсулінорезистентність, функція міокарда.
гипотиреоз, инсулинорезистентность, функция миокарда.
hypothyroidism, insuline resistance, myocardial function.
Статья опубликована на с. 31-35
На сьогодні захворювання щитоподібної залози (ЩЗ) за своєю поширеністю посідають перше місце в структурі ендокринної патології [1]. Відомо, що порушення функціонування ЩЗ призводить до змін усіх видів обміну речовин і істотно впливає на стан серцево-судинної системи. Найчастішим проявом дисфункції ЩЗ є розвиток вторинної ендокринної кардіоміопатії [2]. Тиреоїдна кардіоміопатія розглядається як ураження міокарда з його дисфункцією на тлі порушення функції ЩЗ [4]. Вона характеризується функціональними розладами, а також можливістю розвитку органічних уражень серця (гіперфункція і гіпертрофія кардіоміоцитів із подальшим прогресуванням у кардіосклероз, дилатація порожнин серця з формуванням хронічної серцевої недостатності) [5]. Отримати об’єктивні дані стосовно частоти гіпотиреоїдної кардіоміопатії доволі тяжко у зв’язку з відсутністю уніфікованих критеріїв діагностики. За результатами проведених досліджень реально можливо розглянути лише окремі прояви кардіоміопатії, до яких належать фібриляція передсердя і серцева недостатність — найвагоміші її ускладнення [7]. Диференціальна діагностика функціональних і органічних уражень міокарда при порушенні функції ЩЗ з прогнозуванням розвитку серцевої недостатності залишається актуальною і потребує динамічного вивчення усього спектра клінічних проявів ураження серцево-судинної системи на тлі тиреоїдної дисфункції.
Стан інсулінорезистентності, що супроводжується зниженням чутливості периферичних тканин до біологічної дії інсуліну, трапляється не лише при цукровому діабеті 2-го типу, але й при інших захворюваннях із порушеннями обміну речовин, зокрема при гіпотиреозі [1]. Поєднання таких метаболічних порушень, як ожиріння, дисліпідемія, артеріальна гіпертензія та інсулінорезистентність, що позначається терміном «метаболічний синдром», супроводжується збільшенням ризику серцево–судинних захворювань [6]. Зазначені компоненти метаболічного синдрому трапляються як при явному, так і при субклінічному гіпотиреозі [3]. Тому можна стверджувати, що зниження функції ЩЗ, навіть коли рівень тиреоїдних гормонів залишається в рамках нормальних значень, збільшує серцево-судинний ризик, пов’язаний з метаболічним синдромом.
Метою проведеного дослідження була оцінка впливу зниженої тиреоїдної функції на тлі інсулінорезистентності на окремі ланки метаболізму, структури і функції серця.
Матеріали і методи дослідження
Під спостереженням перебувало 45 жінок, які зверталися по амбулаторну медичну допомогу й перебували на обстеженні в Українському науково-практичному центрі ендокринної хірургії, трансплантації ендокринних органів і тканин. Основним критерієм виключення з дослідження була наявність в анамнезі серцево-судинної патології. Всі пацієнти були розподілені на 3 групи. До першої групи увійшли 16 пацієнтів із явним гіпотиреозом, до другої — 14 осіб із субклінічним гіпотиреозом, до третьої — 15 осіб у стані еутиреозу. У всіх обстежених відзначався стан інсулінорезистентності. У пацієнтів із гіпотиреозом його розвиток був пов’язаний з автоімунним тиреоїдитом. Середній вік обстежених осіб становив 46,7 ± 1,2 року. Тривалість гіпотиреозу становила в середньому 4,3 ± 0,4 року.
Інсулінорезистентність визначали за величиною індексу НОМА, який обчислювався за формулою: глюкоза натще (ммоль/л) x інсулін натще (мкОД/мл)/22,5. Наявність інсулінорезистентності визначали при рівні НОМА ≥ 3,0.
Рівні тиреотропного гормону (ТТГ), вільного тироксину (вТ4), вільного трийодтироніну (вТ3), антитіл до тиреоїдної пероксидази у сироватці крові натще визначалися імуноферментним методом за допомогою реактивів фірми DRG (Німеччина) на автоматичному аналізаторі iEMS Reader MF фірми ThermoLabsystems (Фінляндія). Визначення глюкози в сироватці крові проводили колориметричним методом на автоматичному біохімічному аналізаторі Sapphire-400, Tokio Boek L.T.D. Elitech diagnostics виробництва Seppin S.A.S. (Франція). Для оцінки змін обміну речовин, які супроводжують порушення функції ЩЗ, досліджували показники ліпідограми (загальний холестерин, ліпопротеїни низької (ЛПНЩ), дуже низької і високої щільності, тригліцериди, коефіцієнт атерогенності), лужної фосфатази, загального білка, білірубіну, y-–глутамілтрансферази (ГГТ), креатинфосфокінази (КФК).
Клінічне обстеження включало збір скарг, даних анамнезу, фізикальне дослідження. Електрокардіографічне дослідження (ЕКГ) проводили у 12 відведеннях на стандартних електрокардіографах. Оцінювали частоту серцевих скорочень (ЧСС), наявність екстрасистол, ішемічних змін. З метою інтегральної оцінки процесів реполяризації міокарда проводився аналіз амплітуди зубців Т і розрахунок середньої амплітуди зубців Т (Тсер.) у грудних відведеннях. Серед показників негомогенності реполяризації міокарда шлуночків вивчали інтервал QT і коригований інтервал QT (QTc), який обчислювали за формулою Базетта (QTс = QT/RК1/2 при RR < 1000 мс). Для оцінки негомогенності процесів реполяризації передсердь оцінювали інтервал PQ і його дисперсію (PQd).
Оцінку морфометричних показників лівого шлуночка (ЛШ), діастолічної і скоротливої функції міокарда ЛШ серця проводили шляхом дослідження ехокардіографії на ультразвукових сканерах у стандартних режимах. Оцінювали кінцевий систолічний розмір, кінцевий діастолічний розмір, товщину міжшлуночкової перегородки (МШП) і задньої стінки (ЗС) в діастолу, фракцію викиду (ФВ), масу міокарда лівого шлуночка (ММЛШ) та індекс маси міокарда лівого шлуночку (ІММЛШ). Для вивчення діастолічної функції досліджували такі параметри трансмітрального кровотоку: максимальні швидкості раннього діастолічного наповнення (Е) і наповнення в систолу передсердь (А), час уповільнення кровотоку раннього діастолічного наповнення ЛШ (DT).
Статистична обробка матеріалу виконувалася на персональному комп’ютері з використанням стандартного пакету програм прикладного статистичного аналізу (Statistica for Windows v. 6.0). Для статистичної обробки отриманих даних застосовували t-критерій Стьюдента, ранговий U-критерій Вілкоксона — Манна — Уїтни, критерій Пірсона і метод Фішера та інші. Критичний рівень вірогідності нульової статистичної гіпотези дорівнював 0,05.
Результати дослідження та їх обговорення
При аналізі отриманих лабораторних та інструментальних результатів нами не отримано даних, які б свідчили про розвиток кардіосклеротичних чи ішемічних процесів у міокарді. Нами не зареєстровано випадків розвитку хронічної серцевої недостатності і значущих порушень серцевого ритму. Тому можна стверджувати, що всі наявні суб’єктивні ознаки, об’єктивні дані, структурні й функціональні зміни міокарда у пацієнтів із порушенням функції ЩЗ мали вторинний характер і були відображенням метаболічної ендокринної кардіоміопатії (за класифікацією ВООЗ, 1995 р.). Оскільки під спостереженням перебували тільки жінки, всі отримані нами зміни лабораторних та інструментальних показників у групі гіпотиреозу можуть бути віднесені не лише до факту зниженої функції ЩЗ, але й до факту поєднання гіпотиреозу і жіночої статі.
Пацієнти першої і другої груп вірогідно відрізнялися від групи контролю (з еутиреозом) за рівнем ТТГ і тиреоїдних гормонів (табл. 1).
При оцінці скарг пацієнтів не було виявлено вірогідних відмінностей за частотою відчуття болю в загрудинній ділянці, за відчуттям пришвидшеного серцебиття. Виражені суб’єктивні ознаки ураження серцевого м’яза в обстежених нами хворих із гіпотиреозом були відсутні.
При оцінці антропометричних даних на підставі величини індексу маси тіла (ІМТ) переважна більшість пацієнток з гіпотиреозом мала надмірну масу тіла (28,11 ± 0,89 кг/м2). Отримані дані вірогідно відрізнялися від групи контролю (rs = –0,47; р < 0,05).
При оцінці артеріального тиску (АТ) рівень систолічного АТ був високим нормальним в осіб із гіпотиреозом (133,5 ± 3,4 мм рт.ст.), а в групі контролю — нормальним (124,1 ± 1,7 мм рт.ст.). Ці відмінності були статистично значущими (t = 2,53; р = 0,02; U = 87,50; р = 0,01). Діастолічний АТ у всіх обстежених був нормальним (81,9 ± 1,5 і 80,4 ± 1,1 мм рт.ст. відповідно), вірогідних відмінностей показників діастолічного АТ не відзначалося (t = 0,75; р > 0,1; U = 138,00; р = 0,34).
Нами також не спостерігалося вірогідних відмінностей серед показників ліпідного спектра крові, показників холестазу (лужна фосфатаза, ГГТ) и кардіоміоцитолізу (КФК) між групами гіпотиреозу і контролю.
З метою оцінки процесів реполяризації міокарда, його провідності, а також електричної гомогенності всім пацієнткам проводилося електрокардіографічне дослідження. Отримані результати наведені в табл. 2.
У пацієнток із гіпотиреозом відзначалася чітка тенденція до збільшення варіабельності тривалості інтервалу PQ порівняно з групою контролю (24,2 ± 2,8 мс і 18,6 ± 1,8 мс відповідно), а в групі явного гіпотиреозу цей показник був вірогідно вищий (t = 2,10; р = 0,05; U = 27,00; р = 0,01), що може свідчити про початкове порушення поширення електричного імпульсу по передсердях і, можливо, бути несприятливою прогностичною ознакою стосовно розвитку передсердних порушень ритму.
Оцінка гомогенності процесів реполяризації (дисперсія інтервалу QT) не продемонструвала значущих відмінностей з групою контролю (t = 0,63; р > 0,1; U = 110,00; р = 0,55), але при цьому відзначалася явна тенденція до збільшення дисперсії тривалості інтервалу QT, особливо в групі субклінічного гіпотиреозу (38,1 ± 11,7 мс і 24,1 ± 2,6 мс відповідно). У пацієнтів із гіпотиреозом спостерігалося значуще зменшення амплітуди зубців Т у грудних відведеннях (t = 2,30; р = 0,03; U = 62,00; р = 0,03).
Отже, зниження функції ЩЗ призводить до підвищення негомогенності процесів реполяризації як передсердь, так і шлуночків. При цьому субклінічний гіпотиреоз супроводжується порушенням процесів реполяризації шлуночків, а при явному гіпотиреозі зміни більшою мірою пов’язані з порушенням гомогенності проведення електричного імпульсу по передсердях.
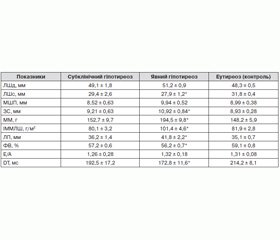
Усім пацієнткам з гіпотиреозом також проводилося ехокардіографічне дослідження. Відзначалося збільшення маси міокарда ЛШ (167,57 ± 11,92 г) і тенденція до збільшення ІММЛШ (89,87 ± 5,31 г/м2). Були виявлені вірогідні відмінності в розмірах задньої стінки ЛШ, розмірах лівого передсердя, систолічної функції ЛШ (фракції викиду) (табл. 3).
При порівняльному аналізі підгруп гіпотиреозу з групою контролю відзначалося вірогідне збільшення маси міокарда ЛШ (t = 3,04; р = 0,001; U = 15,00; р = 0,03), товщини його стінок і порожнини лівого передсердя у пацієнток з явним гіпотиреозом на відміну від обстежених із субклінічним гіпотиреозом, у яких ці зміни були статистично незначущі.
Нами не було отримано переконливих даних щодо порушення діастолічної функції ЛШ у пацієнток із гіпотиреозом. При цьому відзначалося вірогідне зменшення часу уповільнення кровотоку раннього діастолічного наповнення ЛШ (t = 2,37; р = 0,03) при явному гіпотиреозі.
При проведенні кореляційного аналізу були виявлені сильні зв’язки між рівнем периферичних гормонів, здебільшого вТ4, і показниками, що свідчать про розвиток механічної й електричної дисфункції міокарда.
Позитивні кореляційні зв’язки були виявлені з розмірами ЛШ у систолу й діастолу, масою міокарда, показниками трансмітрального кровотоку (Е/А). Між рівнем вільного тироксину і ФВ, швидкістю пізнього наповнення ЛШ (А) встановлені негативні кореляції.
Про вплив гіпотиреозу на проведення електричного імпульсу свідчить виявлення позитивних кореляційних зв’язків вільного тироксину з тривалістю інтервалу PQ, амплітудою зубця Т, ЧСС. При цьому кореляційний зв’язок з показниками реполяризації шлуночків (інтервал QTc) має негативний характер. Також виявлена сильна негативна кореляція з показниками ліпідного обміну, що відповідають за атерогенез (загальний холестерин, ЛПНЩ). Наявність цих зв’язків свідчить про значущу участь нестачі гормонів ЩЗ у розвитку гіпотиреоїдної кардіоміопатії.
При вивченні показників, що відображають морфологію серця, було виявлено значущий вплив рівня гормонів ЩЗ і статі на кінцевий діастолічний розмір ЛШ (F = 15,29; р = 0,001). На показники маси міокарда та ІММЛШ значущий вплив здійснювали стать (F = 21,24; р = 0,001; F = 8,20; р = 0,006) і функція ЩЗ (F = 10,78; р = 0,004; F = 5,02; р = 0,04 відповідно). При вивченні реполяризації шлуночків (QTmax) було виявлено, що єдиним значущим фактором виявилася функція ЩЗ (F = 8,15; р = 0,005). Вплив віку і статі обстежених був статистично не значущим (F = 0,56; р = 0,45; F = l,65; р = 0,27 відповідно). Не було виявлено впливу гормонів ЩЗ на показники реполяризації міокарда, а єдиним з досліджуваних факторів, що вірогідно впливають на цей показник, став вік (F = 6,71; р = 0,02).
Отже, при порушеннях функції ЩЗ основною нозологічною формою ураження міокарда в пацієнток без супутньої серцево–судинної патології є розвиток метаболічної ендокринної кардіоміопатії. Особливістю ураження серця є відсутність розвитку кардіосклеротичних, міокардитичних та ішемічних процесів при гіпотиреозі. Встановлено нечітку клінічну симптоматику з боку серця як при явному, так і при субклінічному гіпотиреозі.
Висновки
1. При субклінічному та явному гіпотиреозі основною кардіальною патологією є метаболічна тиреоїдна кардіоміопатія.
2. Особливостями клінічних, інструментальних і лабораторних змін у пацієнток зі зниженою функцією щитоподібної залози є стертість суб’єктивної симптоматики, тенденція до підвищення систолічного АТ, відсутність значущої дисліпідемії, дисглікемії, кардіоцитолізу і гепатоцитолізу.
3. Нестача гормонів щитоподібної залози асоціюється з підвищенням гетерогенності процесів реполяризації міокарда: субклінічний гіпотиреоз супроводжується порушенням процесів реполяризації і розвитком електричної гетерогенності міокарда шлуночків, а при явному гіпотиреозі зміни більшою мірою пов’язані з порушенням гомогенності проведення електричного імпульсу по передсердях.
1. Балаболкин М.И., Клебанова Е.М., Креминская В.М. Фундаментальная и клиническая тиреоидология: Руководство. — М.: Медицина, 2007. — 816 с.
2. Карась А.С. Щитовидная железа и сердце / Карась А.С., Обрезан А.Г. // Клиническая и экспериментальная тиреоидология. — 2009. — № 3. — С. 37–42.
3. Brenta G. Diabetes and thyroid disorders // British Journal of Diabetes and Vascular Disease. — 2010. — Vol. 10(4). — P. 172–177.
4. Cappola A.R., Fried L.P., Arnold A.M. et al. Thyroid status, cardiovascular risk, and mortality in older adults // JAMA. — 2006 — Vol. 295, № 9. — P. 1033–1041.
5. Flynn R.W., McDonald T.M., Jung R.T. et al. Mortality and vascular outcomes in patients treated for thyroid dysfunction // J. Clin. Endocrinol. Metab. — 2006. — Vol. 91, № 6. — P. 2159–2164.
6. Kahn R., Buse J., Ferrannini E., Stern M.; American Diabetes Association; European Association for the Study of Diabetes. The metabolic syndrome: time for a critical appraisal: joint statement from the American Diabetes Association and the European Association for the Study of Diabetes // Diabetes Care. — 2005. — Vol. 28(9). — P. 2289–2304.
7. Rodondi N., Aujesky D., Vittinghoff E. et al. Subclinical hypothyroidism and the risk of coronary heart disease: a meta–analysis // Am. J. Med. — 2006. — Vol. 119, № 7. — P. 541–551.

/33/33.jpg)
/34/34.jpg)