Международный эндокринологический журнал 4 (60) 2014
Вернуться к номеру
Порушення репродуктивної функції жінки на тлі дисфункції щитоподібної залози (огляд проблеми)
Авторы: Пасєчко Н.В., Гнат С.В. - Тернопільський державний медичний університет ім. І.Я. Горбачевського
Рубрики: Акушерство и гинекология, Эндокринология
Разделы: Справочник специалиста
Версия для печати
У статті узагальнена інформація щодо поширеності у популяції та впливу на репродуктивну систему жінки захворювань, що супроводжуються гіпофункцією щитоподібної залози. Автори провели аналіз літератури, присвяченої цій проблемі. Особливу увагу привертають явища субклінічного гіпотиреозу та можливі порушення репродуктивної сфери у жінок із цим захворюванням. Розглянуто сучасні підходи до тактики скринінгу, діагностики та лікування цієї патології з метою відновлення та забезпечення репродуктивного здоров’я, його особливості за умов йодного дефіциту. Наведені в статті результати досліджень яскраво ілюструють доцільність консолідації довкола вивчення цього питання, створення загальноприйнятих алгоритмів діагностики та лікування жінок дітородного віку із субклінічним гіпотиреозом.
В статье обобщена информация о распространенности в популяции и влиянии на репродуктивную функцию женщины болезней, сопровождающихся гипофункцией щитовидной железы. Авторы проанализировали литературу, посвященную этой проблеме. Особое внимание привлекают явление субклинического гипотиреоза и возможные нарушения репродуктивной сферы у женщин с этим заболеванием. Рассмотрены современные подходы к тактике скрининга, диагностике и лечению этой патологии с целью восстановления и обеспечения репродуктивного здоровья, его особенностей в условиях йодного дефицита. Приведенные в статье результаты исследований ярко иллюстрируют целесообразность консолидации вокруг изучения этого вопроса, создания общепринятых алгоритмов диагностики и лечения женщин детородного возраста с субклиническим гипотиреозом.
The article provides the information on the prevalence in the population and the impact on female reproductive function of diseases associated with thyroid hypofunction. The authors analyzed the literature on this issue. Subclinical hypothyroidism and possible reproductive violations in women with such disease attracts special attention. Modern approaches to the tactics of screening, diagnosis and treatment of this disease in order to restore and provide reproductive health, its features in terms of iodine deficiency. Presented in the paper findings clearly illustrate the feasibility of consolidating around the study of this issue, creattion a common algorithms for diagnosis and treatment of women of childbearing age with subclinical hypothyroidism.
щитоподібна залоза, субклінічний гіпотиреоз, йодний дефіцит, безплідність.
щитовидная железа, субклинический гипотиреоз, йодный дефицит, бесплодие.
thyroid gland, subclinical hypothyroidism, iodine deficiency, infertility.
Статья опубликована на с. 97-102
На початку ХХІ ст. проблема відновлення репродуктивної функції людини залишається надзвичайно актуальною. У 1990 році в світі було зареєстровано 42 млн пар, які не могли мати дітей, у 2010 році кількість бездітних пар зросла до 48,5 млн, серед яких 19,2 млн страждали від первинної безплідності [1].
Відповідно до стандартного протоколу оцінка безплідності зазвичай ідентифікує різні причини, в тому числі чоловічу безплідність (30 %), жіночу безплідність (35 %), комбінацію тієї й іншої (20 %) і, нарешті, безплідність з незрозумілої причини, або ідіопатичну (15 %) [21].
Репродуктивна система жінки є сукупністю взаємопов’язаних структурних елементів: гіпоталамуса, гіпофіза, яєчників, органів-мішеней та інших ендокринних залоз, які забезпечують реалізацію генеративної діяльності. Щитоподібна залоза (ЩЗ) — найважливіша ланка нейроендокринної системи — здійснює суттєвий вплив на репродуктивну функцію [2].
Різні ендокринні захворювання можуть бути основною або супутньою патологією у пацієнток, безплідність яких має також інші причини (наприклад, обумовлене трубно-перитонеальним фактором або ендометріозом). За даними відділу допоміжних репродуктивних технологій (ДРТ), що працює на базі Ендокринологічного наукового центру (м. Москва, Росія), з квітня по жовтень 2009 р. за консультацією з приводу безплідного шлюбу звернулося 388 жінок, які потребували лікування методами ДРТ. Серед них були пацієнтки із синдромом полікістозних яєчників (25,6 %), ожирінням (21,6 %), гормонально неактивною аденомою гіпофіза (6,0 %), хронічною наднирниковою недостатністю (0,3 %), вродженою дисфункцією кори наднирникових залоз (1,3 %), гіпотиреозом (21,4 %, у тому числі після видалення ЩЗ з приводу папілярного раку — 1,3 %, з автоімунним тиреоїдитом — 20,1 %) [13].
Одним з основних чинників, що призводять до ураження ЩЗ, є йодний дефіцит [6]. Варто зауважити, що проблема йодного дефіциту є глобальною для населення всіх континентів. Близько 1,5 млн людей проживає в йододефіцитних регіонах. Це переважно гірські масиви, передгір’я, заплави великих річок, лісисті регіони з підзолистим ґрунтом. В Україні до таких регіонів насамперед належать Карпати, Полісся. У перші післявоєнні роки 50 % населення цих регіонів мало ендемічний зоб. Однак сьогодні проблема дефіциту йоду властива і жителям степової зони, Донбасу, Криму та м. Києва [7].
Невід’ємною складовою продукції тиреоїдних гормонів є йод. Нормальні рівні тиреоїдних гормонів є необхідними для функціонування всіх систем і органів людини. Вони регулюють процеси розвитку, дозрівання всіх тканин, мають вплив на статеве дозрівання, менструальну функцію, фертильність, вагітність, ембріогенез.
При захворюваннях ЩЗ, крім змін у балансі статевих стероїдів, відбуваються розлади гормональної функції гіпоталамо-гіпофізарної системи. Це свідчить про дію гормонів ЩЗ на рівні центральних ендокринних механізмів [15].
При гіпотиреозі відзначається зниження чутливості яєчників до гонадотропних гормонів. При дефіциті тиреоїдних гормонів змінюється метаболізм естрогенів, порушується процес переходу естрадіолу в естрон. Порушення периферичного метаболізму естрогенів призводить до зміни секреції гонадотропінів і виникнення ановуляції [14]. При хронічній ановуляції збільшується секреція яєчникових андрогенів; гіпотиреоз призводить до зменшення концентрації стероїдзв’язуючого глобуліну, що викликає збільшення біологічно активного тестостерону, внаслідок чого у жінок поєднується гіпотиреоз із гірсутизмом [15].
Гіпофункція ЩЗ призводить до підвищення секреції тиреоліберину, що супроводжується збільшенням умісту не тільки тиреотропного гормону (ТТГ), а й пролактину. Внаслідок гіперпролактинемії порушується циклічне виділення гонадотропінів, що сприяє зниженню продукції лютеїнізуючого гормону (ЛГ) і зупиненню овуляції і, відповідно, унеможливлює запліднення [18, 25].
Тиреоїдні гормони впливають на статеві залози, призупиняючи фолікулостимулюючу і підвищуючи лютеїнізуючу функцію, збільшують чутливість яєчників до гонадотропних гормонів та ендометрію до естрогенів. У пубертатний період тиреоїдні гормони активно впливають на організм, стимулюючи разом із статевими стероїдами повноцінне завершення фізичної, статевої та психічної диференціації та сприяють становленню в жіночому організмі нормального двофазного циклу. В період статевого дозрівання спостерігається найбільш висока активність ЩЗ, підвищується секреція ТТГ і тиреоїдних гормонів. При видаленні ЩЗ відзначається зниження концентрації ЛГ і ФСГ і затримка статевого дозрівання [3].
Згідно з дослідженнями, проведеними в Kathmandu University Hospital (Непал) у 2005–2009 рр., серед 825 суб’єктів виявлено певне співвідношення між порушеннями функції ЩЗ [11] (рис. 1).
Загальна поширеність гіпотиреозу у світі сягає 2 % [8], у США — до 4,6 % (0,3 % клінічного гіпотиреозу) (National Health and Nutrition Examination Survey II) (http://press.endocrine.org/doi/abs/10.1210/jcem.87.2.8182). Cеред жінок частота гіпотиреозу становить від 1,4 до 2 %, а серед чоловіків — 0,2 %, співвідношення — близько 10 : 1. В Україні станом на 01.01.2012 р. зареєстровано 90 884 тис. хворих на гіпотиреоз (у 1999 р. — 53 тис.), показник захворюваності населення становив у 2011 році 22,1 на 100 000 [9]. Найбільша поширеність гіпотиреозу спостерігається у віковій групі понад 65 років (1,7 %), а також у людей зазначеного віку із субклінічним гіпотиреозом (13,7 %). У США загальне поширення субклінічного гіпотиреозу становить 4,3 %. Явний гіпотиреоз зареєстрований у 2 % вагітних; у 2,5 % виявлено субклінічний гіпотиреоз (National Health and Nutrition Examination Survey II) (http://press.endocrine.org/doi/abs/10.1210/jcem.87.2.8182).
Вроджений гіпотиреоз — захворювання, що в середньому уражає одного з 4000 новонароджених. Частота вродженого гіпотиреозу приблизно однакова у багатьох країнах і становить у середньому 0,025 % [31].
Яскраво проілюстрована залежність частоти гіпотиреозу від статі та віку досліджуваних (за даними Colorado Thyroid Study, досліджено відсоток пацієнтів із підвищеним рівнем ТТГ серед 25 682 суб’єктів ) [10] (рис. 2).
Поширеність підвищеного рівня ТТГ залежно від статі наведена в табл. 1.
Гіпотиреоз є градуйованим явищем — від дуже легких випадків, при яких наявні біохімічні відхилення, але людина навряд чи помічає симптоми та ознаки дефіциту гормонів ЩЗ, до дуже тяжких станів, при яких існує небезпека втратити життя [27].
Класифікація первинного гіпотиреозу за ступенем тяжкості ґрунтується на даних лабораторної діагностики з урахуванням клінічних проявів:
1. Субклінічний гіпотиреоз — концентрація ТТГ у крові підвищена, вільного T4 — у межах норми; як правило, безсимптомний перебіг або тільки неспецифічні симптоми.
2. Маніфестний гіпотиреоз — концентрація ТТГ у крові підвищена, вільного T4 — знижена; характерні симптоми гіпотиреозу, як правило, є, проте можливий і безсимптомний перебіг: а) компенсований; б) декомпенсований.
3. Ускладнений гіпотиреоз — розгорнута клінічна картина гіпотиреозу, тяжкі ускладнення: полісерозит, серцева недостатність, кретинізм, мікседематозна кома та ін. [29].
Діагностика субклінічного гіпотиреозу проводиться на основі нормального рівня Т4 і помірного підвищення рівня ТТГ (від 4,01 до 10,0 мОд/л) [29].
При вперше виявленому підвищенні рівня ТТГ і нормальному рівні вільного Т4 необхідно повторне дослідження обох показників через 2–3 місяці разом із визначенням рівня антитіл до тиреоїдної пероксидази (ТПО) [5].
У Великобританії під час обстеження 2779 пацієнтів із субклінічним гіпотиреозом упродовж 20 років виявлено: жінки із субклінічним гіпотиреозом більш схильні до розвитку явного гіпотиреозу, якщо у них були антитіла до ТПО. Щорічні темпи прогресування cубклінічного гіпотиреозу в явний у жінок ставновили 4,3 %, якщо ТТГ був вищим за 6 мОд/л і позитивні антитіла до ТПО; 2,6 %, якщо підвищена лише концентрація ТТГ у сироватці, та 2,1 %, якщо антитіла наявні, але концентрація ТТГ у сироватці крові була нормальною [12] (табл. 2).
Про клінічну картину субклінічного гіпотиреозу може йти мова лише ретроспективно, оскільки зазвичай виражена клінічна симптоматика відсутня або неспецифічна. Наявні скарги пов’язують із гіпотиреозом лише після виявлення гормональних змін. Хоча, за визначенням, субклінічний гіпотиреоз асимптоматичний, у 25–50 % пацієнтів спостерігаються помірні ознаки гіпотиреозу [9].
Проаналізувавши результати багатьох досліджень, виявили низку порушень у стані пацієнтів із субклінічним гіпотиреозом [10, 28, 29] (табл. 3).
Також спостерігаються позатиреоїдні прояви ушкоджень органів та систем людини. Зокрема, з боку репродуктивної системи він проявляється еректильною дисфункцією в чоловіків та дисменореєю у жінок. У жінок фертильного віку гіпотиреоз впливає на тривалість циклу, кількість виділень, тобто призводить до оліго- та аменореї, поліменореї та менорагії. Проведене дослідження [19] показало, що серед 171 обстеженої у 40 (23,4 %) жінок із гіпотиреозом були нерегулярні менструації, у 42,5 % цих пацієнтів — олігоменорея, у 15 % — гіпоменорея, у 12,5 % — аменорея і у 30 % — гіперменорея/менорагія [20]. Тривале порушення функції ЩЗ зазвичай супроводжується серйозними розладами менструального циклу, що призводить до безплідності [15].
При проведенні проспективного, перехресного дослідження в йододефіцитному регіоні в північній частині Бангладеш у 2003–2004 рр. переконливих результатів не отримано. Так, під час дослідження обстежено 113 пацієнтів із безплідністю, які були розподілені на дві групи залежно від наявності у них первинної або вторинної безплідності. У цих групах вивчали кореляцію рівнів ТТГ та пролактину в крові. Поширеність гіперпролактинемії була вищою у хворих із первинною безплідністю, а поширеність субклінічного гіпотиреозу — в групі із вторинною безплідністю, причому кореляції між рівнями ТТГ і пролактину в цих двох групах не виявлено [21].
Поєднання гіперпролактинемії та субклінічного гіпотиреозу визначали і на базі Mazandaran University of Medical Sciences. Було проведено дослідження, в якому встановлено, що з 481 пацієнтки із субклінічним гіпотиреозом 98 (20,4 %) мали гіперпролактинемію [22]. Інші дослідження були схожими за результатами (22 %). Учені констатували успішну корекцію рівня пролактину після лікування L-тироксином [23].
Вивчено перебіг 150 вагітностей у 114 жінок (16–39 років) із первинним гіпотиреозом. 51 вагітність була на тлі гіпотиреозу (34 %), із них 16 вагітностей з явним гіпотиреозом і 35 — із субклінічним, 99 випадків вагітності — в еутиреоїдному стані на тлі замісної терапії. У випадках, коли доза левотироксину була недостатньою, аборт був наслідком у 60 % випадків явного гіпотиреозу і в 71,4 % — субклінічного, передчасні пологи — у 20 і 7,2 % відповідно та термінові пологи — у 20 і 21,4 % відповідно. Серед новонароджених 4 дитини мали вроджені вади розвитку, четверо померли. Коли лікування було адекватним, абортів та передчасних пологів не відбувалося. Результати продемонстрували, що перебіг і завершення вагітностей не залежить від виду гіпотиреозу (явний чи субклінічний). Адекватне лікування гіпотиреозу під час вагітності мінімізує ризики і збільшує перспективу перебігу вагітності без ускладнень [17].
Також встановлено, що у жінок із рівнем ТТГ 2,5–5,0 мОд/л частота спонтанного викидня в першому триместрі вагітності становила 6,1 %, а у вагітних із ТТГ < 2,5 мОд/л цей показник був 3,6 % [32].
Стосовно питання, чи потрібно лікувати субклінічний гіпотиреоз у різних вікових групах, продовжуються дискусії. Деякі проведені дослідження не доводять високої ефективності при лікуванні левотироксином у людей старшого віку [24]. Але згідно з припущеннями багатьох авторів наукових статей, лікування субклінічного гіпотиреозу під час вагітності не повинно відрізнятися від лікування маніфестного гіпотиреозу. Доцільність корекції тиреоїдного гомеостазу при субклінічному гіпотиреозі безсумнівна, якщо жінка планує вагітність найближчим часом, а також у пацієнток із безплідністю або невиношуванням вагітності. Додатковими критеріями для такої корекції є високий рівень антитиреоїдних антитіл і збільшення об’єму ЩЗ. При гіпотиреозі як маніфестному, так і субклінічному, вперше виявленому під час вагітності, відразу призначається повна замісна доза левотироксину з розрахунку 2–3 мкг на 1 кг маси тіла. Адекватній замісній терапії гіпотиреозу на тлі вагітності відповідає підтримання низьконормального (менше 2 мОд/л) рівня ТТГ і високонормального рівня вільного Т4. Контроль рівня ТТГ і вільного Т4 проводять кожні 8–10 тижнів. Після пологів доза левотироксину знижується до звичайної замісної (1,6–1,8 мкг на 1 кг маси тіла). Метою замісної терапії первинного гіпотиреозу є підтримання рівня ТТГ у межах 0,5–1,5 мОд/л [2].
Медикаментозно компенсований гіпотиреоз не є протипоказанням для планування жінкою вагітності. Потрібно враховувати, що при вагітності підвищується потреба в левотироксині та його доза повинна бути збільшена. Якщо жінка з компенсованим гіпотиреозом завагітніла, то дозу левотироксину необхідно відразу збільшити на 50 мкг від початкової. Надалі контроль адекватності терпії здійснюється за рівнями ТТГ і вільного Т4. Метою лікування є підтримання низьконормального рівня ТТГ і високонормального рівня Т4. Збільшення дози левотироксину на 50 мкг для жінки з компенсованим гіпотиреозом запобігає розвитку гіпотироксинемії у плода.
На базі клініки акушерства та гінекології департаменту третинної медичної допомоги лікарні при медичному коледжі в Північній Індії з лютого 2007 по березень 2010 року було проведено дослідження, в якому взяли участь 394 жінки (віком 20–40 років) із безплідністю. 76 (19,29 %) жінок мали підвищений рівень ТТГ (із них 59 жінок мали субклінічний гіпотиреоз), у 54 (13,7 %) жінок виявлено гіперпролактинемію, а у 18 (4,57 %) — гіпотиреоз і гіперпролактинемію. Відзначалася позитивна динаміка після призначення замісної терапії левотироксином практично в усіх клінічних випадках [26].
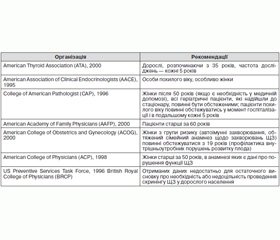
У табл. 4 наведений перелік рекомендацій щодо проведення скринінгу з виявлення захворювань ЩЗ у дорослого клінічно здорового населення [16].
Висновки
1. Безплідність залишається дуже актуальною проблемою і потребує вчасної діагностики та лікування.
2. Гіпофункція щитоподібної залози впливає на репродуктивну систему жінки, призводить до зниження фертильності, порушень менструального циклу, передчасних пологів і вад розвитку плода.
3. Визначення функціонального стану ЩЗ є вкрай необхідним при безплідності, фізіологічній та патологічній вагітності.
1. National, Regional, and Global Trends in Infertility Prevalence Since 1990: A Systematic Analysis of 277 Health Surveys.
2. Татарчук Т.Ф., Давыдова Ю.В., Косянчук Н.Ю. Тиреоидный гомеостаз и репродуктивное здоровье женщины // Новости медицины и фармации. — 2007. — № 13. — С. 14–15.
3. Балаболкин М.И. Эндокринология: учебное пособие. — М.: Медицина, 1989. — 416 с.
4. Трошина Е.А. Гипотиреоз и беременность: общие принципы диагностики и лечения // Международный эндокринологический журнал. — 2008. — № 5(17).
5. Simon H.S. et al. 2013 ETA Guideline: Management of Subclinical Hypothyroidism // Eur. Thyroid. J. — 2013. — 2. — 215–228. DOI: 10.1159/000356507.
6. Ларін О.С., Паньків В.І., Селіваненко М.І., Грачова О.О. Аналіз діяльності ендокринологічної служби України у 2010 році та перспективи розвитку медичної допомоги хворим з ендокринною патологією // Міжнародний ендокринологічний журнал. — 2011. — № 3(35).
7. Боднар П.М., Михальчишин Г.П. Йододефіцитні захворювання та їх профілактика // Міжнародний ендокринологічний журнал. — 2006. — № 4(6).
8. Приступюк О.М. Гіпотиреоз: ушкодження органів та систем // Міжнародний ендокринологічний журнал. — 2011. — № 4(36).
9. Паньків В.І. Синдром гіпотиреозу // Міжнародний неврологічний журнал. — 2013. — № 5(59).
10. Canaris G.J., Manowitz N.R., Mayor G. et al. The Colorado Thyroid Disease Prevalence Study // Arch. Intern. Med. — 2000. — Vol. 16 — P. 526–534.
11. Madhukar Aryal, Prabin Gyawali, Nirakar Rajbhandari, Pratibha Aryal, Dipendra Raj Pandeya. Department of Biochemistry, Kathmandu University School of Medical Sciences / Dhulikhel Hospital–Kathmandu University Hospital, Dhulikhel, Kavre, Nepal, 2010.
12. Vanderpump M.P.J., Tunbridge W.M.G., French J.M. et al. The incidence of thyroid disorders in the community: a twenty-year follow-up of the Whickham Survey // Clin. Endocrinol. — 1995. — Vol. 43. — P. 55–68.
13. Витязєва И.И. Інноваційні технології в лікуванні безплідність в пацієнтів з ендокринопатіями // Міжнародний ендокринологічний журнал. — 2010. — № 7(31).
14. Krassas G.E., Poppe K., Glinoer D. Thyroid Function and Human Reproductive Health // Endocr. Rev. — 2010. — Vol. 31. — P. 702–755.
15. Шаверда Е.В.. Состояние гипофизарно-гонадной системы при нарушении функции щитовидной железы // Медицинские новости. — 2003. — № 11.
16. Zosin Ioana. The Importance of Screening of Thyroid Dysfunctions. Part One // Международный эндокринологический журнал. — 2009. — № 1(19).
17. Abalovich M., Gutierrez S., Alcaraz G., Maccallini G., Garcia A., Levalle O. Overt and subclinical hypothyroidism complicating pregnancy // Thyroid. — 2002 Jan. — № 12(1). — P. 63–8.
18. Дедов И.И., Мельниченко Г.А. Персистирующая галакторея — аменорея. — М.: Медицина, 1985. — 256 с.
19. Krassas G.E., Pontikides N., Kaltsas Th. et al. Disturbances of menstruation in hypothyroidism // Clin. Endocrinol. (Oxf.). — 1999. — Vol. 50. — P. 655–659.
20. Крассас Дж.Е. Reproductive Function in Patients With Thyroid Diseases // Международный эндокринологический журнал. — 2005. — № 1(1).
21. Akhter N., Hassan S. Subclinical hypothyroidism and hyperprolactinemia in infertile women: Bangladesh perspective after universal salt iodination // The Internet Journal of Endocrinology. — 2008. — Vol. 5, № 1.
22. Bahar Adele, Akha Ozra, Kashi Zahra, Vesgari Zakiie. Hyperprolactinemia in association with subclinical hypothyroidism // Caspian. J. Intern. Med. — 2011. — № 2(2). — P. 229–233.
23. Hekimsoy Z., Kafesçiler S., Güçlü F., Ozmen B. The prevalence of hyperprolactinaemia in overt and subclinical hypothyroidism // Endocr. J. — 2010. — № 57(12). — P. 1011–5.
24. Villar H.C., Saconato H., Valente O., Atallah A.N. Thyroid hormone replacement for subclinical hypothyroidism // Cochrane Database Syst. Rev. — 2007. — № 18(3):CD003419.
25. Cramer D.W., Sluss P.M., Powers R.D. et al. Serum prolactin and TSH in an in vitro fertilization population: is there a link between fertilization and thyroid function? // J. Assisted Reprod. Genet. — 2003. — № 20(6). — Р. 210–5.
26. Indu Verma, Renuka Sood, Sunil Juneja and Satinder Kaur. Prevalence of hypothyroidism in infertile women and evaluation of response of treatment for hypothyroidism on infertility // Int. J. Appl. Basic. Med. Res. — 2012. — № 2(1). — Р. 17–19.
27. Spencer C.A., LoPresti J.S., Guttler R.B. et al. Application of a new chemiluminescent thyrotropin assay to subnormal measurements // J. Clin. Endocrinol. Metab. — 1990. — № 70. — Р. 453–460.
28. Staub J.J., Althaus B.U., Engler H. et al. Spectrum of subclinical and overt hypothyroidism: effect on thyrotropin, prolactin, and thyroid reserve, and metabolic impact on peripheral target tissues // Am. J. Med. — 1992. — № 92. — Р. 631–641.
29. Zulewski H., Muller B., Exer P., Miserez A.R., Staub J.J. Estimation of tissue hypothyroidism by a new clinical score: evaluation of patients with various grades of hypothyroidism and controls // J. Clin. Endocrinol. Metab. — 1997. — № 82. — Р. 771–776.
30. Майоров М.В. Щитовидная железа и женское репродуктивное здоровье // Новости медицины и фармации. Акушерство, гинекология, репродуктология. — 2009. — № 275.
31. Паньків В.І., Ендемічний зоб (йододефіцитні захворювання) // Новости медицины и фармации. — 2013. — № 8(456).
32. Negro R. Increased pregnancy loss rate in thyroid antibody negative women with TSH levels between 2.5 and 5.0 in the first trimester of pregnancy / R. Negro, A. Schwartz, R. Gismondi [et al.] // J. Clin. Endocrinol. Metab. — 2010. — Vol. 95, № 9. — Р. 44–48.

/98/98.jpg)
/99/99.jpg)
/100/100.jpg)