Международный эндокринологический журнал 6 (62) 2014
Вернуться к номеру
Вміст селену в біологічних рідинах організму пацієнтів із поєднаною травмою, які проживають в селенодефіцитному регіоні
Авторы: Тулюлюк С.В. - Буковинський державний медичний університет, м. Чернівці
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
У роботі наведено результати дослідження концентрацій селену в біологічних рідинах організму пацієнтів із поєднаною травмою, які проживають у селенодефіцитному регіоні.
В работе представлены результаты исследования концентраций селена в биологических жидкостях организма пациентов с сочетанной травмой, проживающих в селенодефицитном регионе.
The paper presents the results of a study of selenium concentrations in biological fluids of patients with concomitant injury living in selenium-deficient region.
селен, поєднана травма, біологічні рідини.
селен, сочетанная травма, биологические жидкости.
selenium, concomitant injury, biological fluids.
Статья опубликована на с. 24-26
Практично всі континентальні держави, до яких належить і Україна, зазнають дефіциту селену (Sе). Нестача селену відзначається у багатьох регіонах України [1].
Надзвичайно велике значення у захисті організму від впливу вільних радикалів має антиоксидантна система, основним ферментом якої є глутатіонпероксидаза. Цей фермент захищає мамбрани клітин від пошкодження продуктами вільнорадикального окислення (ВРО).
Кофактором глутатіонпериоксидази є селен [2]. На цей час відомо, що селен має потужні антиоксидантні властивості, бере участь у реакціях циклу Кребса та пентозофосфатазному циклі. Селен також активує синтез білків, нормалізує обмін протеїнів та нуклеїнових кислот .
На сьогодні заслуговує на увагу припущення стосовно того, що дефіцит селену є одним із чинників розвитку та прогресування тиреопатій [3, 4]. Щитоподібна залоза (ЩЗ) має особливу потребу в селені та належить до органів із найвищим рівнем цього мікроелемента на 1 г тканини. Селен, як і йод, необхідний для нормальної тиреоїдної функції, підтримання тиреоїдного гомеостазу [5].
Добре відомо, що гормони ЩЗ відіграють важливу роль у рості, розвитку, диференціації й загальному метаболізмі в організмі людини. Синтез гормонів ЩЗ відбувається переважно у формі тироксину (Т4). У периферичних тканинах, зокрема в печінці та нирках, Т4 перетворюється на трийодтиронін (Т3) і ця реакція каталізується дейодиназою. Вважають, що понад 80 % циркулюючого Т3 синтезується за допомогою дейодинази з Т4 у нетиреоїдній тканині.
Дейодинази є селеновмісними ферментами, і їх активність залежить від його кількості. Наприклад, дефіцит надходження селену в щурів протягом 5–6 тижнів призводить до зниження продукції Т3 у мозку, печінці та нирках. Установлено негативні зв’язки між рівнем селену у волоссі та об’ємом ЩЗ.
Сучасна література широко висвітлює роль селену й необхідність його поповнення при різноманітних захворюваннях, однак роботи, що стосуються динаміки концентрації цього мікроелемента в пацієнтів із пошкодженнями опорно-рухового апарату (ОРА) та черепно-мозковою травмою (ЧМТ) в селенодефіцитних регіонах, поодинокі. В той же час загальновідомо, що вивчення метаболізму селену при пошкодженнях опорно-рухового апарату та ЧМТ і розробка схем корекції дозволять значно покращити результати лікування та зменшити наслідки пошкоджень.
Мета дослідження — дослідити концентрацію селену в біологічних рідинах у пацієнтів із поєднаною травмою, які проживають у селенодефіцитному регіоні.
Матеріали та методи
Обстежено 42 пацієнти, які перебували на лікуванні в травматологічному та нейрохірургічному відділеннях лікарні швидкої медичної допомоги в м. Чернівці. Усіх пацієнтів було розділено на 3 групи: І група — пацієнти з тяжкою ЧМТ і пошкодженнями ОРА, які потребували підтримки життєдіяльності; ІІ група — із ЧМТ середнього ступеня тяжкості та пошкодженнями ОРА; ІІІ (контрольна група) — тільки з пошкодженнями ОРА.
У першу групу увійшли 12 пацієнтів, середній вік яких становив 40,8 ± 0,5 року. Жінок було 33,3 % від загальної кількості, чоловіків — 66,7 %. Основною причиною отриманих травм були дорожньо-транспортні пригоди (ДТП) — 8 (75 %). У всіх пацієнтів мала місце поєднана травма. Критерієм відбору до цієї групи була ЧМТ тяжкого ступеня, оцінка за шкалою коми Глазго — 9–11 балів. У 5 (41,6 %) пацієнтів при надходженні спостерігались прояви гіповолемічного шоку. У 6 (50 %) ЧМТ поєднувалась із переломами кісток гомілок, у 5 (41,6 %) — із переломами стегна, в одного (8,3 %) — плечової кістки. Усім пацієнтам було виконано фіксацію уламків апаратами зовнішньої фіксації. Середня тривалість стаціонарного лікування в палатах інтенсивної терапії становила 6,0 ± 2,3 доби.
До другої групи увійшло 16 пацієнтів, середній вік яких становив 39,6 ± 0,5 року. Жінки становили 31,25 % від загальної кількості, чоловіки — 68,75 %. Основною причиною отриманих травм стали ДТП — 11 осіб (68,75 %). У всіх пацієнтів відзначалася поєднана травма. Критерієм відбору була ЧМТ середнього ступеня тяжкості. У 4 (25 %) пацієнтів при надходженні спостерігались прояви гіповолемічного шоку. У 10 осіб (62,5 %) ЧМТ поєднувалась із переломами кісток гомілок, у 5 (41,6 %) — із переломами стегна, в 1 (8,3 %) — плечової кістки. Усім пацієнтам було виконано фіксацію уламків апаратами зовнішньої фіксації. Середня тривалість перебування пацієнтів у відділенні інтенсивної терапії становила 4,0 ± 1,8 доби.
До контрольної групи включено 14 пацієнтів, середній вік яких становив 43,6 ± 0,5 року. Жінок було 35,7 % від загальної кількості, чоловіків — 64,3 %. Основною причиною отриманих травм стали ДТП — у 8 осіб (57,1 %). У всіх пацієнтів спостерігалася поєднана травма. Критерієм відбору була ЧМТ легкого ступеня тяжкості. В 11 осіб (78,5 %) ЧМТ поєднувалась із переломами кісток гомілок, у 5 (21,5 %) — із переломами стегна. Усім пацієнтам було виконано фіксацію уламків апаратами зовнішньої фіксації.
Оцінюючи стан метаболізму селену, досліджували концентрацію селену в плазмі крові, еритроцитах і сечі. Забір матеріалів для дослідження проводили протягом гострого періоду захворювання (на 1-шу, 7-му та 14-ту добу). Забір крові в об’ємі 5 мл виконували шляхом черезшкірної пункції вени з подальшим центрифугуванням. Перед центрифугуванням до крові додавали розчин гепарину із розрахунку 250 Од/мл. Центрифугування виконували з використанням лабораторної центрифуги SM6.03 при швидкості обертання ротора 1500 об/хв. У результаті центрифугування у використаній пробі віділяли дві фракції: плазму крові та формені елементи крові — еритроцити. З отриманих фракцій проводили забір для дослідження в об’ємі 1 мл. Обидві проби піддавали заморожуванню при температурі –33 °С.
Забір сечі проводили з ранкової порції в об’ємі 1 мл, в подальшому сечу заморожували при t –33 °С.
Проби досліджували з використанням селективного атомно-абсорбтивного аналізатора МГА-915.
Статистичну обробку матеріалу проводили з використанням програмного забезпечення Statistica v. 5.5. Нормальність розподілу перевіряли за допомогою тесту Шапіро — Уїлка. Перевірка гіпотези про статистичну однорідність двох вибірок проводилась за допомогою критеріїв Стьюдента, кореляційний аналіз — з використанням критерію Спірмена.
Результати дослідження та їх обговорення
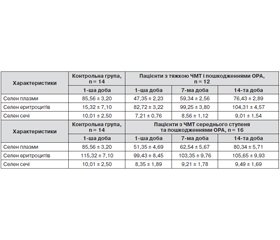
Показники дослідження концентрації селену в плазмі, еритроцитах і сечі в пацієнтів із ЧМТ і пошкодженнями ОРА наведені в табл. 1.
Отримані дані свідчать про зниження концентрації селену у всіх біологічних середовищах (плазмі, еритроцитах, сечі) протягом усього посттравматичного періоду в пацієнтів як із тяжкою ЧМТ і пошкодженнями ОРА, так і з ЧМТ середнього ступеня тяжкості.
Протягом усього посттравматичного періоду концентрація селену в усіх рідинах була знижена як у пацієнтів, які перебували в коматозному стані, так і в пацієнтів із збереженою свідомістю. При цьому значущі відмінності між групами були відсутні, однак указані зміни були вірогідними порівняно з показниками контрольної групи.
Беручи до уваги, що значна частина пацієнтів потребувала використання інтенсивної та специфічної терапії, нами проведено порівняльний аналіз концентрації селену залежно від отриманих травм і використаної терапії. При цьому статистично значущої різниці у показниках не виявлено. Це дало нам змогу зробити висновок, що зниження концентрації селену в біологічних середовищах характерно для будь–якого травматичного пошкодження та може бути ланкою патогенезу синдрому системної запальної відповіді.
Отже, відсутність значних розбіжностей вмісту селену в пацієнтів як із тяжкою ЧМТ і пошкодженнями ОРА, так і з ЧМТ середнього ступеня тяжкості свідчить про неспецифічність виявлених порушень, що є типовим патологічним процесом, характерним для травматичного пошкодження будь-якого генезу та локалізації.
На основі отриманих даних можна стверджувати, що динаміка концентрації селену є автономним процесом, що не залежить від проведення неспецифічної терапії.
Висновки
1. Доведено, що в пацієнтів із тяжкою ЧМТ і пошкодженнями ОРА спостерігаються виражені порушення метаболізму селену, які проявляються зниженням його концентрації у всіх досліджених біологічних середовищах організму протягом гострого періоду травми.
2. Відсутність виражених відмінностей метаболізму селену в пацієнтів як із тяжкою ЧМТ і пошкодженнями ОРА, так і з ЧМТ середнього ступеня тяжкості свідчить про неспецифічність виявлених порушень, що можна розглядати як типовий патологічний процес, притаманний травматичному пошкодженню будь-якого генезу та локалізації.
3. Дефіцит селену потребує використання медикаментозної корекції як у гострому, так і в посттравматичному періодах, особливо в селенодефіцитних регіонах.
1. Караченцев Ю.И., Гончарова О.А., Подорога Е.И. и др. Обеспеченность селеном отдельных регионов Сумской области и особенности частоты патологии щитовидной железы // Міжнародний ендокринологічний журнал. — 2013. — № 5(53). — С. 17–20.
2. Казиахмедов В.А. Содержание селена в биологических жидкостях при тяжелой черепно-мозговой травме / Ю.С. Александрович, В.А. Казиахмедов, В.В. Хорунжий, И.Ю. Аруцова, Г.М. Раевская // Сборник докладов и тезисов III съезда анестезиологов и реаниматологов Северо-Запада России. — СПб., 2005. — С. 102–106.
3. Микроэлементозы человека: этиология, классификация, органопатология / А.Н. Авцын, Л.Л. Жаворонков, М.А. Риш и др. — М., 1991. — 348 с.
4. Бабенко Г.А. Микроэлементозы человека: патогенез, профилактика, лечение / Г.А. Бабенко // Микроэлементы в медицине. — 2001. — Т. 2(1). — С. 2–5.
5. Zagrodzki P., Nicol F., Arthur J.R., Slowiaczek M. Selenoproteins in human thyroid tissues // Biofactors. — 2001. — Vol. 14. — Р. 223–227.
6. Holmgren A. Selenoproteins of the thioredoxin system // Selenium. Its Molecular Biology and Role in Human Health / Ed. by D.L. Hatfield. — Boston, 2001. — P. 189–205.

/25/25.jpg)