Международный эндокринологический журнал 6 (62) 2014
Вернуться к номеру
Гіперлептинемія як один із чинників порушення функції нирок у хворих на гіпотиреоз
Авторы: Дідушко О.М. - Івано-Франківський національний медичний університет
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
Із метою вивчення особливостей функціонального стану нирок у хворих на гіпотиреоз обстежені 132 хворі на первинний гіпотиреоз. Згідно з отриманими результатами, у пацієнтів із маніфестним гіпотиреозом наявна дисфункція нирок, що проявляється підвищенням рівня креатиніну та зниженням швидкості клубочкової фільтрації, розвитку та прогресуванню якої сприяє наявність у пацієнтів чинників ризику — гіперлептинемії, дисліпідемії, надмірної маси тіла та абдомінального ожиріння. Констатовано, що більш значущі показники дисліпідемії асоціювалися з найбільшими проявами абдомінального ожиріння за показниками окружності талії (96,58 ± 1,70 см та 98,73 ± 3,35 см), а також більшим індексом маси тіла.
С целью изучения особенностей функционального состояния почек у больных гипотиреозом обследовано 132 больных первичным гипотиреозом. Согласно полученным результатам, у пациентов с манифестным гипотиреозом имеется дисфункция почек, которая проявляется повышением уровня креатинина и снижением скорости клубочковой фильтрации, развитию и прогрессированию которой способствует наличие у пациентов факторов риска — гиперлептинемии, дислипидемии, избыточной массы тела и абдоминального ожирения. Констатировано, что более значимые показатели дислипидемии ассоциировались с наибольшими проявлениями абдоминального ожирения по показателям окружности талии (96,58 ± 1,70 см и 98,73 ± 3,35 см), а также большим индексом массы тела.
In order to study the features of renal function in patients with hypothyroidism we have examined 132 patients with primary hypothyroidism. The results showed that in patients with overt hypothyroidism there is renal dysfunction manifested by increased serum creatinine level and decreased glomerular filtration rate, the development and progression of which is facilitated by the presence of risk factors in patients — hyperleptinemia, dyslipidemia, overweight and abdominal obesity. It is stated that more significant indicators of dyslipidemia were associated with the greatest manifestations of abdominal obesity in terms of waist circumference (96.58 ± 1.70 cm and 98.73 ± 3.35 cm), as well as greater body mass index.
гіпотиреоз, лептин, функція нирок, абдомінальне ожиріння, дисліпідемія.
гипотиреоз, лептин, функция почек, абдоминальное ожирение, дислипидемия.
hypothyroidism, leptin, renal function, abdominal obesity, dyslipidemia.
Статья опубликована на с. 29-32
Вступ
Гіпотиреоз належить до захворювань, що сприяють розвитку атеросклерозу, дисліпідемії, артеріальної гіпертензії, абдомінального ожиріння, ендотеліальної дисфункції та серцево-судинних ускладнень [3]. За останні роки рівень захворюваності на гіпотиреоз у середньому по Україні збільшився вдвічі. Загалом у світі поширеність маніфестного гіпотиреозу у всій популяції досягла 2–3 %, у той час як поширеність субклінічного гіпотиреозу у жінок незалежно від віку становить у середньому 10 %, а у віці понад 60 років зростає до 20 %. Ниркова функція на тлі гіпотиреозу погіршується вторинно, залучаючи гетерогенні механізми, серед яких домінують гемодинамічні порушення: негативний інотропний ефект на серце, зменшення об’єму циркулюючої крові, підвищення загального периферичного опору судин, що супроводжується нирковою вазоконстрикцією. Первинний гіпотиреоз також пов’язаний з порушенням клубочкової фільтрації, яка є оборотною на тлі замісної гормональної терапії приблизно в 55 % випадків [4, 5]. З іншого боку, навіть незначне зниження функції нирок асоціюється з підвищенням серцево-судинного ризику, що зростає обернено пропорційно до рівня швидкості клубочкової фільтрації (ШКФ). При гіпотиреозі порушення функції ниркових клубочків (зниження ШКФ) та уповільнення швидкості кліренсу холестерину ліпопротеїдів низької щільності (ХС ЛПНЩ) сприяє розвитку дисліпідемії [7, 8]. Нещодавно встановлено, що замісна гормональна терапія при субклінічному гіпотиреозі запобігає прогресуванню ниркової недостатності і сприяє поліпшенню функції нирок [6]. Одночасно інші дослідники вказують на те, що характерними особливостями як маніфестного, так і субклінічного гіпотиреозу є більші прояви абдомінального ожиріння, що асоціюються з проатерогенними змінами ліпідного обміну (підвищення загального ХС та ХС ЛПНЩ) та формуванням проявів інсулінорезистентності за рахунок гіперінсулінемії [7]. Останніми роками приділяється увага вивченню значення адипонектинів, особливо лептину, у регуляції метаболізму в пацієнтів на тлі зниженої функції щитоподібної залози (ЩЗ). Підвищений рівень лептину розглядається як один із прогностичних чинників ризику розвитку серцево-судинних ускладнень [3]. Однак опубліковані дані про те, що лептин справляє пошкоджуючу дію на структуру й функцію нирок [13]. Так, в експерименті було показано, що введення рекомбінантного лептину стимулює проліферацію ендотеліальних клітин клубочка й збільшує експресію м-РНК TGF-b1 і його продукцію. J. Chdek і співавт. [7] продемонстрували, що екзогенне введення лептину протягом декількох тижнів значно збільшує продукцію колагену I і IV типу, призводячи до формування гломерулосклерозу й розвитку протеїнурії навіть при нормальному рівні артеріального тиску. Крім того, описано опосередкований вплив лептину на нирку.
Мета: вивчити взаємозв’язок вмісту лептину з порушенням функції нирок у хворих на первинний гіпотиреоз.
Матеріали та методи дослідження
Клінічні та функціонально-біохімічні обстеження хворих виконані на базі ендокринологічного відділення, диспансерного ендокринологічного відділення Івано-Франківської обласної клінічної лікарні.
У дослідження включені 132 хворі на первинний гіпотиреоз. Критеріями включення були вік пацієнтів від 36 до 60 років, уперше виявлений або декомпенсований гіпотиреоз. Наявність будь-якого гострого або хронічного захворювання нирок, ішемічна хвороба серця були критеріями виключення. Діагноз встановлювався на підставі скарг, даних анамнезу, характерної клінічної картини маніфестного гіпотиреозу й підтверджувався результатами гормонального дослідження. Група порівняння включала 22 особи без порушення функції ЩЗ, порівнянних за статтю й віком.
Усім хворим проводили комплексне загальноклінічне обстеження, визначали окружність талії (ОТ) (см), індекс маси тіла (ІМТ), рівень сечовини, креатиніну, загального білка. Ураження нирок констатували за наявністю порушення проникності клубочкового фільтра — появою мікро/макроальбумінурії і показниками ШКФ, визначеними за формулами MDRD. Рівень гормонів ЩЗ (вТ4 і вТ3), а також тиреотропного гормону (ТТГ) визначали в імунологічній лабораторії обласної клінічної лікарні з використанням аналізатора StatFax 303 та набору реактивів DRG (СШA). Загальний холестерин (ЗХС) і тригліцериди (ТГ) визначали ферментативним методом за допомогою реактивів фірми Human, ЛПВЩ — реактивів фірми «Діакон-ДС» на аналітичному аналізаторі Accept-200. Рівень холестерину ліпопротеїдів дуже низької щільності (ХС ЛПДНЩ) у крові обчислювали, застосовуючи математичну формулу: ЛПДНЩ = ТГ/2,2 ммоль/л, а рівень ХС ЛПНЩ — за математичною формулою: ЛПНЩ = ЗХС – (ЛПВЩ + + ТГ/2,2) ммоль/л. Розраховували також коефіцієнт атерогенності (КА) за формулою: КА = (ХС ЛПВЩ)/ЛПВЩ. Уміст лептину (норма 3,7–11,1 нг/мл) визначали за допомогою набору Diagnostics Biochem Canada Inc.
Обов’язкове інструментальне обстеження включало вимірювання артеріального тиску, ультразвукове дослідження (УЗД) органів сечової системи, ультразвукову допплерографію ниркового кровотоку.
Статистичний аналіз проводився варіаційно-статистичним методом. При аналізі матеріалу розраховували середні величини (M), їх стандартні похибки (m) і довірчий інтервал. Вірогідність відмінностей оцінювали за t-критерієм Стьюдента для залежних і незалежних вибірок, при нерівномірності розподілів використовували непараметричний критерій Mann-Whitney (U), Wilkonson (W). Відмінності вважали вірогідними при р < 0,05. Залежність показників оцінювалася методом Спірмана з обчисленням коефіцієнта кореляції. Статистичне опрацювання матеріалу проведене за допомогою варіаційної й описової статистики за допомогою стандартного пакета статистичних розрахунків Statistica 6.0, Foxbase, Exсel 6.0 на персональному комп’ютері Pentium III.
Результати дослідження та їх обговорення
Виникненню і прогресуванню ниркової дисфункції за умови дефіциту тиреоїдних гормонів сприяє наявність чинників ризику: метаболічних, інтеркурентних, гемодинамічних. Серед 132 обстежених хворих у 47,4 % ураження нирок було відсутнє. Порушення бар’єрної функції виявлено у 52,6 %, із них у 46,6 % виявлена мікроальбумінурія (МАУ), у 6 % — протеїнурія (ПУ). Рання стадія нефропатії (гіперфільтрація без МАУ) визначалася у 24 % хворих. За класифікацією хронічної хвороби нирок I стадія виявлена у 20 %, II — у 17 %, III — у 3 % обстежених хворих.
Установлено, що в пацієнтів із гіпотиреозом частота виявлення МАУ залежить від тривалості захворювання й перебуває в межах від 16,7 до 57,6 %. Наявність гіпотиреозу впродовж п’яти років збільшує ймовірність розвитку МАУ вдвічі порівняно з особами, що мають давність захворювання до одного року. У той же час тривалість гіпотиреозу понад п’ять років підвищує ймовірність виявлення МАУ втричі щодо частоти МАУ в пацієнтів із тривалістю гіпотиреозу менше одного року.
Нами встановлено вірогідний зв’язок між тривалістю гіпотиреозу й частотою виявлення МАУ. Так, при порівнянні частоти МАУ у хворих із давністю гіпотиреозу до одного року й від одного до п’яти років р = 0,04, а при порівнянні пацієнтів із давністю гіпотиреозу до одного року і хворих із тривалістю гіпотиреозу понад п’ять років р = 0,025.
Пацієнтів, у яких було виявлено порушення функції нирок, розподілили на 4 групи, враховуючи ІМТ, оскільки цей чинник істотно впливає на зміни вказаних параметрів. ІА група — хворі на гіпотиреоз на ґрунті автоімунного тиреоїдиту (АІТ) з ІМТ < 24,9 кг/м2; ІБ група — хворі на АІТ з ІМТ > 24,9 кг/м2; ІІА група — хворі на післяопераційний гіпотиреоз (ПГ) з ІМТ < 24,9 кг/м2; ІІБ група — хворі на ПГ з ІМТ > 24,9 кг/м2.
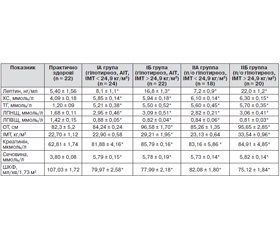
Рівні сечовини сироватки крові в групах пацієнтів з АІТ статистично значуще перевищували ці показники порівняно з групою контролю (р < 0,001); подібна тенденція відзначалася в групі пацієнтів з ПГ. При цьому медіана цього показника перевищувала верхню межу відповідного референтного інтервалу (8,3 ммоль/л для сечовини) (табл. 1). При порівнянні між групами вірогідної різниці виявлено не було.
Незважаючи на те, що рівень креатиніну сироватки крові перебував у межах референтного інтервалу (у чоловіків 97 мкмоль/л, у жінок 80 мкмоль/л), нами виявлено статистично значущі відмінності в групі пацієнтів з АІТ порівняно з контрольною групою: 81,88 ± 4,16 мкмоль/л і 62,81 ± 1,74 мкмоль/л (р < 0,001) та 85,79 ± 0,16 мкмоль/л і 62,81 ± 1,74 мкмоль/л (р < 0,001) у ІІБ групі. Подібні зміни спостерігалися в групі пацієнтів із ПГ порівняно з контролем: 83,16 ± 5,86 мкмоль/л і 62,81 ± 1,74 мкмоль/л (р < 0,001) у ІІА групі та 84,91 ± 4,85 мкмоль/л для ІІБ групи. При цьому в групі хворих з АІТ у трьох пацієнтів рівень креатиніну перевищував 120 мкмоль/л, а у двох пацієнтів групи з ПГ перевищував 115 мкмоль/л. Разом із тим при розрахунку ШКФ за формулою MDRD з урахуванням статі й віку було виявлено її значне зниження: у групі пацієнтів з АІТ в обох групах, проте в другій групі відзначали значно нижчі показники — 77,99 ± 2,18, що мало статистично значущі відмінності за цим показником із групою контролю: 107,03 ± 1,72 мл/хв/1,73 м2 (р < 0,001). У пацієнтів із ПГ також спостерігалося більше зниження ШКФ у групі хворих із надмірною масою тіла порівняно з контролем (р < 0,001).
При оцінці рівня лептину відмічено, що збільшення маси тіла у хворих на гіпотиреоз (як на ґрунті АІТ, так і ПО) супроводжується підвищенням концентрації лептину в сироватці крові. Так, у групі хворих на гіпотиреоз та АІТ рівень лептину був удвічі вищий у групі з ІМТ > 24,9 кг/м2, ніж у групі з ІМТ < 24,9 кг/м2, а в групах із ПО — втричі (рис. 2). Гіперлептинемія тісно пов’язана з антропометричними показниками й функціональними параметрами нирок. Найбільш чіткий зворотний зв’язок виявлено для лептину та ШКФ і прямий — з ОТ, окружністю стегон (ОС), ІМТ та екскрецією альбуміну.
При проведенні УЗД нирок, ультразвукової допплерографії ниркового кровотоку патології виявлено не було.
На початку дослідження медіана рівня ТТГ становила 8,6 мМО/л, що підтверджує той факт, що близько 20 % пацієнтів із гіпотиреозом, які вже отримують замісну гормональну терапію, перебувають у стані субклінічного або навіть явного гіпотиреозу, тобто з тієї чи іншої причини отримують неадекватно низькі дози препаратів тироксину. При оцінці ліпідограми в більшості хворих була виявлена дисліпідемія (79 % — за показниками ТГ та 76 % — за показниками ЛПВЩ). При оцінці вмісту ЗХС (референтний інтервал 3,63–5,20 ммоль/л) виявлено статистично значуще підвищення рівня показника в усіх пацієнтів порівняно з практично здоровими особами. При цьому в обох групах пацієнтів медіана даного показника перевищувала верхню межу відповідного референтного інтервалу. Подібна тенденція відзначалася в групах пацієнтів із гіпотиреозом на тлі АІТ та ПГ при порівнянні рівня ЛПНЩ: 2,95 ± 0,46 ммоль/л та 2,82 ± 0,21 ммоль/л (табл. 1). Подібний розподіл рівнів ЗХС і ЛПНЩ узгоджується з даними літератури про досить високу поширеність дисліпідемії у хворих на первинний гіпотиреоз. Загалом підвищення рівня ХС ЛПВЩ спостерігалося в підгрупах як з ІМТ < 24,9 кг/м2, так і з ІМТ > 25 кг/м2. При аналізі даних між підгрупами хворих на гіпотиреоз залежно від ІМТ зміни в ліпідному обміні спостерігалися в групах із надмірною масою тіла як серед хворих на АІТ, так і ПГ. Проте більш значущі показники дисліпідемії були в ІІБ підгрупі, що асоціювалося з найбільшими проявами абдомінального ожиріння за визначенням ОТ (96,58 ± 1,70 см та 98,73 ± 3,35 см), більшим ІМТ (31,21 ± 1,95 кг/м2 та 33,54 ± 0,96 кг/м2), що відповідав ожирінню I ст., а також найвищим рівнем лептину.
Встановлена нами залежність підтверджує, що гіпотиреоз впливає на ліпідний обмін, а збільшення ІМТ та гіперлептинемія погіршують перебіг захворювання.
Висновки
Згідно з отриманими результатами, у пацієнтів із маніфестним гіпотиреозом наявна дисфункція нирок, розвитку та прогресуванню якої сприяє наявність у пацієнтів чинників ризику — гіперліпідемії, гіперлептинемії, надмірної маси тіла та абдомінального ожиріння. Дослідження функції щитоподібної залози може бути рекомендоване як один із ранніх етапів діагностичного процесу в пацієнтів із порушенням функції нирок нез’ясованої етіології. При цьому маніфестний гіпотиреоз розглядається як одна з можливих причин. Подальші наукові дослідження будуть спрямовані на вивчення шляхів оптимізації профілактики та лікування дисфункції нирок у хворих на гіпотиреоз.
1. Балаболкин М.И., Клебанова Е.М., Креминская В.М. Фундаментальная и клиническая тиреоидология: Руководство. — М.: Медицина, 2007. — 816 с.
2. Гончарова О.А. Латентная вирусная инфекция и аутоиммунный тиреоидит // Международный эндокринологический журнал. — 2008. — № 4 (16).
3. Дедов И.И., Мельниченко Г.А., Фадеев В.В. Эндокринология: Учебник. — 2-е изд. — М.: Медиа, 2009. — 432 с.
4. Казаков А.В., Кравчун Н.А., Ильина И.М. и др. Словарь-справочник эндокринолога. — Харьков: С.А.М., 2009. — 682 с.
5. Каминский А.И. Болезни щитовидной железы // Проблемы эндокринологии. — 2007. — Т. 51, № 7. — C. 7–23.
6. Малахова С.М. Патогенетичний підхід до лікування атеросклерозу у хворих із високим кардіоваскулярним ризиком // Ліки України. — 2009. — № 4. — С. 128–130.
7. Митченко Е.И., Коваленко В.Н. Результаты многоцентрового исследования по выявлению гиперхолестеринемии на основании анализа данных областных липидных центров // Укр. кардіол. журн. — 2008. — Додаток 2. — С. 45–52.
8. Мітченко О.І., Лутай М.І. Дисліпідемії: діагностика, профілактика та лікування. Методичні рекомендації Робочої групи з проблем метаболічного синдрому, діабету та серцево-судинних захворювань та Робочої групи з проблем атеросклерозу та хронічних форм ІХС Української асоціації кардіологів. — К., 2007. — С. 3, 4, 13–15.
9. Наказ МОЗ України № 254 від 27.04.2006 р. Про затвердження протоколів надання медичної допомоги дітям за спеціальністю «дитяча ендокринологія».
10. Паньків В.І. Практична тиреоїдологія. — Донецьк: Видавець Заславський О.Ю., 2011. — 224 с.
11. Панькив В.И. Ранняя диагностика тиреоидной патологии в амбулаторных условиях // 100 избранных лекций по эндокринологии / Под ред. Ю.И. Караченцева и др. — Харьков, 2009. — 948 с.
12. Швед М.І., Пасєчко Н.В., Мартинюк Л.П. та ін. Клінічна ендокринологія в схемах і таблицях. — Тернопіль: Укрмедкнига, 2006. — 344 с.
13. Basu G., Mohapatra A. Interactions between thyroid disorders and kidney disease // Indian J. Endocrinol. Metab. — 2012. — Vol. 16 (2). — P. 204–213.
14. Clinical Management of Thyroid Disease / Ed. by F.E. Wondisford, S. Radovick. — Baltimore, Maryland: John Hopkins University School of Medicine, 2009. — 860 p.
15. Vargas F., Moreno J.M., Rodriguez-Gomez I. et al. Vascular and renal function in experimental thyroid disorders // Eur. J. Endocrinol. — 2006. — Vol. 154. — P. 197–212.
16. Meuwese C.L., Dekker F.W., Lindholm B. et al. Baseline levels and trimestral variation of triiodothyronine and thyroxine and their association with mortality in maintenance hemodialysis patients // Clin. J. Am. Soc. Nephrol. — 2012. — Vol. 7. — P. 131–138.
17. Salman Razvi. The Influence of Age on the relationship between subclinical hypothyroidism and ischemic heart disease: a metaanalisis // J. Clin. Endocrinol. Metabol. — 2008. — Vol. 93, № 8. — P. 59–67.

/31/31.jpg)