Статтю опубліковано на с. 76-79
Вступ
Особливістю більшості захворювань сучасної людини є висока вірогідність поєднання основного захворювання з іншими хворобами та патологічними станами, що взаємно обтяжують одне одного та вимагають комплексного підходу до лікування. Всесвітня організація охорони здоров’я вважає метаболічні порушення в організмі глобальною епідемією сучасності. За даними статистики, з такою проблемою зустрічаються 20 % людей середнього та літнього віку. При цьому паралельно можуть відзначатися часті головні болі, швидка втомлюваність, дратівливість, сльозливість, спалахи гніву. Така сама симптоматика притаманна синдрому хронічної втоми (СХВ).
На жаль, точних даних щодо поширеності СХВ серед населення України немає. Проте вважається, що останніми роками кількість випадків цієї патології значно збільшилася не лише в Україні, а й у всьому світі. Етіологія СХВ до цього часу залишається нечітко визначеною та викликає гострі суперечки, однак нині більшість дослідників визнають поліетіологічність даного захворювання [10]. Значна кількість учених вважає, що в основі СХВ лежать інфекції та дисфункції імунної, нервової та ендокринної систем [6].
Чисельні дані вказують на те, що при СХВ спостерігаються як кількісні, так і функціональні імунологічні порушення. Існує велика кількість «пускових механізмів», що викликають імунологічні реакції. Раніше нами виявлено зниження рівня імуноглобуліну (Ig) G за рахунок G1- та G3-класів, зниження числа лімфоцитів із фенотипом CD3 і CD4, природних кілерів, підвищення рівня циркулюючих комплексів, інтерлейкіну‑1 та інтерферону-гамма, а також фактора некрозу пухлини. Також при СХВ відзначено порушення функції Т-лімфоцитів у вигляді зниження відповіді на стимуляцію мітогенами in vitro [8].
Існуючі схеми лікування вказаних синдромів, хронічних обструктивних захворювань легень (ХОЗЛ) дозволяють лише усунути симптоми захворювання на деякий час після медикаментозної терапії [1, 5]. Для досягнення ж тривалого ефекту необхідний цілий комплекс заходів, що включає усунення факторів ризику, корекцію способу життя, харчових звичок тощо; однак навіть у комплексі це не гарантує стійкої ремісії. Надзвичайно важливим компонентом відновлення загального стану організму є нормалізація вегетативного балансу [1, 4, 5] та імунної системи. Розпочинає регуляторний процес нервова система, а через гіпоталамо-гіпофізарну систему до неї приєднується ендокринна. Отже, стабілізація вегетативних показників має першочергове значення для повноцінного відновлення функціональної активності організму [1]. Традиційні схеми терапії при метаболічному синдромі (МС) та СХВ передбачають окремий та опосередкований вплив на стан імунної системи.
Так, наприклад, позитивні результати щодо впливу на вегетативні порушення у хворих із серцево-судинною патологією продемонструвало застосування препарату ноофен (гідрохлорид бета-феніл-гама-аміномасляна кислота — фенібут). У таких хворих вегетосудинні порушення характеризуються великою кількістю суб’єктивної симптоматики, що характерна й для пацієнтів із МС та СХВ, такої як емоційні розлади, вегетативні прояви, внутрішнє напруження, тривога тощо. Препарат ноофен, маючи протитривожну, ноотропну, транквілізуючу, вегетостабілізуючу дію, покращує стан пацієнтів, тим самим покращуючи якість життя. Практична відсутність побічних ефектів, особливо притаманних міорелаксантам центральної дії та транквілізуючим лікарським засобам, робить ноофен безпечним у використанні при лікуванні вегетативних розладів у хворих із різною патологією внутрішніх органів [5].
З огляду на те, що при ХОЗЛ відзначають порушення цілого ряду показників імунітету (МС та цукровий діабет у пацієнтів з ХОЗЛ можуть погіршувати прогноз [9]), під впливом інфекційного агента може відбутися ще більш глибоке пригнічення імунної відповіді, обумовлене як екзо-, так і ендотоксинами, що звільняються внаслідок бактеріолізу. Традиційна терапія не дозволяє елімінувати персистенцію бактеріальних агентів. У зв’язку з цим доцільним є застосування бактеріальних імуномодуляторів, що позбавлені імуносупресивного компонента (бактеріальних вакцин). Одним із препаратів, що відносяться до подібних вакцин, є бронхо-мунал (Lek Pharmaceutical and Chemical Company, Slovenia). Препарат містить лізат 8 бактерій, які найчастіше є збудниками інфекцій дихальних шляхів: Streptococcus pneumoniae, Haemophilus influenzae, Klebsiella ozaenae, Klebsiella pneumoniae, Staphylococcus aureus, Streptococcus viridans, Streptococcus piogenes, Branhamella catarrhalis. Компоненти препарату індукують антигенспецифічну імунну відповідь, поліклональну стимуляцію В-лімфоцитів, а також активацію фагоцитарної ланки імунітету. Бронхо-мунал підвищує активність NK-клітин, збільшує вироблення цитокінів, кількість циркулюючих Т-лімфоцитів, підвищує рівень загальних IgA, IgG, IgM, а також вміст імуноглобулінів у секреті дихальних шляхів [3].
Мета дослідження: удосконалити лікування хворих на ХОЗЛ з МС та СХВ на підставі визначення клініко-імунологічних особливостей перебігу захворювання та оцінки ефективності запропонованої терапевтичної корекції.
Матеріал і методи
За період 2013–2015 рр. нами обстежено 25 хворих, які звернулися за медичною допомогою до ендокринологічного центру та відділення пульмонології та алергології обласної клінічної лікарні м. Чернівців, та 10 практично здорових осіб. Усі хворі були рандомізовані на дві групи. Серед пацієнтів із встановленим діагнозом ХОЗЛ виділена група (основна) з 16 осіб (жінок — 7, чоловіків — 9, середній вік — 45 років), яким на фоні стандартного лікування додатково (наказ МОЗ України № 555 «Про затвердження та впровадження медико-технологічних документів зі стандартизації медичної допомоги при хронічному обструктивному захворюванні легень) призначали ноотропний препарат ноофен у добовій дозі 750 мг, поділеній на 3 прийоми (по 1 таблетці 250 мг 3 рази на добу після прийому їжі), тривалістю 30 діб, та імуностимулятор мікробного походження бронхо-мунал (натще вранці по 1 капсулі) впродовж 20 днів. Друга група (порівняння) — 9 пацієнтів, які отримували стандартне лікування. Третя група (контрольна) — здорові особи, 10 чоловік.
Критеріями включення в дослідження були: наявність ХОЗЛ, що підтверджене клінічно, спірографічно, рентгенологічно; наявність підтверджених МС та СХВ, вік від 35 до 54 років; відсутність алергічних реакцій в анамнезі; відсутність іншої супутньої патології, згода на прийом препаратів.
Критеріями виключення стали: відмова від прийому препарату; застосування інших адаптогенів і/або імуномодуляторів; гострі інфекційні захворювання; недотримання умов протоколу; наявність в анамнезі життя будь-яких неврологічних або психічних захворювань.
Для встановлення діагнозу СХВ використовували критерії, запропоновані Центром контролю за захворюваннями (США) [8]. Діагноз МС виставляли (після консультації ендокринолога) за наявності наступних критеріїв:
1. Абдомінальне ожиріння (окружність талії у чоловіків ≥ 90 см, у жінок ≥ 80 см).
2. Підвищення рівня тригліцеридів (≥ 1,7 ммоль/л).
3. Зниження рівня холестерину ліпопротеїдів високої щільності (< 1,03 ммоль/л).
4. Підвищення рівня артеріального тиску (систолічний тиск ≥ 130 мм рт.ст., діастолічний тиск ≥ 85 мм рт.ст.).
5. Підвищення рівня глюкози в плазмі натще (≥ 5,6 ммоль/л).
6. Гіперурикемія (рівень сечової кислоти в плазмі крові > 0,383 ммоль/л).
Поєднання окремих компонентів розглядали в рамках МС за наявності трьох із вказаних, обов’язковим з яких є інсулінорезистентність.
Обстеження хворих для визначення динаміки основних проявів поєднаної патології проводилося двічі, при первинному обстеженні та через 4 тижні після початку лікування, шляхом клінічної бесіди та анкетування за формою, аналогічною тій, що використовувалася під час первинного обстеження.
Імунну систему охарактеризовано на підставі імунограми з визначенням субпопуляцій лімфоцитів, рівня імуноглобулінів (лабораторії «Сінево» та «Ескулаб», м. Чернівці).
Ступінь тяжкості вегетативної дисфункції визначали за допомогою анкети-опитувальника О.М. Вейна з визначенням кількості балів перед лікуванням та після нього, що заповнювалася пацієнтом самостійно. Сума балів, що перевищувала 15, свідчила про наявність вегетативної дисфункції [6].
Міжгруповий і внутрішньогруповий статистичний аналіз з метою виявлення розбіжностей для кількісних ознак із нормальним або наближеним до нормального розподілом проводився за допомогою параметричного t-критерію Стьюдента на персональному комп’ютері за допомогою офісного пакету Microsoft Excel та пакету прикладних програм Statistica (StatSoft Inc., США) [7].
Результати дослідження
На початку дослідження основна група та група порівняння не відрізнялись за основними медико-соціальними параметрами та тяжкістю клінічних проявів ХОЗЛ (помірний/тяжкий перебіг захворювання). Частка осіб чоловічої статі неістотно перевищувала частку осіб жіночої.
Субпопуляційний склад лімфоцитів у хворих наведений у табл. 1. У всіх обстежених пацієнтів був знижений їх рівень. У результаті застосування бронхо-муналу та ноофену на фоні базисної терапії ці показники підвищилися, співвідношення CD4/CD8 нормалізувалося (Р < 0,05); у хворих, яких лікували без застосування препаратів, що вивчались, показники змінювалися незначно (Р > 0,5).
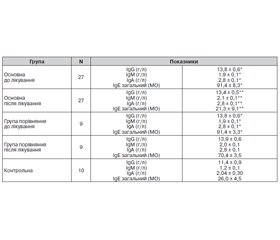
Стан гуморального імунітету наведений у табл. 2. Кількість В-лімфоцитів у результаті лікування вірогідно наближалась до показників норми в усіх хворих, кількість IgG незначно змінювалась. У хворих 1-ї групи вміст IgE до лікування був підвищеним, після лікування бронхо-муналом та ноофеном знизився до норми. У хворих 2-ї групи ці показники змінювалися незначно.
До початку лікування більшість хворих скаржилась на відчуття емоційного напруження, лабільність настрою, підвищену дратівливість, тривогу, порушення сну, підвищену втомлюваність, серцебиття, перебої в роботі серця, кардіалгії. Загальна сума балів, розрахованих за допомогою анкети-опитувальника О.М. Вейна, перевищувала 15 і становила в середньому 42,0.
Обговорення результатів дослідження
Після проведеного лікування ноофеном у більшості хворих основної групи відзначали зменшення або повне усунення тривоги, емоційного напруження, нормалізацію сну, зменшення кардіалгії, серцебиття та перебоїв у роботі серця на відміну від групи порівняння.
За даними нашого дослідження, комбінована терапія із застосуванням ноофену у хворих на ХОЗЛ із СХВ та МС позитивно впливала на якість життя, знижувала ступінь вегетативного дисбалансу за даними шкали вегетативного тонусу (модифікація анкети-опитувальника О.М. Вейна), зменшилась кількість загострень ХОЗЛ впродовж року, хворі відмічали посилення ефекту традиційного лікування. Яких-небудь ускладнень і побічних ефектів, пов’язаних із застосуванням бронхо-муналу та ноофену, не спостерігали.
Висновки
1. Застосування ноофену в складі комбінованої терапії у хворих на хронічне обструктивне захворювання легень із синдромом хронічної втоми та метаболічним синдромом зумовлює нормалізацію емоційного стану, клінічних проявів вегетативної дисфункції та покращання якості життя пацієнтів, що супроводжується добрим сприйняттям призначеного лікування.
2. Імуномодулюючий препарат бронхо-мунал, створений на основі бактеріальних лізатів, сприяє нормалізації кількості імунокомпетентних клітин та є доцільним засобом для застосування у хворих на хронічне обструктивне захворювання легень із синдромом хронічної втоми та метаболічним синдромом у комплексному лікуванні.
3. Комбіноване застосування мікробного імуностимулятора та ноотропного препарату сприяло покращенню загального психоемоційного стану хворих, підвищенню протимікробної резистентності, що проявлялось у зниженні кількості загострень хронічних обструктивних захворювань легень впродовж року, посиленні ефекту загальноприйнятого лікування.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів.
Список литературы
1. Бурчинский С.Г. Нейрометаболическая и вазотропная фармакотерапия в практике семейного врача / С.Г. Бурчинский // Рациональная фармакотерапия. — 2010. — № 1. — С. 16-19.
2. Вейн А.М. Вегетативные расстройства. Клиника, диагностика, лечение. — М.: Медицина, 1998. — 740 с.
3. Каспрук Н.М. Синдром хронічної втоми у хворих на хронічний обструктивний бронхіт та шляхи корекції / Н.М. Каспрук // Буков. мед. вісник. Матеріали 96-ї підсумкової наукової конференції професорсько-викладацького персоналу Буковинського державного медичного університету. — Чернівці, 2014. — С. 303-304.
4. Кішко Н.Ю. Корекція порушень вегетативного гомеостазу у дітей з гастроезофагеальним рефлюксом / Н.Ю. Кішко // Педіатрія, акушерство та гінекологія. — 2003. — № 4. — C. 17-20.
5. Кузьминова Н.В. Вегетативные расстройства у пациентов с гипертонической болезнью: диагностика и медикаментозная коррекция / Н.В. Кузьминова, В.К. Серкова // Укр. терапевтичний журнал. — 2009. — № 2(70). — C. 37-39.
6. Майданник В.Г. Синдром хронічного стомлення у дітей та підлітків / В.Г. Майданник, Н.М. Сотниченко // Педіатрія, акушерство та гінекологія. — 2001. — № 4. — С. 48-53.
7. Реброва О.Ю. Руководство — пакет прикладных программ Statistiсa 6.0. — М.: Синергия, 2003. — 68 с.
8. Сидорчук І.Й., Каспрук Н.М. Синдром хронічної втоми та стан клітинної і гуморальної ланок системного імунітету / І.Й. Сидорчук, Н.М. Каспрук, Я.В. Морозюк, Р.П. Ляшук, К.І. Яковець, Л.П. Петеліна // Буков. мед. вісник. — Чернівці, 2012. — Т. 16, № 4. — С. 145-148.
9. Ikeda A., Nishimura K., Koyama H. et al. Bronchodilating effects of combined therapy with clinical dosages of ipratropium bromide and salbutamol for stable copd — comparison with ipratropium bromide alone // Chest. — 1995. — № 107(2). — Р. 401-405.
10. Reid H., Alam М. Millennium development goals // Tiempo: A Bulletin on Climate and Development. — 2005. — № 54. — Р. 18-22.
1. Burchynskyy SH. [Neurometabolic and vasotropic pharmacotherapy in family doctor’s practice] Ratsyonal'naya farmakoterapyya. 2010;1:16-19. Russian.
2. Veyn AM. [Vegetative disorders. Clinics, diagnosis, treatment]. Moscow: Medytsyna; 1998. 740 p. Russian.
3. Kaspruk NM. [Chronic fatigue syndrome in patients with chronic obstructive bronchitis and treatment approaches]. In: [Materialy 96 pidsumkovoyi naukovoyi konferentsiyi profesors'ko-vykladats'koho personalu Bukovyns'koho derzhavnoho medychnoho universytetu; 2014; Chernivtsi, Ukraine]. Chernivtsi; 2014. p.303-304. Ukrainian.
4. Kishko NYu. [Correction of vegetative homeostasis disturbances in children with gastroesophageal reflux disease]. Pediatriya, akusherstvo ta hinekolohiya. 2003;4:17-20. Ukrainian.
5. Kuz'mynova NV. [Vegetative disorders in patients with arterial hypertension: diagnosis and medicinal correction]. Ukr. terapevtychnyy zhurnal. 2009;2(70):37-39. Russian.
6. Maydannyk VH. [Chronic fatigue syndrome in children and adolecents] Pediatriya, akusherstvo ta hinekolohiya. 2001;4:48-53. Ukrainian.
7. Rebrova OYu. [Guide-package of applied software Statistika 6.0]. – М.: Synerhyya; 2003. 68 p. Russian.
8. Sydorchuk IY, Kaspruk NM, Morozyuk YaV et al. [Chronic fatigue syndrome and condition of cellular and humoral immunity] Bukov. med. visnyk. 2012;16(4):145-148. Ukrainian.
9. Ikeda A, Nishimura K, Koyama H et al. Bronchodilating effects of combined therapy with clinical dosages of ipratropium bromide and salbutamol for stable COPD – comparison with ipratropium bromide alone. Chest. 1995;107(2):401-405.
10. Reid H, Alam M. Millennium development goals. A Bulletin on Climate and Development. 2005;54:18-22.

/78.jpg)