Статтю опубліковано на с. 95-98
Вступ
Дефіцит вітаміну D — загальна та достатньо поширена проблема, що стосується всіх вікових груп населення. Недостатність вітаміну D залучена в патогенез як патології кісткової системи, так і багатьох різних хронічних захворювань, включаючи цукровий діабет (ЦД), серцево-судинні захворювання, ожиріння, дисліпідемію, артеріальну гіпертензію.
За даними W.P.T. James (2008), у світі нараховується 1 млрд людей, які мають дефіцит та недостатність вітаміну D. Головна його причина — недостатній вплив сонячного світла: робота в офісних приміщеннях протягом світлового дня, урбанізація, пов’язана зі зменшенням часу перебування на відкритому повітрі, скорочення відпусток та застосування сонцезахисних засобів зменшують синтез вітаміну D у шкірі більш ніж на 95 %. За данними Всесвітньої організації охорони здоров’я, недостатність вітаміну D має характер пандемії.
Дефіцит вітаміну D — актуальна проблема й для української нації. Під час визначення рівня вітаміну D у сироватці крові мешканців нашої країни нормальний рівень зареєстрований тільки в 4,6 % населення, недостатність — у 13,6 %, дефіцит — у 81,8 % [1].
Згідно із сучасною класифікацією, виражений дефіцит вітаміну D визначається при рівні 25(OH)D, нижчому за 10 нг/мл, дефіцит вітаміну D — рівень 25(OH)D,
менший за 20 нг/мл (50 нмоль/л), недостатність вітаміну D (субоптимальний рівень) — рівень 25(OH)D, що становить 21–29 нг/мл (50,1–74,9 нмоль/л), оптимальний рівень (цільовий статус) — понад 30 нг/мл (75,0 нмоль/л та більше) і високий вміст — 50–100 нг/мл (125–250 нмоль/л) [2].
Останнім часом суттєво змінились дані щодо фізіологічної ролі вітаміну D [2]. Активні метаболіти вітаміну D регулюють проліферацію та диференціацію клітин, синтез ліпідів, білків, ензимів, гормонів, роботу органів і систем. Традиційно вітамін D відносять до жиророзчинних вітамінів, але в організмі він виконує роль гормону. Відкриття рецепторів до гормонально активних форм вітаміну D та їх синтез у клітинах нетрадиційних для цього вітаміну органів та тканин передбачає більш широкий спектр фізіологічного ефекту вітаміну D [3].
Відомо, що кісткова тканина — динамічна система, у якій протягом життя постійно відбуваються цикли ремоделювання (старіння, руйнування й утворення нової тканини). У дитячому віці кістка зазнає найбільш інтенсивного ремоделювання. Особливо виражені процеси росту, гістологічного дозрівання й мінералізації в ранньому віці, препубертатному та пубертатному періодах. Зазначені процеси створюють для кістки особливе становище, коли вона стає надчутливою до будь-яких несприятливих впливів [4].
У дослідженнях педіатрів Школи суспільної охорони здоров’я Джона Хобкінса Блумберга (Балтимор, США) доведено, що в підлітків зменшення рівня вітаміну D становить серйозний ризик для майбутнього стану здоров’я. Зменшення кількості вітаміну D у підлітків пов’язане з ризиком підвищення рівня цукру крові, артеріального тиску та розвитку метаболічного синдрому.
Розширення наших знань про роль вітаміну D в організмі в нормі та при патології розкриває перспективи клінічного використання цього вітаміну для профілактики та лікування ЦД [2]. Достатній рівень вітаміну D у молодому віці може знизити ризик розвитку ЦД у майбутньому на 50 % [5]. Численні публікації, присвячені дослідженням статусу вітаміну D у хворих на ЦД, які були проведені в різних регіонах світу, підтверджують, що хворі на ЦД 1-го та 2-го типу мають знижений рівень вітаміну D. Численні дослідження демонструють, що в пацієнтів із ЦД низькі значення 25(OH)D у сироватці крові асоціюються зі збільшенням рівня глікованого гемоглобіну [6]. Наявні на сьогодні дані свідчать про багатогранність фізіологічних шляхів впливу вітаміну D на функцію β-клітин підшлункової залози та вуглеводний обмін [7].
Мета: аналіз залежності різних чинників компенсації ЦД у підлітків, хворих на ЦД 1-го типу, від рівня вітаміну D у крові.
Матеріали та методи
Дане дослідження проводилось на базі Вінницького обласного клінічного високоспеціалізованого ендокринологічного центру, Вінницької обласної клінічної дитячої лікарні. Були обстежені 54 дитини віком від 12 до 18 років (26 хлопців, 28 дівчат), хворих на ЦД 1-го типу, без ознак затримки фізичного та статевого розвитку, гепатозу та без супутніх захворювань. Дослідження відбулось після підписання інформованої згоди батьків на проведення даних обстежень у їхніх дітей.
Діти були поділені за рівнем вітаміну D на 3 групи: перша група (n = 4, середній вік 13,10 ± 0,58 року) — хворі на ЦД 1-го типу з оптимальним рівнем 25(ОН)D (понад 30 нг/мл), друга група (n = 28, середній вік 14,7 ± 1,2 року) — хворі на ЦД 1-го типу з недостатнім рівнем 25(OH)D (21–29 нг/мл), третя група (n = 22, середній вік 15,1 ± 2,1 року) — хворі на ЦД 1-го типу з дефіцитом вітаміну D (рівень 25(OH) D менший за 20 нг/мл). До контрольної групи включено 11 практично здорових дітей аналогічного віку, які не мали скарг, клінічних ознак, анамнестичних даних, що б свідчили про наявність будь-якого хронічного захворювання.
У дослідженні були використані клініко-анамнестичні, лабораторні та статистичні методи досліджень. Проводився клінічний огляд дітей, що включав оцінку фізичного розвитку, розрахунок індексу маси тіла (ІМТ), об’єктивну оцінку стану різних органів та систем, аналізувалися вік маніфестації та тривалість ЦД. Усім дітям, крім стандартних обстежень, було проведено дослідження — визначення концентрації 25(ОН)D у сироватці крові (забір крові проводився в осінньо-зимово-весняний період). Визначався рівень глікованого гемоглобіну (НbА1с), загального кальцію крові. Рівень вітаміну 25(ОН)D у крові визначали за допомогою імуноферментного аналізу з використанням реактивів фірми Roche diagnostic на аналізаторі Cobas E411 (виробник Німеччина), рівень кальцію крові — реактивами фірми Beckman Coulter на аналізаторі АU480 (виробник США), рівень НbА1с — реактивами фірми Bio-Rad на аналізаторі D10 (виробник Франція).
Статистичний аналіз даних проводили за допомогою статистичних пакетів Statistica 7.0.
Результати
За рівнем вітаміну D обстежені були розподілені на 3 групи. У першу групу увійшли діти із середнім рівнем 25(ОН)D 34,5 ± 1,6 нг/мл (n = 4, 2 дівчат та 2 хлопців, що становило 7,4 % від загальної кількості обстежених підлітків із ЦД 1-го типу). Другу групу обстежених становили підлітки, хворі на ЦД 1-го типу (n = 28, 16 дівчат, 12 хлопців — 51,8 % обстежених), із середнім рівнем 25(ОН)D 24,2 ± 1,3 нг/мл. У третю групу обстежених увійшли підлітки, хворі на ЦД 1-го типу (n = 22, 10 дівчат, 12 хлопців — 40,7 % обстежених), з середнім рівнем 25(ОН)D 18,9 ± 0,6 нг/мл.
При аналізі показників рівня вітаміну D у підлітків із ЦД 1-го типу виявилось, що лише в чотирьох пацієнтів був адекватний рівень вітаміну D, що становило 7,4 % від обстежених пацієнтів. При обстеженні дітей контрольної групи (n = 11) нормальний рівень вітаміну D встановлено в трьох дітей (27,2 %).
При аналізі груп обстежених встановлено, що за статтю і віком групи не відрізнялися (майже половина дівчат, середній пубертатний вік 14,2 ± 2,5 року). У другій та третій групах більша частина (75 %) пацієнтів мала стаж захворювання понад 5 років, а діагноз ЦД 1-го типу був уперше виставлений у віці від 5 до 10 років. Саме на цей віковий період припадають періоди інтенсивного росту. Те, що лише 30 % дітей контрольної групи мали нормальний вміст вітаміну D, вказує на загальну проблему забезпеченості вітаміном D у пубертатному віці. Однак на тлі ЦД у дітей середнього пубертатного віку ця проблема ще більш виражена.
При аналізі анамнестичних даних обстежених встановлено, що до п’яти років життя захворіло на ЦД 1-го типу 13 дітей (24 %), а решта 41 (76 %) — після п’яти років, в період більш інтенсивного росту, пов’язаного з впливом інсуліну та статевих гормонів. Стаж захворювання до п’яти років спостерігався в семи дітей (12,9 %), від 5 до 10 років — у 28 (52 %) і понад 10 років — у 19 (35 %) дітей. При аналізі цих показників видно, що стаж ЦД у дітей перевищував у більшості випадків 5 років і захворіли вони також у віці понад 5 років. При аналізі маси тіла за ІМТ виявлено, що переважали діти з нормальним фізичним розвитком. Дані по групах подані в табл. 1.
Обговорення
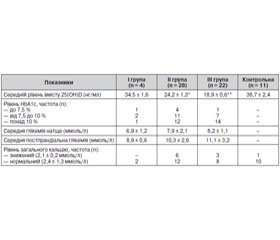
Як видно з табл. 2, у компенсованому стані з приводу ЦД (НbА1с нижче від 7,5 %) перебувало 6 дітей (11,1 %), у 20 обстежених (37 %) показник НbА1с становив від 7,5 до 10 % і понад 10 % — у 27 пацієнтів (50 %). Декомпенсовані пацієнти становили 42,6 % у другій групі обстежених та 54,1 % — у третій групі. Показники глікемії натще та постпрандіальної глікемії в обстежених пацієнтів наведені в табл. 2. Вони суттєво не відрізнялися в обстежених групах. Отже, ступінь декомпенсації не залежав від наявності дефіциту вітаміну D в обстежених підлітків, хворих на ЦД 1-го типу. Аналіз результатів визначення загального кальцію у підлітків, хворих на ЦД 1-го типу, показав переважно нормальний його рівень у крові.
Висновки
Одержані результати демонструють зниження показників вітаміну D (недостатність або дефіцит) у крові дітей із цукровим діабетом 1-го типу. Встановлено наявність статистично значущого зв’язку між дефіцитом або недостатністю вітаміну D і компенсацією ЦД та тривалістю захворювання. Визначення вмісту рівня загального кальцію крові у хворих на ЦД не відображає проблему обмінних процесів за участю вітаміну D. Вплив корекції вмісту вітаміну D на компенсацію захворювання у хворих на ЦД 1-го типу підлітків потребує подальшого вивчення.

/97.jpg)