Резюме
Актуальність. Серед усіх захворювань ревматологічного профілю на частку ревматоїдного артриту (РА) припадає 3 % випадків, причому чисельність таких хворих зростає. Для РА характерне системне ураження судин (ангіопатія), що характеризується за міжнародною Чeпел-Хіллською класифікацією як «васкуліт, пов’язаний із системним захворюванням». Мета роботи: поліпшити якість діагностики, встановити нові ланки патогенезу й виділити прогностичні критерії перебігу ураження судин при РА. Матеріали та методи. Під наглядом перебував 131 хворий на РА. Співвідношення чоловіків і жінок становило 1 : 2, мінімальний, помірний і високий ступінь активності захворювання — відповідно 1 : 2 : 1, середній вік обстежених пацієнтів дорівнював 45,70 ± 1,02 року, тривалість клінічної маніфестації — 9,40 ± 0,68 року, I, II, III і IV стадії діагностовано відповідно у 8, 40, 34 і 19 % від числа хворих. Виконували ехокардіографію, сонографію та ультразвукову допплерографію судин, біомікроскопію кон’юнктиви, морфологічне дослідження нефробіоптатів, визначали інтегральні індекси клінічної та інструментальної судинної патології. Результати. Системна ангіопатія спостерігалась у 61 % від числа хворих на РА, частіше у випадках високого ступеня активності при наявності остеопорозу, при цьому розвиток васкуліту шкіри та периферичної вазонейропатії був тісно пов’язаний із рівнем у сироватці крові антитіл до циклічного цитрулінового пептиду, який разом із концентрацією С-реактивного протеїну має негативну прогностичну значущість щодо судинної патології. Поява дигітального артеріїту визначається активністю суглобового синдрому, гломерулонефриту — високим вмістом у крові циркулюючих імунних комплексів, а наявність ангіопатії відображає підвищення тиску в малому колі кровообігу. Висновки. У хворих на РА розвивається мезангіопроліферативний або мезангіокапілярний гломерулонефрит у співвідношенні 2 : 1 із закономірним тубулоінтерстиціальним компонентом і депозицією імуноглобулінів та компонентів комплементу (у стромі → клубочках → канальцях → судинах), при цьому структурні зміни судин нирок тісно пов’язані з клініко-інструментальними проявами системної ревматоїдної ангіопатії. Показники в крові C-реактивного протеїну більше 25 мг/л і протицитрулінових антитіл більше 40 О/мл є прогнознегативними критеріями щодо системної судинної патології й ушкоджень строми нирок, а тяжкі зміни ниркових канальців належать до чинників ризику високих темпів прогресування суглобового синдрому.
Актуальность. Среди всех болезней ревматологического профиля на долю ревматоидного артрита (РА) приходится 3 % случаев, причем численность таких больных растет. Для РА характерно системное поражение сосудов (ангиопатия), характеризующееся по международной Чэпел-Хиллской классификации как «васкулит, связанный с системным заболеванием». Цель работы: улучшить качество диагностики, установить новые звенья патогенеза и выделить прогностические критерии течения поражения сосудов при РА. Материалы и методы. Под наблюдением находился 131 больной РА. Соотношение мужчин и женщин составило 1 : 2, минимальная, умеренная и высокая степени активности заболевания — соответственно 1 : 2 : 1, средний возраст обследованных пациентов составил 45,70 ± 1,02 года, длительность клинической манифестации — 9,40 ± 0,68 года, I, II, III и IV стадии диагностированы у 8, 40, 34 и 19 % от числа больных соответственно. Выполняли эхокардиографию, сонографию и ультразвуковую допплерографию сосудов, биомикроскопию конъюнктивы, морфологическое исследование нефробиоптатов, определяли интегральные индексы клинической и инструментальной сосудистой патологии. Результаты. Системная ангиопатия наблюдалась у 61 % от числа больных РА, чаще в случаях высокой степени активности при наличии остеопороза, при этом развитие васкулита кожи и периферической вазонейропатии было тесно связано с уровнем в сыворотке крови антител к циклическому цитруллиновому пептиду, который, наряду с концентрацией С-реактивного протеина, обладает негативной прогностической значимостью в отношении сосудистой патологии. Появление дигитального артериита определяется активностью суставного синдрома, гломерулонефрита — высоким содержанием в крови циркулирующих иммунных комплексов, а наличие ангиопатии отражает повышение давления в малом круге кровообращения. Выводы. У больных РА развивается мезангиопролиферативный или мезангиокапиллярный гломерулонефрит в соотношении 2 : 1 с закономерным тубулоинтерстициальным компонентом и депозицией иммуноглобулинов и компонентов комплемента (в строме → клубочках → канальцах → сосудах), при этом структурные изменения сосудов почек тесно связаны с клинико-инструментальными проявлениями системной ревматоидной ангиопатии. Показатели в крови C-реактивного протеина более 25 мг/л и противоцитруллиновых антител более 40 Е/мл являются прогнознегативными критериями в отношении системной сосудистой патологии и повреждений стромы почек, а тяжелые изменения почечных канальцев относятся к факторам риска высоких темпов прогрессирования суставного синдрома.
Background. Among all rheumatologic diseases, rheumatoid arthritis (RA) accounts for 3 % of cases, and the number of such patients is increasing. RA is characterized by systemic vascular lesion (angiopathy), it is determined by the international Chapel Hill classification as “vasculitis associated with systemic disease”. The purpose of the study was to improve the quality of diagnosis, to stablish new links in the pathogenesis and to identify the prognostic criteria for the clinical course of vascular disease in RA. Materials and methods. 131 patients were examined. The ratio of men and women was 1 : 2, the mild, moderate and high degree of the disease activity was 1 : 2 : 1, respectively, the average age of the examined patients was 45.70 ± 1.02 years, the duration of the clinical manifestation was 9.40 ± 0.68 years, I, II, III and IV stages were diagnosed in 8, 40, 34 and 19 % of patients. Echocardiography, sonography and ultrasonic dopplerography of vessels, conjunctival biomicroscopy, morphological examination of kidney biopsy were preformed, integrated indices of clinical and instrumental vascular pathology were determined. Results. Systemic angiopathy is observed in 61 % of patients with RA, more often in cases of high activity with the presence of osteoporosis, the development of skin vasculitis and peripheral vasoneuropathy are closely related to the serum levels of cyclic citrullinated peptide antibodies, which, along with the concentration of C-reactive protein, has a negative prognostic significance for the vascular pathology, and the appearance of digital arteritis is determined by the activity of the joint syndrome, the appearance of glomerulonephritis — by the high content in the blood of circulating immune complexes, and angiopathy presence reflects the pressure increase in the lesser (pulmonary) circulation. Conclusions. In patients with RA, mesangial proliferative and mesangial capillary glomerulonephritis develops in a ratio of 2 : 1, with an appropriate tubulointerstitial component and the immunoglobulins and complement components deposition (in the stroma > glomeruli > tubules > vessels), at that the structural changes in the renal vessels are closely associated with clinical instrumental manifestations of systemic rheumatoid angiopathy. C-reactive protein values in the blood more than 25 mg/L and anti-citrulline antibodies more than 40 U/ml are prognostic negative criteria for systemic vascular pathology and the kidney stroma damage, severe changes in renal tubules are a risk factor for the high rates of the joint syndrome progression.
Введение
Ревматоидный артрит (РА) входит в группу системных аутоиммунных ревматических заболеваний [5–7], а среди всех болезней ревматологического профиля на его долю приходится примерно 3 % [10], причем численность таких больных повсеместно растет [8]. Одним из основных проявлений РА является поражение сосудов (ангиопатия) [2–4], которое по международной Чэпел-Хиллской классификации характеризуется как «васкулит, связанный с системным заболеванием» и клинико-патогенетические особенности которого изучены недостаточно [1, 9].
Цель исследования: улучшить качество диагностики, установить новые звенья патогенеза и выделить прогностические критерии течения поражения сосудов при РА.
Материалы и методы
Обследован 131 больной РА в возрасте от 18 до 69 лет (в среднем 45,70 ± 1,02 года), среди которых было 26,0 % мужчин и 74,1 % женщин. Длительность заболевания составила 9,40 ± 0,68 года, І степень его активности установлена в 26,7 % наблюдений, ІІ — в 42,8 %, ІІІ — в 30,5 %. Показатель активности артрита для 28 суставов (DAS) составил 4,50 ± 0,10 отн. ед.; I, II, III и IV рентгенологические стадии патологического процесса констатированы соответственно в 7,6, 39,7, 33,6 и 19,1 % случаев; серопозитивность по ревматоидному фактору (RF) на момент обследования — в 55,7 %, по антителам к циклическому цитруллиновому пептиду (аССР) — в 82,5 % случаев. Висцеральная системная форма болезни имела место у 25,9 % от числа больных, эйтонический тип вегетативной нервной системы обнаружен в 72,5 % наблюдений, симпатотонический — в 18,3 %, ваготонический — в 9,2 %, вегетативный индекс (ВИ — логарифм квадратического индекса Кердо) составил 5,00 ± 0,17 усл. ед.
Средние показатели индекса Лансбури (LI) составили 131,40 ± 4,46 балла, интегральной тяжести артрита (SAI) — 89,00 ± 1,85 отн. ед., темпов его прогрессирования (PAI) — 1,80 ± 0,20 отн. ед., параметров RF в крови — 15,20 ± 2,04 мЕ/мл, aCCP — 24,30 ± 1,01 Е/мл, С-реактивного протеина (CRP) — 14,30 ± 0,71 мг/л, иммуноглобулина (Ig) G — 17,20 ± 0,26 ммоль/л, IgM — 2,40 ± 0,04 ммоль/л, циркулирующих иммунных комплексов (CIC) — 131,50 ± 5,37 усл. ед. Системный остеопороз выявлен у 74,1 % от числа больных, тендовагиниты — у 42,0 %, спондилопатия — у 38,9 %. Проанализирован характер изменений сосудов в нефробиоптатах 17 больных РА (5 мужчин и 12 женщин) с хронической болезнью почек (ревматоидный гломерулонефрит) в возрасте от 32 до 68 лет (в среднем 50,10 ± 2,33 года). Из анализа были исключены пациенты с вторичным АА-амилоидозом почек.
SAI рассчитывали по формуле: SAI = √LI × DAS. В свою очередь, DAS определяли по формуле: DAS = = [(√RI × 0,54) + (J × 0,065) + (lnQ × 0,33) + 0,224] × 1,072 + 0,94, где RI — индекс Ричи, J — число болезненных суставов, Q — скорость оседания эритроцитов. PAI оценивали по формуле: PAI = [(Rg)2 + S]: Т, где Rg — рентгенологическая стадия болезни, S — сумма рентгеносонографических признаков суставного синдрома, T — продолжительность клинической манифестации заболевания. Определяли интегральный инструментальный индекс сосудистой патологии (Y). При этом каждый средний показатель у больного < М + SD оценивали в 1 балл, М + SD ↔ M + 2SD — в 2 балла, М + 2SD ↔ M + 3SD — в 3 балла, > М + 3SD — в 4 балла. Рассчитывали Y на одного больного по формуле: Y = (A + 2B + 3C + 4D): E, где A, B, C, D — число больных с 1, 2, 3 и 4 баллами соответственно, E — число показателей. Среди клинических признаков ангиопатии у больных РА учитывали наличие кожной пурпуры, синдрома Рейно, телеангиэктазий, капилляритов кистей и стоп, дигитального артериита, увеита, хейлита, лейкоцитокластической энантемы, антифосфолипидного синдрома (АФЛС), дисциркуляторной энцефалопатии, периферической вазонейропатии, гломерулонефрита, артериальной периферической и легочной гипертензии. Изучали интегральный индекс клинической тяжести течения сосудистой патологии заболевания (W) по формуле: W = (S : N) × √S, где S — сумма баллов всех клинических признаков заболевания, N — число признаков, S — степень активности заболевания.
Больным выполняли эхокардиографию («Acuson-Aspen-Siemens», Германия и «HD-11-XE-Philips», Нидерланды), рентгенологическое исследование суставов («Multix-Compact-Siеmens», Германия), сонографию сосудов, опорно-двигательного аппарата и внутренних органов (сканер «Envisor-Philips», Нидерланды), ультразвуковую допплерографию сосудов (ангио–граф «Aplia-XG-Toshiba», Япония), биомикроскопию сосудов конъюнктивы (щелевая лампа «Haag-Streit-Bern-900», Швейцария). Определяли среднее давление в легочной артерии (ЛАД), периферическое и легочное сосудистое сопротивление (соответственно ПСС и ЛСС), интравазальный (ИВИ), общий вазальный (ОВИ) и экстравазальный индексы (ЭВИ), исходный диаметр плечевой артерии (ДИ), степень вазодилатации (ВД), диаметр во время вазодилатации (ДВ) и индекс сосудистого напряжения (ИСН) по формуле: ИСН = ПСС:√ВД . Сосудистый вегетативный индекс (СВИ) оценивали по формуле: СВИ = ВИ × ПСС.
С помощью анализатора «Olympus-AU-640» (Япония) исследовали в сыворотке крови уровни RF, CRP, IgG, IgM и CIC, иммуноферментным методом (ридер «PR2100 Sanofi diagnostic pasteur», Франция) изучали содержание aCCP. Нефробиопсию выполняли на фоне атаралгезии под контролем ультразвукового исследования почки. Использовалась методика True Cut («настоящего среза») с применением высокоскоростного пистолета «Biopty-Bard», а гистологические срезы тканей почек окрашивали гематоксилином и эозином, альциановым синим (на гликопротеиды) и по Ван Гизону (коллагеновые и эластические волокна), ставилась PAS-реакция. Кроме того, использовали иммуноферментный (с пероксидазной меткой) и иммунофлюоресцентный методы исследования тканей почек. Оценивали отложения IgA, IgG, IgM, C3- и Cq1-компонентов комплемента (микроскопы «Olympus-AX40» и «Olympus-AX70-Provis», цифровая видеокамера «Olympus-DP50»). При иммуногистохимическом исследовании с вышеуказанными маркерами изучали 30 полей зрения. Поражение сосудов и других почечных структур (клубочков, канальцев, стромы) оценивали в баллах (от 0 до 3). При этом подсчитывали средний показатель повреждений (J) по формуле: J = (a + 2b + 3c) : (a + b + c + d), где a, b, c — число больных с 1, 2 и 3 баллами соответственно, а d — число больных с отсутствием данного признака.
Статистическая обработка полученных результатов исследований проведена путем компьютерного вариационного, непараметрического, корреляционного, регрессионного, одно- (ANOVA) и многофакторного (ANOVA/MANOVA) дисперсионного анализа (программы «Microsoft Excel» и «Statistica-Stat-Soft», США). Оценивали средние значения (M), их стандартные отклонения (SD) и ошибки, коэффициенты параметрической корреляции Пирсона и непараметрической Кендалла, критерии дисперсии Брауна-Форсайта, Уилкоксона-Рао, множественной регрессии, различий Стьюдента и Макнемара-Фишера, достоверность статистических показателей.
Результаты
У 61,1 % от числа больных РА установлен инте–гральный синдром ангиопатии. Эти пациенты включены в основную группу обследованных, а остальные 38,9 % составили контрольную группу. Однофакторный дисперсионный анализ Брауна — Форсайта и непараметрический корреляционный Кендалла выявили, что ангиопатия при РА прямо связана с висцеральной формой болезни, наличием системного остеопороза и уровнем CRP. В связи с этим можно считать, что показатель в крови CRP > 24 мг/л (> M + SD больных РА с ангиопатией) является прогнознегативным критерием в отношении сосудистой патологии.
По данным критерия Макнемара-Фишера, в основной группе больных была большей активность патологического процесса, но меньшей — степень костно-суставной деструкции (рентгенологической стадийности) РА. Пациенты обеих групп не отличались между собой частотой серопозитивности по RF и аССР. Необходимо отметить, что в случаях наличия ангиопатии в 2,7 раза чаще диагностировали висцеральную форму РА и на 30 % достоверно чаще выявляли остеопороз.
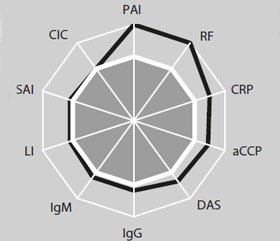
Гломерулонефрит диагностирован у 26,3 % от числа больных, увеит — у 23,8 %, периферическая нейропатия и легочная гипертензия (среднее давление > 15 мм рт.ст.) — соответственно у 21,3 %, поражение кожи — у 20,0 %, синдром Рейно — у 18,8 %, артериальная гипертензия (среднее давление > 115 мм рт.ст.) — у 16,3 %, дигитальный артериит — у 12,5 %, АФЛС — у 8,8 %, дисциркуляторная энцефалопатия — у 6,3 %. Показатель W был равен 12,70 ± 0,46 отн. ед., а среднее количество сосудистых признаков на одного больного — 1,760 ± 0,101 абс. ед. Основная группа больных РА с ангиопатией отличалась от контрольной достоверно большими (на 17 %) показателями DAS, уровнем в крови aCCP (на 22 %), концентрацией CRP (на 25 %), IgG и IgM соответственно (на 9 %) (рис. 1).
/29-1.jpg)
У больных РА основной группы показатели периферического артериального давления (ПАД) составили 104,40 ± 1,28 мм рт.ст., ЛАД — 13,00 ± 0,34 мм рт.ст., ЛАД/ПАД — 12,50 ± 0,34 %, ПСС — 2,40 ± 0,08 дин × с × см–8, ЛСС — 232,90 ± 8,12 дин × с × см–5, ЛСС/ПСС — 10,80 ± 0,53 %, СВИ — 11,70 ± 0,66 отн. ед., ИВИ — 2,10 ± 0,07 балла, ОВИ — 8,20 ± 0,20 балла, ЭВИ — 5,10 ± 0,16 балла, ДИ — 4,30 ± 0,03 мм, ВД — 15,10 ± 0,72 %, ДВ — 5,50 ± 0,04 мм, ИСН — 1,00 ± 0,072 отн.ед. По сравнению с контрольной группой (рис. 2) оказались достоверно большими — на 14 % — значения ЛАД и на 9 % — уровень соотношения ЛАД/ПАД.
Обсуждение
По данным дисперсионного анализа Брауна-Форсайта и непараметрического корреляционного анализа Кендалла, обнаружена связь с содержанием аССР в крови тяжести поражения кожи и периферической нервной системы, с параметрами DAS — развития дигитального артериита, с концентрацией СІС — гломерулонефрита. У 31,3 % от числа больных основной группы обнаружены изменения аорты, у 11,3 % — общих сонных артерий, у 5,0 % — внутренних сонных артерий, на степень сужения которых оказывает дисперсионное влияние тяжесть течения суставного процесса. Показатель ЛАД/ПАД прямо зависит от параметра DAS, СВИ — от содержания в крови CRP, ОВИ — от уровня RF. Значения DSI и W прямо коррелируют между собой, при этом существует достоверное дисперсионное влияние Брауна-Форсайта на уровень W концентраций в крови аССР, IgG и IgM. Имеет место прямая корреляция Пирсона значений W с содержанием в крови аССР. C учетом представленных данных можно считать, что показатель аССР > 40 Е/мл (> M + SD больных с ангиопатией) является фактором риска при РА развития тяжелых сосудистых расстройств.
/30-1.jpg)
Соотношение мезангиопролиферативного и мезангиокапиллярного вариантов ревматоидного гломерулонефрита составило 2 : 1. J клубочков был равен 0,70 ± 0,058 отн. ед., стромы — 1,240 ± 0,067 отн. ед., канальцев — 0,830 ± 0,079 отн. ед., сосудов — 0,430 ± 0,050 отн. ед. В интерстиции, клубочках, канальцах, сосудах отмечалась частота локализации иммунных депозитов, достоверность отличий которой подтвердил непараметрический анализ Макнемара — Фишера. Соотношение отложений IgA, IgG, IgM, C3 и C1q в клубочках составило 8 : 7 : 7 : 3 : 1, в строме — 3 : 3 : 3 : 2 : 1, канальцах — 2 : 3 : 1 : 2 : 1, сосудах — 4 : 4 : 1 : 1 : 1.
По данным многофакторного дисперсионного анализа Уилкоксона — Рао, на морфологические признаки поражений сосудов оказывает влияние серопозитивность болезни по RF. Для оценки влияния отдельных факторов течения РА на те или иные морфологические сосудистые признаки гломеруло–нефрита, мы отобрали параметры, которые одно–временно соответствовали достоверным критериям дисперсионного анализа Брауна — Форсайта и непараметрического корреляционного анализа Кендалла. Оказалось, что от длительности заболевания прямо зависит фибриноидное набухание сосудистой стенки, от стадии РА — гиалиноз артериол, от серопозитивности по аССР — депозиция IgG в сосудах. Показатель J сосудов прямо коррелирует с длительностью заболевания, рентгенологической стадией артрита и наличием тендовагинитов, что демонстрирует анализ Кендалла. Как показывает критерий Брауна — Форсайта, степень лимфогистиоцитарной инфильтрации сосудов оказывает прямое воздействие на параметры ПСС, а с выраженностью депозиции IgM в сосудах обратно соотносится скорость клубочковой фильтрации.
Дополнительно проанализированы взаимоотношения морфологических признаков васкулопатии в почках с общими клинико-инструментальными признаками состояния сосудистой патологии. Так, от показателя ДИ зависит уровень фибриноидного набухания стенок артериол, от ИСН — формирование артериолосклероза, от ВИ — пролиферация сосудистого эндотелия, от СВИ — лимфогистиоцитарная инфильтрация и депозиция IgA.
Выводы
1. Системная ангиопатия наблюдается у 61 % от числа больных РА, чаще в случаях высокой степени активности висцеральной формы с наличием остеопороза.
2. Развитие васкулита кожи и периферической вазонейропатии тесно связано с уровнем в сыворотке крови аССР, который наряду с концентрацией CRP обладает негативной прогностической значимостью в отношении сосудистой патологии, при этом появление дигитального артериита определяется активностью суставного синдрома, гломерулонефрита — высоким содержанием в крови CIC, а наличие ангиопатии отражает повышение давления в малом круге крово–обращения.
3. У больных РА развивается мезангиопролиферативный или мезангиокапиллярный гломерулонефрит в соотношении 2 : 1 с закономерным тубулоинтерстициальным компонентом и сосудистой депозицией IgA, IgG, IgM, C3 и C1q; при этом структурные изменения сосудов почек тесно связаны с клинико-инструментальными проявлениями системной ревматоидной ангиопатии.
4. В будущем будут актуальными своевременная диагностика ангиопатии и дальнейшее прогнозирование ее течения у больных РА для проведения последующих реабилитационных мероприятий, а оценка характера сосудистой патологии может иметь практическую значимость в качестве факторов риска отдельных экстравазальных признаков заболевания.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов, при этом авторы не получали от отдельных лиц и организаций финансовой поддержки исследования, гонораров и других форм вознаграждения.
Информация о вкладе каждого автора
Синяченко О.В. Концепция и дизайн исследования, анализ полученных данных, написание текста.
Егудина Е.Д. Обзор литературы по проблеме, сбор материала, анализ клинико-инструментальных данных исследования.
Ханюков А.А. Обследование больных, анализ морфологических данных исследования нефробио–птатов.
Ермолаева М.В. Клинико-инструментальное обследование больных, статистическая обработка полученных данных, подготовка иллюстраций.
Список литературы
1. Anic B. New classification of vasculitis. Lijec Vjesn. 2014; 136(7-8):226-8.
2. Baerwald C, Kneitz C, Bach M, Licht M. Extra-arti–cular manifestations of rheumatoid arthritis. Z Rheumatol. 2012;71(10):841-9. doi: 10.1007/s00393-011-0928-x.
3. Elshabrawy HA, Chen Z, Volin MV, Ravella S, Virupannavar S, Shahrara S. The pathogenic role of angiogenesis in rheumatoid arthritis. Angiogenesis. 2015;18(4):433-48. doi: 10.1007/s10456-015-9477-2.
4. Haavisto M, Saraste A, Pirilä L, Hannukainen JC, Kalliokoski KK, Kirjavainen A, Kemppainen J, Möttönen T, Knuuti J, Yli-Kerttula T, Roivainen A. Influence of triple disease modifying anti-rheumatic drug therapy on carotid artery inflammation in drug-naive patients with recent onset of rheumatoid arthritis. Rheumatology. 2016;55(10):1777-85. doi: 10.1093/rheumatology/kew240.
5. Heijnen T, Wilmer A, Blockmans D, Henckaerts L. Outcome of patients with systemic diseases admitted to the medical intensive care unit of a tertiary referral hospital: a single-centre retrospective study. Scand J Rheumatol. 2016;45(2):146-50. doi: 10.3109/03009742.2015.1067329.
6. Holle JU. ANCA-associated vasculitis. Internist. 2015;56(1):41-50. doi: 10.1007/s00108-014-3613-8.
7. Kuo CF, Grainge MJ, Valdes AM, See LC, Luo SF, Yu KH, Zhang W, Doherty M. Familial aggregation of systemic lupus erythematosus and coaggregation of autoimmune diseases in affected families. JAMA Intern Med. 2015;175(9):1518-26. doi: 10.1001/jamainternmed.2015.3528.
8. Ramos-Casals M, Brito-Zerón P, Kostov B, Sisó-Almirall A, Bosch X, Buss D, Trilla A, Stone JH, Khamashta MA, Shoenfeld Y. Google-driven search for big data in autoimmune geoepidemiology: analysis of 394,827 patients with systemic autoimmune diseases. Autoimmun Rev. 2015;14(8):670-9. doi: 10.1016/j.autrev.2015.03.008.
9. Sharma A, Dhooria A, Aggarwal A, Rathi M, Chandran V. Connective tissue disorder-associated vasculitis. Curr Rheumatol Rep. 2016;18(6):31-41. doi: 10.1007/s11926-016-0584-x.
10. Yang Z, Ren Y, Liu D, Lin F, Liang Y. Prevalence of systemic autoimmune rheumatic diseases and clinical significance of ANA profile: data from a tertiary hospital in Shanghai, China. APMIS. 2016;124(9):805-11. doi: 10.1111/apm.12564.

/29-1.jpg)
/29-2.jpg)
/30-1.jpg)