Резюме
Актуальність. Остеопороз — відоме пізнє ускладнення травми хребта та спинного мозку (ТХСМ). Актуальність проблеми наростає пропорційно соціальній адаптації пацієнтів з пара- та тетраплегіями. Мета дослідження: вивчення ефективності комбінованої схеми лікування остеопорозу, індукованого ТХСМ. Матеріали та методи. Було обстежено 29 пацієнтів чоловічої статі з ТХСМ (A, В за AIS) із тривалістю посттравматичного періоду не менше від 12 місяців, із них 17 пацієнтів, які отримували комплексне лікування із застосуванням препаратів кальцію, вітаміну D та ібандронової кислоти, становили групу І, а 12 пацієнтів, які з різних причин не отримували призначене лікування, становили групу ІІ. Мінеральну щільність кісткової тканини (МЩКТ) визначали на рівні всього скелета, поперекового відділу хребта та проксимального відділу стегнової кістки двічі (до початку лікування та через 12 місяців) методом двофотонної рентгенівської абсорбціометрії (рентгенівської денситометрії), яку виконували на приладі Prodіgy (GE, 2005). Результати. У пацієнтів групи ІІ, які не отримували лікування, за 12 місяців зареєстровано вірогідне зниження МЩКТ на рівні всього скелета на 3,7 % (1,111 ± 0,023 г/см2 та 1,005 ± 0,031 г/см2 відповідно, p < 0,05), проксимального відділу стегнових кісток — на 11,6 % (0,852 ± 0,018 г/см2 та 0,756 ± 0,023 г/см2 відповідно, p < 0,05) та нижніх кінцівок при проведенні обстеження всього скелета — на 10,2 % (1,193 ± 0,019 г/см2 та 1,061 ± 0,027 г/см2 відповідно, p < 0,05). У результаті проведеного лікування в пацієнтів у групі І зареєстрована стабілізація МЩКТ у регіонах скелета, розташованих нижче від рівня травми, та вірогідне збільшення МЩКТ на рівні поперекового відділу хребта на 5,6 % (1,097 ± 0,022 г/см2 та 1,158 ± 0,019 г/см2 відповідно, p < 0,05). Висновки. Застосування комплексної терапії в пацієнтів з остеопорозом, індукованим ТХСМ, дозволило зменшити втрату МЩКТ нижніх кінцівок та ризик виникнення переломів унаслідок низькоенергетичної травми, що може покращити реабілітаційні можливості та якість життя пацієнтів із ТХСМ. Запропонований метод лікування остеопорозу, індукованого травмою хребта та спинного мозку, є ефективним та безпечним, що дозволяє рекомендувати його для використання в клінічній практиці.
Актуальность. Остеопороз — известное позднее осложнение травмы позвоночника и спинного мозга (ТПСМ). Актуальность проблемы нарастает пропорционально социальной адаптации пациентов с пара- и тетраплегией. Цель исследования: изучение эффективности комбинированной схемы лечения остеопороза, индуцированного ТПСМ. Материалы и методы. Было обследовано 29 пациентов мужского пола с ТПСМ (A, В по AIS) с продолжительностью посттравматического периода не менее 12 месяцев, из них 17 пациентов, получавших комплексное лечение с применением препаратов кальция, витамина D и ибандроновой кислоты, составили группу I, а 12 пациентов, которые по разным причинам не получали назначенное лечение, составили группу II. Минеральную плотность костной ткани (МПКТ) определяли на уровне всего скелета, поясничного отдела позвоночника и проксимального отдела бедренной кости дважды (до начала лечения и через 12 месяцев) методом двухфотонной рентгеновской абсорбциометрии (рентгеновской денситометрии), которую выполняли на аппарате Prodіgy (GE, 2005). Результаты. У пациентов группы І, не получавших лечения, за 12 месяцев зарегистрировано достоверное снижение МПКТ на уровне всего скелета на 3,7 % (1,111 ± 0,023 г/см2 и 1,005 ± 0,031 г/см2 соответственно, p < 0,05), проксимального отдела бедренной кости — на 11,6 % (0,852 ± 0,018 г/см2 и 0,756 ± 0,023 г/см2 соответственно, p < 0,05) и нижних конечностей при проведении обследования всего скелета — на 10,2 % (1,193 ± 0,019 г/см2 и 1,061 ± 0,027 г/см2 соответственно, p < 0,05). В результате проведенного лечения в пациентов группы I зарегистрированы стабилизация МПКТ в регионах скелета, расположенных ниже уровня травмы, и достоверное увеличение МПКТ на уровне поясничного отдела позвоночника на 5,6 % (1,097 ± 0,022 г/см2 и 1,158 ± 0,019 г/см2 соответственно, p < 0,05). Выводы. Применение комплексной терапии у пациентов с остеопорозом, индуцированным ТПСМ, позволило уменьшить потерю МПКТ нижних конечностей и уменьшить риск возникновения переломов вследствие низкоэнергетической травмы, что может улучшить реабилитационные возможности и качество жизни пациентов с ТПСМ. Предложенные методы лечения остеопороза, индуцированного травмой позвоночника и спинного мозга, являются эффективными и безопасными, что позволяет рекомендовать их для использования в клинической практике.
Background. Osteoporosis is a well-known complication of spinal cord injury (SCI). Significance of this problem grows proportionally to the social adaptation of para- and tetraplegic patients. The purpose of the study was to evaluate the effectiveness of the combined treatment for SCI-induced osteoporosis. Materials and methods. Twenty-nine male patients with SCI (AIS A, B) with a duration of post-traumatic period at least 12 months were examined, 17 of whom received comprehensive treatment with calcium, vitamin D and ibandronic acid (group I), and 12 patients, who did not received the prescribed treatment for various reasons (group II). The bone mineral density (BMD) was determined at the total body, lumbar spine and total hip twice (before treatment and 12 months later) by X-ray absorptiometry (X-ray densitometry), which was performed on Prodigy (GE, 2005). Results. It was shown a significant reduction in BMD at the level of total body — by 3.7 % (1.111 ± 0.023 versus 1.005 ± 0.031 g/cm2, respectively; p < 0.05), total hip — by 11.6 % (0.852 ± 0.018 versus 0.756 ± 0.023 g/cm2, respectively; p < 0.05) and lower extremities — by 10.2 % (1.193 ± 0.019 versus 1.061 ± 0.027 g/cm2, respectively; p < 0.05) in patients of group II, who did not receive treatment. BMD in regions of the skeleton located below the level of trauma was stabilized, and BMD at the level of the lumbar spine was significantly increased by 5.6 % (1.097 ± 0.022 versus 1.158 ± 0.019 g/cm2, respectively; p < 0.05) in group I as a result of the treatment. Conclusions. The comprehensive therapy in patients with SCI-induced osteoporosis made it possible to reduce the loss of BMD of the lower extremities and the risk of fractures due to low-energy trauma that can improve the rehabilitation possibilities and quality of life in patients with SCI. The proposed method for treating SCI-induced osteoporosis is effective and safe, which allows it to be recommended for use in clinical practice.
Вступ
Кількість травматичних ушкоджень хребта та спинного мозку зростає з кожним роком. Покращання якості та доступності ранньої хірургічної допомоги зменшує летальність пацієнтів із тяжкими ушкодженнями спинного мозку, а отже, у популяції росте кількість осіб з пара- та тетраплегіями. Збільшення тривалості життя цих хворих призводить до підвищення чисельності пізніх ускладнень травми хребта та спинного мозку (ТХСМ), до яких відносять остеопороз — найбільш поширене метаболічне захворювання скелета, що характеризується зменшенням кісткової маси, порушенням мікроархітектури кістки з подальшим збільшенням її крихкості та збільшенням ризику переломів. Актуальність проблеми наростає пропорційно соціальній адаптації пацієнтів з травмами хребта та спинного мозку.
Після травми хребта та спинного мозку нейронні, судинні, гормональні й механічні порушення призводять до швидкої втрати кісткової маси в усьому скелеті, за винятком черепа. У перший місяць демінералізація кісткової тканини відбувається виключно в ділянках скелета, розташованих нижче від рівня травми та позбавлених осьового навантаження, а саме кістках нижніх кінцівок (НК). Слід зазначити, що ці втрати є нерівномірними. Так, у кістках з однаковим навантаженням демінералізація переважає в ділянках з губчастою кістковою тканиною, тому найбільше уражені дистальний відділ стегнової кістки й проксимальний відділ великогомілкової кістки (кістки нижніх кінцівок навантажуються тільки в положенні стоячи) та кістки таза (частково навантажуються при сидінні). Втрата кісткової маси досягає 52 % на рівні дистального відділу стегнової кістки та 70 % — на рівні проксимального відділу великогомілкової кістки [1]. При цьому на рівні епіфіза втрата становить 50 % для стегнової кістки і 60 % — для великогомілкової кістки, а на рівні діафіза, який складається переважно з кортикальної кістки, — 35 % на рівні стегнової кістки і 25 % — на рівні великогомілкової кістки. Крім того, зареєстровано зменшення товщини кіркового шару на 0,25 мм/рік протягом перших 5–7 років після травми хребта та спинного мозку [2].
Частота переломів у осіб з ТХСМ збільшується зі збільшенням посттравматичного періоду й становить приблизно 1 % на рік у осіб із тривалістю посттравматичного періоду менше від 10 років, і від 3,4 до 4,6 % на рік — у хворих з давниною травми понад 10 років. Поширеність переломів в осіб із ТХСМ сягає близько 40 % [3].
Локалізація переломів відповідає ділянкам скелета з найнижчою мінеральною щільністю кісткової тканини (МЩКТ) — нижня третина стегнової кістки чи верхня третина великогомілкової кістки. Частота переломів нижніх кінцівок у 10 разів вища в пацієнтів з повним пошкодженням спинного мозку, ніж у хворих із частковим пошкодженням. Пацієнти з параплегією мають вищий ризик переломів, ніж хворі з тетраплегією, що зумовлено вищим рівнем фізичних можливостей та більшою мобільністю [4].
Переломи в осіб з ТХСМ супроводжуються високою частотою ускладнень: тривала госпіталізація, формування трофічних виразок, посилення спастичності, уповільнення консолідації, ампутація кінцівки та збільшення смертності [3, 5]. Незважаючи на серйозність проблеми (частота ускладнень при переломах у пацієнтів становить 53–54 %), існує безліч перешкод для діагностики та лікування остеопорозу в пацієнтів із ТХСМ [3, 5].
Нині активно дискутується питання створення діагностичних критеріїв та терапевтичних підходів до остеопорозу, індукованого травмою хребта та спинного мозку. На сьогодні розроблені тільки рекомендації щодо діагностики та лікування остеопорозу для жінок у постменопаузальному періоді та чоловіків, старших від 50 років, а переважна більшість пацієнтів із ТХСМ (близько 75 %) — це молоді чоловіки віком до 30 років.
При тяжкому пошкодженні спинного мозку — ступінь А та В згідно зі шкалою пошкодження спинного мозку, розробленою Американською асоціацією травми спинного мозку (American spinal cord injury association Impairment Scale — AIS) — у гострому періоді травми на перший план виходить надання невідкладної допомоги, а саме забезпечення життєвих функцій пацієнта та усунення компресії спинного мозку (у максимально короткий термін). Ефективні методи допомоги в гострому та ранньому періоді травми призвели до збільшення рівня виживання осіб із тяжкими ТХСМ та зростання тривалості їх життя, що, у свою чергу, призвело до збільшення частоти розвитку пізніх ускладнень ТХСМ, таких як остеопороз, про які раніше повідомлялося вкрай рідко.
На сьогодні втрата кісткової тканини у хворих із ТХСМ розглядається як поліетіологічний стан із недостатньо з’ясованим механізмом розвитку, хоча цю проблему вивчають вже понад 50 років.
Після ТХСМ зміни кісткової тканини розвиваються дуже швидко, а отже, і профілактичні та лікувальні заходи мають розпочатися якомога швидше. Той факт, що на сьогодні не існує засобів, здатних повною мірою відновити кісткову масу, втрачену внаслідок ТХСМ, обґрунтовує необхідність раннього припинення резорбції кісткової тканини. Основним профілактичним засобом є рання активізація пацієнта, включаючи відновлення осьового навантаження, що здатна уповільнити резорбцію та зменшити ступінь втрати кісткової маси. Доведено, що вагонавантажувальні вправи у вертикальному положенні ефективні щодо уповільнення втрати кісткової маси [6]. Крім того, підтримання адекватних рівнів вітаміну D знижує прогресування остеопорозу й може знизити ризик виникнення переломів. У дослідженні W. Bauman та співавт. (2005) показано, що додатковий прийом вітаміну D сприяв стабілізації МЩКТ нижніх кінцівок у пацієнтів зі тетраплегією [7]. На відміну від вищезазначеного, дефіцит вітаміну D може призвести до вторинного гіперпаратиреозу, збільшення ризику падінь, додаткової м’язової слабкості, що значно підвищує ризик переломів [1, 8].
Згідно із сучасними літературними даними, лікування остеопорозу, індукованого травмою хребта та спинного мозку, складається з ранньої активізації пацієнтів, забезпечення достатнього вмісту кальцію в дієті (1000–1500 мг/д) та підтримання цільових рівнів вітаміну D (30–50 нг/мл). Серед остеотропних препаратів застосовують бісфосфонати, як найбільш вивчені. Ці засоби досліджуються в пацієнтів з ТХСМ з 1981 року, але, не зважаючи на це, їх роль у підтриманні МЩКТ після ТХСМ залишається суперечливою [9]. Неоднозначні результати при вивченні ефективності бісфосфонатів обумовлені різними дозами, шляхами та періодичністю введення препаратів, неоднорідністю пацієнтів, які беруть участь у дослідженні, та методологією дослідження [9].
Незважаючи на досягнення в оцінці стану кісткової тканини, остеопороз у пацієнтів із ТХСМ діагностується тільки після виникнення перелому, крім того, навіть наявність перелому не завжди ініціює діагностику стану МЩКТ та призначення остеотропної терапії. Складність проблеми зумовлена багатьма чинниками, але основний, на нашу думку, — це відсутність критеріїв діагностики та терапії остеопорозу, індукованого ТХСМ. На сьогодні не існує міжнародних рекомендацій щодо ведення таких пацієнтів, що могли б стати основою для створення їх української версії.
У рамках співпраці Української асоціації остеопорозу та Української асоціації інвалідів-спінальників було проведено обстеження пацієнтів з ТХСМ з метою вивчення ефективності комбінованої схеми лікування остеопорозу, індукованого ТХСМ.
Матеріали та методи
У відділі клінічної фізіології та патології опорно-рухового апарату ДУ «Інститут геронтології імені Д.Ф. Чеботарьова НАМН України» було обстежено 29 пацієнтів чоловічої статі з остеопорозом, індукованим ТХСМ.
Критерії включення:
1) пацієнти з ТХСМ з пошкодженням спинного мозку на рівні шийного, грудного та поперекового відділу хребта (ПВХ) з нижньою параплегією або глибоким нижнім парапарезом, що виключає можливість стояння та ходьби (ступінь пошкодження спинного мозку за AIS — A, B);
2) тривалість посттравматичного періоду не менше від 12 місяців.
Критерії виключення:
1) наявність ендокринних розладів, що б могли впливати на кальцієвий обмін або потребували б спеціальної терапії (цукровий діабет, гіпотиреоз), прийом глюкокортикостероїдів та антиконвульсантів;
2) наявність масивних осифікатів у ділянці кульшових суглобів, що не дозволяють адекватно оцінити стан кісткової тканини;
3) наявність супутніх масивних травм кістково-м’язової системи під час отримання травми хребта та спинного мозку.
Усі пацієнти користувались інвалідним візком і перебували в вертикальному положенні 30–60 хв на добу 5–7 разів на тиждень у рамках занять лікувальною фізкультурою.
Пацієнтам із ТХСМ діагноз «остеопороз, індукований ТХСМ» встановлювали на підставі визначення мінеральної щільності кісткової тканини на рівні шийки та/або проксимального відділу стегнової кістки (ПВСК) методом двофотонної рентгенівської абсорбціометрії. Інтерпретацію даних рентгенівської денситометрії проводили згідно з рекомендаціями Міжнародного товариства клінічної денситометрії (International society for clinical densitometry) для молодих дорослих осіб за Z-показником (відмінність МЩКТ пацієнта від показника умовно здорових дорослих осіб того ж віку відображена в середньоквадратичних відхиленнях (SD)). Значення Z-показника > –2 SD вважали таким, що перебуває в межах вікової норми, значення Z-показника < –2 SD вважали нижчим від референтних значень для відповідного віку, а МЩКТ оцінювалась як низька. Згідно з рекомендаціями National Osteoporosis Foundation від 2014 року, ТХСМ належить до захворювань та станів, що сприяють розвитку остеопорозу та переломів, а отже, пацієнтам із ТХСМ та низькою МЩКТ може бути встановлений діагноз «остеопороз, індукований травмою спинного мозку».
Усім пацієнтам із діагнозом «остеопороз, індукований ТХСМ» було призначене лікування, що включало:
1. Збільшення осьового навантаження на нижні кінцівки. Перебування у вертикальній позі не менше від 40 хв на добу.
2. Прийом комплексних препаратів кальцію та вітаміну D3 з розрахунку: кальцій 1000 мг/добу + вітамін D3 800 МО/добу в складі комплексного препарату тривалістю 12 місяців.
3. Додатковий прийом вітаміну D при рівні загального вітаміну D у сироватці крові менше від цільового — 30 нг/мл.
Корекцію рівня вітаміну D проводили за формулою, запропонованою відділом клінічної фізіології та патології опорно-рухового апарату ДУ «Інститут геронтології імені Д.Ф. Чеботарьова НАМН України». Для досягнення цільового рівня призначали насичуючу дозу вітаміну D 3000 МО на період, який визначали за формулою [10]:
n = (100 –РВD) х МТ/100,
де n — тривалість курсу терапії насичення, дні; РВD — рівень 25(ОН)D у сироватці крові, нг/мл; МТ — маса тіла, кг.
4. Ібандронова кислота в дозі 3 мг внутрішньовенно струминно 1 раз у 3 місяці протягом 12 місяців. Вибір препарату був обумовлений не тільки фармакологічними властивостями препарату, а й клінікою ТХСМ. У пацієнтів із травмою хребта та спинного мозку тяжкого ступеня (A, B за AIS) обмежене застосування пер–оральних бісфосфонатів у зв’язку з особливостями прийому препаратів, зокрема необхідністю перебувати у вертикальному положенні 30–40 хвилин після прийому препарату. Крім того, порушення функції кишечника, як симптом ураження нервової системи, при ТХСМ також може впливати на абсорбцію препарату. Тому препаратами вибору для цієї категорії хворих є парентеральні бісфосфонати. Вибір ібандронової кислоти був обумовлений літературними даними щодо її позитивного впливу на товщину кортикального шару стегнової кістки в осіб із низькою МЩКТ [11].
5. Для оцінки ефективності терапії остеопорозу серед цих хворих було обрано 29 пацієнтів із ТХСМ — AIS A з тривалістю посттравматичного періоду не менше від 12 місяців, із них 17 пацієнтів, які отримували лікування згідно з наведеною схемою, увійшли в групу І, а 12 пацієнтів, які з різних причин не отримували призначене лікування, становили групу ІІ.
Методи дослідження:
1. Визначення ступеня пошкодження спинного мозку згідно з AIS.
2. Визначення МЩКТ на рівні всього скелета (ВС), поперекового відділу хребта та проксимального відділу стегнової кістки двічі (до початку лікування та через 12 місяців) методом двофотонної рентгенівської абсорбціометрії (рентгенівської денситометрії), яку виконували на приладі Prodіgy (GE, 2005).
3. Статистичні методи обробки отриманих результатів: критерій Стьюдента для пов’язаних та непов’язаних вибірок. Результати подані у вигляді M ± m.
Результати
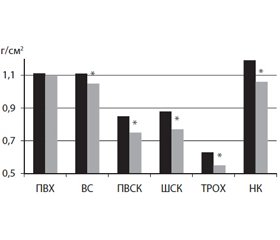
У пацієнтів групи ІІ, які не отримували лікування, за 12 місяців зареєстровано вірогідне зниження МЩКТ на рівні всього скелета (ВС) — 1,111 ± 0,023 г/см2 та 1,005 ± 0,031 г/см2 відповідно, p < 0,05, проксимального відділу стегнових кісток — 0,852 ± 0,018 г/см2 та 0,756 ± 0,023 г/см2 відповідно, p < 0,05, та нижніх кінцівок — 1,193 ± 0,019 г/см2 та 1,061 ± 0,027 г/см2 відповідно, p < 0,05 (рис. 1).
У результаті проведеного лікування в пацієнтів групи І зареєстрована стабілізація МЩКТ у регіонах скелета, розташованих нижче від рівня травми, та вірогідне збільшення МЩКТ на рівні поперекового відділу хребта — 1,097 ± 0,022 г/см2 та 1,158 ± 0,019 г/см2 відповідно, p < 0,05 (рис. 2).
Запропонована терапія приводила до вірогідного зменшення втрати кісткової маси на рівні нижніх кінцівок, проксимального відділу стегнової кістки та всього скелета порівняно з пацієнтами групи ІІ (рис. 3). У пацієнтів групи ІІ втрата кісткової маси становила на рівні всього скелета 3,7 ± 0,3 %, на рівні проксимального відділу стегнових кісток — 11,6 ± 1,7 % та на рівні НК — 10,2 ±1,5 %. У результаті проведеного лікування в пацієнтів групи І зареєстроване вірогідне збільшення МЩКТ на рівні поперекового відділу хребта на 5,6 ± 2,1 % (p < 0,05) та стабілізація МЩКТ у регіонах скелета, розташованих нижче від рівня травми (рис. 3).
/28-1.jpg)
Зважаючи на те, що формування остеопорозу в пацієнтів із ТХСМ обумовлене інтенсивною резорбцією кісткової тканини в перші роки після травми, метою терапії в першу чергу є зменшення втрати кісткової маси нижніх кінцівок, чого і вдалося досягти в результаті лікування. Приріст кісткової тканини на рівні нижніх кінцівок у пацієнтів із параплегією можливий лише за умови збільшення навантаження, зокрема часу перебування у вертикальному положенні з опорою на нижні кінцівки.
Під час прийому комплексних препаратів кальцію та вітаміну D не було зареєстровано будь-яких побічних ефектів. При контрольному визначенні рівня кальцію та вітаміну D у сироватці крові не було зареєстровано відхилень від нормативних значень.
Після введення першої ін’єкції ібандронової кислоти в усіх пацієнтів спостерігалась грипоподібна реакція — стан, що проявлявся відчуттям ломоти в тілі, підвищенням температури тіла до фебрильних цифр, болем у кістках, відчуттям загальної слабкості. З метою зменшення тяжкості побічного ефекту пацієнти отримували парацетамол у дозі 500–2000 мг/добу (1–4 таблетки по 500 мг) залежно від стану. Першу таблетку випивали всі пацієнти за 30 хв до ін’єкції, наступні таблетки — при посиленні больового синдрому або підвищенні температури тіла. У всіх пацієнтів нормалізація стану настала через 24–36 годин після ін’єкції без додаткових засобів лікування. Жодному пацієнту не була відмінена терапія в зв’язку з розвитком побічного ефекту. Кожна наступна ін’єкція ібандронової кислоти переносилась краще за попередню, проте підвищення температури тіла та загальна слабкість реєструвались після кожного введення препарату. Інших побічних ефектів зареєстровано не було.
Обговорення
Втрата кісткової маси після ТХСМ із повним поперечним пошкодженням спинного мозку унікальна. Швидкість втрати кісткової маси досягає 1 % на тиждень протягом перших кількох місяців. У подальшому (через 12 місяців) вона уповільнюється, але залишається високою ще принаймні протягом наступних 3–8 років [1]. Швидкість втрати кісткової маси у пацієнтів з ТХСМ істотно більша, ніж та, що спостерігається при інших типах іммобілізації, не пов’язаних із паралічем м’язів (тобто відсутність гравітації (0,25 % на тиждень) або постільний режим (0,1 % на тиждень)), або в жінок у постменопаузальному періоді, які не приймають антирезорбенти (3–5 % на рік) [1].
Застосування інгібіторів резорбції кісткової тканини бісфосфонати вважалося найбільш доцільною терапією для пацієнтів з ТХСМ протягом декількох десятиліть. Результати численних досліджень, проведених у цій групі пацієнтів, показують зниження гіперкальціємії та втрати кісткової маси при початку лікування в період 12 місяців після пошкодження. Проте інші дослідження показали обмежену ефективність бісфосфонатів щодо МЩКТ нижніх кінцівок [6]. Досліджень з вивчення ефективності застосування ібандронової кислоти в цієї категорії пацієнтів у літературі не було знайдено, але застосування інших бісфосфонатів (алендронової, золендронової кислоти) призводило до підвищення МЩКТ на рівні поперекового відділу хребта та стабілізації на рівні стегнової кістки [6, 9]. Незважаючи на тривале вивчення проблеми, питання корекції втрати кісткової маси після ТХСМ залишається відкритим. В огляді 2017 року, присвяченому лікуванню та профілактиці остеопорозу в пацієнтів з ТХСМ, на підставі аналізу 16 рандомізованих досліджень із включенням 368 пацієнтів не знайдено доказів достатньої сили для створення рекомендацій [12].
Результати нашого дослідження показують, що в пацієнтів з остеопорозом, індукованим ТХСМ, і через рік після травми продовжується втрата кісткової маси, вона становить на рівні проксимального відділу стегнових кісток 11,6 % та рівні нижніх кінцівок — 10,2 % за 12 місяців. Застосування препаратів кальцію, вітаміну D та ібандронової кислоти ефективно пригнічує резорбцію кісткової тканини й призводить до стабілізація МЩКТ нижніх кінцівок. Отримані результати схожі з результатами застосування інших бісфосфонатів, зокрема алендронової [9] та золендронової кислоти [13].
Висновки
Отже, застосування комплексної терапії в пацієнтів з остеопорозом, індукованим ТХСМ, дозволило зменшити втрату МЩКТ нижніх кінцівок та ризик виникнення переломів унаслідок низькоенергетичної травми, що може покращити реабілітаційні можливості та якість життя пацієнтів із ТХСМ. Запропонований метод лікування остеопорозу, індукованого травмою хребта та спинного мозку, є ефективним та безпечним, що дозволяє рекомендувати його для використання в клінічній практиці.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Bauman W, Cardozo C. Osteoporosis in individuals with spinal cord injury. PM R. 2015; 7(2):188-201.
2. Eser P, Frotzler A, Zehnder Y, et al. Relationship between the duration of paralysis and bone structure: A pQCT study of spinal cord injured individuals. Bone. 2004;34:869-880.
3. Troy KL, Morse LR. Measurement of bone: diagnosis of SCI-induced osteoporosis and fracture risk prediction. Top Spinal Cord Inj Rehabil. 2015;21(4):267-274. doi:10.1310/sci2104-267.
4. Carbone L, Chin AS, Lee TA, et al. The association of anticonvulsant use with fractures in spinal cord injury. Am J Phys Med Rehabil. 2013; 92:1037-1046.
5. Morse LR, Battaglino RA, Stolzmann K, et al. Osteoporotic fractures and hospitalization risk in chronic spinal cord injury. Osteoporos Int. 2009;20:385-392.
6. Charmetant C, Phaner V, Condemine A, Calmels P. Diagnosis and treatment of osteoporosis in spinal cord injury patients: a literature review. Ann Phys Rehabil Med. 2010;53:655-668. doi:10.1016/j.rehab.2010.10.001.
7. Bauman W, Spungen A, Morrison N, Zhang R, Schwartz E. Effect of a vitamin D analog on leg bone mineral density in patients with chronic spinal cord injury. J Rehabil Res. 2005;42(5):625-634.
8. Battaglino R., Lazzari A., Garshick E., Morse L. Spinal cord injury-induced osteoporosis: pathogenesis and emerging therapies. Curr Osteoporos Rep. 2012;10(4): 278-285.
9. Chang K, Hung C, Chen W, Lai M, Chien K, Han D. Effectiveness of bisphosphonate analogues and functional electrical stimulation on attenuating post-injury osteoporosis in spinal cord injury patients — a systematic review and meta-analysis. PLoS One. 2013; 8(11). https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3838359/.
10. Patent Ukrainy 112357 MPK51A61K31/592 (2006.01). Sposib indyvidualnoi tsilovoi terapii defitsytu vitaminu D u patsiientiv iz zakhvoriuvanniamy kistkovo-miazovoi systemy / Povorozniuk VV, Balatska NI, Dzerovych NI, Muts VYa, Synenkyi OV: zaiavl. 12.12.2014; opublik. 25.08.2016, Biul. № 16. 4 s.
11. Genant H, Lewiecki E, Fuerst T, Fries M. Effect of monthly ibandronate on hip structural geometry in men with low bone density. Osteoporos Int. 2012 Jan; 23(1): 257-65. doi: 10.1007/s00198-011-1732-9.
12. Soleyman-Jahi S, Yousefian A, Maheronnaghsh R, et al. Evidence-based prevention and treatment of osteoporosis after spinal cord injury: a systematic review. Eur Spine J. 2017;May 11. doi: 10.1007/s00586-017-5114-7.
13. Varghese SM, Chandy BR, Thomas R, Tharion G. Effect of zoledronic acid on osteoporosis after chronic spinal cord injury: a randomized controlled trial. Critical Reviews™ in Physical and Rehabilitation Medicine. 2016;28(1–2):85-93. doi: 10.1615/CritRevPhysRehabilMed.2016018768.

/27-1.jpg)
/28-1.jpg)