Журнал «Боль. Суставы. Позвоночник» Том 9, №1, 2019
Вернуться к номеру
Фастум® гель и Лиотон® 1000 гель в комплексном лечении гонартроза
Авторы: Рушай А.К., Климовицкий В.Г., Богданова Л.В., Богданова К.И.
Научно-исследовательский институт травматологии и ортопедии Донецкого национального медицинского университета, г. Лиман, Украина
Рубрики: Ревматология, Травматология и ортопедия
Разделы: Справочник специалиста
Версия для печати
Узагальнено досвід лікування 60 хворих на остеоартроз колінного суглоба (гонартроз). Визначена висока ефективність консервативного лікування гонартрозу з застосуванням фонофорезу препаратів Фастум® гель і Ліотон® 1000 гель. Динаміка больового синдрому, термоасиметрії та сумарного індексу опитувальника КООS свідчила про тривалий позитивний ефект. Проведення процедур було безпечним, побічних явищ виявлено не було.
Обобщен опыт лечения 60 больных с остеоартрозом коленного сустава (гонартрозом). Определена высокая эффективность консервативного лечения гонартроза с применением фонофореза препаратов Фастум® гель и Лиотон® 1000 гель. Динамика болевого синдрома, термоасимметрии и суммарного индекса опросника КООS свидетельствовала о длительном положительном эффекте. Проведение процедур было безопасным, побочных явлений выявлено не было.
The experience of treating 60 patients with osteoarthrosis of the knee joint (gonarthrosis) was summarized. The high efficiency of conservative treatment for gonarthrosis with the use of Fastum® gel and Lioton® 1000 gel phonophoresis has been determined. The dynamics of pain syndrome, thermal asymmetry, and the overall Knee injury and Osteoarthritis Outcome Score indicates a long-lasting positive effect. The procedures were safe, no side effects were detected.
гонартроз; фонофорез; Фастум® гель; Ліотон® 1000 гель
гонартроз; фонофорез; Фастум® гель; Лиотон® 1000 гель
gonarthrosis; phonophoresis; Fastum® gel; Lioton® 1000 gel
Введение
Значительная распространенность гонартроза, прогрессирующее течение, частые обострения, постоянный болевой синдром, существенное нарушение двигательной активности резко снижают качество жизни пациентов.
Комплексная консервативная терапия не ведет к выздоровлению, однако позволяет затормозить прогрессирование процесса, снять острые явления при обострении.
Длительное энтеральное систематическое применение нестероидных противовоспалительных препаратов (НПВП), которые составляют основу противовоспалительного и обезболивающего лечения, не лишено побочных эффектов. Они оказывают нежелательное воздействие на желудочно-кишечный тракт (диспепсии, эрозии, язвы, кровотечения); со стороны почек происходит уменьшение экскреции натрия, реагирует интерстиций; нарушается микроциркуляция и агрегация тромбоцитов; может развиться бронхоспазм [2, 3].
Коленный сустав имеет сложное анатомическое и биомеханическое строение, подвергается значительным постоянным функциональным нагрузкам, частой травматизации. При реактивных процессах коленный сустав реагирует чаще, чем другие суставы.
При гонартрозе в патологический процесс вовлекаются все структуры сустава — хрящ, субхондральные участки кости, связки, суставная капсула, синовиальные оболочки [1]. Поэтому медикаментозная направленность консервативного лечения должна быть нацелена не только на воспалительные процессы в хряще, но и на другие структуры сустава.
НПВП назначаются чаще всего перорально. Осложнения такого лечения стимулировали поиски более безопасных средств и путей введения. Однако оказалось, что использование селективных безопас–ных форм не превосходит традиционные неселективные НПВП по своей противовоспалительной активности, хотя и обеспечивает большую безопас–ность применения. Эти свойства резко ограничивают их эффективность при лечении обострений.
Обоснованным и широко распространенным является комплексное патогенетически обоснованное использование препаратов и методов, разных по механизму действия, влияющих на различные звенья воспалительного процесса. Так, использование топикальных средств в сочетании с ультразвуком не только создает высокие местные концентрации действующих веществ в структурах пораженного сустава, но и оказывает потенцирующий эффект за счет собственного противовоспалительного действия ультразвука. Такой мультимодальный подход является, на наш взгляд, перспективным направлением консервативного лечения гонартроза.
Цель: повысить эффективность консервативного лечения гонартроза с помощью фонофореза препаратов Фастум® гель и Лиотон® 1000 гель.
Задачи:
— выяснить обоснованность и безопасность применения фонофореза препаратов Фастум® гель и Лиотон® 1000 гель в лечении гонартроза;
— определить эффективность предложенной методики.
Материалы и методы
Под нашим наблюдением находилось 60 больных с остеоартрозом коленного сустава (гонартрозом). Преобладали женщины 45–65 лет (43–71,67 %). Проводилась рентгенография коленного сустава в двух стандартных проекциях и определялась стадия дегенеративного процесса. Производилась периартикулярная термография в динамике. Базовая терапия (пероральный прием диклофенака в течение 5 суток) дополнялась фонофорезом с препаратами Фастум® гель (А. Менарини Мануфактуринг Логистикс энд Сервисес С.р.Л.) и Лиотон® 1000 гель (А. Менарини Мануфактуринг Логистикс энд Сервисес С.р.Л.).
Основное действующее вещество препарата Фастум® гель — кетопрофен (НПВП); вспомогательные вещества — карбомер, этанол 96%, масло неролиевое, масло лавандиновое, триэтаноламин. Механизм действия препарата связан с ингибированием синтеза простагландинов. Гель обладает анальгезирующим и противовоcпалительным действием. Кетопрофен, проникая через кожу, достигает очага воспаления, обеспечивая, таким образом, возможность местного лечения поражений (суставов, сухожилий, связок и мышц), сопровождающихся болевым синдромом. Формула препарата обеспечивает его преимущества при местном применении по сравнению с другими НПВП [4, 5, 7].
Всасывание кетопрофена из очага происходит крайне медленно, он практически не кумулируется в организме.
Основным действующим веществом препарата Лиотон® 1000 гель является гепарина натриевая соль (антикоагулянтное средство прямого действия для местного применения). Вспомогательные вещества: этанол 96%, карбомер 940, триэтаноламин, метилпарабен, пропилпарабен, неролиевое масло, лавандовое масло.
Гепарин — антикоагулянт прямого действия, относится к группе среднемолекулярных гепаринов. Препятствует тромбообразованию, угнетает активность гиалуронидазы, активирует фибринолитические свойства крови.
При наружном применении оказывает местное антитромботическое, противоотечное и противовоспалительное действие, улучшает микроциркуляцию крови и активирует тканевый обмен, вследствие чего ускоряются процессы рассасывания гематом, предотвращается образование микротромбов, уменьшается отечность тканей.
При наружном применении в системный кровоток проникает незначительное количество гепарина, не оказывая системного действия, не вызывая каких-либо изменений параметров свертывания крови.
При местном лечении воспалительных заболеваний суставов используются мазевые, кремовые формы противовоспалительных препаратов. Наиболее удачной формой мы считаем гель. Его применение более гигиенично, чем применение мазей; спиртовые растворители обеспечивают быстрое впитывание лекарственного средства в кожу и максимальное прохождение препарата через кожный барьер, что создает его высокую концентрацию в очаге. Кроме того, в состав гелей (и Фастум® гель, и Лиотон® 1000 гель) входят вещества, обеспечивающие проведение действующего вещества через дерму и подлежащие ткани. Используемый в гелях триэтаноламин является наиболее безопасным [2–4].
Современные представления о патогенезе воспалительного процесса показывают его многокомпонентность; ведущая роль в нем отводится простагландиновому и лейкотриеновому факторам, провоспалительным цитокинам, активации экспрессии молекул адгезии эндотелиальными клетками и трансмиграции лейкоцитов в ткани с последующим усилением воспалительного процесса, фактору агрегации тромбоцитов, комплементу, оксиду азота (NO).
Поэтому использование в лечении и реабилитации предложенных препаратов является обоснованным; их воздействие следует рассматривать как потенцирующее, влияющее на основные факторы воспалительного процесса.
С учетом высокой уязвимости костной ткани к микроциркуляторным и гемодинамическим нарушениям, сопровождающим воспалительный синдром, очень важным является улучшение реологических свойств крови, а также обеспечение относительного преобладания ее антисвертывающей и фибринолитической активности в области поражения.
Ультразвук обладает хорошим восстановительным эффектом. В основе его действия лежит влияние механических колебаний, которые обеспечивают микромассаж клеток и тканей, рефлекторное расширение сосудов, усиление кровотока на микроциркуляторном уровне, повышение интенсивности и качества биохимических процессов. Усиление проницаемости клеточных мембран, активация процессов диффузии и адсорбции ведут к значительному улучшению лимфо- и кровотока, ускорению репарации и регенерации. Лечебные свойства ультразвука могут быть значительно усилены добавлением медицинских гелей с активными веществами. Гелевые формы являются наиболее сочетаемыми с ультразвуком.
Процедура фонофореза проводилась следующим образом. Препараты Фастум® гель и Лиотон® 1000 гель наносились на область коленного сустава двумя параллельными полосками длиной 5–10 см. Затем зигзагообразными движениями пальцев смешивали гели, смесь равномерно распределялась по области воздействия (передняя и боковые поверх–ности коленного сустава) волновода ультразвукового аппарата (рис. 1). Режим аппарата ультразвука был непрерывный, плотность излучения — от 0,7 до 1,0 Вт/см2, по 5–10 минут ежедневно. Курс лечения составлял 10 сеансов. Кроме того, в домашних условиях препараты наносились еще 2 раза в день.
Для определения эффективности выбранного лечения использовались объективные и субъективные методы исследования. К объективным методам относились: наличие локальной реакции на проводимое лечение и ее выраженность, данные тепло–графии (термоасимметрия DТ), определение боли по визуально-аналоговой шкале (ВАШ).
Оценка функции коленного сустава производилась по шкале исхода травмы и остеоартроза коленного сустава (Knee Injury and Osteoarthritis Outcome Score — KOOS), динамика болевого синдрома — по ВАШ до, во время и после окончания курса лечения.
Шкала KOOS [6] разработана как инструмент для оценки мнения пациента о своем коленном суставе и связанных с этим суставом проблемах. Шкала предназначена для использования как при травмах коленного сустава, результатом которых может быть развитие посттравматического остеоартрита, так и для оценки изменения состояния пациентов в течение нескольких недель при проведении различных видов лечения (медикаментозного, оперативного, кинезотерапии), или в течение нескольких лет с момента получения травмы, или при развитии посттравматического остеоартрита. Она может быть повторно использована через короткие или длительные временные промежутки для оценки состояния как отдельных пациентов, так и групп больных.
KOOS состоит из 5 подшкал (боль; другие жалобы-симптомы; ADL; функция ноги во время спорта и отдыха; качество жизни, связанное с коленным суставом). При ответах на вопросы учитывалась оценка состояния пациента за последнюю неделю. На каждый вопрос предлагались 4 варианта ответов, которые оценивались в баллах от 0 до 4 (нет — 0, незначительно — 1, умеренно — 2, сильно — 3, чрезмерно — 4). Для каждой подшкалы подсчитывалась сумма баллов. Затем производился пересчет баллов по специальным формулам, что позволяло по каждой подшкале получить балльную оценку от 100 до 0. При этом 100 баллов соответствовали отсутствию симптомов, а 0 баллов показывал, что симптомы резко выражены. По результатам анкетирования выстраивался так называемый профиль исхода.
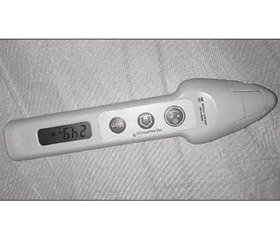
Измерение местной температуры Т производилось инфракрасным бесконтактным термометром Termofocus 01500A3 (рис. 2). Наиболее информативным был градиент температур коленных суставов (DТ).
Оценка субъективного и объективного статуса пациентов проводилась до старта терапии, через 10, 20 и 30 дней от начала лечения.
Результаты и обсуждение
В результате проведенной терапии удалось достичь клинически значимого улучшения у всех наблюдаемых пациентов. Выраженность болевого синдрома по ВАШ к 10-м суткам лечения значительно снижалась — с 4,9 ± 0,7 до 2,8 ± 0,8 (рис. 3).
Достаточно информативна была и динамика термоасимметрии DТ: исходный уровень, во время лечения и после его окончания — 3,1 ± 0,4 до начала лечения, 2,0 ± 0,5 через 10 суток и 2,4 ± 0,5 через 20 (рис. 4).
Перед началом лечения суммарный индекс шкалы КООS составлял 67,2 ± 9,1; на 10-е сутки он вырос до 84,4 ± 11,2. Свое состояние больные характеризовали как значительное уменьшение болей (особенно ночных), возможность бытового самообслуживания, комфортный отдых и передвижение на небольшие расстояния. На 20-е сутки после начала лечения индекс возрос до 87,4 ± 10,4, что соответствовало уменьшению патологических симптомов, умеренным болям при движении в коленном суставе, появлялась возможность полноценно заниматься трудовой деятельностью. На 30-е сутки индекс составлял 75,8 ± 12,7, что свидетельствовало о достаточно длительном лечебном эффекте (рис. 5).
Все больные хорошо переносили фонофорез препаратов Фастум® гель и Лиотон® 1000 гель. Неприятных ощущений, местных кожных, а тем более общих реакций не было.
Таким образом, была продемонстрирована высокая эффективность проводимой терапии. Динамика термоасимметрии DТ свидетельствовала о нормализации нарушений Т, кровообращения и острых явлений воспаления в области пораженного коленного сустава.
Данные опросника КООS (динамика суммарного индекса) свидетельствовали о выраженном положительном эффекте начиная с 10-х суток после начала лечения, а также о длительности достигнутого результата (на 30-е сутки он составил 75,8 ± 12,7). Была установлена хорошая переносимость фонофореза препаратов Фастум® гель и Лиотон® 1000 гель пациентами с гонартрозом.
Выводы
Использование препаратов Фастум® гель и Лиотон® 1000 гель при проведении фонофореза у больных гонартрозом было патогенетически обоснованным.
Динамика болевого синдрома, термоасимметрии и суммарного индекса опросника КООS свидетельствовала о длительном положительном эффекте.
Проведение процедур было безопасным, побочных явлений выявлено не было.
Конфликт интересов. Не заявлен.
1. Худобин В.Ю. Оптимизация топикальной терапии пациентов с остеоартрозом коленного сустава / Худобин В.Ю., Солоницин Е.А., Боровой И.С. // Травма. — 2013. — Т. 14, № 4. — С. 41-44.
2. Физиотерапевтическая реабилитация больных с поражениями голени и голеностопного сустава с использованием препаратов Фастум® гель и Лиотон® гель / Рушай А.К., Климовицкий В.Г., Богданова Л.В., Чучварев Р.В., Валюшко Т.В. // Травма. — 2015. — Т. 16, № 1. — С. 45-49.
3. American College of Rheumatology 2012 Re–commendations for the Use of Nonpharmacologic and Pharmacologic Therapies in Osteoarthritis of the Hand, Hip, and Knee // Arthritis Care & Research. — 2012. — Vol. 64, № 4. — Р. 465-474. doi: 10.1002/acr.21596.
4. Effect of Phonophoresis on Skin Permeation of Commercial Anti-inflammatory Gels: Sodium Diclo–fenac and Ketoprofen / Souza J., Meira A., Volpato N.M., Mayorga Р., Gottfried С. // Ultrasound in Med. & Biol. — 2013. — Vol. 39, № 9. — Р. 1623-1630. doi: https://doi.org/10.1016/j.ultrasmedbio.2013.02.009.
5. Phonophoresis Versus Topical Application of Ketoprofen: Comparison Between Tissue and Plasma Levels / Cagnie В., Vinck Е., Rimbaut S., Vanderstraeten G. // J. Physical. Therapy. — 2003. — Vol. 83, № 8. — Р. 707-712.
6. Roos Е.М. Knee injury and Osteoarthritis Outcomes Score (KOOS)-development of a self administered outcome measure / E.M. Roos, H.P. Roos, L.S. Lohmander // The Journal of Orthopaedic and Sports Physical Therapy. — 1998. — Vol. 78, № 2. — P. 88-96.
7. Topical NSAIDs for osteoarthritic pain. Consensus recommendations for managing osteoarthritic pain with topical NSAIDs in Asia-Pacific // J. Pain Manag. — 2017. — Р. 14-28.

/59-1.jpg)
/60-1.jpg)
/60-2.jpg)