Международный эндокринологический журнал Том 15, №3, 2019
Вернуться к номеру
Ефективність застосування Нейромідину® в комплексному лікуванні діабетичної дистальної симетричної полінейропатії
Авторы: Пашковська Н.В., Пашковський В.М., Зорій І.А.
Вищий державний навчальний заклад України «Буковинський державний медичний університет», м. Чернівці, Україна
Рубрики: Эндокринология
Разделы: Справочник специалиста
Версия для печати
Мета: встановлення ефективності й безпеки застосування препарату іпідакрину (Нейромідин®) у хворих на цукровий діабет, ускладнений дистальною симетричною полінейропатією (ДСПН). Матеріали та методи. Обстежено 110 хворих на ДСПН. Відібрані пацієнти були поділені на дві групи: І група (24 хворі) — особи, які отримували базисну терапію; ІІ група (50 хворих) — пацієнти, які на тлі базисного лікування отримували препарат Нейромідин® у вигляді внутрішньом’язових ін’єкцій по 5 мг двічі на добу протягом 10 днів, потім перорально по 20 мг тричі на добу впродовж 20 днів. Проводилося неврологічне обстеження за шкалами нейропатичного симптоматичного підрахунку, модифікованого нейропатичного дисфункціонального підрахунку, електронейроміографічне (ЕНМГ) тестування периферичних нервів нижніх кінцівок. З метою встановлення особливостей когнітивних функцій використовували тест Mini-Mental State Examination. Також оцінювали показники тривожності й депресії в динаміці лікування. Результати. У групі осіб, які на тлі базисної терапії отримували Нейромідин®, відзначалося вірогідне покращення показників суб’єктивної й об’єктивної симптоматики. Прояви аксонопатії й мієлінопатії за результатами ЕНМГ-тестування периферичних нервів вірогідно зменшувались у групі пацієнтів, які приймали на тлі базисної терапії Нейромідин®. Також на тлі прийому Нейромідину® встановлено статистично значуще покращання когнітивних функцій, зменшення проявів тривоги й депресії. Висновки. Застосування Нейромідину® на тлі базисної терапії у хворих на ДСПН покращує процеси регенерації й реіннервації периферичних нервів нижніх кінцівок і, покращуючи проведення збудження моторними волокнами за даними ЕНМГ-параметрів, позитивно впливає на клінічній перебіг захворювання, а також дозволяє покращити когнітивні функції, зменшити прояви тривоги й депресії.
Цель: определение эффективности и безопасности применения препарата ипидакрина (Нейромидин®) у больных сахарным диабетом, осложненным дистальной симметричной полинейропатией (ДСПН). Материалы и методы. Обследовано 110 больных с ДСПН. Отобранные пациенты были разделены на две группы: I группа (24 больных) — пациенты, которые получали базисную терапию; II группа (50 больных) — пациенты, которые на фоне базисного лечения получали препарат Нейромидин® в виде внутримышечных инъекций по 5 мг 2 раза в сутки в течение 10 дней, затем перорально по 20 мг 3 раза в сутки в течение 20 дней. Проводились неврологическое обследование по шкалам нейропатического симптоматического подсчета, модифицированного нейропатического дисфункционального подсчета, электронейромиографическое (ЭНМГ) тестирование периферических нервов нижних конечностей. С целью установления особенностей когнитивных функций использовали тест Mini-Mental State Examination. Также оценивали показатели тревожности и депрессии в динамике лечения. Результаты. В группе лиц, которые на фоне базисной терапии получали Нейромидин®, отмечалось достоверное улучшение показателей субъективной и объективной симптоматики. Проявления аксонопатии и миелинопатии по результатам ЭНМГ-тестирования периферических нервов достоверно уменьшались в группе пациентов, принимавших на фоне базисной терапии Нейромидин®. Также установлены статистически значимое улучшение когнитивных функций, уменьшение проявлений тревоги и депрессии. Выводы. Применение Нейромидина® на фоне базисной терапии у больных с ДСПН улучшает процессы регенерации и реиннервации периферических нервов нижних конечностей и улучшает проведения возбуждения моторными волокнами по данным ЭНМГ-параметров, оказывает позитивное влияние на клиническое течение заболевания, а также позволяет улучшить когнитивные функции, уменьшить проявления тревоги и депрессии.
Background. The purpose of the study is to establish the efficiency and safety of the use of ipidacrine (Neuromidin) in patients with type 2 diabetes mellitus complicated by distal symmetric polyneuropathy. Materials and methods. One hundred ten patients with distal symmetric polyneuropathy were examined. Selected patients were divided into 2 groups: group I (n = 24) — persons receiving basic treatment; group II (n = 50) — patients who received Neuromidin, in the form of intramuscular injections of 5 mg 2 times a day for 10 days, then orally 20 mg 3 times a day for 20 days. All patients underwent neurological examination using Neuropathy Symptom Score, Neuropathy Disability Score, electroneuromyographic (ENMG) testing of the peripheral nerves of the lower extremities. In order to establish the peculiarities of cognitive functions, Mini-Mental State Examination was used. Also, the rates of anxiety and depression in the dynamics of treatment were assessed. Results. In the group of people who received Neuromidin on the background of basic treatment, there was a significant improvement in the subjective and objective symptoms. The manifestations of axonopathy and myelinopathy according to the results of ENMG testing of peripheral nerves were believed to decrease in the group of patients taking Neuromidin against the background of basic treatment. Also, a statistically significant improvement of cognitive functions, reduction of anxiety and depression manifestations was established with the administration of Neuromidin. Conclusions. The application of Neuromidin on the background of basic therapy in patients with distal symmetric polyneuropathy improves the processes of regeneration and reinnervation of the peripheral nerves of the lower extremities and improves motor fibers conduction according to the ENMG parameters, has a positive effect on the clinical course of the disease, as well as improves cognitive function, reduces manifestations of anxiety and depression.
цукровий діабет; дистальна симетрична полінейропатія; електронейроміографія; Нейромідин®
сахарный диабет; дистальная симметричная полинейропатия; электронейромиография; Нейромидин®
type 2 diabetes mellitus; distal symmetric polyneuropathy; electroneuromyography; Neuromidin
Вступ
Дистальна симетрична полінейропатія (ДСПН) — одне з найчастіших пізніх ускладнень у пацієнтів із цукровим діабетом (ЦД) обох типів. Імовірність виявлення ДСПН при традиційному неврологічному обстеженні становить близько 30 %, а при проведенні електронейроміографії (ЕНМГ) — понад 80 % [1].
Розвиток ДСПН значно знижує якість життя хворого, створює передумови розвитку нейропатичної форми синдрому діабетичної стопи, нейроостео–артропатії (суглоб Шарко), а також є причиною 55–75 % усіх ампутацій при ЦД [2]. Незважаючи на численні дослідження, присвячені розробці заходів лікування ДСПН, в основі більшості з них лежать симптоматичні підходи, на той час як запропоновані методи патогенетичної корекції виявляють слабку ефективність.
На сьогодні ДСПН розглядають як результат дій комплексу чинників, що спричиняють метаболічні й судинні порушення й призводять до розвитку морфофункціональних змін і нейрофізіологічних відхилень із пригніченням провідності в демієлінізованих нервових волокнах (моторних, сенсорних і вегетативних) [3]. Тому покращання синаптичної передачі в комплексній терапії діабетичної нейропатії є одним з найважливіших напрямків в лікуванні цієї категорії хворих. Також відомо, що в пацієнтів із больовою формою діабетичної нейропатії часто виникають тривожно–депресивні розлади, а зростання тривалості ДСПН супроводжується когнітивною дисфункцією внаслідок паралельного розвитку й прогресування діабетичних церебральних порушень.
З огляду на вищевказане на особливу увагу заслуговують препарати, здатні відновлювати рівень ацетилхоліну — провідного нейромедіатора, зв’язування якого з ацетилхоліновим рецептором на волокнах посмугованих м’язів відкриває канали в мембрані. Іони натрію заходять до саркоплазми волокна, викликаючи появу потенціалу дії й стимулюючи м’язове скорочення. До того ж ацетилхолін є збудливим медіатором у головному мозку, відновлення якого призводить до покращання когнітивних функцій.
До антихолінестеразних засобів, що є найбільш перспективними в лікуванні ДСПН, належить іпідакрин (Нейромідин®) — поліметиленове похідне 4–амінопіридину, що має як периферичний, так і центральний ефекти [4, 5]. Нейромідину® притаманна унікальна подвійна дія, що забезпечує більш ефективне посилення синаптичної передачі. З одного боку, він блокує потенціалзалежні К+–канали пресинаптичної частини, подовжує стан збудження в пресинапсі, що сприяє більшому вивільненню ацетилхоліну. З іншого боку, препарат обернено пригнічує ацетилхолінестеразу постсинаптичної мембрани, перешкоджаючи руйнуванню ацетилхоліну, що покращує передачу нервових імпульсів через холінергічні синапси [6].
Мета дослідження: вивчити ефективність і безпеку застосування препарату Нейромідин® у хворих на цукровий діабет, ускладнений дистальною симетричною полінейропатією.
Матеріали та методи
В обстежені взяли участь 74 хворі на ЦД типу 1 і 2, ускладнений ДСПН (середній вік 56,6 ± 6,7 року), які перебували на лікуванні в ОКУ «Чернівецький обласний ендокринологічний центр», і 20 практично здорових осіб, які становили контрольну групу. Серед хворих було 41 жінка і 33 чоловіки.
Базисна терапія хворих на ЦД, ускладнений ДСПН, включала низьковуглеводну дієту, цукро–знижувальну терапію в адекватних дозах, що проводилася відповідно до чинних настанов [7], і препарати α–ліпоєвої кислоти.
Методом простої рандомізації пацієнтів було поділено на дві групи: І група (n = 24) — особи, які отримували базисну терапію; ІІ група (n = 50) — пацієнти, які на тлі базисного лікування отримували препарат Нейромідин® (виробник «Олайнфарм», Латвія). Препарат призначали у вигляді внутрішньом’язових ін’єкцій по 5 мг двічі на добу протягом 10 днів, потім перорально по 20 мг тричі на добу впродовж 20 днів.
До лікування й після завершення курсу терапії усім хворим проводилося клінічно–нейрофізіологічне обстеження.
Усім пацієнтам здійснювалося неврологічне обстеження: для характеристики суб’єктивних симптомів ДСПН використовували шкалу нейропатичного симптоматичного розрахунку (NSS), об’єктивне дослідження периферичних нервів оцінювали за шкалою нейропатичного дисфункціонального розрахунку (NDS). Усім пацієнтам проводилося електронейроміографічне обстеження. При цьому вивчали: амплітуду потенціалів максимальної рухової відповіді (М–відповідь), швидкість проведення збудження (ШПЗ) (м/с), резидуальну латентність (мс) при тестуванні малогомілкового й великогомілкового нервів. Для оцінки параметрів F–хвилі великогомілкових нервів визначали мінімальну латенцію (мс), середню амплітуду (мкВ), середню ШПЗ (м/с) і хронодисперсію (мс). З метою встановлення особливостей когнітивних функцій використовували тест MMSE (Mini Mental State Examination — міні–тест оцінки психічного статусу). Для оцінки особистісної й реактивної тривожності використовували шкалу Ч.Д. Спілбергера, адаптовану Ю.Л. Ханіним, для визначення ступеня депресивних розладів — шкалу А.Т. Бека.
Статистичний аналіз результатів дослідження здійснювався за спеціальними програмами із застосуванням параметричних (t–критерій Стьюдента) і непараметричних (ранговий критерій Манна — Уїтні, парний Т–критерій Вілкоксона) методів варіаційної статистики, що порівнювалися з адекватними групами контролю.
Результати
При оцінці суб’єктивних проявів ДСПН найбільш поширеними скаргами в обстежених хворих до лікування були відчуття печіння (67,5 %), парестезії (60,0 %), поколювання (62,3 %), оніміння (65,7 %) і біль (77,4 %) у нижніх кінцівках, дещо рідше траплялися судоми (52,3 %) і нічний біль у ногах (47,4 %).
При огляді нижніх кінцівок сухість шкіри виявлялася в 95 % хворих, гіперкератоз — у 65 %. При дослідженні неврологічного статусу в 72,5 % випадків реєструвалося зниження сухожильних рефлексів. Підошовний рефлекс був відсутній у 36,2 % пацієнтів. Пропріоцепція, тактильна, больова, температурна чутливість була знижена в 70,1 % хворих, відсутність чутливості спостерігали в 25,3 % пацієнтів.
Сума балів за шкалою NSS у пацієнтів із суб’єктивними проявами ДСПН становила від 3 до 11. За даними оцінки неврологічних розладів за шкалою NDS, у 19 хворих (25,7 %) встановлено початковий ступінь тяжкості ДСПН, у 29 (39,2 %) — помірний, у 26 (35,1 %) — виражений ступінь тяжкості ДСПН.
Пацієнти обох груп відзначали позитивну динаміку після курсу лікування, зокрема зменшення або зниження болю в ногах у нічний час і покращання загального стану. Вплив лікування на суб’єктивну симптоматику ДСПН у хворих І і ІІ груп подано в табл. 1.
Як видно з даних табл. 1, після лікування у хворих першої й другої груп інтенсивність частоти зазначених скарг вірогідно зменшувалася: у пацієнтів першої групи — на 18,6 % (5,78 ± 0,49 бала; р = 0,048), другої групи — на 36,5 % (4,66 ± 0,63 бала; р = 0,0019) за шкалою NSS порівняно з показниками до лікування. Слід зазначити, що в групі осіб, які на тлі базисної терапії отримували Нейромідин®, відсоток покращення показника суб’єктивної симптоматики був значно вищим після лікування. Окрім того, нами відзначалося повне зникнення скарг у 20,5 % пацієнтів другої групи після терапії (у контролі — тільки у 8,5 %), що на нашу думку, забезпечується впливом Нейромідину® на потенціал–залежні Na+–канали з блокуванням і забезпеченням аналгетичного ефекту, що досягається за рахунок гальмування ектопічних розрядів та ефаптичної передачі збудження в ушкодженому нерві, регенеруючих аксональних розгалуженнях у результаті колатерального спраутингу, а також зниження збудливості центральних нейронів.
Оцінка показників NDS (табл. 1) у динаміці лікування показала, що в другій групі спостерігався вірогідно більший відсоток зниження об’єктивної симптоматики (26,2 %; середній бал: 6,87 ± 0,61; р = 0,049) порівняно з показниками першої групи (19,5 %; середній бал: 7,20 ± 1,02; р = 0,210).
При аналізі ЕНМГ–параметрів периферичних нервів у пацієнтів із ДСПН на тлі ЦД 2–го типу (табл. 2) до лікування спостерігали вірогідні порушення відповідно до нормальних значень: зниження швидкості проведення збудження моторними волокнами при тестуванні малогомілкового й великогомілкового нервів, зниження амплітуди й збільшення площі моторної відповіді м’язів флексорів та екстензорів стопи й пальців, збільшення резидуальної латентності й латентності F–хвилі.
Дослідження функції рухових нервів нижніх кінцівок (малогомілкового й великогомілкового) (табл. 2) дало змогу встановити низку характерних особливостей на тлі запропонованого лікування. Вірогідні зміни показників аксонопатії відзначалися в другій групі при тестуванні великогомілкових нер–вів: підвищення амплітуд на 13,2 % порівняно з показниками до лікування проти 4,2 % у групі порівняння, що вказує на достатню регенерацію осьового циліндра під дією препарату. Вірогідні покращення показників мієлінопатії спостерігали в групі пацієнтів, які приймали на тлі базисної терапії Нейромідин®: збільшення ШПЗ на 9,9 проти 2,0 % в осіб, які приймали виключно базисну терапію, вірогідне вкорочення латентності F–хвилі на 15,1 проти 7,5 % відповідно.
Отже, застосування Нейромідину® на тлі базисної терапії у хворих із ДСПН покращує процеси регенерації й реіннервації периферичних нервів нижніх кінцівок, стимулює нервово–м’язову передачу, покращуючи проведення збудження периферичними нервами, унаслідок цього підвищується скоротлива здатність розгиначів і згиначів стопи й пальців.
Обговорення
Сприятливий вплив Нейромідину® на перебіг ДСПН пов’язаний, з одного боку, з блокадою калієвої проникності мембрани, з іншого — зі зворотним інгібуванням холінестерази. При цьому вирішальну роль відіграє блокада калієвої проникності мембрани, що спричиняє подовження фази реполяризації потенціалу дії мембрани й підвищення активності пресинаптичного аксона. Це супроводжується збільшенням входу іонів кальцію до пресинаптичної терминалі і, внаслідок цього, посиленням викиду медіатора до синаптичної щілини в усіх синапсах. Підвищення концентрації медіатора в синаптичній щілині сприяє посиленню стимуляції постсинаптичної клітини внаслідок медіатор–рецепторної взаємодії. У холінергічних синапсах інгібування холінестерази спричиняє подальше накопичення нейромедіатора в синаптичній щілині й посилення функціональної активності постсинаптичної клітини. Отже, Нейромідин® потужно діє на всі ланки в ланцюгу процесів, які забезпечують проведення збудження.
Наступний етап нашого дослідження полягав у вивченні ефективності Нейромідину® в лікуванні інтелектуально–мнестичних розладів хворих на ЦД.
У більшості пацієнтів із ЦД обох груп до лікування відмічалися зміни на рівні помірних когнітивних порушень. Відомо, що мнестичні розлади при ЦД пов’язані з центральним холінергічним дефіцитом. При цьому порушуються як пресинаптичний, так і постсинаптичний компоненти центральних холінергічних синапсів, розташованих у корі великих півкуль і гіпокампі, у результаті чого зменшується вивільнення ацетилхоліну й знижується чутливість до нього.
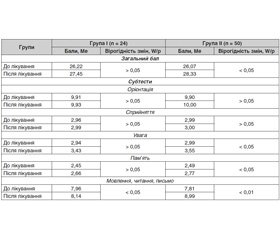
Динаміка показників когнітивних функцій у хворих на ЦД за даними MMSE на тлі призначеного лікування наведена в табл. 3.
Як видно з наведених даних, у хворих обох груп зростав загальний бал тесту MMSE, водночас статистично значуще в пацієнтів, яким додатково призначався Нейромідин® (на 8,7 %, р < 0,05), що, очевидно, пов’язано з активізацією холінергічної системи. Найбільш суттєві позитивні зміни встановлені за субтестами дослідження уваги, пам’яті й перцептивно–гностичної сфери зі збільшенням досліджуваних показників на 24,6 і 12,0 % відповідно, на той час як у групі порівняння спостерігалися тільки невірогідні тенденції до їх зростання. Показник перцептивно–гностичної сфери після базисної терапії незначно (на 6,4 %), але вірогідно збільшувався. Застосування на тлі загальноприйнятої терапії Нейромідину® сприяло помітному його зростанню (на 15,1 %).
Позитивний вплив Нейромідину® на когнітивні функції й емоційно–особистісні реакції у хворих на ДСПН, очевидно, досягається за рахунок унікального механізму дії препарату, а саме покращання проведення збудження в центральній нервовій системі шляхом стимуляції пресинаптичного нервового волокна, збільшення викиду головного нейромедіатора ацетилхоліну в синаптичну щілину, зменшення його руйнування ферментом, а також підвищення активності постсинаптичної клітини прямим мембранним і опосередкованим медіаторним впливом із прискоренням процесів нейропластичності. До того ж, як показали попередні дослідження, застосування Нейромідину® дозволяє покращити показники церебральної гемодинаміки в пацієнтів із ЦД, що сприяє покращанню когнітивних функцій [8].
Дослідження динаміки показників емоційно–особистісних реакцій встановило статистично значуще зниження параметрів реактивної тривожності в пацієнтів обох груп, проте суттєвішим воно було в осіб, які додатково отримували Нейромідин® (на 13,6 % проти зменшення на 7,4 % у групі порівняння, р < 0,05) без вірогідних змін показників особистісної тривожності. Показник депресії вірогідно знижувався на 11,3 % (р < 0,05) тільки в групі пацієн–тів, які додатково отримували в комплексному лікуванні Нейромідин®. На нашу думку, це пов’язано, з одного боку, зі зменшенням проявів ДСПН, зокре–ма больового синдрому, з іншого — з покращанням церебрального метаболізму.
Слід зазначити, що препарат переносився пацієнтами добре, побічних реакцій на тлі його лікування зафіксовано не було.
Отже, Нейромідин®, що діє на всі ланки в ланцюгу процесів, які забезпечують проведення збудження, сприяє відновленню аксонального транспорту в пацієнтів із ДСПН із покращанням сенсорних і моторних показників, прискорює процеси нейропластичності, а також чинить надзвичайно важливу для цієї категорії хворих аналгетичну дію. Препарат має високий рівень безпеки й добру переносимість. До того ж застосування Нейромідину® дозволяє покращити когнітивні функції, зменшити прояви тривожності й депресії і, відповідно, покращити якість життя пацієнтів.
Висновки
1. Використання Нейромідину® в комплексному лікуванні хворих на діабетичну дистальну симетричну полінейропатію сприяє ефективному покращенню клінічного перебігу захворювання із зменшенням нейропатичних скарг та об’єктивних проявів.
2. Нейромідин® позитивно впливає на функціональний стан периферичних нервів нижніх кінцівок за даними електронейроміографії з вірогідним підвищенням амплітуди моторної відповіді, збільшенням швидкості проведення збудження моторними волокнами периферичних нервів.
3. Застосування в комплексному лікуванні хворих на діабетичну дистальну симетричну полінейропатію Нейромідину® сприяє ефективному покращанню когнітивних функцій із статистично значущим зростанням показника MMSE–тесту (Mini Mental State Examination) на 8,7 %, а також ефективно зменшує прояви тривоги й депресії.
Конфлікт інтересів. Не заявлений.

/232-1.jpg)
/233-1.jpg)
/235-1.jpg)