Международный эндокринологический журнал Том 15, №3, 2019
Вернуться к номеру
Мужской фактор бесплодия: алгоритм лабораторной диагностики причин (часть 2)
Авторы: Рыкова О.В.
Руководитель клинического направления лабораторной диагностики лаборатории «Синэво», г. Киев, Украина
Рубрики: Эндокринология
Разделы: Справочник специалиста
Версия для печати
Раніше були висвітлені теми лабораторної діагностики: оцінка андрогенного статусу чоловіка: що вибрати — тестостерон загальний або вільний; або використовувати розрахунковий показник — індекс вільного тестостерону; що важливо враховувати при направленні на оцінку рівня тестостерону; як правильно інтерпретувати результат з урахуванням залежності від цілої низки чинників; чому необхідно як мінімум двічі оцінити рівень тестостерону; які критерії постановки діагнозу чоловічого гіпогонадизму; яке подальше обстеження слід проводити після встановлення діагнозу. У даній статті ми продовжуємо розглядати лабораторні алгоритми діагностики цілої низки причин гіпогонадизму. Окремо зупинимося на спермограмі як тесті, що дозволяє комплексно оцінити роботу всіх систем, відповідальних за формування сперми.
Ранее были освещены темы лабораторной диагностики: оценка андрогенного статуса мужчины: что выбрать — тестостерон общий или свободный; или использовать расчетный показатель — индекс свободного тестостерона; что важно учитывать при направлении на оценку уровня тестостерона; как правильно интерпретировать результат с учетом зависимости от целого ряда факторов; почему необходимо как минимум дважды оценить уровень тестостерона; каковы критерии постановки диагноза мужского гипогонадизма; какое дальнейшее обследование следует проводить после установления диагноза. В данной статье мы продолжаем рассматривать лабораторные алгоритмы диагностики целого ряда причин гипогонадизма. Отдельно остановимся на спермограмме как тесте, позволяющем комплексно оценить работу всех систем, ответственных за формирование спермы.
Previously, the topics of laboratory diagnosis were covered: assessment of the male androgenic status: what to choose — total or free testosterone; or use an estimated indicator — free testosterone index; what is important to consider when referring to an assessment of testosterone levels; how to correctly interpret the result, taking into account the dependence on a number of factors; why it is necessary to at least twice assess the level of testosterone; what are the criteria for making a diagnosis of male hypogonadism; what further examination should be carried out after diagnosis. In this article, we continue to consider laboratory algorithms for diagnosing a variety of causes of hypogonadism. Separately, we will focus on spermogram as a test, which allows a comprehensive assessment of the functioning of all systems responsible for the formation of sperm.
чоловічий фактор безпліддя; спермограма; гіпогонадизм
мужской фактор бесплодия; спермограмма; гипогонадизм
male factor of sterility; spermogram; hypogonadism
Гиперпролактинемия
Гиперпролактинемия является одной из функциональных причин вторичного гипогонадизма и должна быть обязательно исключена у каждого мужчины с гипогонадизмом.
Согласно руководству «Diagnosis and Treatment of Hyperprolactinemia: An Endocrine Society Clinical Practice Guideline» (2011), для постановки диагноза гиперпролактинемии рекомендовано однократное определение уровня пролактина (ПРЛ) при условии исключения влияния факторов, которые могут повышать уровни его синтеза.
1. Физиологические причины повышения уровня ПРЛ: коитус, интенсивные физические нагрузки, сон, стресс (включая стресс при венепунк-
ции).
2. Прием медикаментов: эстрогенсодержащие, блокаторы рецепторов допамина (фенотиазины), антагонисты допамина (метоклопрамид), антигипертензивные препараты, антигистаминные препараты (Н2), холинергические агонисты, анестетики, противосудорожные, антидепрессанты, антипсихотические препараты, нейролептики, нейропептиды, опиаты и антагонисты опиатов.
Согласно руководству, данные препараты должны быть отменены (при клинической возможности) на 3 дня или заменены на препараты, которые не стимулируют синтез ПРЛ. В случае получения повышенных уровней ПРЛ на фоне приема данных препаратов необходимо повторное тестирование (в условиях отмены) или учет возможности препарат-индуцированной гиперпролактинемии.
Уровни пролактина, которые позволяют установить диагноз гиперпролактинемии, согласно руководству, следующие:
— гиперпролактинемия — повышение более 25 нг/мл;
— повышение более 200 нг/мл, наиболее вероятно, обусловлено пролактиномой;
— повышение более 200 нг/мл может быть при приеме препаратов;
— уровень более 500 нг/мл характерен для макроаденомы.
После установления гиперпролактинемии необходимо дообследование для исключения целого ряда состояний и заболеваний:
1. Патология щитовидной железы (гипоти–реоз) — определение ТТГ и свободного тироксина (Т4 свободный). Выявление гипотиреоза требует заместительной терапии, на фоне которой возможна нормализация уровня пролактина без назначения специфического лечения гиперпролактинемии.
2. Опухоли гипоталамо-гипофизарной области, соматотропиномы, краниофарингеномы, герминомы, менингиомы, гранулемы, травмы, включая операционные, воспалительные поражения, воздействие облучения — проведение инструментальных методов визуализации, определение других гормонов гипофиза.
3. Почечная недостаточность — оценка уровня креатинина.
4. Гиперпролактинемия за счет увеличения макропролактина — определение макропролактина. Уровень макропролактина более 60 % (Roche, Cobas) будет свидетельствовать о макропролактинемии (увеличение ПРЛ за счет гормонально неактивной фракции). Это необходимо учитывать при определении тактики лечения гиперпролактинемии.
5. Целый ряд других причин, включая травмы грудной клетки, эпилептические эпизоды.
При направлении на определение уровня ПРЛ необходимо учитывать:
— суточную вариабельность ПРЛ. Максимальные уровни наблюдаются в период 2:00 — 4:00. Это определяет необходимость сдавать ПРЛ в утреннее время, натощак, с учетом времени подъема после сна. При повторном обследовании оптимально оценивать ПРЛ в аналогичное время;
— вариабельность при определении на приборах и реагентах разных производителей. Оценку ПРЛ необходимо проводить в одной лаборатории (на аппарате и реагентах одного производителя), т.к. минимальные отличия в определяемом уровне ПРЛ присутствуют;
— вариабельность при стрессе. Важно соблюдать физический, эмоциональный и сексуальный покой перед сдачей анализа, в том числе нормальный режим сна. Это особенно важно для тех, кто работает в ночное время, летает со сменой часовых поясов — все это может отразиться на уровне ПРЛ.
При интерпретации уровня ПРЛ необходимо учитывать:
— референтные пределы — это уровни ПРЛ только у 95 % всех здоровых людей, 5 % здоровых имеют уровни ПРЛ несколько выше или ниже пределов. Это определяет необходимость дополнительного обследования и учета клинической картины в случаях, когда уровень ПРЛ незначительно выходит за референтные пределы, в первую очередь факторы стресса;
— диагностические пороги — в руководстве по диагностике гиперпролактинемии за диагностический порог ПРЛ принят уровень 25 нг/мл;
— возможность «hook-effect»: лабораторный эффект, который может наблюдаться при крайне высоких уровнях гормона. Это ведет к невозможности определить истинный уровень гормона и выдаче ложнонормальных результатов при макроаденоме. Для реагентов Roche на аппаратах Cobas данный эффект может быть при уровнях ПРЛ, превышающих 12 690 нг/мл. Данные уровни ПРЛ могут наблюдаться при макроаденомах, которые сопровождаются не только клиникой гиперпролактинемии, но и эффектами сдавления опухолью окружающих тканей (выраженными головными болями, нарушением полей зрения). Согласно вышеуказанному руководству, в ситуациях наличия клиники (особенно наличия головных болей, нарушений зрения), данных МРТ о макроаденоме и уровнях ПРЛ в пределах референтных значений необходимо повторное тестирование уровня ПРЛ в пробах с разведением 1 : 100 для возможности получения истинного уровня гормона, определения объема терапии и контроля эффективности лечения (снижения уровня ПРЛ);
— вариабельность ПРЛ — суточную, о которой сказано выше, а также вследствие стресса, физической и сексуальной активности.
Патология щитовидной железы
В руководстве отмечается, что патология щитовидной железы как причина гипогонадизма встречается редко, однако в случаях выявления гиперпролактинемии требуется обязательная оценка ее функционального статуса. На первом этапе обследования достаточно определения тиреотропного гормона (ТТГ), который позволит выделить три категории пациентов:
— с эутиреоидным статусом (уровень ТТГ в пределах референтных значений лаборатории);
— с повышенными уровнями ТТГ, что будет свидетельствовать о гипотиреозе. Для решения вопроса, манифестный это гипотиреоз или субклинический, необходимо будет дообследование: определение свободных фракций Т4, Т3 (при необходимости), наличия антител к тиреоидной перо–ксидазе (ТПО), тиреоглобулину (при необходимости). Объем исследований будет определять эндокринолог;
— со снижением уровня ТТГ, что может свидетельствовать не только о тиреотоксикозе, но и о вторичном гипотиреозе. Для решения вопроса, манифестный это гипотиреоз или субклинический, и проведения дифференциальной диагностики со вторичным гипотиреозом необходимо дообследование: определение свободных фракций Т4, Т3 (при необходимости), наличия антител к рецептору ТТГ (АТ рТТГ). Объем исследований будет определять эндокринолог.
При направлении на определение уровня ТТГ необходимо учитывать:
— суточную вариабельность ТТГ. Максимальные уровни наблюдаются в период 2:00 — 4:00, минимальные уровни — в 14:00 — 16:00. Данные исследований суточной вариабельности свидетельствуют, что в период с 8:00 до 9:30 уровень ТТГ может быть снижен на 50 % (по сравнению с ночным пиком). Все эти данные о вариабельности данного гормона определяют необходимость сдавать ТТГ в утреннее время, натощак и с учетом времени сдачи. При повторном обследовании оптимально оценивать ТТГ в аналогичное время;
— вариабельность при определении на приборах и реагентах разных производителей;
— вариабельность при стрессе.
При интерпретации уровня ТТГ необходимо учитывать:
— референтные пределы;
— диагностические пороги;
— суточную вариабельность ТТГ.
Синдром перегрузки железом
Это патологическое состояние, которое характеризуется количественным увеличением железа в организме, что ведет к повреждению органов и тканей вследствие токсического воздействия его избытка. Может быть:
— первичным (результат генетических изменений);
— вторичным (в результате другого заболевания или состояния, возникающего на фоне нарушения эритропоэза, заболеваний печени, которые являются основными факторами, предрасполагающими к развитию синдрома перегрузки железом — СПЖ).
Целый ряд факторов может увеличивать риски развития данного синдрома: неконтролируемый прием железосодержащих препаратов, гемотранс–фузии, гепатит С, анемии (талассемия) и др. Важно учитывать, что данный синдром чаще проявляется у мужчин, чем у женщин, потому, что нет ежемесячной потери крови.
Основой поражения органов при данном синдроме является железоиндуцированный оксидативный стресс. Избыток железа выступает катализатором перекисного окисления липидов, что приводит к усилению образования коллагена и фиброзу в местах отложения микроэлемента.
Данный синдром требует особого внимания с учетом того, что клинические проявления неспецифичны за счет мультиорганности поражения. Некоторые схожи с клиникой анемии, что может приводить к дополнительному приему препаратов железа, если не проведено комплексное обследование для исключения данного синдрома. Показатели общего анализа крови в данном случае не решают диагностический вопрос.
Наиболее эффективным комплексом является определение:
— процента насыщения трансферрина железом;
— ферритина.
Несмотря на то что при СПЖ увеличение концентрации сывороточного ферритина идет пропорционально интенсивности избытка железа, отражая состояние депо данного микроэлемента, следует учитывать, что ферритин является острофазовым белком, что может вести к гиперферритинемии при целом ряде других состояний (воспаление, цитолиз, неоплазия и др.). Поэтому ключевая роль отводится проценту насыщения трансферрина.
Важно отметить, что целый ряд других эндокринопатий — синдром Кушинга, акромегалия — могут сопровождаться развитием гипогонадного гипогонадизма и каждый из них требует использования рекомендованных мировыми руководствами наиболее чувствительных лабораторных тестов.
Спермограмма
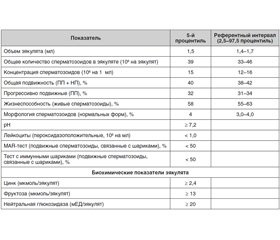
Спермограмма — исследование эякулята для оценки оплодотворяющей способности спермы (фертильности мужчины) и выявления различных урологических заболеваний, инфекционных процессов, гормональных нарушений. Это связано с тем, что в процессе формирования эякулята участвует вся репродуктивная система мужчины: яички с придатками, семенные протоки, семенные пузырьки, предстательная железа и бульбоуретральные железы, контролируют процесс формирования гормоны гипофиза и гонад. Всемирная организация здравоохранения (ВОЗ) регламентирует вопросы, связанные с правилами тестирования эякулята, референтные интервалы и перечень показателей в спермограмме. В 2010 году вышло пятое издание «Руководства по исследованию и обработке эякулята», в котором изменены критерии оценки эякулята, предложенные в четвертом издании 1999 года. Были внесены изменения в референтные значения количества и подвижности сперматозоидов, принципы категоризации подвижности: сперматозоиды с прогрессивно подвижным движением (ПП), непрогрессивно подвижным движением (НП) и неподвижные. Значительно изменены критерии количества нормальных форм сперматозоидов (строгие критерии Крюгера). Если оценить в целом характер изменений, то они отражают общую тенденцию к снижению требований к понятию фертильного эяку–лята: согласно последнему документу, достаточно более 4 % морфологически нормальных сперматозоидов. Основные характеристики, соответствующие критериям ВОЗ 2010 г., представлены в табл. 1.
Оценка количества, подвижности и морфологии сперматозоидов лежит в основе классификации нарушений: важно учитывать, что «спермия» относится к оценке эякулята, а «зооспермия» — к оценке сперматозоидов. Термины, описывающие изменения эякулята, отражают только характер изменений, но не их причины, которые зачастую могут быть связаны не только с патологическими состояниями, но и с воздействием целого ряда внешних факторов. Именно поэтому необходимо строгое соблюдение правил подготовки к сдаче данного лабораторного теста.
Правила подготовки к сдаче спермограммы:
1. Соблюдение сроков полового воздержания (включая мастурбацию): 2–7 дней. Важно акцентировать внимание мужчины на том, что он должен указать количество дней воздержания при сдаче эяку–лята в лаборатории. Это позволит не только учесть данный фактор влияния на качество эякулята, но и в случае необходимости повторного тестирования зафиксировать день, в который необходимо будет сдавать анализ. Данные о периоде воздержания позволяют правильно интерпретировать количество сперматозоидов и их морфологию, объем спермы: укорочение срока и частые половые контакты могут привести к физиологическому уменьшению объема эякулята, общего количества сперматозоидов, воздержание более 7 суток может привести к тому, что часть «старых» сперматозоидов сбрасывается в семенные пузырьки, где погибает, и это ведет к снижению процента живых сперматозоидов. Более длительное отсутствие полового акта (больше месяца) может привести к появлению старых дегенеративных форм сперматозоидов, которые не способны к оплодотворению.
2. Важно исключить факторы, которые влияют на подвижность сперматозоидов: это в первую очередь любые тепловые процедуры, включая использование подогрева сидений в зимнее время и общее перегревание организма в сауне.
3. Алкоголь аналогично ведет к снижению по–движности сперматозоидов, поэтому за 3 дня до сдачи эякулята необходимо исключить прием любых алкогольных напитков.
4. Комплексное воздействие на показатели эяку–лята оказывает наличие острого заболевания: это и повышенная температура, и прием медикаментов, и оксидативный стресс. Сдача спермограммы должна проводиться не ранее чем через 2–3 недели после перенесенного острого заболевания.
5. Перед сдачей анализа необходимо избегать тяжелых физических нагрузок, т.к. накопление молочной кислоты может отрицательно сказаться на качестве сперматозоидов, эмоциональное перенапряжение и стрессы могут привести к нарушениям в гормональном фоне и, соответственно, к изменениям в показателях спермограммы.
Одним из важных факторов в обеспечении качества оценки фертильных возможностей является сбор всей порции эякулята, т.к. это является залогом не только корректной оценки количества и концентрации сперматозоидов, объема спермы, но и данных о подвижности, вязкости и морфологии сперматозоидов. Критична потеря первой порции, наиболее богатой сперматозоидами. Если это произошло, то повторная сдача возможна только через 2–7 дней воздержания.
При интерпретации результатов спермограммы необходимо учитывать возможное влияние вышеперечисленных факторов в случае выявления тех или иных отклонений и повторить данное исследование через 3–4 недели. Важно повторное тестирование проводить на тот же день воздержания, что и при первичном тестировании, для получения сравнимых результатов. Одним из важных аспектов оценки фертильности эякулята является сопоставление количества неподвижных сперматозоидов с показателем процента живых сперматозоидов: высокий процент неподвижных, но живых сперматозоидов говорит о возможном наличии патологии жгутика, а если это сочетается с высоким процентом неживых сперматозоидов (некрозооспермия) — то о патологии эпидидимиса.
Однократное исследование эякулята рассматривается только в случаях нормозооспермии или азо–оспермии (в случаях небольших по объему яичек или данных о врожденной патологии).
Следует учитывать, что нормозооспермия — это количество, подвижность и морфология сперматозоидов в пределах референтных значений. Однако отсутствие изменений в этих показателях не может исключить наличия антиспермальных антител (АСАТ) — одной из причин бесплодия.
Определение антиспермальных антител
Согласно современным данным о структуре причин мужского фактора бесплодия, 10–20 % случаев связано с иммунологическими факторами. К сожалению, заподозрить наличие этих антител по данным спермограммы не всегда возможно; наличие агглютинации сперматозоидов может косвенно указывать на наличие АСАТ, однако целый ряд других факторов может привести к склеиванию сперматозоидов, с одной стороны, а с другой — отсутствие агглютинации не исключает наличия данных антител. Именно поэтому ВОЗ включила в обязательный комплекс обследования мужчины с бесплодием при исследовании эякулята необходимость определения наличия АСАТ, которые являются одной из основных иммунологических причин бесплодия, с использованием специальных тестов.
АСАТ относятся к иммуноглобулинам изотипов IgG, IgA и/или IgM, однако в эякуляте IgМ не обнаруживаются в силу большой молекулярной массы. У мужчин они образуются в яичках, их придатках, в семявыносящих протоках и направлены против антигенов мембраны разных частей сперматозоида — головки, хвоста, средней части или их комбинации. Наличие данных антител приводит к нарушению в первую очередь способности сперматозоидов проникать через цервикальную слизь и оплодотворять яйцеклетку. При этом сами сперматозоиды могут быть в достаточном количестве, с достаточной по–движностью и нормальной морфологией. Причин появления данных антител несколько, одна из основных — хронические воспалительные процессы, а также травмы, обструкции семявыносящих протоков, варикоцеле, крипторхизм, гормональные нарушения.
АСАТ могут выявляться не только в эякуляте, но и в крови. Однако определение в крови менее информативно по сравнению с оценкой в эякуляте, поэтому проводится либо при отсутствии АСАТ в эякуляте, либо при недостаточном количестве по–движных форм сперматозоидов. Рекомендованным тестом определения АСАТ в эякуляте (согласно рекомендациям ВОЗ) является MAR-тест (Mixed agglutination reaction). В данном исследовании под микроскопом определяется процент активно-по–движных сперматозоидов, покрытых АСАТ, от общего количества сперматозоидов с теми же характеристиками при исследовании спермы после обработки специальным реагентом. MAR-тест считается положительным, если активно-подвижных сперматозоидов, покрытых АСАТ, больше 50 %. В данном случае можно говорить о наличии иммунологического фактора. Данное исследование целесообразно проводить только при нормальной концентрации и подвижности сперматозоидов (учитывая, что главным критерием оценки является определение соотношения подвижных сперматозоидов). В случае нарушения этих показателей рекомендовано оценивать наличие АСАТ в крови.
Посткоитальный тест
Посткоитальный тест — это определение наличия подвижных сперматозоидов в цервикальной слизи, взятой через некоторое время после полового акта. Данный тест отражает способность сперматозоидов проникать через цервикальную слизь для оплодотворения яйцеклетки. Наличие АСАТ может стать препятствием для их проникновения, отражая иммунологический фактор бесплодия. Оптимальный срок проведения теста — строго в овуляторный период, когда наблюдаются наиболее благоприятные условия для сперматозоидов (вязкость слизи минимальна в результате влияния эстрогенов). Для определения дня проведения теста можно использовать данные о продолжительности менструального цикла, базальной температуре, изменениях цервикальной слизи, определение уровня эстрогенов или ЛГ, УЗИ яичников.
Эффективность данного теста в выявлении цервикального фактора бесплодия будет зависеть не только от корректности определения овуляторного периода, но и от строгого соблюдения правил подготовки, которые могут существенно повлиять на результаты:
— воздержаться от половых актов, мастурбации в течение двух дней до проведения теста;
— категорически запрещается использование любых внутривагинальных средств. После полового акта можно принять душ, подмываться нельзя;
— не рекомендуется сдавать в период острых заболеваний и в течение первых недель реконвалесценции;
— исключить тепловые процедуры, тяжелые физические нагрузки, прием медикаментов.
По рекомендациям ВОЗ, цервикальную слизь необходимо оценивать в промежуток времени от 9 до 14 часов после полового акта. Критерии оценки приведены в табл. 2.
Положительный результат позволяет исключить иммунологический фактор бесплодия вследствие наличия антиспермальных антител. Критерии положительного результата могут колебаться в разных лабораториях, отражая разные подходы. В данном случае представлены рекомендации ВОЗ 2010 г. В случае получения сомнительных и отрицательных результатов необходимо повторное тестирование в условиях исключения возможных факторов, которые могли привести к данным результатам. Очень часто причиной отрицательного посткоитального теста становится слишком раннее или слишком позднее проведение исследования, местные воспалительные процессы, повышение вязкости цервикальной слизи, связанное с низким уровнем эстрогенов перед овуляцией в цикле исследования. В случае отрицательного результата рекомендуется повторное проведение теста в следующем цикле, иногда в нескольких циклах, а в ряде случаев — проведение теста in vitro. Особенно это важно в случаях положительных результатов тестов на наличие АСАТ (MAR-тест, определение АСАТ в крови, цервикальной слизи).
В руководстве ВОЗ отмечается, что в некоторых случаях посткоитальный тест может быть использован для оценки эякулята у мужчин, которые не могут сдать сперму в условиях лабораторных центров взятия материала.
Заключение
Оценка мужского фактора бесплодия должна быть комплексной и включать тесты, позволяющие оценить не только результат наличия каких-либо заболеваний, но и сами заболевания, что позволит выбрать наиболее эффективную тактику лечения.
Направляя пациента на лабораторное тестирование, необходимо обязательно определить для него условия сдачи анализа (время суток) и правила подготовки. Особенно это важно для показателей, имеющих суточную вариабельность.
Особое внимание следует уделить оценке медикаментозного анамнеза. В случае приема препаратов, которые могут повлиять на тестируемый показатель, отменить их при клинической возможности на рекомендуемый период. Если такой возможности нет, проводить интерпретацию с учетом данного медикаментозного влияния.
Нужно помнить, что каждая лаборатория отличается приборами и реагентами, что ведет к целесообразности тестирования в одной лаборатории для получения наиболее корректных для сравнения в динамике показателей.
При направлении на спермограмму важно рекомендовать пациенту строгое соблюдение правил подготовки и оптимально дополнять определением АСАТ (MAR-теста), которые могут быть причиной мужского бесплодия (иммунного). Важно учитывать, что наличие нормальных показателей спермограммы не исключает наличия данных антител. Определение этих антител в эякуляте проводится при нормальных показателях подвижности сперматозоидов. В случае снижения процента подвижности оптимально провести определение АСАТ в крови или посткоитальный тест. При интерпретации положительных результатов MAR-теста необходимо учитывать, что данные антитела могут выявляться у здоровых мужчин с доказанной фертильностью в 1–10 % случаев. Поэтому всегда необходимо дополнить исследование проведением посткоитального теста для подтверждения клинической значимости выявленных АСАТ.
Мы рассмотрели целый комплекс лабораторных тестов, которые позволят выявить основные причины мужского фактора бесплодия и выбрать оптимальную тактику ведения пациента.
Комплекс лабораторных тестов
1. Спермограмма + MAR-тест. Комплексная оценка фертильности мужчины, исключение иммунного фактора бесплодия, особенно в случаях нормальных показателей спермограммы.
2. Индекс свободного тестостерона. Расчетный показатель оценки андрогенного статуса с учетом уровня синтеза глобулинсвязывающих половых гормонов, играющего ключевую роль в правильной интерпретации уровней общего тестостерона.
3. Пролактин. Исключение одной из самых распространенных причин вторичного гипогонадизма.
4. Тиреотропный гормон. Скрининговый тест функционального статуса щитовидной железы, играющей ключевую роль в репродуктивном здоровье.
5. ЛГ/ФСГ. Тесты дифференциальной диагностики первичного/вторичного гипогонадизма.
6. Процент насыщения трансферрина/ферритин. Оптимальный комплекс исключения синдрома перегрузки железом как одной из органических причин вторичного гипогонадизма.
Конфликт интересов. Не заявлен.

/248-1.jpg)
/249-1.jpg)
/251-1.jpg)