Журнал «Боль. Суставы. Позвоночник» Том 9, №3, 2019
Вернуться к номеру
Питание как фактор риска и вмешательство при ревматических заболеваниях
Авторы: Пузанова О.Г.
Киевский медицинский университет, г. Киев, Украина
Рубрики: Ревматология, Травматология и ортопедия
Разделы: Справочник специалиста
Версия для печати
Мета публікації — огляд ефектів харчування як чинника ризику та втручання в аспекті ревматичних захворювань. З використанням методів інформаційного аналізу досліджено понад 100 джерел спеціальної літератури та комп’ютерних ресурсів доказової медицини. У великих обсерваційних дослідженнях, систематичних оглядах і метааналізах, присвячених профілактичному, терапевтичному потенціалу та безпеці застосування різних харчових продуктів, дієт, мікронутрієнтів і пробіотиків, у тому числі за наявності пов’язаних провідних чинників ризику неінфекційних захворювань (вживання тютюну, алкоголю, підвищеного індексу маси тіла тощо), встановлено, що значущість харчування як чинника ризику розвитку та кінцевих результатів доведено насамперед для ревматоїдного артриту та подагри. Патогенетичну роль харчування розглянуто в контексті його впливу на кишкову мікробіоту. Показано необхідність проведення рандомізованих контрольованих досліджень для оцінки протективного потенціалу різних моделей харчування й ефектів дотримання модифікованої середземноморської дієти та вживання певних дієтичних добавок і пробіотиків при ревматичних захворюваннях, а в кінцевому результаті — для розробки спеціальних настанов із харчування для хворих ревматологічного профілю. Відзначено достатню доказову базу профілактичного консультування таких пацієнтів з питань харчування з метою зниження кардіоваскулярного ризику.
Цель публикации — обзор эффектов питания как фактора риска и вмешательства в аспекте ревматических заболеваний. С применением методов информационного анализа изучено более 100 источников специальной литературы и компьютерных ресурсов доказательной медицины. В крупных обсервационных исследованиях, систематических обзорах и метаанализах, предметом которых были профилактический, терапевтический потенциал и безопасность применения различных пищевых продуктов, диет, микронутриентов и пробиотиков, в том числе в связи с сопряженными ведущими факторами риска неинфекционных заболеваний (курением, употреблением алкоголя, повышенным индексом массы тела), доказана значимость питания как фактора риска развития и исходов прежде всего ревматоидного артрита и подагры. Патогенетическая роль питания рассмотрена в контексте его влияния на кишечную микробиоту. Показана необходимость проведения рандомизированных контролируемых исследований для оценки протективного потенциала различных моделей питания и эффектов применения модифицированной средиземноморской диеты, ряда диетических добавок и пробиотиков при ревматических заболеваниях, а в конечном итоге — для разработки специальных рекомендаций по питанию больных ревматологического профиля. Отмечена достаточная доказательная база профилактического консультирования таких пациентов по вопросам питания с целью снижения кардиоваскулярного риска.
The purpose of the paper is to provide a review of the effects of nutrition as a risk factor and intervention in the aspect of rheumatic diseases. Using information analysis methods, more than 100 special literature sources have been studied, including evidence based medicine computer databases. The significance of nutrition as a risk factor for the development and outcomes, first of all for rheumatoid arthritis and gout, is proved in large observational studies, systematic reviews and meta-analysis dedicated to both preventive and therapeutic potential as well as to safety of different food products, diets, micronutrients and probiotics, including in connection with associated main risk factors of non-infectious diseases (tobacco smoking, alcohol consumption, increased body mass index). The pathogenetic role of nutrition is considered in the context of its influence on gut microbiota. Necessity of the randomized controlled trials is shown in order to assess the protective potential of different nutritional patterns, as well as the effects of modified Mediterranean diet, some dietary supplements and probiotics intake in rheumatic diseases, and as a result — to develop special guidelines on nutrition in rheumatic patients. There is a sufficient evidence base of preventive counseling of such patients on nutritional issues with the aim of cardiovascular risk reduction.
ревматичні захворювання; харчування; чинник ризику; втручання; огляд
ревматические заболевания; питание; фактор риска; вмешательство; обзор
rheumatic diseases; nutrition; risk factor; intervention; review
Интерес к эффектам питания при хронических болезнях всегда был высок. Наблюдаемый в обществе рост осознания тесной связи питания, здоровья и ожидаемой продолжительности жизни сопряжен с ренессансом экспериментальных и клинических исследований, научных и научно–популярных публикаций на тему питания, кишечной микробиоты и неинфекционных заболеваний (НИЗ), включая ревматические (РЗ). При этом специальные международные рекомендации по питанию больных РЗ не разработаны. В попытках повлиять на прогноз и качество жизни, связанные с болезнью и побочными эффектами (ПЭ) фармакотерапии, многие пациенты обращаются к средствам комплементарной и альтернативной медицины, интересуются влиянием различных диет и диетических добавок на проявления и исходы заболеваний [1–7].
В патогенезе большинства РЗ — заболеваний со–единительной ткани, спондилоартритов (СпА), системных васкулитов — факторам внешней среды (химическим, физическим, инфекционным, а также питанию, курению, психоэмоциональному стрессу, приему алкоголя, лекарственных средств и изменениям микробиоты) в основном отводят роль триггеров реализации эффектов генетических факторов риска (ФР) развития аутоиммунных нарушений [8–13]. При этом изучению эффектов внешних факторов уделяют все больше внимания [14–19]. С генетической предрасположенностью связывают 30–60 % риска развития ревматоидного артрита (РА), а с влиянием факторов внешней среды — 40–70 %, причем величина их эффекта зависит от пола и возраста пациентов [20, 21]. Причинно–следственная связь с питанием более очевидна для других РЗ: например, связь приступов подагры с употреблением богатой пуринами пищи, развития остеоартрита коленных суставов — с увеличением массы тела. Но и при этих РЗ важную роль играют генетические факторы, сопутствующие болезни и фармакотерапия, тренированность мышц и пр. [5, 19].
Популярным в последние десятилетия стало использование различных диетических добавок, особенно содержащих витамины и микроэлементы: в 2000 г. в США их употребляла половина населения. Большая распространенность РЗ в этой стране — ими страдает каждая 12–я женщина и каждый 20–й мужчина — позволила получить эпидемиологические доказательства влияния приема таких добавок на развитие и исходы прежде всего РА [22, 23].
Основу доказательной базы эффектов факторов внешней среды при РЗ составляют результаты таких мощных обсервационных исследований, как Nurses’ Health Study (NHS), Sister Study Cohort, Iowa Women’s Health Study (IWHS), Melbourne Collaborative Cohort Study и др. Они предоставляют доказательства, касающиеся пищевых продуктов, компонентов, добавок и диет как ФР развития и исходов ряда НИЗ. Согласно принципам доказательной медицины (ДМ), эталоном оценки эффектов пищевых продуктов, компонентов, добавок, диет как вмешательств (при РЗ или в группах риска их развития) является проведение рандомизированных клинических исследований (РКИ) — разновидности интервенционных или экспериментальных исследований.
Анализ более чем 100 источников специальной литературы показал, что изучение роли питания при РЗ на принципах ДМ еще 15 лет назад ограничивалось обсервационными исследованиями, а в РКИ до сих пор получено немного доказательств. По мнению G. Keyβer (2018), это связано с необходимостью «непрерывного скрупулезного описания приемов пищи» с использованием специальных валидизированных опросников типа Food frequency questionnaire (FFQ) и последующей стратификацией пациентов [5].
Инструментарий оценки эффектов питания, апробированный при ряде НИЗ, включает такие шкалы и индексы, как Healthy Eating Index (HEI), Alternative Healthy Eating Index (AHEI — 2010), Dietary Inflammatory Index (DII), Mediterranean Diet Score (MDS) и пр. С их помощью в эпидемиологических исследованиях изучают и доказывают влияние питания на интегральные показатели здоровья — уровни смертности, заболеваемости и пр. На сегодня связь различных моделей питания с рисками развития и другими исходами доказана прежде всего для сердечно–сосудистых заболеваний (ССЗ) и некоторых форм рака [1, 24]. Полученные в последнее десятилетие доказательства связи хронического воспаления при РЗ с повышенным кардиоваскулярным риском [25, 26] позволили выдвинуть гипотезу о профилактическом и лечебном действии различных диет, пищевых компонентов, продуктов и добавок.
На сегодня триггерный потенциал диет, продуктов и компонентов питания лучше всего изучен при РА. Определенный вклад в это внесли результаты крупных исследований когорт американских медсестер круга Nurses’ Health Studies (NHS, NHS II, NHS III), полученные в 1976–2016 гг. [20, 27–32]. В них установлены сильная обратная связь продолжительности грудного вскармливания младенцев–девочек в течение ≥ 12 мес. с вероятностью развития у них РА во взрослом возрасте, ряд эффектов курения, употребления кофе и алкоголя в отношении риска развития РА, системной красной волчанки (СКВ) и т.д. С отсутствием грудного вскармливания в младенчестве связывают и повышенный риск заболевания СпА, но доказательства этого эффекта слабее, чем для РА [5].
В 2013 г. C.G. Parks и соавт. [33] опубликовали итоги Sister Study Cohort — исследования когорты более чем 50 тыс. белокожих женщин — жительниц США в возрасте 35–74 лет, инициированного Национальным институтом здоровья и экологии (National Institute of Environmental Health Sciences, NIЕHS). Они доказали значительное (на 50 %) повышение риска развития РА в связи с низким весом при рождении, небезопасным питанием (а именно — недоеданием) в детстве, низким качеством домашнего образования и в целом низким социально–экономическим статусом. При этом никакие продукты питания не были идентифицированы как ФР развития РА.
Ранее с учетом доказанного влияния 11 нутриентов и пищевых продуктов на риск развития основных НИЗ (ССЗ, некоторых форм рака и сахарного диабета 2–го типа) был предложен такой показатель качества питания, как альтернативный индекс здорового питания AHEI–2010. Здоровым питанием названо употребление овощей, фруктов, орехов, продуктов из цельного зерна, полиненасыщенных жирных кислот (ПНЖК), омега–3–ПНЖК и умеренное употребление алкоголя. Компонентами нездорового питания являются сладкие напитки (включая подслащенные фруктовые соки), насыщенные жиры, трансжиры, соль, красное и обработанное мясо.
Отмечая отсутствие исследований влияния качества питания на развитие аутоиммунных заболеваний, в 2017 г. Y. Hu и соавт. [20] оценили связь AHEI–2010 с риском развития РА и впервые установили, что плохое качество питания (низкий счет AHEI–2010, нездоровое питание) является ФР развития этой болезни. Источником доказательства стало проспективное сравнительное исследование женщин из двух когорт: NHS (n = 76 597) и NHSII (n = 93 392). На момент начала исследования возраст участниц 1–й когорты составил 30–55 лет, 2–й — 25–42 года, никто из них не страдал РА или другим заболеванием соединительной ткани. Каждые 2 года проводили сбор антропометрических данных и информации об образе жизни и воздействии факторов внешней среды. Первичными конечными точками были определены частота развития РА и его серовариантов. В ходе исследования диагноз РА установили у 1007 участниц. При этом у женщин в возрасте ≤ 55 лет более качественное питание (по сравнению с менее качественным, Q4 vs Q1) оказалось сопряжено с более низким риском развития РА: коэффициент опасности (hazard ratio, HR) составил 0,67, 95% доверительный интервал (95% ДИ) — 0,51–0,58. Эта ассоциация была более сильной для серопозитивного РА по сравнению с серонегативным (HR = 0,60; 95% ДИ 0,42–0,86). У женщин старше 55 лет связь риска развития РА с качеством питания не подтвердилась. Был сделан вывод о том, что нездоровое питание является ФР развития РА, особенно серопозитивного, у женщин в возрасте ≤ 55 лет.
Негативное влияние приема популярных в США витаминно–минеральных диетических добавок на здоровье отразили итоги Iowa Women’s Health Study (1986–2008). В этом обсервационном исследовании приняли участие 38 772 женщины, средний возраст которых на момент его начала составил 61,6 года. Информацию о приеме добавок они предоставляли трижды. Оказалось, что в 1986 г. хотя бы одну добавку ежедневно принимали 63 % опрошенных, в 1997 г. — 75 %, а в 2004 г. — 85 %, при этом 27 % женщин принимали ≥ 4 добавок. За весь период наблюдения умерло 40,2 % участниц исследования (n = 15 594). Анализ его результатов показал связь употребления поливитаминных добавок с повышением уровня смертности от всех причин. Как видно из табл. 1, особенно сильным оказался эффект медьсодержащих добавок: повышение абсолютного риска (absolute risk increasing, ARI) смерти достигло 18 %. По мнению J. Mursu и соавт. (2011) [22], наиболее вероятным было негативное влияние дополнительного приема железа, тогда как добавление кальция ассоциировалось со снижением риска смерти: показатель HR составил 0,91 (95% ДИ 0,88–0,94), снижение абсолютного риска (absolute risk reduction, ARR) — 3,8 %. Авторы указали, что в США именно пожилые женщины являются основными потребителями витаминно–минеральных добавок, безусловно полезных для здоровья при наличии установленного дефицита этих веществ. Они также отметили: 1) неоднородность имеющихся доказательств, в том числе метаанализов L. Bazzano и соавт. (2006) и G. Bjelakovic и соавт. (2007); 2) изученность в большинстве РКИ эффектов витаминов В, С, D, Е и кальция (а именно — наличие вреда или отсутствие такой пользы, как снижение риска смерти); 3) необходимость дальнейших исследований эффектов длительного приема добавок, содержащих поливитамины, железо и другие микроэлементы.
Курение. Следует подчеркнуть, что все исследования эффектов питания как ФР и вмешательства при РЗ должны учитывать статус курения пациентов. Результаты анализа имеющихся доказательств позволяют считать самой эффективной технологией первичной профилактики РА (а именно его наиболее неблагоприятного варианта — серопозитивного) полный отказ от курения [5, 30, 34–36]. В соответствии с принятой терминологией, представленной на веб–сайте Центра профилактики и контроля заболеваний (www.cdc.gov/nchs/nhis/tobacco/tobacco_glossary.htm; дата доступа: 07.07.2019), когда–либо курившим считается человек, выкуривший ≥ 100 сигарет. Биологические эффекты непродолжительного «социального» курения называют сомнительными.
В 2014 г. D. di Giusepe и соавт. [36] изучена зависимость риска развития РА от экспозиции к курению сигарет в метаанализе 10 обсервационных исследований, отобранных в компьютерных базах данных MEDLINE и EMBASE из публикаций 1966–2013 гг. По итогам метаанализа трех проспективных когортных и семи ретроспективных исследований типа «случай — конт–роль» (всего 4552 случая РА) установлено повышение риска развития РА у курильщиков по сравнению с никогда не курившими на 26 % при индексе курения 1–10 пачко–лет (относительный риск (ОР) 1,26; 95% ДИ 1,14–1,39) и двукратное — при индексе курения > 20. При индексе курения 21–30 пачко–лет ОР развития РА составил 1,94 (95% ДИ 1,65–2,27), при индексе курения > 40 — 2,07 (95% ДИ 1,15–3,73). Независимо от индекса курения повышенный риск развития РА, серопозитивного по ревматоидному фактору (РФ), был большим (ОР = 2,47; 95% ДИ 2,02–3,73), чем повышенный риск развития серонегативного РА (ОР = 1,58; 95% ДИ 1,15–2,18). Таким образом, оказалось, что даже незначительная экспозиция к курению повышает риск развития РА в течение жизни; этот риск максимален (вдвое больше, чем у никогда не куривших) при индексе курения > 20 пачко–лет, и дальнейшее увеличение дозы экспозиции не влияет на эффект.
Уже в 2019 г. X. Liu и соавт. [30] представили результаты проведенного ими анализа данных исследований Nurses’ Health Studies. Доказано следующее:
1) курящие женщины по сравнению с никогда не курившими имеют повышенный риск развития РА — на 47 % (HR = 1,47; 95% ДИ 1,27–1,72), особенно серопозитивного РА (т.е. с большей активностью болезни, тяжелых суставных деструкций и внесуставных проявлений) — на 67 % (HR = 1,67; 95% ДИ 1,38–2,01);
2) длительность периода отказа от курения является благоприятным ФР в отношении вероятности развития РА, прежде всего серопозитивного: бросившие курить > 30 лет назад имеют на 37 % меньший риск развития серопозитивного РА (HR = 0,63; 95% ДИ 0,44–0,90), чем отказавшиеся от табака в течение последних 5 лет. Но и бросившие курить давно (> 30 лет назад) по сравнению с никогда не курившими имеют умеренно повышенный риск развития РА (HR = 1,25; 95% ДИ 1,02–1,53) и серопозитивного варианта болезни (HR = 1,30; 95% ДИ 1,01–1,68);
3) доказана лишь тенденция связи длительности курения в прошлом с повышением риска развития РА;
4) в отличие от результатов метаанализа D. di Giusepe и соавт. (2014) влияние курения на риск развития серонегативного РА не подтвердилось (HR = 1,20; 95% ДИ 0,93–1,55).
Таким образом, вслед за установлением дозозависимого (кумулятивного) эффекта курения как ФР развития РА у генетически предрасположенных лиц совсем недавно был впервые доказан положительный профилактический эффект изменений поведения, а именно длительного (> 10 лет) устойчивого отказа от табака, в отношении снижения риска развития этой болезни. Доказательства были получены в итоге 38–летнего наблюдения группы жительниц США — всего 230 732, из которых у 1528 развился РА (серопозитивный в 63,4 % случаев). Сами авторы публикации критикуют валидность исследования — как внешнюю (т.е. возможность экстраполировать его результаты на общую популяцию с учетом смещенного характера выборки — преимущественно образованных женщин европеоидной расы), так и внутреннюю (с учетом 2–летних интервалов оценки статуса курения — не чаще). Остается слабой доказательная база влияния отказа от курения на исходы при установленном диагнозе РА: прекращая курить, пациенты могут снизить риски, связанные с заболеванием [30].
Итак, принимая во внимание тот факт, что курение является сильным ФР развития серопозитивного РА, при планировании, проведении и интерпретации результатов исследований, посвященных эффектам питания при этом РЗ, курение следует считать вмешивающимся, или мешающим, фактором (confounding factor), как и при других НИЗ (раке легкого и т.д.).
Ряд исследований влияния пищевых и других внешних факторов на исходы при РА уже проведен с учетом статуса курения. Примером является исследование эффектов употребления алкоголя H. Kallberg и соавт. (2009) [34]. Курение как мешающий ФР учтено и в одном из первых исследований эффектов употребления кофе, а именно — изучении M. Heliövaara и соавт. (2000) связи титра РФ в крови у 6809 пациентов, не имевших РА в анамнезе и на момент включения в это перекрестное исследование, с количеством чашек кофе, выпиваемых в сутки [37]. Многофакторный анализ выявил связь употребления кофе с риском развития серопозитивного РА: употребление ≥ 4 чашек в сутки сопровождалось двукратным увеличением риска по сравнению с употреблением меньших доз (ОР = 2,2; 95% ДИ 1,13–4,27). Этот эффект кофе был доказан в когорте мужчин и женщин (n = 18 981), включенных в исследование в 1973–1976 гг.; по состоянию на 1989 г. диагноз РА установили у 126 из них (0,7 %), часть серопозитивных составила 70,6 %.
В 2002–2003 гг. были опубликованы еще две статьи, представившие результаты исследований влияния кофе, декофеинизированного кофе, чая и кофеина на риск развития РА, проведенных в США. Цель работы T.R. Mikuls и соавт. (2002) [38] состояла в оценке употребления кофе, чая и кофеина как ФР дебюта РА у пожилых женщин. Это проспективное когортное исследование началось в 1986 г. и включило 31 336 женщин в возрасте 55–69 лет без РА в анамнезе; через 10 лет диагноз РА был установлен у 0,5 % участниц (n = 158). Результаты исследования показали более чем двукратное повышение риска развития РА при употреблении ≥ 4 чашек/сут декофеинизированного кофе по сравнению с неупотреблением этого напитка (ОР = 2,58; 95% ДИ 1,63–4,06). Женщины, выпивающие > 3 чашек чая в сутки, имели меньший риск развития РА по сравнению с теми, кто не пил чая (ОР = 0,39; 95% ДИ 0,16–0,97). Влияние «обычного» кофе и кофеина на развитие РА не подтвердилось. Полученные результаты подтвердил многофакторный анализ, в котором были учтены возраст, статусы курения, употребления алкоголя и гормонозаместительной терапии, возраст наступления менопаузы и семейное положение. Связь повышенного риска позднего дебюта РА с высоким уровнем употребления декофеинизированного кофе (ОР = 3,10; 95% ДИ 1,75–5,48) и чая (ОР = 0,24; 95% ДИ 0,06–0,98) оказалась более сильной у женщин с серопозитивным РА (ОР = 1,54; 95% ДИ 0,62–3,84), чем с серонегативным (ОР = 0,93; 95% ДИ 0,27–3,20). Вывод исследователей состоял в том, что у женщин, находящихся в постменопаузе, употребление декофеинизированного кофе является ФР развития РА, а употребление чая связано со снижением этого риска.
В 2003 г. представители медицинской школы Гарварда E.W. Karlson и соавт. [32] опубликовали итоги изучения ими эффектов этих же напитков (кофе, декофеинизированного кофе, чая) и кофеина как ФР развития РА по результатам исследования NHS 1980–1998 гг. В исследуемую когорту включили 121 701 женщину, но первичную анкету FFQ корректно заполнили лишь 68,3 % (n = 83 124), и в дальнейшем их опрашивали каждые 4 года. В течение 20 лет диагноз РА был установлен в 0,58 % случаев (n = 480). Итоги исследования показали отсутствие значимой связи употребления больших доз кофе (≥ 4 чашек/сут) — и обычного, и декофеинизированного — с уровнем заболеваемости РА, а также отсутствие кумулятивного эффекта употребления больших доз кофе и чая (> 3 чашек/сут) на риск развития РА по сравнению с неупотреблением этих напитков: ОР = 1,1 (95% ДИ 0,8–1,6) и 1,1 (95% ДИ 0,7–1,8) соответственно. Не выявили и связи суммарного употребления кофе и кофеина с повышенным риском развития РА.
Итак, эффекты употребления кофе, чая, декофеинизированного кофе и кофеина в отношении риска развития РА были оценены в 2000–2003 гг. в трех обсервационных исследованиях, проведенных в Финляндии и США, длившихся по 10–20 лет и включивших более 133 тыс. участников, в основном женщин. Полученные доказательства оказались гетерогенными.
Алкоголь. Информационный анализ показал, что у лиц, генетически предрасположенных к развитию РА, низкое и умеренное употребление алкоголя (1–5 доз/нед) улучшает прогноз, т.е. значительно снижает риск развития этой болезни [34], а именно серопозитивного РА [27, 39], и именно у женщин [14, 27]. При употреблении алкоголя в количестве > 10 г/сут (в пересчете на чистый спирт) его протективный эффект исчезает [27].
Отметим, что, в соответствии с рекомендациями Центра профилактики и контроля заболеваний (www.cdc.gov/alcohol/fact–sheets/alcohol–use.htm) и Всемирной организации здравоохранения (www.euro.who.int/ru/health–topic/disease–prevention/alcohol–use/do–you–drink–too–much–test–your–own–alcohol–consumption–with–the–audit–test; дата доступа: 07.07.2019), стандартной дозой (или порцией, единицей) алкоголя считают 10 г чистого спирта. Очень низким принято считать употребление алкоголя в количестве < 1 дозы/нед, умеренным — в количестве ≤ 1 дозы/сут для женщин и ≤ 2 дозы/сут для мужчин, достигших возраста 21 года, исключая беременных и подразумевая употребление алкоголя в отдельные дни недели, но не ежедневно. Стандартная доза алкоголя содержится примерно в 425 мл пива крепостью 2,7 %, 285 мл пива крепостью 4,8 %, 100 мл шампанского или вина крепостью 13 %, 60 мл вина крепостью 20 %, 30 мл крепкого алкогольного напитка (джина, рома, водки, виски). В США стандартной дозой (drink) считают 12 унций пива крепостью 5 % (т.е. 354 мл), 8 унций солодового ликера крепостью 7 % (237 мл), 5 унций вина крепостью 12 % (148 мл), 1,5 унции 40% чистого спирта, т.е. крепкого алкогольного напитка (44,4 мл).
В 2009 г. H. Kallberg и соавт. [34], изучив итоги двух исследований типа «случай — контроль» (EIRA и CACORA), установили связь между риском развития РА и употреблением алкоголя с учетом статуса курения и генетического фактора (носительства HLA–DRB1). Исследование EIRA было проведено в Швеции и включало 1204 случая и 871 контроль; исследование CACORA — в Дании, в нем приняли участие 444 больных РА и 533 пациента контрольной группы. В итоге H. Kallberg и соавт. обнаружили значительно большую распространенность употребления алкоголя в группах контроля, чем среди больных РА, и выявили дозозависимый эффект алкоголя в отношении снижения риска развития РА в обоих исследованиях. При сравнении рисков развития РА у потреблявших наибольшие и наи–меньшие дозы алкоголя, у первых наблюдали лучшие исходы: в EIRA показатель ОР составил 0,5 (95% ДИ 0,4–0,6), в CACORA — 0,6 (95% ДИ 0,4–0,9). Употребление алкоголя ассоциировалось со снижением риска развития РА, серопозитивного по антителам к циклическому цитруллинированному пептиду (АЦЦП), в основном у курильщиков — носителей аллелей HLA–DRB1.
На основании установления обратной связи употребления алкоголя и риска развития РА и принимая во внимание результаты экспериментальных исследований, авторы выдвинули гипотезу о протективном эффекте алкоголя в отношении развития РА и сделали вывод о значимости факторов образа жизни (отказа от курения, но не обязательно от употребления алкоголя) для снижения риска развития этого заболевания.
Через 4 года гипотезу H. Kallberg и соавт. поддержали результаты систематического обзора I.C. Scott и соавт. [39], а именно выявление обратной связи между употреблением алкоголя и риском развития АЦЦП–позитивного РА. Обзор провели с целью оценки эффекта употребления алкоголя в отношении развития РА с учетом количества, длительности приема и АЦЦП–статуса пациентов и с помощью метаанализа. Первоисточники искали в компьютерных базах данных MEDLINE и EMBASE, период поиска — 1946 — июль 2012 г. В итоге было отобрано девять обсервационных исследований: шесть исследований типа «случай — контроль» (3564 случая, 8477 контролей) и три когортных исследования (444 случая, 84 421 конт–роль). Такой показатель риска развития болезни, как отношение шансов (odds ratio, OR), у употребляющих алкоголь по сравнению с неупотребляющими составил 0,78 (95% ДИ 0,63–0,96). Эффект ограничился АЦЦП–серопозитивным РА (OR = 0,52; 95% ДИ 0,36–0,76), влияние алкоголя на риск развития серонегативного РА не подтвердилось (OR = 0,74; 95% ДИ 0,53–1,05). Авторы обзора считают необходимым усиление доказательной базы вывода о протективной роли употреб–ления алкоголя для снижения риска развития РА, а именно — проведение проспективных исследований АЦЦП–позитивных когорт.
Используя такой ресурс, как две крупные проспективные когорты круга Nurses’ Health Studies, B. Lu и соавт. (2014) [27] оценили риск развития РА в связи с употреблением алкоголя у женщин. В NHS, начатом в 1976 г., участвовали 121 701 пациентка, в NHSII, начатом в 1989 г., — 116 430. Их анкетировали каждые 2 года, что позволило установить влияние ряда факторов внешней среды и образа жизни; для оценки эффектов употребления алкоголя женщины каждые 4 года заполняли опросник FFQ. В 2008–2009 гг. количество больных РА в когортах оказалось следующим: в NHS — 580, в NHSII — 323. При употреблении алкоголя в количестве 5,0–9,9 г/сут показатель риска развития болезни HR составил 0,78 (95% ДИ 0,61–1,00), более сильная связь подтвердилась для серопозитивного РА (HR = 0,69; 95% ДИ 0,50–0,95). Кроме того, был выявлен благоприятный эффект употребления пива: женщины, употреблявшие его 2–4 раза в неделю, имели на 31 % меньший риск развития РА по сравнению с теми, кто пива не пил. Установив умеренно сильную связь длительного умеренного употребления алкоголя со снижением риска развития РА, B. Lu и соавт. считали необходимым усиление доказательной базы этого вывода.
В том же году Z. Jin и соавт. [14] опубликовали метаанализ восьми проспективных исследований влияния употребления алкоголя на риск развития РА. Мощность этого исследования отражает общее количество участников — 195 029, включая 1878 больных РА. Протективный эффект в отношении развития РА доказан для низкого и умеренного употребления алкоголя (ОР = 0,86; 95% ДИ 0,78–0,94), причем зависимость эффекта от дозы не является линейной. По сравнению с неупотреблением алкоголя ОР развития РА при употреблении его в дозе 3 г/сут составил 0,93 (95% ДИ 0,88–0,98), для 9 г/сут — 0,86 (95% ДИ 0,76–0,97), для 12 г/сут — 0,88 (95% ДИ 0,78–0,99), для 15 г/сут — 0,91 (95% ДИ 0,81–1,03), для 30 г/сут — 1,28 (95% ДИ 0,94–1,73). Анализ в подгруппах выявил снижение риска развития РА на 19 % у женщин, употреблявших алкоголь в низких и умеренных дозах. Независимо от пола длительное (в течение ≥ 10 лет) постоянное употребление алкоголя в таком количестве снижало риск развития РА на 17 %. Вывод авторов состоял в подтверждении протективного эффекта низкого и умеренного употребления алкоголя в отношении риска развития РА и зависимости этого эффекта от дозы, длительности употребления алкоголя и пола пациентов. По мнению Z. Jin и соавт., изучение в крупных проспективных исследованиях эффектов взаимодействия генов и факторов окружающей среды открывает перспективу установления этиологии РА.
В целом, по данным G.D. Kitas и соавт. (2011) [25], профилактическая эффективность умеренного употреб–ления алкоголя состоит в снижении риска развития и уровня заболеваемости серопозитивным РА, а терапевтическая — в незначительном снижении активности РА. Кроме того, M.J. Nissen и соавт. (2010) [40] наблюдали замедление прогрессирования суставной деструкции у больных РА мужчин, употреблявших алкоголь в количестве ≤ 1 дозы/сут в течение 4 лет; злоупотребление же алкоголем повышало активность болезни.
Как было отмечено выше, в когортах Nurses’ Health Studies установлена обратная связь умеренного употребления алкоголя с риском развития не только РА, но и СКВ, что объясняют противовоспалительным действием такого количества алкоголя. M. Barbhaija и соавт. (2017) [29] представили результаты проспективного наблюдения 204 055 участниц когорт NHS (период 1980–2012 гг.) и NHSII (1989–2011 гг.), не имевших заболеваний соединительной ткани и предоставивших сведения об употреблении алкогольных напитков (в том числе пива, вина, крепких напитков) на момент начала исследования. В дальнейшем они сообщали такие данные, заполняя полуколичественный опросник FFQ каждые 2–4 года. Частота развития СКВ в обеих когортах составила 0,12 % (125 случаев у женщин в возрасте 55,8 ± 9,5 года, 119 — в возрасте 43,4 ± 7,7 года). Результаты показали значительное снижение риска развития СКВ при употреблении алкоголя (в кумулятивной дозе ≥ 5 мг или 0,5 дозы в сутки) по сравнению с неупотреблением (HR = 0,61, 95% ДИ 0,41–0,91). Значительно меньший риск развития СКВ имели женщины, употреблявшие ≥ 2 порций вина в неделю, по сравнению с теми, кто не пил вина (HR = 0,65; 95% ДИ 0,45–0,96).
Отметим также связь повышенного риска развития РА с употреблением напитков с высоким содержанием фруктозы в молодом возрасте, выявленную L.R. DeChristopher и соавт. (2016) [41] по итогам исследования когорты 20–30–летних американцев.
Индекс массы тела (ИМТ), как и курение, изучается как сопряженный с питанием (а возможно, и мешающий) ФР развития и исходов некоторых РЗ. Ряд преимуществ имеют больные РА с избыточной массой тела (т.е. ИМТ 25–30 кг/м2), которую G. Keyβer (2018) [5] назвал оптимальной при этом заболевании. Во–первых, в дебюте РА избыточная масса тела сопряжена с вероятностью достижения ремиссии и замедления прогрессирования суставной деструкции [42]; во–вторых, риск развития ССЗ у больных РА с избыточной массой тела ниже, чем у больных с недостаточной массой тела [25]. Наличие же ожирения (ИМТ ≥ 30 кг/м2) является ФР развития РА [7], а у больных связано с большей активностью РА, выраженностью артралгий и количеством сопутствующих заболеваний [43]. Что касается эффектов недостаточной массы тела, а также ревматоидной саркопении, ревматоидной кахексии и метаболического синдрома, то они являются предметом ряда обсервационных исследований [16].
Пищевые и сопряженные с питанием ФР развития РА у курильщиков. Курильщики болеют РА чаще и тяжелее, чем некурящие [5, 35]. Значительный добавочный риск развития этой болезни у курящих связан с пищевыми факторами, особенно употреблением поваренной соли. В 2015 г. В. Sundstrom и соавт. [44] по итогам исследования типа «случай — контроль» установили двукратное повышение риска развития РА среди курящих, употребляющих 5,5 г/сут соли, по сравнению с риском развития РА у курящих, употребляющих 3,8 г/сут соли, и выявили связь этого эффекта с длительностью курения. Остается открытым вопрос, является ли соль самостоятельным (и вмешивающимся) ФР развития РА или же повышение риска развития РА связано с употреблением определенных сольсодержащих продуктов.
Повышенный ИМТ у некурящих сопряжен со снижением риска развития РА, а у курильщиков — со значительным повышением такого риска. В 2013 г. M.J. de Hair и соавт. исследовали когорту курящих [45]: оказалось, что кумулятивный риск развития РА в течение 2–3 лет у лиц с избыточной массой тела на 70 % больше, чем у лиц с ИМТ < 25 кг/м2.
Отметим также, что курение наряду с моделью питания, употреблением лекарственных средств и психоэмоциональным стрессом является фактором, влияющим на кишечную микробиоту.
Мясо, рыба, предпочитаемые продукты питания и риск развития РА. Представление о связи потребления красного мяса (говядины, свинины, дичи) с развитием РА широко распространено, однако информационный анализ подтверждает слабость доказательной базы этого утверждения.
В приведенном выше исследовании связи индекса AHEI–2010 и заболеваемости РА красное мясо было рассмотрено не как самостоятельный ФР, а как компонент нездорового питания, повышающего риск развития РА [20]. В литературе найдено немного доказательств прямого эффекта употребления красного мяса, причем сила этого эффекта оценена как слабая и неопределенная в когортных исследованиях 26 тыс. и 80 тыс. пациентов соответственно [46, 47]. Важно, что последние — участницы NHS — сообщали о своих пищевых привычках регулярно в течение более чем 20 лет.
Что касается употребления рыбы, то еще 15 лет тому назад британские ученые D.J. Pattison и соавт. (2004) [46] отмечали как однородность, последовательность доказательств положительного влияния употребления рыбьего жира на выраженность симптомов РА, так и отсутствие доказательств влияния содержащихся в рыбьем жире ПНЖК на риск развития этой болезни. Они указали на более легкое течение РА в Италии и Греции, где уровень потребления жирной рыбы, фруктов, овощей и оливкового масла значительно превышает таковой во многих других странах, а также на связь повышенной заболеваемости РА в Норфолке (Англия) с низким уровнем потребления овощей, фруктов и витамина С.
На сегодня доказательная база снижения риска развития РА при употреблении жирной рыбы считается слабой [5]. Повышенное же употребление более пост–ной (нежирной) рыбы сопровождается повышением такого риска. Впервые это установили M. Pedersen и соавт. (2005) [48] по результатам 5–летнего проспективного когортного исследования 57 тыс. пациентов, заполнявших специальную анкету FFQ. Результаты исследования сопоставили с данными Датского национального реестра пациентов, и оказалось, что диагноз РА имели 69 его участников (0,12 %). Важный итог этого исследования состоит в установлении снижения риска развития РА на 49 % при употреблении 30 г/сут рыбьего жира (в составе жирной рыбы, содержащей ≥ 8 г жира/100 г) и значительного повышения риска развития РА при употреблении менее жирной рыбы (содержащей 3–7 г жира/100 г). Не было выявлено связи между риском развития РА и употреблением фруктов, кофе, оливкового масла, мяса, длинноцепочечных жирных кислот, железа, цинка, селена, витаминов A, E, C и D. Авторы указали, что от низкой оценки роли пищевых факторов в развитии РА по итогам данного крупного когортного исследования их удержало небольшое количество участников, у которых развился РА. Была выдвинута гипотеза о влиянии более раннего (или большего) периода употребления некоторых компонентов пищи на риск развития РА и, соответственно, о необходимости более длительного наблюдения.
Итак, по современным представлениям, факторы внешней среды важны в развитии РА. Единственным установленным сильным ФР развития болезни (а именно — ее прогностически неблагоприятного АЦЦП–позитивного варианта у носителей определенного генотипа) до недавнего времени было курение. В ряде когортных исследований были получены доказательства влияния на риск развития РА употребления алкоголя и кофе. Проведенный нами информационный анализ показал, что полезные и вредные эффекты других пищевых продуктов, компонентов, привычек, диет и добавок в отношении рисков, связанных с РА, также являлись предметом научных исследований и дискуссий повсеместно и постоянно в течение последних 40 лет [4, 5, 49–52].
В Китае их изучали J. He и соавт. [52], представившие в 2016 г. итоги многоцентрового ретроспективного исследования связи предпочтительного употребления некоторых продуктов питания с заболеваемостью РА. С мая 2012 до сентября 2013 г. в это исследование типа «случай — контроль» включили более 2 тыс. участников, в том числе 968 больных РА. В группу контроля, сопоставимую с группой случаев по этническому происхождению, региону проживания, среднему возрасту и гендерному распределению, вошли 1037 здоровых лиц. Анкетирование участников («Употребляли ли вы продукты из данного перечня в течение недели, и если да, то в каком количестве?») позволило получить подробную информацию об их модели питания в течение 5 лет, предшествовавших дебюту РА (в группе случаев) или включению в исследование (в группе контроля). Перечень включал красное мясо, птицу, рыбу, овощи, картофель, фасоль, орехи, грибы, молоко и молочные продукты, яйца, фрукты, цитрусовые и др. Анализ результатов показал, что в течение 5 лет до дебюта РА пациенты употребляли гораздо меньше рыбы, птицы, фасоли, цитрусовых, молочных продуктов, грибов и потрохов, чем здоровые участники контрольной группы.
По итогам многофакторного анализа авторы установили ФР развития РА в китайской когорте: женский пол (OR = 2,4) и возраст > 50 лет (OR = 3,4 для 51–60–летних, 5,5 для 61–70–летних, 3,8 для лиц в возрасте ≥ 71 год) — и выявили прямую связь употребления картофеля и фруктов (кроме цитрусовых) с заболеваемостью РА. Более низкий риск развития РА ассоциировался с повышенным употреблением грибов, молочных продуктов и цитрусовых. Что касается красного мяса и овощей, то связи между уровнем их употребления и заболеваемостью РА в этой выборке не обнаружили; ожидаемый протективный эффект повышенного употребления рыбы и фасоли также не подтвердился (хотя была отмечена тенденция).
Учитывая гораздо более низкий уровень потребления красного мяса в Китае, чем в развитых западных странах, J. He и соавт. [52] отметили необходимость дальнейшего изучения эффектов этого пищевого фактора в проспективных исследованиях. Важным итогом исследования следует считать выдвижение научной гипотезы о связи развития РА с определенными пищевыми привычками (пристрастиями).
Отсутствие последовательных доказательств протективного эффекта употребления одних нутриентов и продуктов (высоких доз алкоголя, рыбы, нерафинированного оливкового масла, тушеных овощей и т.д.) и негативного эффекта других (красного мяса, сладких напитков) в отношении риска развития РА Hu Y. и соавт. (2017) [20] объясняют тем, что такие эффекты возможны лишь при сочетанном действии нескольких пищевых факторов.
Средиземноморская диета, ее модификация и риск развития РА. Средиземноморская диета подразумевает преобладание в рационе растительной пищи, овощей, фруктов, продуктов из цельного зерна, рыбы и морепродуктов при ограниченном употреблении красного мяса и молочных продуктов. Важным источником жиров является нерафинированное оливковое масло, важным источником углеводов — сухофрукты и мед. Несмотря на благоприятный метаболический эффект такого питания, подтвержденный экспертами Dietary Intervention Randomized Controlled Trial Group (DIRECT) [53], его влияние на риск развития РА не доказано [6, 7, 54]. Учитывая популярность взглядов на средиземноморскую диету как технологию первичной профилактики РА, C. Forsyth и соавт. (2018) [3] в систематическом обзоре отметили недостаточность доказательств в поддержку этой распространенной рекомендации.
E. Philippou и соавт. (2018) [7] пишут о возможной связи развития РА с западным типом питания, который характеризуется употреблением высококалорийной пищи, значительного количества насыщенных жиров, рафинированных углеводов и сахара, несбалансированным употреблением коротко– и длинноцепочечных жирных кислот, низким содержанием в рационе пищевых волокон и антиоксидантов. Этот риск повышается прямо (через поддержание воспаления) и опо–средованно (через развитие инсулинорезистентности и ожирения). Профилактический потенциал употреб–ления длинноцепочечных омега–3–ПНЖК — эйкозапентаеновой (ЭПК) и докозагексаеновой (ДГК) — Е. Philippou и соавт. связывают с их противовоспалительными свойствами. Опираясь на доказательства, ученые допускают, что со снижением риска развития РА может быть сопряжена приверженность «усиленной» средиземноморской диете — с повышенным употреблением жирной рыбы, низким употреблением сахара, поддержанием нормальной массы тела. Итогом дальнейших исследований они видят разработку более специфических рекомендаций по питанию для профилактики развития РА.
Витамины и микроэлементы как ФР развития РА. Влияние дополнительного употребления (в составе диетических добавок) некоторых витаминов и минеральных веществ на заболеваемость РА изучено на материалах 2 крупных исследований — обсервационного IWHS и интервенционного рандомизированного плацебо–контролируемого Women’s Health Initiative CaD trial. В итоге в IWHS доказан незначительный протективный эффект дополнительного приема цинка, а также b–криптоксантина — провитамина витамина А, содержащегося в цитрусовых, яблоках, физалисе и других растительных продуктах [22, 55, 56].
Целью исследования IWHS было изучение связи внутренних, пищевых и связанных с образом жизни факторов и частоты развития рака у пожилых женщин. После исключения некорректно заполнивших анкету по питанию и приему диетических добавок в 1986 г. дальнейшему наблюдению подлежали 38 772 участницы, в 1997 г. — 29 230, в 2004 г. — 19 124. В 1997 г. оценивали лишь сведения о добавках (но не о питании). Инструментом исследования были две валидизированные версии Гарвардского опросника FFQ, состав пищи оценивали с помощью специальных баз данных. Изучены эффекты 15 добавок, включая добавки витаминов А, В6, С, D, E, железа, кальция, селена, цинка (все в известных дозах), а также мультивитаминов, комплексов витаминов группы В, β–каротина, фолиевой кислоты, магния и меди. Эффекты холекальциферола и эргокальциферола отдельно не оценивались. В итоге наиболее популярными оказались добавки, содержащие кальций, поливитамины, витамины С, Е, и комплексные добавки на основе кальция (с поливитаминами, витамином С, поливитаминами и витамином С).
Характеризуя потребителей витаминно–минеральных диетических добавок (доля которых в структуре участниц IWHS за 18 лет увеличилась с 63 до 85 %), J. Mursu и соавт. (2011) [22] пишут, что в начале исследования они реже, чем непотребители, курили, жили в сельской местности и страдали сахарным диабетом и артериальной гипертензией. Эти женщины были более образованны и физически активны, имели меньший ИМТ и соотношение объема талии и бедер, чаще получали гормонозаместительную терапию. Привычное питание потребителей добавок было менее калорийным, содержало меньше насыщенных жиров, но больше белка, ПНЖК, углеводов, алкоголя, цельнозерновых продуктов, овощей и фруктов. Подобный паттерн наблюдали также в конце исследования и отдельно среди потребителей добавок, содержащих железо и кальций.
Известным итогом IWHS является подтверждение гипотезы о том, что прием диетических добавок не сопровождается снижением смертности от всех причин у пожилых женщин. Выводы J. Mursu и соавт. (2011) состояли, во–первых, в установлении связи приема популярных витаминно–минеральных добавок с повышенным уровнем общей смертности. Во–вторых, дополнительный прием железа оказался сильным ФР смерти от всех причин у пожилых женщин, в том числе не имеющих ССЗ, рака, сахарного диабета, на разных этапах 19–летнего периода наблюдения. Этот факт объяснили тем, что избыток железа катализирует реакции, в результате которых образуются оксиданты; также не исключали связь повышенной смертности с болезнями и травмами, приведшими к развитию анемии и назначению железа. В–третьих, был впервые доказан такой эффект приема добавок кальция, как снижение уровня общей смертности, но влияния дозы на эффект не наблюдали. Более ранний метаанализ проспективных исследований L. Wang и соавт. (2010) выявил тенденцию к снижению кардиоваскулярного риска в связи с приемом витамина D (HR = 0,9; 95% ДИ 0,77–1,05), но не кальция (HR = 1,14; 95% ДИ 0,92–1,41) [22].
Имеющиеся доказательства влияния дополнительного приема витамина D на заболеваемость РА непоследовательны: по итогам одного исследования сообщали о небольшом протективном эффекте [57], в других наблюдали увеличение частоты развития РА при повышенном употреблении этого витамина и кальция. В 2012 г. M. Racovan и соавт. [58] доложили о результатах крупного плацебо–контролируемого РКИ влияния на заболеваемость РА приема добавок, содержащих кальций и витамин D, в когорте женщин — участниц Women’s Health Initiative CaD trial (n = 36 282). Пациентки основной группы ежедневно принимали 1000 мг кальция карбоната и 400 МЕ витамина D3. По демографическим параметрам, уровням индивидуального потребления витамина D и солнечной экспозиции различий с группой плацебо не отмечалось. Анализ результатов проведен у 32 435 участниц без РА в анамнезе; в течение 5,1 года наблюдения этот диагноз был установлен у 163 (0,5 %) из них. В итоге связи уровня заболеваемости РА у женщин, находящихся в постменопаузе, с приемом добавок, содержащих кальций и витамин D, не наблюдали (HR = 1,04; 95% ДИ 0,76–1,41) и рекомендовали продолжить исследования эффектов (в том числе побочных) приема более высоких доз витамина D для первичной профилактики РА.
Диетические вмешательства у больных РА. По словам японского исследователя K. Masuko (2018) [16], применение при РА некоторых диет «может быть рассмотрено с учетом частых сопутствующих ССЗ… и в основном неопределенного модулирующего эффекта» таких вмешательств.
Среди прочих факторов важно учитывать исходно измененную кишечную микробиоту у больных РА, СпА, СКВ по сравнению со здоровыми людьми, а при синдроме Шегрена — также и микробиоты ротовой полости [9–13] и возможное нарушение ее состава при ограничении приема некоторых пищевых веществ и продуктов или их повышенном употреблении [7, 16].
В кокрановском обзоре и метаанализе K.B. Hagen и соавт. (2009) [59] обобщены результаты 14 РКИ различных диет, которых придерживались 837 пациентов с РА, и сделан вывод о наличии лишь нескольких фактов в пользу их эффективности. Критике подлежали малые размеры выборок и дизайн РКИ. Большое количество досрочно выбывших пациентов было расценено авторами обзора как результат развития нежелательных эффектов. Имеющаяся доказательная база не позволила рекомендовать ведение пациентов с активным РА на основе диетотерапии как альтернативы медикаментозной базисной терапии. Отмечена также неопределенность влияния диетических вмешательств при РА в долгосрочной перспективе.
Исследования питания как вмешательства при РА. Целью интервенционных исследований является выявление факта и оценка меры влияния нутритивных вмешательств (прежде всего диет) на активность РА. С другой стороны, добавление в рацион таких больных витаминов, микроэлементов, антиоксидантов может способствовать достижению цели лечения — клинической ремиссии/минимальной активности РА, и эффекты указанных диетических добавок тоже нужно изучать.
В течение последних 20 лет в когортах больных РА проведен ряд исследований эффектов элементарных, элиминационных (аглютеновой и пр.), веганских и вегетарианских диет [60–63]. Их методология исключает процедуру «ослепления» и предполагает основательное обучение, мотивированность участников и наличие систематических ошибок отбора (в смещенных выборках преобладают пациенты, настроенные на изменение своего питания), однако ни в одном таком исследовании не доказан стойкий эффект диет в отношении активности РА. Многие пациенты досрочно прекращают в них участие [62, 63], что, по мнению G. Keyβer (2018) [5], наглядно демонстрирует возможность существенного снижения качества жизни в результате вмешательств в привычное питание.
Анализируя ниже наличие и величину эффектов различных пищевых вмешательств при РА, установленных в интервенционных исследованиях, сошлемся на S. Petersson и соавт. (2018) [6], указавших на ограниченную валидность итогов таких испытаний в связи со сложностью их методологии.
Элементарные диеты представляют собой сокращение питания до употребления простейших компонентов — глюкозы, альбумина, эссенциальных аминокислот, витаминов и др. Теоретически такое питание обеспечивает элиминацию всех антигенов пищевых продуктов, которые являются триггерами артрита. В пилотном исследовании T. Podas и соавт. (2007) [64] были оценены эффекты элементарной диеты как двухнедельного вмешательства при РА, но субъективное улучшение (уменьшение боли и утренней скованности) не было стойким.
Элиминационные диеты как вмешательство и диагностический тест применяют в аллергологии для устранения симптомов и идентификации пищевого продукта, являющегося аллергеном, соответственно. После начала безаллергенного питания список разрешенных к употреблению продуктов постепенно расширяют, что позволяет определить продукт, усиливающий проявления РА. На практике больные порой отмечают усиление артралгий и отечности суставов после употребления некоторых продуктов с высокой индивидуальной вариабельностью — от мяса, молока и цитрусовых до кофе и сладостей [65, 66]. Несмотря на слабость доказательной базы эффектов элиминационных диет при РА, врачам многих европейских клиник рекомендовано обращать внимание больных на зависимость симптомов от меню и избегать употребления соответствующих продуктов [5].
Голодание, веганство, лактовегетарианство. 40 лет тому назад L. Sköldstam и соавт. (1979) [49] провели контролируемое исследование эффектов 7–10–дневного голодания с переходом на 9–недельную лактовегетарианскую диету у 16 больных РА. В контрольную группу вошли 10 больных РА, которые придерживались обычного питания. В итоге у 33 % участников основной группы наблюдали кратковременное улучшение клинических проявлений РА и лабораторных маркеров воспаления. В 1991 г. подобное исследование провели J. Kjeldsen–Kragh и соавт. [50]: 1–й этап состоял в 7–10–дневном голодании, 2–й этап — в 3–5 месяцах веганства и аглютеновой диеты, затем до года длился этап лактовегетарианства. Пациенты контрольной группы придерживались обычного питания. Как и в предыдущем исследовании, после периода голодания больные отмечали значительное уменьшение проявлений РА, и этот эффект сохранялся на последующих этапах. Отметим, что валидность результатов описанных исследований снижает нерепрезентативность выборок и несоответствие актуальным принципам ведения больных РА.
Наконец, в 2001 г. H. Müller и соавт. [67] издали систематический обзор, посвященный влиянию голодания и последующего питания по вегетарианской системе на исходы при РА. Ими подтвержден небольшой позитивный эффект голодания, длящегося не более двух недель, в отношении выраженности суставной боли.
Средиземноморская диета и ее модификация. В литературе часто цитируют исследование L. Sköldstam и соавт. (2003) [68], посвященное влиянию средиземноморской диеты на активность РА. У больных, питавшихся по этой системе в течение 12 нед., наблюдали тенденцию к снижению активности РА, но эффект не был статистически значимым и уступал базисной терапии. В последующие 15 лет были получены результаты еще четырех меньших контролируемых исследований, их систематического обзора и метаанализа C. Forsyth и соавт. (2018) [3]. Итоги двух интервенционных исследований доказали положительный эффект средиземноморской диеты на выраженность боли и качество жизни, связанное с заболеванием; еще одно исследование доказало влияние диеты на активность РА (снижение индекса DAS28). Авторы обзора сделали вывод о пользе применения средиземноморской диеты при РА, состоящей в уменьшении суставной боли и улучшении функций.
Другие эксперты [5, 20] считают, что благоприятное влияние на исходы при РА оказывает повышенное употребление отдельных компонентов средиземноморской диеты. В 2018 г. подведены итоги трех конт–ролируемых исследований этого вопроса: выявлена обратная корреляция активности РА с уровнем потребления рыбы [69] и с содержанием мононенасыщенных жирных кислот в ежедневном рационе [70]. Изданный в конце прошлого года литературный обзор S. Petersson и соавт. [6] содержит вывод о небольшом количестве исследований эффектов средиземноморской диеты при РА и наличии большего количества и более качественных доказательств благоприятных клинических эффектов дополнительного приема ПНЖК. Этому выводу вторят G. Keyβer (2018) [5], E. Philippou и соавт. (2018) [7] и др.
Прошедший 2018 год интересен изданием ряда несистематических обзоров литературы: 1) доказательств роли питания в развитии РА и рекомендаций по снижению риска развития РА у предрасположенных лиц — E. Philippou и соавт. [7]; 2) эффектов питания, употребления никотина и алкоголя при РА — Y. Grygielska и соавт. [4]; 3) данных, касающихся предполагаемой связи поступающих с пищей углеводов, кишечной микробиоты и патогенеза РА — K. Masuko [16].
Говоря о неопределенном модулирующем действии питания и повышенном риске развития ССЗ при РА, K. Masuko (2018) [16] указывает на необходимость –изучения эффектов низкоуглеводной диеты у таких больных и предлагает рекомендовать им сбалансированное питание с адекватным содержанием углеводов, особенно пищевых волокон, информируя о важности такого питания для поддержания симбиоза кишечной флоры, что может предотвратить развитие аутоиммунного процесса. На рис. 1 представлена схема взаимодействия питания, кишечной микробиоты и иммунного ответа при РА. Известно, что питание и другие внешние факторы (курение, психоэмоциональный стресс, прием лекарственных средств) влияют на состав кишечной микробиоты человека, а та, в свою очередь, регулирует местные и системные иммунные реакции. Недостаточное или неадекватное питание или потребление углеводов (как источников энергии и пищевых волокон) может опосредованно, через микробиоту, влиять на уровень физической активности, метаболизм и иммунные реакции, что приводит к развитию у больных РА инсулинорезистентности, саркопении, ожирения или кахексии.
Все больший интерес вызывает болезнь–модифицирующий потенциал питания. Получены данные о влиянии микробиоты ротовой полости и толстой кишки на цитруллинирование белков [11], о преобладании энтеротипа Prevotella у приверженцев диеты, богатой углеводами [71], — именно этот микроб выглядит значимым в патогенезе РА [72], и именно с угнетением индуцированного Prevotella воспаления связывают протективный эффект омега–3–ПНЖК [73]. Напротив, повышенное употребление белков и жиров животного происхождения сопряжено с преобладанием Bacteroides в составе кишечной микробиоты [16].
Информационный анализ показал, что в последние годы ученые уделяли особое внимание оценке болезнь–модифицирующего потенциала применения при РА средиземноморской и вегетарианской диет, а также полифенолов и омега–3–ПНЖК. Однако значимый вклад этих диет и веществ не был доказан. В пользу рекомендации больным РА придерживаться определенной диеты приводят довод о высоком риске развития метаболического синдрома (вследствие гиподинамии, усиленного катаболизма, накопления жира, развития саркопении и ревматоидной кахексии и в связи с персистирующим воспалением и повышенным содержанием провоспалительных цитокинов). Применение базисных противоревматических средств может значительно уменьшить этот риск, но даже в случае эффективной фармакотерапии у больных РА должна быть рассмотрена соответствующая диета.
Говоря о практических рекомендациях по питанию для больных РА, эксперты советуют также учитывать трудности, которые те испытывают при приготовлении и приеме пищи, в связи с болью и ограничением подвижности.
Диетические добавки при РА. Употребление диетических добавок широко распространено, его относят к ведению более здорового образа жизни, и в исследовании IWHS на нем не отразилось даже возникновение случаев рака у пожилых женщин в течение 19–летнего периода наблюдения [22]. Как указано выше, особый интерес представляют эффекты приема омега–3–ПНЖК у больных ревматологического профиля. Их доказательную базу при РА составляют 3 систематических обзора с метаанализами [74–76].
Поступление в организм незаменимых длинноцепочечных омега–3–ПНЖК — ДГК (цервоновой кислоты) и ЭГК (тимнодоновой кислоты) — необходимо для синтеза противовоспалительных веществ. При РЗ противовоспалительный эффект этих кислот реализуется через воздействие на рецепторы активатора пролиферации пероксидаз [16, 77] и подавление индуцированного Prevotella воспаления [73].
ДГК входит в состав липидов большинства животных тканей; в большом количестве ее содержат жир лосося и атлантической сельди, зоопланктон, морские моллюски и микроводоросли. ЭГК богаты жирная морская рыба (сельдь, скумбрия, лосось), сардины, печень трески, морские моллюски и грудное молоко. Известно, что употребление рыбы не может обеспечить поступление этих ПНЖК в количестве, достаточном для терапевтического эффекта, поэтому обычно их принимают в виде капсул рыбьего жира. Другими важными источниками ДГК и ЭГК в рационе являются орехи, растительные масла и семена [78, 79].
Эффективность приема ДГК/ЭГК в дозе ≥ 2,7 г/сут в течение 3–6 мес. доказана R.G. Goldberg и соавт. (2007) [74] в кокрановском метаанализе 17 исследований, в которых приняли участие 823 пациента с РА. Позитивный эффект добавления этих ПНЖК состоял в уменьшении утренней скованности и потребности в нестероидных противовоспалительных средствах (НПВС).
НПВС–сберегающий эффект омега–3–ПНЖК, принимаемых в дозе ≥ 2,7 г/сут в течение ≥ 3 мес., подтвержден в метаанализе Y.H. Lee и соавт. (2012) [75], причем все 10 РКИ–первоисточников были гомогенными. Отметим небольшую мощность этого метаанализа (183 больных РА получали добавки омега–3–ПНЖК, 187 — плацебо), отбор первоисточников лишь в 2 компьютерных базах данных ДМ (MEDLINE и CENTRAL), а также отсутствие доказанного влияния приема омега–3–ПНЖК на утреннюю скованность, количество болезненных и припухших суставов и их функцию.
В 2015 г. S.M. Proudman и соавт. [80] оценили эффекты применения при РА различных доз омега–3–ПНЖК — высоких (> 5,5 г/сут) и низких (0,4 г/сут). Количество пациентов, достигших ремиссии или не нуждавшихся в эскалации терапии, оказалось значительно большим среди принимавших высокие дозы этих кислот.
В 2018 г. A. Gioxari и соавт. [76] издан систематический обзор и метаанализ исходов применения омега–3–ПНЖК у больных РА. В 20 первичных РКИ, отобранных в PubMed, EMBASE и Scopus, показана эффективность трехмесячного перорального приема этих кислот или рыбьего жира (как их источника) в отношении снижения уровня маркеров активности РА и улучшения липидного профиля. От метаанализа Y.H. Lee и соавт. (2012) данное исследование отличается не только ресурсами поиска, но и большей мощностью: в него вошли 717 больных РА, получавших омега–3–ПНЖК, и 535 пациентов, получавших плацебо. В итоге A. Gioxari и соавт. впервые доказан благоприятный эффект добавления омега–3–ПНЖК на липидный профиль пациентов с РА и содержание лейкотриена В4 и подтверждено влияние употребления этих кислот на лабораторные маркеры активности РА, несмотря на в целом низкое качество доказательств.
Статистическая значимость и последовательность доказательств противовоспалительных и метаболических эффектов дополнительного приема омега–3–ПНЖК при РА подвергается критике [5, 16, 80]; эксперты поддерживают необходимость проведения плацебо–контролируемых РКИ. Обращают внимание и на то, что длительный прием высоких доз ПНЖК у больных РА может сопровождаться развитием кровотечений, а избыточное потребление жира — увеличением калоража и несбалансированностью рациона, что может повлиять на течение иммунных реакций и важные для здоровья исходы.
Говоря об ограниченных перспективах производства капсул рыбьего жира как источника высоких доз –омега–3–ПНЖК, в том числе для эффективной адъювантной терапии в ревматологии, приведем цитату G. Keyβer (2018): «В условиях чрезмерного вылова океанической рыбы экологически приемлемой альтернативой является использование других ресурсов ПНЖК» [5], а именно — очищенных липидных экстрактов моллюсков и растительных масел.
Микроэлементы, витамины, антиоксиданты. В ряде работ [5, 81, 82] отмечена необходимость достаточного поступления железа с пищей у больных РА в связи с высокой вероятностью развития у них железодефицита. Несмотря на распространенность дефицита селена и цинка при РА, благоприятный эффект добавления этих микроэлементов на активность заболевания не доказан. Разочаровывают и результаты исследований эффектов комплексных диетических добавок, содержащих кверцетин, альфа–липоевую кислоту, линоленовую кислоту, витамин С, железо, цинк и селен: их применение не влияло на такие маркеры активности РА, как количество болезненных и припухших суставов и уровень С–реактивного белка (СРБ).
Следует помнить и о том, что прием витаминов и микроэлементов у больных РА может быть сопряжен с повышенным риском серьезных ПЭ. Кроме итогов исследования IWHS, известен результат метаанализа E.R. Miller и соавт. (2005) [83] 19 исследований, посвященных эффектам добавок витамина Е: доказано повышение уровня смертности от всех причин при его употреблении в дозах ≥ 150 МЕ/сут. Что касается витамина D, то G. Keyβer (2018) называет его добавление «бесспорно необходимым… в соответствии с имеющимися рекомендациями по профилактике и лечению остеопороза» [5]. Известно, что риск развития остеопороза и его осложнений при РА и других системных РЗ повышен, как и риск развития железодефицита.
Принимая во внимание доказанность связи сывороточного содержания витамина D с наличием и активностью ряда РЗ в основном в обсервационных исследованиях, A.S. Franco и соавт. (2017) [84] впервые провели систематический обзор РКИ этого вопроса. Поиск РКИ, в которых витамин D или его аналоги применяли при РЗ в течение ≥ 3 мес., был осуществлен в основных компьютерных базах данных ДМ (Cochrane library, MEDLINЕ, EMBASE), а также в компьютерных базах данных LILACS и CINAHL. Из 668 первоисточников отобрано девять, включая пять РКИ, посвященных эффектам витамина D при РА, три — при СКВ, одно — при системной склеродермии; в метаанализ включено семь из них. Результаты метаанализа доказали благоприятное влияние достаточного употребления витамина D на содержание специфических антител при СКВ и, возможно, на частоту рецидивов РА. У больных РА добавление витамина D сопровождалось небольшой редукцией частоты рецидивов (разница рисков составила –0,10; 95% ДИ — от –0,21 до 0,00), но на выраженность боли и индекс DAS28 это вмешательство не повлияло. У больных СКВ прием витамина D был сопряжен с существенным снижением уровня антител к нДНК (разница рисков –0,10; 95% ДИ от –0,18 до –0,03). Авторы считают необходимыми подтверждение и оценку величины этих и других эффектов приема витамина D при РЗ в дальнейших исследованиях.
Подагра. Доказательства влияния на частоту и риск развития подагры таких факторов, как употребление алкоголя и безалкогольных напитков, получены в последнее десятилетие. Ранее эффекты алкоголя, оцененные в обсервационных исследованиях, не были однородными. В 2013 г. M. Wang и соавт. [85] опубликовали метаанализ 17 исследований (общее количество участников — 42 924), доказавший двукратное повышение риска развития подагры у потребителей высоких доз алкоголя по сравнению с трезвенниками и теми, кто употреблял алкоголь редко (ОР = 1,98; 95% ДИ 1,52–2,58). Зависимость этого эффекта от дозы отражена в табл. 2. Именно метаанализ подтвердил, что употребление алкоголя является ФР развития подагры. Отметим, что низкие и умеренные дозы алкоголя не оказывают протективного влияния на развитие подагры (в отличие от РА и СКВ).
Представляют интерес научные факты, установленные в Канаде H.K. Choi и соавт. (2007) [86]. В течение 12 лет они наблюдали 45 869 мужчин, не страдавших подагрой на момент начала исследования, и каждые 4 года с помощью опросников FFQ оценивали употреб–ление ими кофе, декофеинизированного кофе, чая и кофеина. В ходе этого проспективного исследования диагноз подагры был установлен у 757 (1,7 %) участников. Полученные результаты подтвердили благоприятный эффект длительного употребления кофе (в дозах ≥ 4 чашек/сут, а декофеинизированного — 1–3 чашек/сут) в отношении риска развития подагры. Рассчитаны следующие показатели ОР: при неупотреб–лении кофе — 1,00, при употреблении кофе < 1 чашки/сут — 0,97, 1–3 чашек/сут — 0,92, 4–5 чашек/сут — 0,60 (95% ДИ 0,41–0,87), > 6 чашек/сут — 0,41 (95% ДИ 0,19–0,88). Показатели ОР развития подагры в зависимости от суточной дозы декофеинизированного кофе: при неупотреблении — 1,00, при употреблении < 1 чашки/сут — 0,83, 1–3 чашек/сут — 0,67 (95% ДИ 0,54–0,82), ≥ 4 чашек/сут — 0,73 (95% ДИ 0,46–1,17). Как и в случае РА [32], суммарное употребление кофеина на риск развития подагры не влияло.
Основой ведения пациентов с установленным диагнозом подагры в рекомендациях Европейской противоревматической лиги (EULAR, 2006), Американской коллегии ревматологов (ACR, 2012), Немецкого общества врачей общей практики и семейной медицины (DEGAM, 2009), Немецкого ревматологического общества (DGRh, 2017) и других признана модификация образа жизни, потенциально обеспечивающая снижение сывороточного содержания мочевой кислоты (сМК) на 10–15 %. Она предполагает модификацию фармакотерапии (отмену диуретиков, салицилатов, циклоспорина А, b–адреноблокаторов; предпочтительное применение лозартана, фенофибрата, антагонистов кальциевых каналов) и модификацию питания (ограничение употребления продуктов, богатых пуринами, — жареного мяса, шпрот, сельди, сардин, морского языка, пива, других алкогольных и фруктозосодержащих напитков; увеличение употребления молочных продуктов, вишни, кофе, витамина С), а также достаточное употребление жидкости, медленное снижение массы тела и умеренную физическую активность. При этом в 2017 г. эксперты DGRh подтвердили отсутствие клинических исследований эффектов употребления мяса и алкоголя в популяции пациентов с подагрой [87].
Проведенный нами информационный анализ показал, что результаты модификации образа жизни при подагре отражены в трех кокрановских обзорах [88–90].
В обзоре J.H. Moi и соавт. (2013) [88] у больных подагрой впервые изучены эффекты вмешательств по изменению образа жизни. Поиск первоисточников проведен авторами в основных компьютерных базах данных ДМ (CENTRAL, MEDLINE и EMBASE; до 05.04.2013) и среди резюме EULAR и ACR 2010–2011 гг. Были отобраны РКИ и квазирандомизированные исследования, в которых эффекты изменения образа жизни сравнивали с эффектами другого лечения (активного или плацебо). Планировали оценить влияние вмешательств на следующие исходы: частота приступов подагры, выраженность артралгии, уровень сМК, размер тофусов, функция суставов, качество жизни и ПЭ. В итоге в обзор включили лишь одно РКИ (120 участников–мужчин в возрасте 50–60 лет с тяжелой подагрой, риск систематической ошибки умеренный). В течение 3 мес. пациенты основной группы получали обезжиренное сухое молоко, обогащенное гликомакропептидом SMP/GMP/G600, пациенты двух конт–рольных групп — необогащенное сухое молоко или порошок лактозы. В результате: 1) частота приступов подагры и выраженность артралгий уменьшились во всех группах; 2) доказательства низкого качества показали сходство групп и по развитию ПЭ — чаще всего желудочно–кишечных, в том числе приведших к госпитализации. О влиянии вмешательств на уровень сМК, регресс тофусов, функцию суставов и качество жизни в данном РКИ не сообщалось. Авторы обзора указали на недостаток наилучших доказательств из РКИ для поддержания или отклонения вмешательств по изменению образа жизни при подагре, несмотря на наличие хороших доказательств связи различных факторов образа жизни с повышенным риском развития подагры, полученных в обсервационных исследованиях.
Два месяца спустя описанное исследование вошло в кокрановский обзор M. Andrés и соавт. (2014) [89], в котором была дана оценка эффективности и безопас–ности применения диетических добавок у взрослых, больных хронической подагрой. Первоисточники также отбирали без ограничений по языку публикации — в MEDLINE, EMBASE, CINAHL и среди резюме EULAR и ACR (2010–2013). Были отобраны РКИ и квазирандомизированные исследования, в которых эффект применения диетических добавок сравнивали с эффектами их неприменения, применения плацебо, других добавок или лекарственных средств. В состав диетических добавок входили аминокислоты, антиоксиданты, незаменимые микроэлементы, ПНЖК, пребиотики, пробиотики, витамины и другие вещества. Основными конечными точками были уменьшение частоты приступов подагры и выход пациентов из исследований из–за развития ПЭ. Учитывали и такие исходы, как снижение выраженности боли, связанное с болезнью качество жизни, нормализация уровня сМК, функция суставов, регресс тофусов, частота серьезных ПЭ.
В обзор вошло 2 РКИ, всего включавших 160 пациентов, из них 120 участников РКИ эффектов обогащенного гликомакропептидом обезжиренного сухого молока (см. выше) и 40 участников РКИ эффектов витамина С по сравнению с аллопуринолом и комбинацией аллопуринола и витамина С. Исследования различались валидностью (во 2–м объем выборки меньше, но репрезентативность лучше, вероятность систематической ошибки больше) и основными конечными точками (во 2–м это был уровень сМК). Результаты 2–го РКИ показали меньшее снижение уровня сМК при применении витамина С по сравнению с аллопуринолом (низкое качество доказательств) и хорошую переносимость этой добавки. Вывод M. Andrés и соавт. был следующим: «Несмотря на широкое применение диетических добавок при подагре, данный обзор демонстрирует малочисленность релевантных доказательств высокого качества».
Положительные и побочные эффекты снижения веса у больных подагрой с избыточной массой тела и ожирением оценены в кокрановском обзоре S.M. Nielsen и соавт. (2017) [90]. Поиск исследований, в которых –изучали эффекты снижения веса у таких пациентов, проведен авторами в шести компьютерных базах данных ДМ, при этом оценен риск систематических ошибок и качество доказательств, и в итоге из 3991 первоисточника отобрано лишь 10, среди которых одно РКИ. С отсутствием вмешательств сравнивали такие вмешательства, как диетотерапия (в сочетании с физической нагрузкой и без нее), бариатрическая хирургия, применение диуретиков и метформина. Анализ первичных исследований показал, что потеря веса их участниками составляла от 3 до 34 кг, снижение уровня сМК — от 30 до 168 мкмоль/л, целевого уровня сМК 360 мкмоль/л достигали от 0 до 60 % пациентов. Уменьшение частоты обострений подагры при снижении веса наблюдали в 75 % (6 из 8) исследований, при этом в двух исследованиях выявили зависимость эффекта от дозы (частота обострений подагры коррелировала со снижением уровня сМК и достижением целевого показателя). В краткосрочной перспективе после бариатрических хирургических вмешательств по поводу ожирения наблюдали тенденцию к повышению уровня сМК и частоты приступов подагры. Итоги обзора следующие: 1) доказана польза снижения веса у больных подагрой с избыточной массой тела и ожирением; 2) определено невысокое качество доказательств (в отношении снижения уровня сМК и приступов подагры — низкое, в отношении достижения целевого уровня сМК — среднее) и в целом слабость доказательной базы (лишь несколько обсервационных исследований низкого методологического качества); 3) указана срочная необходимость инициировать проведение проспективных исследований, предпочтительно РКИ.
Итак, влияние качества питания, употребления определенных пищевых продуктов и алкоголя на риск развития РЗ доказано прежде всего для РА и подагры, в меньшей мере — для СпА и СКВ. Сильным ФР развития РА у предрасположенных лиц является курение, а избыточное употребление соли и повышенный ИМТ увеличивают этот риск. Современная наука располагает доказательствами влияния ряда диет на исходы при РА. Качество большинства контролируемых исследований и влияние таких вмешательств на качество жизни пациентов подвергается критике экспертов, которые все же предлагают работникам здравоохранения пропагандировать средиземноморскую диету среди больных РА, учитывая ее благоприятное влияние на кардиоваскулярный риск. По мнению G. Keyβer (2018) [5], пациентам с избыточной массой тела и стабильным течением РА можно рекомендовать краткосрочное голодание. С учетом влияния на иммунные, метаболические нарушения и кишечную микробиоту при РА научно обоснована целесообразность применения диеты, сбалансированной по углеводам (Masuko K., 2018) [16].
Говоря о сопряженных с питанием внешних ФР развития и исходов РЗ, перейдем к доказанным эффектам микробиоты и ее коррекции при этих болезнях. Известно, что триггерная и модулирующая роль микробиоты ротовой полости и кишечника в развитии иммунных реакций установлена и подтверждена экспериментально [9]. Именно на иммуномодулирующих свойствах основаны попытки применения для адъювантной терапии РЗ пробиотиков и пребиотиков [10–12].
Пробиотиками называют живые микроорганизмы, которые, поступая в организм в достаточном количестве, оказывают благоприятные для здоровья эффекты. Дольше других пробиотиков используют лактобактерии (большую доказательную базу имеет и их применение при РА), а также применяют бифидобактерии, B.clausii, дрожжи и т.д. Существует ряд форм применения пробиотиков: 1) в составе обогащенных ими продуктов питания; 2) как диетические добавки; 3) как лекарственные средства.
Научные исследования эффектов пробиотиков при хронических воспалительных заболеваниях проводят с тех пор, как стала очевидна сопряженность РА, СпА и других РЗ с патологическими изменениями кишечной микрофлоры [10, 15, 91, 92]. Роль кишечной микробиоты является значимой также в патогенезе СКВ, синдрома Шегрена [13] и подагры [93].
Отмечая практически повсеместную (в США, Китае, Финляндии) распространенность дисбиоза кишечника у больных РА, японские ученые Y. Maeda и соавт. (2016) [9] допускают, что результаты современных лабораторных исследований применения пробиотиков и пребиотиков дают надежду на новую терапевтическую и профилактическую стратегию при этом заболевании. Эту гипотезу поддерживают Y. Kang и соавт. (2017) [10]: «Пероральный прием пробиотиков и пребиотиков при РА можно рассматривать как терапевтический подход. Однако релевантные научные исследования только начаты, и имеющиеся доказательства ограниченны». Доказательная база эффектов пробиотиков при РА описана A. Schorpion и соавт. (2017) [11]: «Клинические исследования характеризуются небольшими выборками и небольшой длительностью наблюдения… их конечные точки различны, а клиническое значение результатов не определено. Тем не менее использование пребиотиков и пробиотиков как средств адъювантной терапии аутоиммунных заболеваний теоретически обосновано».
Эффекты применения пробиотиков при СпА оценены K. Jenks и соавт. (2010) [94] в небольшом плацебо–контролируемом РКИ (63 участника), проведенном в Новой Зеландии. Использованы шкалы BASDAI, BASFI, MASES, ASAS, ASQoL, DISQ; доказано отсутствие позитивного влияния Streptococcus salivarius, Bifidobacterium lactis и Lactobacillus acidofillus.
Клинические исследования пробиотиков проведены в последнее десятилетие и при других РЗ, но основной массив доказательств накоплен при РА [95–100], и эти эффекты неоднозначны.
В частности, в 2011 г. L. Pineda Mde и соавт. (Канада) [95] представили результаты пилотного трехмесячного двойного слепого плацебо–контролируемого РКИ, в котором участвовали 29 пациентов со стабильным течением РА, не принимавшие глюкокортикоиды в ходе исследования и в течение месяца до включения в него. 15 пациентов принимали per os капсулы, содержащие лактобактерии L.rhamnosus GR–1 и L.reuteri RC–14; в группу контроля вошли 14 пациентов. В итоге в группе контроля выявили более значимые изменения уровня цитокинов; эффект приема пробиотика был сопоставим с плацебо и состоял в улучшении функционального статуса и качества жизни (оцененного с помощью опросника HAQ).
В 2014 г. обнадеживающие результаты применения пробиотика как средства адъювантной терапии при РА были получены в Иране [96, 97] по итогам 8–недельного двойного слепого плацебо–контролируемого РКИ эффектов перорального применения капсул, содержащих L.casei 01, в дозе не менее 108 КОЕ/сут. Были исследованы 46 женщин в возрасте 20–80 лет с ИМТ < 40 кг/м2 и диагнозом РА, установленным не менее чем за год, со стабильным течением болезни не менее 3 мес. до включения в РКИ. Пациентки основной группы получали капсулы, содержащие L.casei 01. В итоге у них наблюдали более выраженное снижение активности РА (оцененной по индексу DAS28) и более выраженное благоприятное изменение цитокинового профиля (снижение уровня TNFa, IL–6 и IL–12 в крови, но не IL–1b; повышение уровня IL–10 и соотношения IL–10/IL–12), чем у получавших плацебо (капсулы, содержащие мальтодекстрин).
В работе других иранских ученых, B. Zamani и соавт. (2016) [98], проведена оценка влияния пробиотика на клинический и метаболический статус больных РА. В 8–недельном двойном слепом плацебо–контролируемом РКИ приняли участие 60 пациентов в возрасте 25–70 лет. Пациенты основной группы ежедневно принимали per os капсулы, содержащие три живых лиофилизированных штамма лакто– и бифидобактерий: L. acidophillus, L. casei и B. bifidum, каждый в дозе 2 ´ 109 КОЕ/сут. Пациенты контрольной группы получали капсулы, содержащие целлюлозу. Результаты показали эффективность применения данного поликомпонентного пробиотика в комплексном лечении больных РА: у них наблюдали более значимое по сравнению с плацебо уменьшение индекса DAS28, индекса HOMA–B, уровня инсулина и высокочувствительного СРБ (вчСРБ) в крови.
Снижение уровня вчСРБ у больных РА при пер–оральном приеме капсул монокомпонентного пробиотика, содержащих L. casei, установили B. Alipour и соавт. (2014) [96]. Клиническая значимость этих метаболических эффектов пробиотиков требует уточнения в дальнейших исследованиях.
Наконец, эффективность пробиотиков как адъювантной терапии при РА оценена в систематическом обзоре и метаанализе A.T. Mohammed и соавт. (2017) [99]. В девяти компьютерных базах данных ДМ были отобраны девять первичных исследований (всего 361 участник). У пациентов, получавших пробиотик, отмечали более низкий уровень IL–6 в крови, чем у получавших плацебо, но разницы между группами по активности РА (индексу DAS28) не наблюдали. Авторы пришли к выводу о необходимости новых исследований эффектов пробиотиков при РА для подтверждения их клинической значимости.
Несколько иные результаты получены S.M. Aqaeinezhad Rudbane и соавт. (2018) [100] в метаанализе 4 РКИ, цель которого также состояла в сравнении эффектов применения пробиотиков и плацебо у больных РА. Общую когорту участников составили 153 пациента, в основном женщины (89 %). Прием пробиотика не повлиял на уровни CОЭ, провоспалительных цитокинов (TNFa, IL–1b, IL–6, IL–12) и маркеров оксидативного стресса (общей антиоксидантной активности плазмы, малонового диальдегида), но сопровождался снижением содержания СРБ в крови и индекса DAS28. Авторы отметили малую мощность метаанализа, не позволившую сделать вывод о зависимости эффектов пробиотика от его состава, дозы и длительности применения, однако предварительно эффективность пробиотиков при РА была расценена ими как незначительная.
Итак, ряд клинических исследований, проведенных в Канаде, Новой Зеландии и Иране с целью оценки противовоспалительных эффектов пробиотиков при РЗ, дал неутешительные результаты. У больных СпА оказался неэффективен поликомпонентный пробиотик, у больных РА клиническое улучшение отсутствовало после применения лактобацилл.
Отметим, что в 2012 г. F.A. Mendoza и соавт. [101] описали два случая развития тяжелого эозинофильного мышечного синдрома в хронологической связи с приемом пробиотика. Вскоре было опубликовано альтернативное мнение A.C. Ouwehand и соавт. (2013) о триггерной роли препарата наряду с призывом осуществлять тщательный контроль качества и мониторинг переносимости пробиотиков «у лиц с тяжелыми иммунными нарушениями, которые, вероятно, имеют повышенный риск развития ПЭ» [102].
В приведенных выше исследованиях подобных и других ПЭ пробиотиков у пациентов с РЗ не наблюдали.
Выводы
1. Крупные когортные исследования, проведенные прежде всего в США, обеспечили доказательствами тезис о значимости питания в развитии РЗ и особенно РА. Они предоставили доказательства протективного потенциала длительного грудного вскармливания, безопасного (достаточного) питания в детстве и здорового питания во взрослом возрасте наряду с пользой полного и как можно более раннего отказа от курения как наиболее эффективной технологии первичной профилактики РА. Крупных РКИ влияния питания на активность и другие исходы РА в последние годы не проведено, а проведено лишь несколько небольших.
2. Употребление табака является сильным ФР развития РА в течение жизни у предрасположенных лиц, имеет самую мощную доказательную базу среди всех внешних факторов и должно учитываться как мешающий фактор при планировании, проведении и оценке результатов любых исследований эффектов питания при этом РЗ. Риск развития РА у курильщиков повышают избыточное употребление соли и повышенный ИМТ. Реализация эффектов курения может быть опосредована его влиянием на кишечную микробиоту наряду с психоэмоциональным стрессом, питанием и употреблением лекарственных средств.
3. Роль употребления алкоголя как ФР развития и исходов доказана прежде всего для РА (протективный эффект низкого и умеренного употребления, неблагоприятный эффект злоупотребления) и подагры (неблагоприятный дозозависимый эффект). Умеренное употребление алкоголя, возможно, снижает риск развития СКВ у женщин. Протективный эффект в отношении возникновения симптомов РА может оказывать употребление жирной морской рыбы и цитрусовых, а также отказ от сладких безалкогольных напитков в молодом возрасте. Эффект употребления кофе в отношении риска развития подагры (благоприятный), кофе и чая — в отношении риска развития РА (неоднозначный), по–видимому, не связан с содержанием в них кофеина.
4. Непоследовательность доказательств протективного эффекта употребления одних пищевых продуктов и компонентов (алкоголя, поваренной соли, рыбы, нерафинированного оливкового масла, овощей) и негативного эффекта других (красного мяса, сладких напитков) в отношении риска развития РА объясняют возможностью реализации этих эффектов лишь при сочетании пищевых факторов, приверженности к определенному типу питания и т.п. Профилактический потенциал и безопасность приема диетических добавок подлежат дальнейшему изучению в исследованиях; возможное незначительное снижение риска развития РА выявлено лишь при употреблении добавок цинка и b–криптоксантина.
5. Потенциальная польза средиземноморской диеты для первичной профилактики РЗ связана с ее благоприятным влиянием на риск развития метаболического синдрома и ССЗ. Итоги двух систематических обзоров 2018 года показали слабость доказательств в поддержку такого питания как технологии первичной профилактики РА и позволили выдвинуть гипотезу о большей эффективности модифицированной средиземноморской диеты — с повышенным употреблением жирной рыбы, низким употреблением сахара и поддержанием нормальной массы тела.
6. Качество доказательств эффектов применения при РА различных диет невысокое и не конкурирует с доказательной базой фармакотерапии. Польза средиземноморской диеты, доказанная недавно в систематическом обзоре, состоит в уменьшении выраженности артралгий и улучшении функции суставов. Болезнь–модифицирующий потенциал этой диеты при РА (как и вегетарианства и добавления полифенолов и омега–3–ПНЖК) не доказан, но допускается целесо–образность сочетания эффективной базисной терапии с соответствующим питанием (возможно, сбалансированным по содержанию углеводов) с целью снижения риска развития метаболического синдрома. Эта гипотеза требует подтверждения в эпидемиологических исследованиях.
7. При подагре доказательства эффектов вмешательств в плане модификации питания, доказательства эффектов употребления диетических добавок, а также доказательства пользы снижения веса при избыточной массе тела и ожирении в трех кокрановских обзорах последних лет признаны слабыми. Выводы обзоров побуждают усилить доказательную базу указанных факторов при подагре путем проведения соответствующих РКИ высокого методологического качества.
8. В лечении пациентов с РЗ не оставляют попыток использования витаминных, минеральных и других диетических добавок. Благоприятные эффекты доказаны в систематических обзорах и метаанализах лишь для капсул рыбьего жира, содержащих высокие дозы омега–3–ПНЖК (≥ 2,7 г/сут), при РА (НПВС–сберегающий эффект и снижение активности болезни), а также для достаточного употребления витамина D при СКВ (снижение уровня специфических антител) и РА (уменьшение частоты рецидивов). Учитывая риск развития нежелательных эффектов, прием витамин D– и железосодержащих добавок у больных РЗ должен строго соответствовать имеющимся рекомендациям.
9. Научный интерес к патогенетически обоснованному применению пробиотиков в ревматологической практике, возросший в последние годы, реализован в немногочисленных контролируемых исследованиях их эффектов при РА (на примере добавок лактобактерий), и убедительных доказательств их эффективности не получено. Продолжение исследований в этом направлении считается перспективным. Достаточная доказательная база позволит подтвердить или опровергнуть гипотезу о целесообразности применения пробиотиков у пациентов с РА и другими РЗ и обосновать новую стратегию их ведения.
10. Исследования эффектов питания при РЗ по–прежнему актуальны. Разработка специальных рекомендаций по питанию больных ревматологического профиля, безусловно, является перспективной научной задачей. Практическое значение на сегодня имеет такой компонент ведения пациентов с РЗ, как профилактическое консультирование по вопросам питания с целью снижения кардиоваскулярного риска.
Конфликт интересов. Автор заявляет об отсутствии какого–либо конфликта интересов при подготовке данной статьи.
1. Dinu M., Abbate R., Gensini G.F., Casini A., Sofi A. Vegetarian, vegan diets and multiple health outcomes: A systematic review with meta–analysis of observational stu–dies. Critical Reviews in Food Science and Nutrition. 2017. 57 (17). 3640–3649. doi: https://doi.org/10.1080/10408398.2016.1138447.
2. Stange R., Leitzmann C. Ernährung und Fasten als Therapie. 2017. Springer–Verlag, 2. Auflage, 348 S.
3. Forsyth C., Kouvari M., D’Cunha N.M., Georgouspoulou E.N., Panagiotakis D.B., Mellor D.D., Kellett J., Naumovski N. The effects of the Mediterranean diet on rheumatoid arthritis prevention and treatment: a systematic review of human prospective studies. Rheumatol Int. 2018. 38 (5). 737–747. doi: 10.1007/s00296–017–3912–1.
4. Grygielska Y., Raciborski F., Kłak A., Owoc J. The impact of nutrition and generally available products such as nicotine and alcohol on rheumatoid arthritis — review of the literature. Reumatologia. 2018. 56, 2. 121–127. doi: https://doi.org/10.5114/reum.2018.75524.
5. Keyβer G. Ernährung bei rheumatischen Erkrankungen. Einflüsse auf Erkrankungsrisiko und Verlauf. Arthritis + rheuma. 2018. 4 (38). 258–264.
6. Petersson S., Philippou E., Rodomar C., Nikiphorou E. The Mediterranean diet, fish oil supplements and rheumatoid arthritis outcomes: evidence from clinical trials. Autoimmun Rev. 2018. 17 (11). 1105–1114. doi: 10.1016/j.autrev.2018.06.007.
7. Philippou E., Nikiphorou E. Are we really what we eat? Nutrition and its role in the onset of rheumatoid arthritis. Autoimmun Rev. 2018. 17(11). 1074–1077. doi: 10.1016/j.autrev.2018.05.009.
8. Niklas K., Niklas A.A., Majewski D., Puczczewicz M. Rheumatic diseases induced by drugs and environmental factors: the state–of–the–art — part one. Reumatologia. 2016. 54, 3. 122–127. doi: 10.5114/reum.2016.61212.
9. Maeda Y., Kumanogoh A., Takeda K. Altered composition of gut microbiota in rheumatoid arthritis patients. Nihon Rinsho Meneki Gakkai Kaishi. 2016. 39 (1). 59–63. doi: 10.2177/jsci.39.59.
10. Kang Y., Cai Y., Zhang X., Kong X., Su J. Altered gut microbiota in rheumatoid arthritis: implications for treatment. Z. Rheumatol. 2017. 76. 451–457. doi: 10.1007/s00393–016–0237–5.
11. Schorpion A., Kolasinski S.L. Can Probiotic Supplements Improve Outcomes in Rheumatoid Arthritis? Curr. Rheumatol. Rep. 2017. 19 (11). 73. doi: 10.1007/s11926–017–0696–y.
12. Yang L., Wang L., Wang X., Xian C.L., Lu H. A Possible Role of Intestinal Microbiota in the Pathogenesis of Ankylosing Spondylitis. Int. J. Mol. Sci. 2016. 17 (12). 2126. doi: 10.3390/ijms17122126.
13. Silvermann G.J. The microbiome in SLE pathoge–nesis. Nat. Rev. Rheum. 2019. 15. 72–74.
14. Jin Z., Xiang C., Cai Q., Wei X., He J. Alcohol consumption as a preventive factor for developing rheumatoid arthritis: a dose–response meta–analysis of prospective stu–dies. Ann. Rheum. Dis. 2014. 73. 1962–1967. doi: 10.1136/annrheumdis–2013–203323.
15. Arleevskaya M., Kravtsova O., Lemerle L., Renaudineau Y., Tsibulkin A.P. How rheumatiod arthritis can result from provocation of the immune system by microorga–nisms and viruses. Front. Microbiol. 2016. 7. 1296.
16. Masuko K. A Potential Benefit of “Balanced Diet” for Rheumatoid Arthritis. Front. Med. 2018. 5. 141. doi: 10.3389/fmed.2018.00141.
17. Skoczyńska M., Świerkot J. The role of diet in rheumatoid arthritis. Reumatologia. 2018. 56, 4. 259–267. doi: 10.5114/reum.2018.77979.
18. Andreica I., Braun J. Spondyloarthritiden und Le–bensstil (Lifestyle). Arthritis + rheuma. 2018. 4 (38). 246–252.
19. Kiltz U., Braun J., Tausche A.K. Gicht und Lifestyle. Arthritis + rheuma. 2018. 4 (38). 253–257.
20. Hu Y., Sparks J.A., Malspeis S., Costenbader K.H., Hu F.B., Karlson E.W., Lu B. Long–term dietary qua–lity and risk of developing rheumatoid arthritis in women. Ann. Rheum. Dis. 2017. 76 (8). 1357–1364. doi: 10.1136/annrheumdis–2016–210431.
21. Туаева Н.О., Носырев А.Е., Ренадино И., Арлеевская М.И. Психологический стресс и ревматоидный артрит — интерференция патогенетических механизмов. Научно–практическая ревматология. 2019. 57 (1). 83–90. doi: 10.14412/1995–4484–2019–83–90.
22. Mursu J., Robien K., Harnach L.J., Park K., Jacobs D.R. Dietary supplements in older women: the Iowa Women’s Health Study. Arch. Intern. Med. 2011. 171 (8). 1625–1633. doi: 10.1001/archinternmed.2011.445.
23. Crowson C.S., Matteson E.L., Myasoedova E., Michet C.J., Ernste F.C., Warrington K.J., Davis J.M. 3rd, Hunder G.G., Therneau T.M., Gabriel S.E. The lifetime risk of adult–onset rheumatoid arthritis and other inflammatory autoimmune rheumatic diseases. Arthritis. Rheum. 2011. 63 (3). 633–639. doi: 10.1002/art.30155.
24. Hodge A.M., Bassett J.K., Dugue P.A., Shivappa N., Hebert J.R., Milne R.L., English D.R., Giles G.G. Dietary inflammatory index or Mediterranean score as risk factors for total and cardiovascular mortality. Nutr. Metab. Cardiovasc. Dis. 2018. 28 (5). 461–469. doi: 10.1016/j.numecd.2018.01.010.
25. Kitas G.D., Gabriel S.E. Cardiovascular disease in rheumatoid arthritis: state of the art and future perspectives. Ann. Rheum. Dis. 2011. 70 (1). 8–14. doi: 10.1136/ard.2010.142133.
26. Zou K., Xiao F.K., Li H.Y., Zhou K., Ban L., Yang M., Kuo C.F., Zhang W. Risk of cardiovascular disease in Chinese patients with rheumatoid arthritis: A cross–sectional study based on hospital medical records in 10 years. PLoS One. 2017. 12 (7). e0180376. doi: 10.1371/journal.pone.0180376.
27. Lu B., Solomon D.H., Costenbader K.H., Karlson E.W. Alcohol consumption and risk of incident of rheumatoid arthritis in women: a prospective study. Arthritis. Rheumatol. 2014. 66. 1998–2005. doi: 10.1002/art.38634.
28. Colditz G.A., Philipott S.E., Hunkinson S.E. The Impact of the Nurses’ Health Study on Population Health: Prevention, Translation, and Control. Am. J. Public Health. 2016. 106 (9). 1540–1545. doi: 10.2105/AJPH.2016.303343.
29. Barbhaiya M., Lu B., Sparks J.A., Malspeis S., Chang S.C., Karlson E.W., Costenbader K.H. Influence of Alcohol Consumption on the Risk of Systemic Lupus Erythematosus Among Women in the Nurses’ Health Study Cohort. Arthritis. Care Res. (Hoboken). 2017. 69 (3). 384–392. doi: 10.1002/acr.22945.
30. Liu X., Tedeschi S.K., Barbhaiya M., Leatherwood C.L., Speyer C.B., Lu B., Costenbader K.H., Karlson E.W., Sparks J.A. Impact and timing of smoking cessation on reducing risk for rheumatoid arthritis among women in the Nurses’ Health Studies. Arthritis. Res. Care (Hoboken). 2019 Feb 21. [Epub ahead of print]. doi: 10.1002/acr.23837.
31. Karlson E.W., Mandl L.A., Hankinson S.E., Grodstein F. Do breast–feeding and other reproductive factors influence future risk of rheumatoid arthritis: Results from the Nurses’ Health Study. Arthritis. Rheum. 2004. 50 (11). 3458–3467.
32. Karlson E.W., Mandl L.A., Aweh G.N., Grodstein F. Coffee consumption and risk of rheumatoid arthritis. Arthritis. Rheum. 2003. 48 (11). 3055–3060.
33. Parks C.G., D’Aloisio A.A., DeRoo L.A., Huiber K., Rider L.G., Miller F.W., Sandler D.P. Childhood socioeconomic factors and perinatal characteristics influence development of rheumatoid arthritis in adulthood. Ann. Rheum. Dis. 2013. 72 (3). 350–356. doi: 10.1136/annrheumdis–2011–201083.
34. Kallberg H., Jacobsen S., Bengtsson C., Pedersen M., Padyukov L., Garred P., Frisch M., Karlson E.W., Klareskog L., Alfredsson L. Alcohol consumption is associated with decreased risk of rheumatoid arthritis: results from two Scandinavian case–control studies. Ann. Rheum. Dis. 2009. 68. 222–227. doi: 10.1136/ard.2007.086314.
35. Kallberg H., Ding B., Padyukov L., Bengtsson C., Rönnelid J., Klareskog L., Alfredsson L.; EIRA Study Group. Smoking is a major preventable risk factor for rheumatoid arthritis: estimation of risks after various exposures to cigarette smoke. Ann. Rheum. Dis. 2011. 70. 508–511. doi: 10.1136/ard.2009.120899.
36. Di Giusepe D., Discaciati A., Orsini N., Wolk A. Cigarette smoking and risk of rheumatoid arthritis: a dose–response meta–analysis. Arthritis. Res. Ther. 2014. 16 (2). R61. doi: 10.1136/ar4498.
37. Heliõvaara M., Aho K., Knekt P., Impivaara O., Reunanen A., Aromaa A. Coffee consumption, rheumatoid factor, and the risk of rheumatoid arthritis. Ann. Rheum. Dis. 2000. 59 (8). 631–635.
38. Mikuls T.R., Cerhan J.R., Criswell L.A., Merlino L., Mudano A.S., Burma M., Folsom A.R., Saag K.G. Coffee, tea, and caffeine consumption and risk of rheumatoid arthritis: results from the Iowa Women’s Health Study. Arthritis. Rheum. 2002. 46 (1). 83–91.
39. Scott I.C., Tan R., Stahl D., Steer S., Lewis C.M., Cope A.P. The protective effect of alcohol on developing rheumatoid arthritis: a systematic review and meta–analysis. Rheumatology (Oxford). 2013. 52 (5). 856–867. doi: 10.1093/rheumatology/kes376.
40. Nissen M.J., Gabay C., Scherer A., Finckh A.; Swiss Clinical Quality management Project in Rheumatoid Arthritis. The effect of alcohol on radiographic progression in rheumatoid arthritis. Arthritis. Rheum. 2010. 62 (5). 1265–1272. doi: 10.1002/art.27388.
41. DeChristopher L.R., Uribarri J., Tucker K.L. Intake of high–fructose corn syrup sweetened soft drinks, fruit drinks and apple juice is associated with prevalent arthritis in US adults, aged 20–30 years. Nutr. Diabetes. 2016. 6. e199. doi: 10.1038/nutd.2016.7.
42. Westhoff G., Rau R., Zink A. Radiographic joint damage in early rheumatoid arthritis is highly dependent on body mass index. Arthritis. Rheum. 2007. 56 (11). 3575–3582.
43. Ajeganova S., Andersson M.I., Hafstrom I.; BARFOT Study Group. Association of obesity with worse disease activity in rheumatoid arthritis as well as with comorbidities: a long–term follow–up from disease onset. Arthritis. Care Res. (Hoboken). 2013. 65 (1). 78–87. doi: 10.1002/acr.21710.
44. Sundstrom B., Johansson I., Kantapaa–Dahlqvist S. Interaction between dietary sodium and smoking increase the risk for rheumatoid arthritis: results from a nested case–control study. Rheumatology (Oxford). 2015. 54 (3). 487–493. doi: 10.1093/rheumatology/keu330.
45. de Hair M.J., Landewe R.B., van de Sande M.G., van Schaardenburg D., van Baarsen L.G., Gerlag D.M., Tak P.P. Smoking and overweight determine the likelihood of developing rheumatoid arthritis. Ann. Rheum. Dis. 2013. 72. 1654–1658. doi: 10.1136/annrheumdis–2012–202254.
46. Pattison D.J., Symmons D.P., Young A. Does diet have a role in the etiology of rheumatoid arthritis? Proc. Nutr. Soc. 2004. 63 (1). 137–143.
47. Benito–Garcia E., Feskanich D., Hu F.B., –Mandl L.A., Karlson E.W. Protein, iron, and meat consumption and risk for rheumatoid arthritis: a prospective cohort study. Arthritis. Res. Ther. 2007. 9. R16.
48. Pedersen M., Stripp C., Klarlung M., Olsen S.F., Tjønneland A.M., Frisch M. Diet and risk of rheumatoid arthritis in a prospective cohort. J. Rheumatol. 2005. 32 (7). 1249–1252.
49. Sköldstam L., Larsson L., Lindsröm F.D. Effect of fasting and lactovegetarian diet on rheumatoid arthritis. Scand. J. Rheumatol. 1979. 8 (4). 249–255.
50. Kjeldsen–Kragh J., Haugen M., Borchgrevnik C.F., Laerum E., Eek M., Mowinkel P., Hovi K., Førre O. Controlled trial of fasting and one–year vegetarian diet in rheumatoid arthritis. Lancet. 1991. 338 (8772). 899–902.
51. Klareskog L., Catrina A.I., Paget S. Rheumatoid arthritis. Lancet. 2009. 373 (9664). 659–672. doi: 10.1016/S0140–6736(09)60008–8.
52. He J., Wang Y., Feng M. et al. Dietary intake and risk of rheumatoid arthritis — a cross section multicenter study. Clin. Rheumatol. 2016. 35 (12). 2902–2908. doi: 10.1007/s10067–016–3383–x.
53. Shai I., Schwarzfuchs D., Henkin Y. et al.; Dietary Intervention Randomized Controlled Trial (DIRECT) Group. Weight loss with a low–carbohydrate, Mediterranean, or low–fat diet. NEJM. 2008. 359 (3). 229–241. doi: 10.1056/NEJMoa0708681.
54. Hu Y., Costenbader K.H., Gao X., Hu F.B., Karlson E.W., Lu B. Mediterranean diet and incidence of rheumatoid arthritis in women. Arthritis. Care Res. (Hoboken). 2014. 67 (5). 597–606. doi: 10.1002/acr.22481.
55. Cerhan J.R., Saag K.G., Merlino L.A., Mikuls T.R., Criswell L.A. Antioxidant micronutrients and risk of rheumatoid arthritis in cohort of older women. Am. J. Epidemiol. 2003. 157 (4). 345–354.
56. Pattison D.J., Symmons D.P., Lunt M., Welch A., Bingham S.A., Day N.E., Silman A.J. Dietary beta–cryptoxantin and inflammatory polyarthritis: results from a population–based prospective study. Am. J. Clin. Nutr. 2005. 82 (2). 451–455.
57. Merlino L.A., Curtis J., Mikuls T.R., Cerhan J.R., Criswell L.A., Saag K.G.; Iowa Women’s Health Study. Vitamin D intake is inversely associated with rheumatoid arthritis: results from the Iowa Women’s Health Study. Arthritis. Rheum. 2004. 50. 72–77.
58. Racovan M., Walitt B., Collins C.E., Pettinger M., Parks C.G., Shikany J.M., Wactawski–Wende J., Manson J.E., Moreland L., Wright N., Jackson R., Howard B.V. Calcium and vitamin D supplementation and incident rheumatoid arthritis: the Women’s Health Initiative Calcium plus Vitamin D trial. Rheumatol. Int. 2012. 32 (12). 3823–3830. doi: 10.1007/s00296–011–2268–1.
59. Hagen K.B., Byfuglien M.G., Falzon L., Olsen S.U., Smedslung G. Dietary interventions for rheumatoid arthritis. Cochrane Database Syst. Rev. 2009. CD006400. doi: 10.1002/14651858.CD006400.
60. Kavanaghi R., Workman E., Nash O., Smith M., Hazleman B.L., Hunter J.O. The effects of elemental diet and subsequent food reintroduction on rheumatoid arthritis. Br. J. Rheumatol. 1995. 34 (3). 270–273.
61. Holst–Jensen S.E., Pfeiffer–Jensen M., Monsrud M., Tarp U., Buus A., Hessov I., Thorling E., Stengaard–Pedersen K. Treatment of rheumatoid arthritis with a peptide diet: a randomized, controlled trial. Scand. J. Rheumatol. 1998. 27 (5). 329–336.
62. Hafstrom I., Ringertz B., Spångberg A., von Zweigbergk L., Brannemark S., Nylander I., Rönnelid J., Laaso–nen L., Klareskog L. A vegan diet free of gluten improves the signs and symptoms of rheumatoid arthritis: the effects on arthritis correlate with a reduction in antibodies to food antigens. Rheumatology (Oxford). 2001. 40 (10). 1175–1179.
63. Khanna S., Jaiswai K.S., Gupta B. Managing Rheumatoid Arthritis with Dietary Interventions. Front. Nutr. 2017. 4. 52. doi: 10.3389/fnut.2017.00052.
64. Podas T., Nightingale J.M., Oldham R., Roy S., Sheehan N.J., Mayberry J.F. Is rheumatoid arthritis a dise–ase that starts in the intestine? A pilot study comparing an elemental diet with oral prednisolone. Postgrad. Med. J. 2007. 83 (976). 128–131.
65. Haugen M., Kjeldsen–Kragh J., Nordvåg B.Y., Førre O. Diet and disease symptoms in rheumatic disea–ses — results of a questionnaire based survey. Clin. Rheumatol. 1991. 10. 401–407.
66. van de Laar M.A., van der Korst J.K. Food intole–rance in rheumatoid arthritis. I. A double blind, controlled trial of the clinical effects of elimination of milk allergens and azo dyes. Ann. Rheum. Dis. 1992. 51. 298–302.
67. Müller H., de Toledo F.W., Resch K.L. Fasting followed by vegetarian diet in patients with rheumatoid arthritis: a systematic review. Scand. J. Rheumatol. 2001. 30 (1). 1–10.
68. Sköldstam L., Hagfors I., Johansson G. An experimental study of a Mediterranean diet intervention for patients with rheumatoid arthritis. Ann. Rheum. Dis. 2003. 62. 208–214. doi: 10.1136/ard.62.3.208.
69. Tedeschi S.K., Bathon J.M., Giles J.T., Lin T.C., Yoshida K., Solomon D.H. Relationship Between Fish Consumption and Disease Activity in Rheumatoid Arthritis. Arthritis. Res. Care. 2018. 70 (3). 327–332. doi: 10.1002/acr.23295.
70. Matsumoto Y., Sugioka Y., Tada M., Okano T., Mamoto K., Inui K., Habu D., Koike T. Monounsaturated fatty acids might be key factors in the Mediterranean diet that suppress rheumatoid arthritis disease activity: The –TOMORROW study. Clin. Nutr. (Edinburgh). 2018. 37 (2). 675–680. doi: 10.1016/j.clnu.2017.02.011.
71. Wu G.D., Chen J., Hoffmann C., Bittinger K., Chen Y.Y., Keilbaugh S.A., Bewtra M., Knights D., Walters W.A., Knights R., Sinha R., Gilroy E., Gupta K., Baldassano R., Nessel L., Li H., Bushman F.D., Lewis J.D. Linking long–term dietary patterns with gut microbial enterotypes. Science. 2011. 334 (6052). 105–108. doi: 10.1126/science.1208344.
72. Wong G.M. Gut microbiota and cardiometabolic outcomes:influence of dietary patterns and their associated components. Am. J. Clin. Nutr. 2014; 100 (suppl. 1). 369–377s. doi: 10.3945/ajcn.113.071639.
73. Choi E.Y., Jin J.Y., Choi I.S., Kim S.J. DHA suppresses Prevotella imtermedia lipopolysaccharide–induced production of proinflammatory mediators in murine macrophages. Brit. J. Nutr. 2014. 111. 1221–1230. doi: 10.1017/S0007114513003681.
74. Goldberg R.G., Katz J. A meta–analysis of the –analgesic effects of omega–3 polyunsaturated fatty acid supplementation for inflammatory joint pain. Pain. 2007. 129 (1–2). 210–223.
75. Lee Y.H., Bae S.C., Song G.G. Omega–3 polyunsatu–rated fatty acids and the treatment of rheumatoid arthritis: a meta–analysis. Arch. Med. Res. 2012. 43 (5). 356–362. doi: 10.1016/j.archmed.2012.06.011.
76. Gioxari A., Kaliora A.C., Marantidou F., Panagiotakos D.P. Intake of omega–3 polyunsaturated fatty acids in patients with rheumatoid arthritis: a systematic review and meta–analysis. Nutrition. 2018. 45. 114–124.e4. doi: 10.1016/j.nut.2017.06.023.
77. Kolahi S., Ghorbanihaghijo A., Alizadeh S., Rashtchizadeh N., Argani H., Khabazzi A.R., Hajialilo M., Bahreini E. Fish oil supplementation decreases serum so–luble receptor activator of nuclear factor–kappa B ligand/osteoprotegerin ratio in female patients with rheumatoid arthritis. Clin. Biochem. 2010. 43 (6). 576–580. doi: 10.1016/j.clinbiochem.2009.12.011.
78. Simopoulos A.P. The importance of the omega–6/omega–3 fatty acid ratio in cardiovascular disease and other chronic diseases. Exp. Biol. Med. (Maywood). 2008. 233 (6). 674–688. doi: 10.3181/0711–MR–311.
79. Fu Y., Li G., Zhang X., Xing G. Lipid Extract from Hard–Shelled Mussel (Mytilus coruscus) Improves Clinical Conditions of Patients with Rheumatoid Arthritis: A Randomized Controlled Trial. Nutrients. 2015. 7 (1). 625–645. doi: 10.3390/nu7010625.
80. Proudman S.M., James M.J., Spargo L.D., Metcalf R.G., Sullivan T.R., Rischmueller M., Flabouris K., Wechalekar M.D., Lee A.T., Cleland L.G. Fish oil in recent onset rheumatoid arthritis: a randomized, double–blind controlled trial within algorithm–based drug use. Ann. Rheum. Dis. 2015. 74 (1). 89–95. doi: 10.1136/annrheumdis–2013–204145.
81. Remans P.H., Sont J.K., Wagenaar L.W., Wou–ters–Wesseling W., Zuijderduin W.M., Jongma A., Breedveld F.C., Van Laar J.M. Nutrient supplementation with polyunsaturated fatty acids and micronutrients in rheumatoid arthritis: clinical and biochemical effects. Eur. J. Clin. Nutr. 2004. 58 (6). 839–845.
82. Bae S.C., Jung W.J., Lee E.J., Yu R., Sung M.K. Effects of antioxidant supplements intervention on the level of plasma inflammatory molecules and disease activity of rheumatoid arthritis patients. J. Am. Coll. Nutr. 2009. 28 (1). 56–62.
83. Miller E.R. 3rd, Pastor–Barriuso R., Dalal D., Riemersma R.A., Appel L.J., Guallar E. Meta–analysis: high–dosage vitamin E supplementation may increase all–cause mortality. Ann. Intern. Med. 2005. 142 (1). 37–46.
84. Franco A.S., Freitas T.Q., Bernardo W.M., Pereira R.M.R. Vitamin D supplementation and di–sease activity in patients with immune–mediated rheumatic diseases: A systematic review and meta–analysis. Medicine (Baltimore). 2017. 96. e7024. doi: 10.1097/MD.0000000000007024.
85. Wang M., Jiang X., Wu W., Zhang D. A meta–analysis of alcohol consumption and the risk of gout. Clin Rheumatol. 2013. 32 (11). 1641–1648. doi: 10.1007/s10067–013–2319–y.
86. Choi H.K., Willett W., Curhan G. Coffee consumption and risk of incident gout in men: a prospective study. Arthritis. Rheum. 2007. 56 (6). 2019–2055.
87. Пузанова О.Г. К юбилею Немецкого ревматологического общества: актуальные темы Объединенного конгресса DGRh, DGORh и GKJR 2017 г. Therapia. Український медичний вісник. 2018. 1 (126). 43–48.
88. Moi J.H., Sriranganathan M.K., Edwards C.J., Buchbinder R. Lifestyle interventions for chronic gout. Cochrane Database Syst. Rev. 2013. 5. CD010039. doi: 10.1002/14651858.CD010039.pub2.
89. Andrés M., Sivera F., Falzon L., Buchbinder R., Carmona L. Cochrane Database Syst. Rev. 2014. 10. CD010156. doi: 10.1002/14651858.CD010156.
90. Nielsen S.M., Bartels E.M., Henriksen M., Wæhrens E.E., Gudbergsen H., Bliddal H., Astrup A., Knop F.K., Carmona L., Taylor W.J., Singh J.A., Perez–Ruis F., Kristensen L.E., Christensen R. Weight loss for overweight and obese individuals with gout: a systematic review of longitudinal studies. Ann. Rheum. Dis. 2017. 76 (11). 1870–1882. doi: 10.1136/annrheumdis–2017–211472.
91. Pianta A., Arvikar S., Strle K., Drouin E.E., Wang Q., Costello C.E., Steere A.C. Evidence of the Immune Re–levance of Prevotella copti, a Gut Microbe, in Patients with Rheumatoid Arthritis. Arthr. Rheum. 2017. 69 (5). 964–975. doi: 10.1002/art.40003.
92. Головач І.Ю., Єгудіна Є.Д. Роль мікробіому при спондилоартритах. Трансплантація фекальної мікробіоти при спондилоартритах готова до клінічних випробувань? Клінічна імунологія. Алергологія. Інфектологія. 2019. 1 (114). 52–61.
93. Кондратюк В.Є., Тарасенко О.М. Сучасний погляд на патогенетичні аспекти подагри. Український ревматологічний журнал. 2018. 4 (74). 32–37.
94. Jenks K., Stebbings S., Burton J., Schultz M., Herbison P., Highton J. Probiotic therapy for the treatment of spondyloarthritis: a randomized controlled trial. J. Rheumatol. 2010. 37 (10). 2118–2125. doi: 10.3899/jrheum.100193.
95. Pineda Mde L., Thompson S.F., Summers K., de Leon F., Pope J., Reid G. A randomized, double–blind, placebo–controlled pilot study of probiotics in active rheumatoid arthritis. Med. Sci Monit. 2011. 17 (6). CR347–354.
96. Alipour B., Homayouni–Rad A., Vagnef–Mehrabany E., Sharif S.K., Vagnef–Mehrabany L., Asghani–Jafarabadi M., Nakhjavani M.R., Montadi–Nia J. Effects of Lactobacillus casei supplementation on disease activity and inflammatory cytokines in rheumatoid arthritis patients: a randomized double–blind clinical trial. Int. J. Rheum. Dis. 2014. 17. 519–527. doi: 10.1111/17–56–185X.12333.
97. Vagnef–Mehrabany E., Alipour B., Homayouni–Rad A., Sharif S.K., Asghani–Jafarabadi M., Zavvari S. Probiotic supplementation improves inflammatory status in patients with rheumatoid arthritis. Nutrition (Burbank). 2014. 30. 430–435. doi: 10.1016/j.nut.2013.09.007.
98. Zamani B., Golkar H.R., Farshbaf S., Emadi–Baygi M., Tajabadi–Ebrahimi M., Jafari P., Akhavan R., Taghizadeh M., Memarzadeh M.R., Asemi Z. Clinical and metabolic response to probiotic supplementation in patients with rheumatoid arthritis: a randomized, double–blind, placebo–controlled trial. Int. J. Rheum. Dis. 2016. 19 (9). 869–879. doi: 10.1111/1756–186X.12888.
99. Mohammed A.T., Knattab M., Ahmed A.M., Turk T., Sakr N., M. Khalil A., Abdelhalim M., Sawaf B., Hirayama K., Huy N.T. The therapeutic effect of probiotics on rheumatoid arthritis: a systematic review and meta–analysis of randomized control trials. Clin. Rheumatol. 2017. 36 (12). 2697–2707. doi: 10.1007/s10067–017–3814–3.
100. Aqaeinezhad Rudbane S.M., Rahmdel S., Abdollahzadeh S.M., Zare M., Bazrafshan A., Mazloomi S.M. The efficacy of probiotic supplementation in rheumatoid arthritis: a meta–analysis of randomized, controlled trials. Inflammopharmacology. 2018. 26 (1). 67–76. doi: 10.1007/s10787–017–0436–y.
101. Mendoza F.A., Purohit S., Kenyon I., Jimenez S.A. Severe eosinophilic syndrome associated with the use of probiotic supplements: a new entity? Case Rep. Rheumatol. 2012. 2012. 934324. doi: 10.1155/2012/934324.
102. Ouwehand A.C., Rijkers G.T. Severe eosinophilic syndrome: highly unlikely associated with the use of probiotic supplements! Case Rep. Rheumatol. 2013. 2013. 769127. doi: 10.1155/2013/769127.

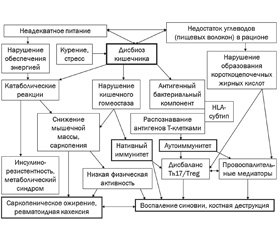
/151-1.jpg)
/159-1.jpg)
/161-1.jpg)