Международный эндокринологический журнал Том 15, №5, 2019
Вернуться к номеру
Застосування Нуклео Ц.М.Ф. форте в комплексному лікуванні діабетичної полінейропатії
Авторы: Власенко М.В.(1), Паламарчук А.В.(1), Шкарівська С.В.(2)
(1) — Вінницький національний медичний університет ім. М.І. Пирогова, м. Вінниця, Україна
(2) — Вінницький обласний клінічний високоспеціалізований ендокринологічний центр, м. Вінниця, Україна
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
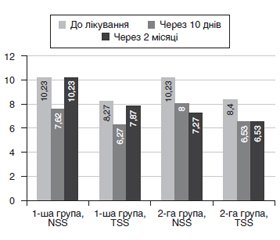
Актуальність. Цукровий діабет (ЦД) є одним із соціально значущих захворювань. На момент маніфестації ЦД до 6 % хворих мають ознаки діабетичної полінейропатії (ДПН), через 5 років захворювання її спостерігають у 15 % пацієнтів, а через 15 років — у 25 % хворих на ЦД. Близько 80 % пацієнтів із ДПН мають безсимптомну форму, а больова форма ДПН діагностується в 10–20 % випадків. ДПН у деяких випадках передує появі клінічних ознак ЦД. Для адекватного лікування ДПН необхідно знати, що патогенез нейропатії при ЦД пов’язаний із комплексним ураженням нейрональних мембран метаболічного характеру. Метою нашого дослідження було вивчення ефективності препарату Нуклео Ц.М.Ф. форте в комплексному лікуванні ДПН. Матеріали та методи. Було обстежено 30 хворих на ЦД 1-го і 2-го типу (8 чоловіків і 22 жінки) з ДПН. Рівень глікованого гемоглобіну становив від 7,1 до 10,4 %. Перша група (15 пацієнтів) отримувала: альфа-ліпоєву кислоту в дозуванні 600 мг внутрішньовенно, вітаміни групи В ін’єкційно протягом 10 днів під час перебування в стаціонарі й у таблетованій формі — протягом місяця лікування в домашніх умовах. Друга група (15 пацієнтів) на додаток до терапії, яку отримувала перша група, одержувала Нуклео Ц.М.Ф. форте внутрішньом’язово протягом 10 днів під час перебування в стаціонарі, потім по 1 капсулі 2 рази на день протягом 2 місяців. Усім пацієнтам до прийому препарату, через 10 днів лікування в умовах стаціонару й через 2 місяці після лікування для оцінки неврологічного статусу проводилося клінічне неврологічне обстеження, а також динамічне обстеження пацієнтів за спеціальними клінічними опитувальниками (шкалами): нейропатичного симптоматичного рахунку і загального симптоматичного рахунку. Результати. У хворих як першої, так і другої групи спостерігався статистично позитивний вплив на симптоматику через 10 днів лікування в умовах стаціонару відповідно до шкали нейропатичного симптоматичного рахунку. Cимптоматика нейропатії в першій групі до лікування становила 10,23 ± 0,35 бала, а після лікування — 7,62 ± 0,26 бала, p < 0,001; у другій групі до лікування — 10,23 ± 0,35 бала, а після лікування — 8,00 ± 0,30 бала, p < 0,001. Відповідно до шкали загального симптоматичного рахунку інтенсивність симптомів нейропатії значно зменшилась як у першій групі (8,27 ± 0,47 бала до лікування і 6,27 ± 0,12 бала після лікування, p < 0,001), так і в другій групі (8,40 ± 0,45 бала до лікування і 6,53 ± 0,14 бала після лікування, p < 0,001). Подальші дослідження показали, що через 2 місяці від початку лікування в пацієнтів першої групи показники нейропатичного симптоматичного рахунку (10,23 ± 0,35 бала, p > 0,05) і загального симптоматичного рахунку (7,87 ± 0,38 бала, p > 0,05) повернулися до початкових або зміни були невірогідними. Двомісячне застосування Нуклео Ц.М.Ф. форте мало статистично позитивний вплив на симптоматику нейропатії відповідно до показників нейропатичного симптоматичного рахунку (7,27 ± 0,51 бала, p < 0,001) і загального симптоматичного рахунку (6,53 ± 0,14 бала, p < 0,001). Висновки. Застосування препарату Нуклео Ц.М.Ф. форте в комплексній терапії хворих на цукровий діабет може запобігти порушенням, що виникають унаслідок діабетичної полінейропатії. Виявлено довготривалий статистично значущий позитивний вплив препарату Нуклео Ц.М.Ф. форте на симптоматику нейропатії.
Актуальность. Сахарный диабет (СД) является одним из социально значимых заболеваний. На момент манифестации СД до 6 % больных имеют признаки диабетической полинейропатии (ДПН), через 5 лет заболевания ее наблюдают у 15 % пациентов, а через 15 лет — у 25 % больных СД. Около 80 % пациентов с ДПН имеют бессимптомную форму, а болевая форма ДПН диагностируется в 10–20 % случаев. ДПН в некоторых случаях предшествует появлению клинических признаков СД. Для адекватного лечения ДПН необходимо знать, что патогенез нейропатии при СД связан с комплексным поражением нейрональных мембран метаболического характера. Целью нашего исследования было изучение эффективности препарата Нуклео Ц.М.Ф. форте в комплексном лечении ДПН. Материалы и методы. Было обследовано 30 больных СД 1-го и 2-го типа (8 мужчин и 22 женщины) с ДПН. Уровень гликированного гемоглобина составлял от 7,1 до 10,4 %. Первая группа (15 пациентов) получала: альфа-липоевую кислоту в дозировке 600 мг, витамины группы В инъекционно в течение 10 дней во время пребывания в стационаре и в таблетированной форме — в течение месяца лечения в домашних условиях. Вторая группа (15 пациентов) вдобавок к терапии, которую получала первая группа, получала Нуклео Ц.М.Ф. форте внутримышечно в течение 10 дней во время пребывания в стационаре, затем по 1 капсуле 2 раза в день в течение 2 месяцев. Всем пациентам до приема препарата, через 10 дней лечения в условиях стационара и через 2 месяца после лечения для оценки неврологического статуса проводилось клиническое неврологическое обследование, а также динамическое обследование пациентов по специальным клиническим опросникам (шкалам): нейропатического симптоматического счета и общего симптоматического счета. Результаты. У больных как первой, так и второй группы наблюдалось статистически положительное влияние на симптоматику через 10 дней лечения в условиях стационара в соответствии со шкалой нейропатического симптоматического счета. Cимптоматика нейропатии в первой группе до лечения составляла 10,23 ± 0,35 балла, а после лечения — 7,62 ± 0,26 балла, p < 0,001; во второй группе до лечения — 10,23 ± 0,35 балла, а после лечения — 8,00 ± 0,30 балла, p < 0,001. В соответствии со шкалой общего симптоматического счета интенсивность симптомов нейропатии значительно уменьшилась как в первой группе (8,27 ± 0,47 балла до лечения и 6,27 ± 0,12 балла после лечения, p < 0,001), так и во второй группе (8,40 ± 0,45 балла до лечения и 6,53 ± 0,14 балла после лечения, p < 0,001). Дальнейшие исследования показали, что через 2 месяца после начала лечения у пациентов первой группы показатели нейропатического симптоматического счета (10,23 ± 0,35 балла, p < 0,05) и общего симптоматического счета (7,87 ± 0,38 балла, p > 0,05) вернулись к исходным или изменения были недостоверными. Двухмесячное применение Нуклео Ц.М.Ф. форте оказало статистически положительное влияние на симптоматику нейропатии в соответствии с показателями нейропатического симптоматического счета (7,27 ± 0,51 балла, p < 0,001) и общего симптоматического счета (6,53 ± 0,14 балла, p < 0,001). Выводы. Применение препарата Нуклео Ц.М.Ф. форте в комплексной терапии больных сахарным диабетом может предотвратить нарушения, возникающие вследствие диабетической полинейропатии. Выявлено длительное статистически значимое положительное влияние препарата Нуклео Ц.М.Ф. форте на симптоматику нейропатии.
Background. Diabetes mellitus (DM) is one of the socially significant diseases. At the time of manifestation of DM, up to 6 % of patients have signs of diabetic polyneuropathy (DPN), after 5 years of the disease, they are observed in 15 %, and after 15 years — in 25 % of patients with DM. About 80 % of patients with DPN are asymptomatic, and the painful form of DPN is diagnosed in 10–20 % of cases. Sometimes, DPN precedes the onset of clinical signs of DM. For adequate treatment of DPN, it is necessary to know that pathogenesis of neuropathy in DM is associated with overall metabolic lesion of neuronal membranes. The objective was to study the effectiveness of Nucleo C.M.P. Forte in the comprehensive treatment of DPN. Materials and methods. Thirty patients with DM types 1 and 2 (8 men and 22 women) and DPN were examined. The level of glycated hemoglobin was from 7.1 to 10.4 %. The first group (15 patients) received: alpha-lipoic acid at a dose of 600 mg intravenously, B vitamins: injections — for 10 days while in hospital and tablets — for one month at home. The second group (15 patients) before treatment received by group 1 was treated with Nucleo C.M.P. Forte intramuscularly for 10 days while in hospital, then 1 capsule twice a day for 2 months. In all patients before administration of the drug, after 10 days of in-hospital treatment and 2 months after treatment, clinical neurological examination was performed to evaluate neurological status, as well as dynamic examination using special clinical questionnaires (scales): Neurological Symptom Score and Total Symptom Score. Results. Patients in both the first group and the second groups had a statistically positive effect on the symptoms after 10 days of in-patient treatment according to Neurological Symptom Score. The severity of neuropathy in first group before treatment was 10.23 ± 0.35 points, and after treatment — 7.62 ± 0.26 points, p < 0.001; in the second group, before treatment — 10.23 ± 0.35 points, and after treatment — 8.00 ± 0.30 points, p < 0.001. According to Total Symptom Score, the severity of neuropathy symptoms decreased significantly in both group 1 (8.27 ± 0.47 points before treatment and 6.27 ± 0.12 points after treatment, p < 0.001) and group 2 (8.40 ± 0.45 points before treatment and 6.53 ± 0.14 points after treatment, p < 0.001). Further studies showed that after 2 months of treatment in patients in first group, Neurological Symptom Score (10.23 ± 0.35 points, p > 0.05) and Total Symptom Score (7.87 ± 0.38 points, p > 0.05) returned to the baseline or the changes were unreliable. Two-month administration of Nucleo C.M.P. Forte had a statistically positive effect on the symptoms of neuropathy according to Neurological Symptom Score (7.27 ± 0.51 points, p < 0.001) and Total Symptom Score (6.53 ± 0.14 points, p < 0.001). Conclusions. The use of Nucleo C.M.P. Forte in the comprehensive treatment of patients with diabetes mellitus can prevent disorders that occur as a result of diabetic polyneuropathy. Long-term statistically significant positive effect of Nucleo C.M.P. Forte on neuropathy symptoms was revealed.
цукровий діабет; діабетична полінейропатія; Нуклео Ц.М.Ф. форте
сахарный диабет; диабетическая полинейропатия; Нуклео Ц.М.Ф. форте
diabetes mellitus; diabetic polyneuropathy; Nucleo C.M.P. Forte
Вступ
Матеріали та методи
Результати
/35.jpg)
Oбговорення
Висновки
1. Pop-Busui R., Boulton A.J.M., Feldman E.J. et al. Diabetic neuropathy: a position statement by the American Diabetes Association. Diabetes Care. 2017. 40. 136-154.
2. Shillo P., Sloan G., Greig M. et al. Painful and Painless Diabetic Neuropathies: What Is the Difference? Curr. Diab. Rep. 2019. 19(6). 32. doi: 10.1007/s11892-019-1150-5.
3. Moghtaderi A., Bakhshipour A., Rashidi H. Validation of Michigan neuropathy screening instrument for diabetic peripheral neuropathy. Clin. Neurol. Neurosurg. 2006. 108. 477-481.
4. Ziegler D., Rathmann W., Dickhaus T., Meisinger C., Mielck A.; KORA Study Group. Neuropathic pain in diabetes, prediabetes and normal glucose tolerance: the MONICA/KORA Augsburg Surveys S2 and S3. Pain Med. 2009. 10(2). 393-400. doi: 10.1111/j.1526-4637.2008.00555.x.
5. Herder C., Lankisch M., Ziegler D. et al. Subclinical inflammation and diabetic polyneuropathy: MONICA/KORA Survey F3 (Augsburg, Germany). Diabetes Care. 2009. 32(4). 680-2. doi: 10.2337/dc08-2011.
6. Tesfaye S., Boulton A.J., Dyck P.J. et al. Diabetic neuropathies: update on definitions, diagnostic criteria, estimation of severity, and treatments. Diabetes Care. 2010. 33. 2285-2293.
7. Sadosky A., Mardekian J., Parsons B., Hopps M., Bienen E.J., Markman J. Healthcare utilization and costs in diabetes relative to the clinical spectrum of painful diabetic peripheral neuropathy. J. Diabetes Complicat. 2015. 29. 212-217.
8. Van Acker K., Bouhassira D., De Bacquer D. et al. Prevalence and impact on quality of life of peripheral neuropathy with or without neuropathic pain in type 1 and type 2 diabetic patients attending hospital outpatients clinics. Diabetes Metab. 2009. 35. 206-213.
9. Alleman C.J., Westerhout K.Y., Hensen M. et al. Humanistic and economic burden of painful diabetic peripheral neuropathy in Europe: a review of the literature. Diabetes Res. Clin. Pract. 2015. 109. 215-225.
10. Binns-Hall O., Selvarajah D., Sanger D., Walker J., Scott A., Tesfaye S. One-stop microvascular screening service: an effective model for the early detection of diabetic peripheral neuropathy and the high-risk foot. Diabet Med. 2018. 35. 887-894.
11. Паньків В.І. Ефективність терапії альфа-ліпоєвою кислотою при діабетичній невропатії. Міжнародний ендокринологічний журнал. 2015. 2(66).
12. Власенко М.В. Якість життя хворих на цукровий діабет 2-го типу з метаболічною нейропатією на тлі патогенетичної терапії. Міжнародний ендокринологічний журнал. 2013. 1(49).