Журнал «Боль. Суставы. Позвоночник» Том 9, №4, 2019
Вернуться к номеру
Українська версія FRAX: критерії діагностики й лікування остеопорозу
Авторы: Поворознюк В.В. (1), Григор’єва Н.В. (1), Kanis J.A. (2), Johansson H. (2), McCloskey E.V. (2)
1 - Український науково-медичний центр проблем остеопорозу, ДУ «Інститут геронтології імені Д.Ф. Чеботарьова НАМН України», м. Київ, Україна
2 - University of Sheffield Medical School, Beech Hill Road, Sheffield S10 2RX, UK
Рубрики: Ревматология, Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
Актуальність. На сьогодні алгоритм FRAX® є інформативним методом оцінки ризику остеопоротичних переломів, імплементованим в європейські й американські рекомендації щодо менеджменту остеопорозу. Проте існують відмінності щодо меж втручання для антиостеопоротичного лікування, що залежать від країни, моделі надання медичної допомоги та повернення коштів за лікування. Власна модель FRAX з’явилась в Україні в 2016 році, проте межі втручання досі розроблені не були. Мета дослідження: визначити межі для фармакологічного лікування остеопорозу та додаткового обстеження населення України за допомогою національної моделі FRAX. Матеріали та методи. Обстежено 3790 амбулаторних жінок віком 40–90 років (середній вік — 61,9 ± 10,0 року). Розробка меж втручання та додаткової оцінки стану кісткової тканини з використанням двохенергетичної рентгенівської денситометрії (ДРА) передбачала застосування методології, прийнятої National Osteoporosis Guideline Group у Великій Британії, яка використана і в європейських рекомендаціях. Результати. Встановлено зростання з віком межі для фармакологічного втручання (верхня межа) з 6,6 % у 40 років до 13 % у 75–85 років. Нижня межа втручання (необхідність обстеження) вірогідно збільшувалась з 2,4 % у 40 років до 6,9 % у жінок віком 85 років. Стратегія оцінки починається з аналізу в анамнезі низькотравматичного перелому. За його наявності приймається рішення про початок антиостеопоротичного лікування без проведення ДРА. За відсутності перелому в анамнезі необхідна оцінка ризику переломів за FRAX. При перевищенні верхньої межі рекомендовано антиостеопоротичне лікування без проведення ДРА, при його значеннях менше за нижню межу — додаткове обстеження чи лікування не потрібні. За умови наявності проміжних показників ризику необхідне проведення ДРА з переоцінкою ризику переломів і тактики ведення. Висновки. Доведено ефективність використання принципів оцінки FRAX, що застосовуються в європейських рекомендаціях, але з урахуванням епідеміології остеопоротичних переломів в Україні. Незважаючи на те, що даний підхід є економічно ефективним в інших країнах, його застосування в Україні може відрізнятись і потребує подальшого вивчення з економічною оцінкою затрат і переваг.
Актуальность. На сегодняшний день алгоритм FRAX® является информативным методом оценки риска остеопоротических переломов, реализованным в европейские и американские рекомендации по менеджменту остеопороза. Однако существуют различия относительно границ вмешательства для антиостеопоротического лечения, зависящие от страны, модели оказания медицинской помощи и возвращения средств за лечение. Собственная модель FRAX появилась в Украине в 2016 году, однако границы вмешательства до сих пор разработаны не были. Цель исследования: определить границы для фармакологического лечения остеопороза и дополнительного обследования населения Украины с помощью национальной модели FRAX. Материалы и методы. Обследовано 3790 амбулаторных женщин в возрасте 40–90 лет (средний возраст — 61,9 ± 10,0 года). Разработка границ вмешательства и дополнительной оценки состояния костной ткани с использованием двухэнергетической рентгеновской денситометрии (ДРА) предусматривала применение методологии, принятой National Osteoporosis Guideline Group в Великобритании, которая использована и в европейских рекомендациях. Результаты. Установлено повышение с возрастом границы для фармакологического вмешательства (верхняя граница) с 6,6 % в 40 лет до 13 % в 75–85 лет. Нижняя граница вмешательства (необходимость обследования) достоверно увеличивалась с 2,4 % в 40 лет до 6,9 % у женщин в возрасте 85 лет. Стратегия оценки начинается с анализа в анамнезе низкотравматического перелома. При его наличии принимается решение о начале антиостеопоротического лечения без проведения ДРА. При отсутствии перелома в анамнезе необходима оценка риска переломов по FRAX. При превышении верхней границы рекомендуется антиостеопоротическое лечение без проведения ДРА, при его значениях меньше нижней границы — дополнительное обследование или лечение не нужны. При наличии промежуточных показателей риска необходимо проведение ДРА с переоценкой риска переломов и тактики ведения. Выводы. Доказана эффективность использования принципов оценки FRAX, применяемых в европейских рекомендациях, но с учетом эпидемиологии остеопоротических переломов в Украине. Несмотря на то, что данный подход является экономически эффективным в других странах, его применение в Украине может отличаться и требует дальнейшего изучения с экономической оценкой затрат и преимуществ.
Background. Nowadays, FRAX® algorithm is an informative method for evaluation of the risk of osteoporotic fractures, implemented in European and American guidelines for osteoporosis management. However, there are differences in “intervention thresholds” for antiosteoporotic treatment, which depend on the country, the model of health care system and the reimbursement for treatment. Ukrainian version of FRAX appeared in Ukraine in 2016, but the thresholds for intervention have not yet been developed. The purpose of the study was to determine the “thresholds” for the pharmacological treatment of osteoporosis and for additional diagnostic examination of Ukrainian population using national FRAX model. Materials and methods. 3790 outpatients aged 40–90 years (mean age 61.9 ± 10.0 years) were examined. The development of the “thresholds” for intervention and additional assessment of the bone using dual-energy X-ray densitometry (DXA) based on the methodology adopted by the National Osteoporosis Guideline Group in UK, which is further used in European guidelines. Results. There was an increase of the “threshold” for pharmacological intervention (“upper threshold”) with age from 6.6 % at the age of 40 to 13 % at the age of 75–85 years. The “lower threshold” (threshold for additional examination) increased significantly from 2.4 % at the age of 40 to 6.9 % in women aged 85 years. The evaluation strategy begins with an analysis of the history of low-traumatic fracture. In its presence, a decision to start antiosteoporotic treatment without DXA should be made. In patients without history of fracture, calculation of fracture risk according to FRAX is required. When the risk exceeds the limit of the “upper threshold” antiosteoporotic treatment without DXA is recommended, when its values below the limit of “lower threshold” — additional examination or treatment is not required. In case of intermediate risk of fracture a DXA should be conducted with a reassessment of fracture risk and management tactics. Conclusions. The effectiveness of FRAX principles which uses in European guideline, but with particularities of the epidemiology of osteoporotic fractures in Ukraine, has been proved. Although this approach is cost-effective in other countries, its use in Ukraine may differ and may need to be further explored with an economic assessment of costs and benefits.
FRAX®; остеопороз; межа втручання; лікування; діагностика; ризик остеопоротичних переломів
FRAX®; остеопороз; граница вмешательства; лечение; диагностика; риск остеопоротических переломов
FRAX®; osteoporosis; threshold of intervention; treatment; diagnosis; risk of osteoporotic fractures
Вступ
На сьогодні своєчасна діагностика остеопорозу та його ускладнень має надзвичайно важливе значення. Останніми роками важливим інструментом оцінки ризику остеопоротичних переломів, який все більше впроваджується в клінічну практику, є алгоритм FRAX® (Fracture Risk Assessment Tool) — метод оцінки 10-річної ймовірності (ризику) основних остеопоротичних переломів (переломи стегнової та плечової кісток, кісток передпліччя й клінічно значущі переломи тіл хребців) й окремо переломів стегнової кістки в осіб віком 40 років і старше [1].
На даний час встановлено, що показник мінеральної щільності кісткової тканини (МЩКТ), отриманий за результатами двохенергетичної рентгенівської абсорбціометрії (ДРА), є важливим, проте не єдиним критерієм у визначенні ризику остеопоротичних переломів. І якщо в 90-х роках минулого сторіччя його зниження (Т ≤ –2,5 SD) було одним з важливих критеріїв для ініціації антиостеопоротичного лікування, то сьогодні продемонстровано, що переломи можуть виникати на тлі остеопенії чи нормальних показників МЩКТ. У зв’язку з цим на даний час велику роль приділяють іншим факторам, що визначають як «чинники ризику остеопорозу та остеопоротичних переломів», які є важливими в розрахунку цього ризику. Вивчення ролі різних факторів ризику остеопорозу дозволило накопичити велику доказову базу, визначити їх роль у виникненні переломів [2] та стало підґрунтям для розробки алгоритму FRAX. Алгоритм передбачає розрахунок 10-річної ймовірності основних остеопоротичних переломів та переломів стегнової кістки з урахуванням показників віку, індексу маси тіла (ІМТ) та різних клінічних факторів ризику переломів з дослідженням показника МЩКТ шийки стегнової кістки чи без нього.
Розробка й валідизація опитувальника FRAX детально описані у зарубіжних і вітчизняних публікаціях [1–5]. На сьогодні оцінка 10-річної ймовірності остеопоротичних переломів згідно з FRAX є важливим критерієм для початку лікування та визначення необхідності інструментального дообстеження хворих як в європейських, так і в американських рекомендаціях [6, 7].
Використання FRAX для оцінки ризику основних остеопоротичних переломів почалось у 2008 році, хоч шлях до його створення розпочався на початку –2000-х років [3]. В Українському науково-медичному центрі проблем остеопорозу алгоритм FRAX активно використовується в оцінці ризику остеопоротичних переломів з 2010 року [4]. Проведені нами дослідження із застосуванням моделей інших країн в українських чоловіків і жінок продемонстрували, що для оцінки ризику переломів можуть використовуватись різні моделі, важливими залишаються лише країно-специфічні значення межі для ініціації лікування чи додаткового обстеження [8, 9]. Крім того, результати наших досліджень встановили, що критерії, які використовуються в американських та деяких інших рекомендаціях для початку лікування (20 і більше для основних остеопоротичних переломів й 3 і більше — для переломів стегнової кістки), не можуть бути застосовані для оцінки ризику переломів в українській популяції, оскільки за умови використання моделей сусідніх країн (через відсутність в Україні власної моделі на момент проведення дослідження) вони є значно вищими [10]. У подальшому нами розроблені й запропоновані до застосування критерії втручання з використанням австрійської моделі FRAX [8, 11], які успішно використовувались до появи оригінальної української моделі FRAX.
Літом 2016 року силами співробітників ДУ «Інститут геронтології імені Д.Ф. Чеботарьова НАМН України» та Українського науково-медичного центру проблем остеопорозу опитувальник було адаптовано українською мовою, а восени того ж року завдяки авторам статті на офіційному інтернет-ресурсі FRAX (https://www.sheffield.ac.uk/FRAX) з’явилась нова українська модель. Її створення базується на результатах епідеміологічних досліджень, проведених у 1997–2002 та 2011–2012 роках членами Української асоціації остеопорозу за підтримки Української асоціації травматологів-ортопедів. Вітчизняна модель FRAX стала першою й унікальною моделлю прогнозування ризику основних остеопоротичних переломів у населення України. Її побудова передбачала наявність певних коефіцієнтів для факторів ризику в оригінальній моделі FRAX, а також вікових і статевих показників захворюваності щодо переломів проксимального відділу стегнової кістки, які були отримані в результаті епідеміологічних досліджень. При розробці даної моделі автори вважали, що значення b-коефіцієнтів для переломів було аналогічне до тих, що були визначені в раніше проведених метааналізах [3, 8].
На даний час алгоритм FRAX доступний у вільному доступі в Інтернеті (http://www.shef.ac.uk/FRAX) на 35 мовах для 65 країн з 71 моделлю й являє собою опитувальник, що складається з 12 питань, останнім (і не обов’язковим) з яких є показник МЩКТ стегнової кістки (рис. 1). На сьогодні більше 25 тисяч обчислень ризику переломів за допомогою української моделі FRAX виконано на його сайті.
Як зазначалось вище, важлива практична значущість FRAX у клінічній практиці полягає у прогнозуванні ризику основних остеопоротичних переломів. Проте, зважаючи на їх регіональні особливості, різні підходи менеджменту хворих, на сьогодні існують різні критерії як для початку антиостеопоротичного лікування (межа втручання), так і для оцінки показників МЩКТ (межа додаткового обстеження). В одному з останніх систематичних аналізів, проведеному групою розробників FRAX [5], проаналізовано межі втручань для різних популяцій, які значно відрізняються за підходами залежно від країни, моделі надання медичної допомоги та повернення коштів за лікування. До цього часу в Україні власна модель FRAX не мала своїх меж втручання, розрахованих згідно з епідеміологічною ситуацією щодо основних остеопоротичних переломів, що і стало предметом даної роботи.
Мета дослідження: визначити межі для фармакологічного лікування та додаткового обстеження хворих щодо остеопорозу за допомогою української моделі FRAX.
Матеріали та методи
Для оцінки меж для фармакологічного втручання та додаткового обстеження щодо ризику остеопоротичних переломів в українських жінок нами на базі Українського науково-медичного центру проблем остеопорозу, ДУ «Інститут геронтології імені Д.Ф. Чеботарьова НАМН України» проведено дослідження із залученням 3790 амбулаторних жінок віком 40–90 років (середній вік (M ± SD) — 61,9 ± 10,0 року). Серед обстежених у 71 особи дані щодо можливих причин вторинного остеопорозу були сумнівними, у зв’язку з чим вони були виключені з подальшого аналізу.
Дослідження було затверджено Комітетом з питань етики інституту (17.05.2017, протокол № 5) та проводилось з 05.2017 по 05.2019. Усі обстежені підписали добровільну інформовану згоду на участь в ньому з проведенням відповідних процедур дослідження.
Серед обстежених жінок 3209 (84,7 %) були в пост–менопаузальному періоді (середній вік менопаузи — 48,4 ± 5,2 року, тривалість постменопаузи — 15,3 ± 8,9 року). Основні антропометричні параметри (зріст, маса тіла) вимірювали за допомогою рутинних методів і за загальноприйнятною формулою розраховували ІМТ (ці параметри становили відповідно: зріст — 162,1 ± 6,5 см, маса тіла — 73,1 ± 14,5 кг, ІМТ — 27,8 ± 5,3 кг/м2).
Десятирічну ймовірність основних остеопоротичних переломів (MOF) та переломів стегнової кістки (HF) обчислювали за допомогою української версії FRAX на офіційному інтернет-ресурсі FRAX (https://www.sheffield.ac.uk/FRAX) з використанням показника МЩКТ та без нього.
За допомогою ДРА вимірювали МЩКТ шийки стегнової кістки й розраховували показники Т і Z на двох приладах (PRODIGY, GEHC Lunar, Madison, WI, США, та DISCOVERY Wi, Hologic, Inc., США).
Підхід до встановлення меж втручання та додаткової оцінки стану кісткової тканини із застосуванням ДРА включав використання методології, прийнятої Національною групою щодо створення рекомендацій (National Osteoporosis Guideline Group, NOGG)) щодо остеопорозу на основі FRAX у Великій Британії [12, 13], який у подальшому був застосований і в європейських рекомендаціях [6].
Критерієм, згідно з яким пацієнту необхідно рекомендувати фармакологічне втручання (межа втручання), у жінок була наявність низькотравматичного перелому в анамнезі, оскільки сучасні численні рекомендації щодо ведення пацієнтів з остеопорозом рекомендують розглядати цей факт як ключовий у пост–менопаузальних жінок та чоловіків старшого віку. За оцінкою Всесвітньої організації охорони здоров’я (ВООЗ), низькотравматичним переломом (Fragility fracture) є перелом, що виникає за дії сили, еквівалентній падінню з висоти власного зросту чи нижче [14]. Факторами його ризику є, зокрема, вік, стать, низька МЩКТ, сімейний анамнез остеопорозу, переломи в анамнезі тощо. Найчастіше це хребці, проксимальний відділ стегнової кістки й дистальний відділ кісток передпліччя (променева кістка), а також плечова кістка, кістки таза, ребра та інші.
Зважаючи на те, що попередній низькотравматичний перелом вважали достатнім ризиком, щоб рекомендувати лікування, межа втручання для жінок без попереднього перелому встановлювалася за показником вік-залежного 10-річного ризику основних остеопоротичних переломів, еквівалентним жінкам з попереднім низькотравматичним переломом при обчисленні за допомогою української моделі FRAX. Розрахунок проводили при ІМТ 25 кг/м2.
Для розробки межових значень для тестування показників МЩКТ були розглянуті два підходи, що використовувались раніше при адаптації інших моделей FRAX [12, 13]:
1) ймовірність, нижче якої не слід розглядати ні лікування, ні додаткове обстеження пацієнта на ДРА (нижня межа оцінки);
2) ймовірність, вище якої може бути рекомендовано лікування незалежно від показників МЩКТ (верхня межа оцінки).
Нижня межа оцінки була встановлена для виключення необхідності проводити ДРА з метою визначення МЩКТ у жінок без клінічних факторів ризику, як це й рекомендовано в чинних європейських рекомендаціях [6], тоді як верхня межа оцінки необхідна для мінімізації ймовірності того, що пацієнт з високим ризиком лише на основі факторів ризику буде перекласифікований у групу низького ризику на основі додаткової інформації щодо МЩКТ [15].
Верхня межа оцінки була встановлена в 1,2 раза вищою, ніж межа втручання. Подібний підхід використовується й у Великій Британії [16]. Нижня межа оцінки встановлювалась відповідно до вік-залежного 10-річного ризику остеопоротичних переломів, еквівалентного особам без клінічних факторів ризику.
При розробці стратегії оцінки жінок з низькотравматичним переломом в анамнезі розцінювали як кандидатів на лікування без необхідності додаткової оцінки показників МЩКТ. У жінок без низькотравматичного перелому в анамнезі рекомендації щодо ризику базувались на оцінці 10-річної ймовірності основних остеопоротичних переломів, що відповідала показникам в даній віковій підгрупі.
Жінки з імовірністю, яка була меншою за нижню межу оцінки, не потребували лікування. Особи з 10-річною ймовірністю основних остеопоротичних переломів, що перевищувала верхню межу оцінки, вважалися придатними до лікування. Жінки з імовірністю між верхнім і нижнім межовими рівнями оцінки вважались особами, яких слід скеровувати на додаткове вимірювання показників МЩКТ і в яких у подальшому необхідно переоцінювати їх ризик переломів. Під час повторної оцінки ризику основних остеопоротичних переломів з включенням показників МЩКТ шийки стегнової кістки особи вважалися придатними до лікування, коли 10-річна ймовірність перелому була вищою за межу втручання, навіть за умови нормальних показників МЩКТ чи остеопенії згідно з ДРА.
Результати
Аналіз показників 10-річної ймовірності основних остеопоротичних переломів згідно з FRAX виявив їх вірогідне зростання з віком, за виключенням ризику основних остеопоротичних переломів з урахуванням показників МЩКТ у жінок віком 80–89 років. Крім того, 10-річна ймовірність переломів з урахуванням показників МЩКТ була вищою за відповідну без їх урахування в усіх вікових групах, за винятком вікової групи 80–89 років.
Отримані нами результати засвідчили зростання з віком межі для фармакологічного втручання (верхня межа оцінки) з 6,6 % у 40 років до 13 % у 75 років. У подальшому (до віку 85 років) не встановлено збільшення даної межі, а в жінок віком 90 років цей показник дещо знижувався й становив 12 %. На відміну від вищезазначеного, нижня межа оцінки вірогідно збільшувалась з 2,4 % у 40 років до 6,9 % у жінок віком 85 років, зменшуючись при цьому лише в осіб віком 90 років (табл. 1, рис. 2). Середній показник FRAX для основних остеопоротичних переломів за умови використання параметра МЩКТ у моделі становив 8,7 %, показники нижньої та верхньої межі втручання — 4,6 та 10,5 % відповідно.
Аналіз досліджуваної нами когорти виявив, що 51,3 % жінок мали низькотравматичний перелом і, таким чином, потребували антиостеопоротичного лікування без визначення показників МЩКТ. При подальшому аналізі показників встановлено, що 1,5 % (0,7 % усієї обстеженої популяції) жінок мали ризик вище верхньої межі оцінки й також потребували лікування, а 61 % (29,7 % усієї обстеженої популяції) мали показники менше за нижню межу оцінки й не вимагали лікування. Жінки з проміжним ризиком становили 37,6 % (18,3 % усієї обстеженої популяції) й потребували подальшого вимірювання МЩКТ для визначення тактики подальшого ведення. З них у 12,9 % ризик був низьким, а в 5,4 % — високим.
Характеристики ризику та необхідність проведення ДРА залежали від віку. З віком збільшувалась частка жінок з низькотравматичними переломами в анамнезі (з 34,3 % у 40–49 років до 66,3 % у 70–79 років, середній показник — 52,4 %) та потреба в антиостеопоротичному лікуванні (44,1 % у 40–49 років до 66,8 % у 80–89 років, середній показник — 58,2 %). На відміну від цього, з віком зменшувалась частка жінок з помірним ризиком переломів, що потребувала проведення ДРА (з 34,8 % у 40–49 років до 8,4 % у 70–79 років, середній показник — 18,6 %).
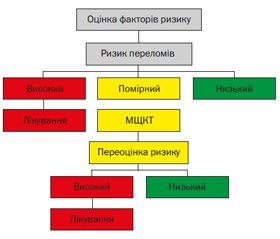
Стратегія ведення жінок з урахуванням ризику остеопоротичних переломів починається з аналізу в анамнезі низькотравматичного перелому. За його наявності рішення про початок антиостеопоротичного лікування може бути прийнято без проведення ДРА. У жінки без попереднього низькотравматичного перелому необхідна оцінка ризику основних остеопоротичних переломів згідно з алгоритмом FRAX з урахуванням віку, статі й клінічних факторів ризику. Якщо ризик перевищує верхню межу оцінки, рекомендовано антиостеопоротичне лікування без проведення ДРА (ДРА може бути виконана для подальшого моніторингу ефективності лікування). Якщо ризик менше за нижню межу оцінки, жінка не потребує ні додаткового обстеження, ні лікування. За умови, якщо особа має проміжні показники ризику, необхідне проведення ДРА з переоцінкою ризику переломів і тактики ведення обстеженого (рис. 3).
Таким чином, для української жінки в постменопаузальному періоді віком 60 років проведення ДРА з вимірюванням показників МЩКТ не рекомендовано за наявності 10-річної ймовірності основних остеопоротичних переломів менше 4 %. Лікування повинно бути рекомендованим без визначення показників МЩКТ (для оцінки ризику переломів) за наявності 10-річної ймовірності основних остеопоротичних переломів більше 10 %. Проте проведення ДРА може бути рекомендованим для моніторингу ефективності антиостеопоротичної терапії. При цьому, якщо цей ризик лежить у межах від 4 до 10 %, рекомендована додаткова оцінка показників МЩКТ й переоцінка ризику переломів. Якщо за даними ДРА виявлено остеопороз — необхідно призначення лікування. Якщо виявлена остеопенія чи нормальні показники МЩКТ — необхідна переоцінка ризику основних остепоротичних переломів згідно з показниками вік-залежної межі втручання. Особам віком 60 років, яким проведена ДРА, лікування рекомендовано за показника 10-річної ймовірності основних остеопоротичних переломів 8,3 % чи більше незалежно від наявності остеопенії чи нормальних показників МЩКТ.
Якщо ризик перелому базується лише на обчисленні клінічних факторів ризику (вік, стать та інші) без показників МЩКТ, зазначені межі стосуються лише рекомендацій щодо лікування чи необхідності додаткового проведення ДРА.
Також слід підкреслити, що межі оцінки за умови додаткового обстеження (вік-залежний інтервал між нижньою та верхньою межею) можуть використовуватись лише з застосуванням показників МЩКТ стегнової кістки, а не іншої локалізації (поперековий відділ хребта чи кістки передпліччя). Крім того, використання будь-яких інших методів дослідження стану кісткової тканини (ультразвукова денситометрія чи комп’ютерна томографія) для даного обчислення не придатні.
Обговорення
На даний час у світі існують три основні стратегії для початку антиостеопоротичного лікування, які прийняті не в усіх, проте в більшості європейських та американських рекомендацій.
1. Низький показник Т (≤ –2,5 SD, визначений за критеріями ВООЗ як остеопороз) на рівні поперекового відділу хребта, стегнової кістки чи її шийки, визначений за допомогою ДРА, який є універсальним інструментальним критерієм у постменопаузальних жінок та чоловіків віком 50 років та старше. Оцінка ризику в молодих жінок (репродуктивний період) та чоловіків (молодше 50 років) проводиться згідно з критерієм Z. Його зниження < –2,0 SD описується як «нижче очікуваного діапазону в даному віці», не є діагнозом і потребує подальшого дообстеження для визначення причин зниження МЩКТ.
2. Наявність низькотравматичного перелому в чоловіків і жінок у постменопаузі [5, 6, 13] є показанням до фармакологічного втручання без визначення показників МЩКТ у численних рекомендаціях. Проте у деяких країнах (Канада, США, Японія та Шотландія) лікування рекомендують лише пацієнтам із переломами хребців і стегнової кістки [5].
3. Високий ризик остеопоротичних переломів, розрахований за допомогою алгоритму FRAX, у хворих з низькими показниками МЩКТ (показник Т у межах > –2,5 і ≤ –1,0 SD) [5, 7] рекомендований для прийняття рішення про початок антиостеопоротичного лікування в більшості сучасних рекомендацій з використанням різних стратегій ведення.
На сьогодні при розробці меж втручання щодо FRAX використовують три підходи: перший — використання фіксованих значень, другий — вік-залежний підхід, третій — гібридні моделі (комбінація першої та другої моделі з різною послідовністю) (рис. 4).
Фіксовані межі визначались на основі дискримінаційних тестів щодо епідеміології переломів (Гонконг), медико-економічних оцінок (США, Швейцарія), частоти остеопорозу (Китай) та аналізу економічних затрат на відшкодування лікування (Японія, Польща) [5]. Вік-залежні межі втручання вперше розроблені NOGG у Великій Британії, а потім впроваджені в інших країнах Європи й імплементовані в чинні європейські рекомендації щодо менеджменту постменопаузального остеопорозу [6].
На сьогодні серед фіксованих меж втручання найнижче межове значення у Китаї: 4 % — для основних остеопоротичних переломів та 1,3 % — для переломів стегнової кістки.
У численних американських рекомендаціях, виданих різними товариствами (National Osteoporosis Foundation [7], Endocrine Society [17], American College of Obstetricians and Gynecologists [18], North American Menopause Society [19], Family practice [20], National Comprehensive Cancer Network (NCCN) [21], Institute for Clinical Systems Improvement [22]), як і канадськими товариствами (Osteoporosis Canada [23], Ministry of Health, British Columbia [24], Society of Obstetricians and Gynaecologists of Canada [25]), межовим значенням визнано 20 %. Разом з тим іншими американськими товариствами пропонується значно нижча (9,3 %) межа оцінки для додаткового визначення показників МЩКТ (US Preventive Services Task Force [26], Michigan Quality Improvement Consortiu [27], American Academy of Family Physicians [28], Institute for Clinical Systems Improvement [29]).
У рекомендаціях National Osteoporosis Foundation (NOF, 2014) [7] виділяють такі критерії щодо ініціації антиостеопоротичного лікування в постменопаузальних жінок і чоловіків віком 50 років і старше:
— перелом стегнової кістки чи хребця (клінічний чи асимптомний);
— показник Т < –2,5 SD на рівні всієї стегнової кістки, її шийки чи поперекового відділу хребта за даними ДРА;
— низька МЩКТ (Т-показник між –1,0 та –2,5 SD) на рівні стегнової кістки, її шийки чи поперекового відділу хребта за даними ДРА та 10-річний ризик переломів стегнової кістки ≥ 3 і ≥ 20 для основних остеопоротичних переломів згідно з FRAX.
Ці ж критерії рекомендовані до використання й у чоловіків у рекомендаціях Асоціації ендокринологів (2012) [17].
Вищезазначені параметри були дещо розширені в подальшому в рекомендаціях Національного альянсу з кісткового здоров’я (The National Bone Health Alliance®, NBHA) у США, що включає в себе 54 організації-члени, а також організації, що представляють центри контролю та профілактики захворювань (Centers for Disease Control and Prevention), Національну аеронавтику та космічну адміністрацію (National Aeronautics and Space Administration), Національний інститут охорони здоров’я (National Institutes of Health) та Управління контролю над продуктами харчування та ліками (US Food and Drug Administration) [30].
У цих рекомендаціях визначені такі критерії діагностики остеопорозу у жінок у постменопаузі та чоловіків віком 50 років і старше:
— перелом стегнової кістки (незалежно від показників МЩКТ);
— показник T ≤ –2,5 SD на рівні поперекового відділу хребта чи стегнової кістки;
— остеопенія (показник Т у межах > –2,5 і ≤ –1,0 SD) та попередній клінічний чи морфометрично підтверджений перелом тіла хребця, перелом проксимального відділу плечової кістки, кісток таза або, в деяких випадках, дистального відділу кісток передпліччя;
— 10-річна ймовірність перелому стегнової кістки згідно з алгоритмом FRAX ≥ 3 % або 10-річна ймовірність основних остеопоротичних переломів ≥ 20 % в осіб з остеопенією (показник Т у межах > –2,5 і ≤ –1,0 SD) [30].
Подібна межа 10-річного ризику основних остеопоротичних переломів (20 %) рекомендована й у деяких європейських рекомендаціях у Словакії [31], Словенії [32], Угорщині [33], Португалії [34], Іспанії [35, 36], Греції [37], Австрії [38], Бельгії [39].
Дещо нижча межа втручання (15 %) рекомендована до використання у Японії (Japan Osteoporosis Society; Japanese Society for Bone and Mineral Research; Japan Osteoporosis Foundation) [40] та Швейцарії [41]. Частина країн (Фінляндія [42], Південна Корея [43] та American College of Rheumatology [44]) використовують два критерії — найчастіше 10 та 20 % [5].
Як зазначалось раніше, на сьогодні у сучасних європейських рекомендаціях [6] щодо ведення постменопаузального остеопорозу використовується вік-залежний підхід до оцінки ризику основних остеопоротичних переломів. Подібний підхід було використано й при розробці меж для антиостеопоротичного лікування для української популяції. Якщо у більшості європейських рекомендацій оцінка факторів ризику остеопорозу з обмеженням проведення ДРА є цінним інструментом для прийняття рішення про початок антиостеопоротичного лікування, то в американських рекомендаціях рекомендовано проводити оцінку показників МЩКТ [7]. Як і в чинних європейських рекомендаціях [6], нами рекомендовано проведення ДРА лише у пацієнтів із помірним та високим ризиком за FRAX. Доцільність такого підходу полягає в оптимізації використання рентгенівських денситометрів.
Переоцінка ризику остеопоротичних переломів після визначення показників МЩКТ (з помірного на високий чи низький) є більш частою за умови, коли цей ризик, оцінений без показників ДРА, є помірним. Проте ймовірність переоцінки зменшується, чим далі оцінка ймовірності від меж втручання [15]. Цей підхід був апробований та доведений у Великій Британії та Канаді [15, 45, 46].
Використання даного підходу передбачає, що пацієнти високого ризику, встановленого без показників МЩКТ, будуть добре відповідати на фармакологічне втручання, що продемонстровано в раніше проведених дослідженнях [47–49], й доведено, що такий підхід є економічно ефективним [50].
Обмеженнями даного дослідження є те, що, незважаючи на величину когорти обстежених (3790 амбулаторних жінок), дослідження проводилось в одному центрі (Український науково-медичний центр проблем остеопорозу), а він є високоспеціалізованим центром для надання допомоги хворим з остеопорозом, тому дана вибірка може бути не повністю репрезентативною для України. Крім того, висока частка попередніх переломів та низької МЩКТ в обстежених також можуть впливати на результати дослідження.
Крім того, слід зазначити, що деякі значущі фактори ризику остеопоротичних переломів (втрата зросту, грудний кіфоз, низький рівень кальцію та вітаміну D у раціоні харчування, високий ризик падінь, доза глюкокортикоїдів) не включені в алгоритм FRAX, хоча ці фактори чинять негативний вплив на темпи втрати кісткової тканини й ризик остеопорозу. Тому додатковий їх аналіз разом з оцінкою 10-річної ймовірності остеопоротичних переломів може підвищувати інформативність даної оцінки і повинно бути рекомендованим у клінічній практиці.
Висновки
Наше дослідження довело ефективність використання принципів оцінки FRAX, які застосовуються в інших європейських рекомендаціях, але з урахуванням епідеміології остеопоротичних переломів в Україні. Очевидно, що розширення показань до лікування остеопорозу (крім показника Т –2,5 SD за результатами ДРА) за результатами оцінки ризику остеопоротичних переломів призведе до збільшення числа хворих, які потребують лікування, й матиме економічні наслідки. Незважаючи на те, що даний підхід є економічно ефективним в інших країнах, його використання в Україні може відрізнятись і потребує подальшого вивчення з економічною оцінкою затрат та переваг.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
1. Kanis J.A. on behalf of the World Health Organization Scientific Group. Assessment of osteoporosis at the primary healthcare level. Technical Report. WHO Collaborating Centre, University of Sheffield, UK. Available at http://www.shef.ac.uk/FRAX/pdfs/WHO_Technical_Report.pdf [Accessed November 22 2019].
2. Поворознюк В.В., Григорьева Н.В., Орлик Т.В., Нишкумай О.И., Дзерович Н.И., Балацкая Н.И. Остео–пороз в практике врача-интерниста. К., 2014. 198 с. [in Ukrainian].
3. Kanis J.A., Johansson H., Harvey N.C., McCloskey E.V. A brief history of FRAX. Arch. Osteoporos. 2018. 13(1). 118. doi: 10.1007/s11657-018-0510-0.
4. Поворознюк В.В., Григорьева Н.В. Роль FRAX в прогнозировании риска переломов. Новости медицины и фармации. 2011. 16(379). http://www.mif-ua.com/archive/article/21687 [Article in Ukrainian].
5. Kanis J.A., Harvey N.C., Cooper C., Johansson H., Odén A., McCloskey E.V. the Advisory Board of the National Osteoporosis Guideline Group. A systematic review of intervention thresholds based on FRAX. A report prepared for the National Osteoporosis Guideline Group and the International Osteoporosis Foundation. Arch. Osteoporos. 2016. 11(1). 25. doi: 10.1007/s11657-016-0278-z.
6. Kanis J.A., Cooper C., Rizzoli R., Reginster J.-Y. Scientific Advisory Board of the European Society for Clinical and Economic Aspects of Osteoporosis (ESCEO) and the Committees of Scientific Advisors and National Societies of the International Osteoporosis Foundation (IOF). European guidance for the diagnosis and management of osteoporosis in postmenopausal women. Osteoporos. Int. 2019. 30(1). 3-44. doi: 10.1007/s00198-018-4704-5.
7. Cosman F., deBeur S.J., LeBoff M.S. et al. Clinician’s guide to prevention and treatment of osteoporosis. Osteoporos. Int. 2014. 25(10). 2359-2381. doi: 10.1007/s00198-014-2794-2.
8. Povoroznуuk V.V., Grуgorieva N.V., Kanis J.A., McCloskey E.V., Johansson H. Ukrainian Version of FRAX: from Creation to Validation. Pain. Joints. Spine. 2016. 3(23). 6-14 [Article in Ukrainian]. doi: 10.22141/2224-1507.3.23.2016.85000.
9. Поворознюк В.В., Григорьева Н.В. Информативность различных моделей FRAX в оценке риска остео–поротических переломов у женщин Украины. Боль. Суставы. Позвоночник. 2013. 2. http://cyberleninka.ru/article/n/informativnost-razlichnyh-modeley-frax-v-otsenke-riska-osteoporoticheskih-perelomov-u-zhenschin-ukrainy [Article in Ukrainian].
10. Поворознюк В.В., Григорьева Н.В. Оценка возможностей использования австрийской модели FRAX в прогнозировании риска остеопоротических переломов у украинских женщин. Боль. Суставы. Позвоночник. 2013. 3. http://www.mif-ua.com/archive/article/37586 [Article in Ukrainian].
11. Povoroznyuk V.V., Grygorieva N.V., Kanis J.A. et al. Epidemiology of hip fracture and the development of FRAX in Ukraine. Arch. Osteoporos. 2017. 12(1). 53. doi: 10.1007/s11657-017-0343-2.
12. Kanis J.A., Johnell O., Oden A., Johansson H., McCloskey E. FRAX™ and the assessment of fracture probability in men and women from the UK. Osteoporos. Int. 2008. 19(4). 385-97. doi: 10.1007/s00198-007-0543-5.
13. Compston J., Cooper A., Cooper C. et al. National Osteoporosis Guideline Group (NOGG). UK clinical guideline for the prevention and treatment of osteoporosis. Arch. Osteoporos. 2017. 12(1). 43. doi: 10.1007/s11657-017-0324-5.
14. Osteoporosis: Fragility Fracture Risk: Osteoporosis: Assessing the Risk of Fragility Fracture. NICE Clinical Guidelines, No. 146. National Clinical Guideline Centre (UK). London: Royal College of Physicians (UK); 2012 Aug. https://www.ncbi.nlm.nih.gov/books/NBK115326.
15. Johansson H., Oden A., Johnell O. et al. Optimisation of BMD measurements to identify high risk groups for treatment — a test analysis. J. Bone Miner. Res. 2004. 19(6). 906-13. doi: 10.1359/jbmr.2004.19.6.906.
16. Kanis J.A., McCloskey E.V., Johansson H., Strom O., Borgstrom F., Oden A. the National Osteoporosis Guideline Group Case finding for the management of osteoporosis with FRAX® — assessment and intervention thresholds for the UK. Osteoporos. Int. 2008. 19(10). 1395-408. doi: 10.1007/s00198-008-0712-1.
17. Watts N.B., Adler R.A., Bilezikian J.P. et al. Osteoporosis in Men: An Endocrine Society Clinical Practice Guideline. The Journal of Clinical Endocrinology & Metabolism. 2012. 97(6). 1802-22. doi: 10.1210/jc.2011-3045.
18. American College of Obstetricians and Gynecologists (ACOG). Osteoporosis. Washington (DC): American College of Obstetricians and Gynecologists (AC OG). 2012 Sep. 17 p. (ACOG practice bulletin; no. 129).
19. North American Menopause Society (NAMS). Management of osteoporosis in postmenopausal women position statement of The North American Menopause Society. Menopause. 2010. 17. 25-54.
20. Sweet M.G., Sweet J.M., Jeremiah M.P., Galaska S.S. Diagnosis and Treatment of Osteoporosis. American Family Physician. 2008. 79. 193-200.
21. Gralow J.R., Biermann J.S., Farooki A. et al. NCCN Task Force Report: Bone Health in Cancer Care. Journal of the National Comprehensive Cancer Network. 2009. 7. S1-32.
22. Florence R., Allen S., Benedict L. et al. Diagnosis and treatment of osteoporosis. Bloomington (MN): Institute for Clinical Systems Improvement (ICSI). 2013. https://www.icsi.org/guideline/osteoporosis [Accessed November 22, 2019].
23. Papaioannou A., Morin S., Cheung A.M. et al. 2010 Clinical practice guidelines for the diagnosis and management of osteoporosis in Canada: summary. CMAJ. 2010. 182(17). 1864-73. doi: 10.1503/cmaj.100771.
24. British Columbia Medical Association. Osteoporosis: Diagnosis, Treatment and Fracture Prevention. British Columbia Medical Association and British Columbia Ministry of health. 2012.
25. Khan A., Fortier M. Osteoporosis in menopause. J. Obstet. Gynaecol. Can. 2014. 36(9 eSuppl. C). S1-15.
26. Nelson H.D., Haney E.M., Chou R., Dana T., Fu R., Bougatsos C. Screening for osteoporosis: syste–matic review to update the 2002 US Preventive Services Task Force Recom–mendation. Evidence Syntheses No. 77. 2010 AHRQ Publication No. 10-05145-EF-1.
27. Michigan Quality Improvement Consortium Guideline Management and Prevention of Osteoporosis Michigan Quality Improvement Consortium. 2014 [Accessed November 22, 2019].
28. Jeremiah M.P., Unwin B.K., Greenawald M.H., Casiano V.E. Diagnosis and management of osteoporosis. Am. Fam. Physician. 2015. 92. 261-8.
29. Institute for Clinical Systems Improvement. Diagnosis and treatment of osteoporosis. 2013. http://www.isci.org/guidelines_more [Accessed November 22, 2019].
30. Siris E.S., Adler R., Bilezikian J. et al. The clinical diagnosis of osteoporosis: a position statement from the National Bone Health Alliance Working Group. Osteoporos. Int. 2014. 25(5). 1439-43. doi: 10.1007/s00198-014-2655-z.
31. Niemethova E., Killinger Z., Payer J. Fracture risk prediction with FRAX in Slovak postmenopausal women. Cent. Eur. J. Med. 2013. 8. 571-86.
32. Kocjan T., Prezelj J., Pfeifer M., Sever M.J., Cokolic M., Zavratnik A. Guidelines for the detection and treatment of osteoporosis. Zdravniski Vestnik-Slovenian Medical Journal. 2013. 82. 207-17. https://vestnik.szd.si/index.php/ZdravVest/article/view/635.
33. Lakatos P., Szekeres L., Takács I. et al. Magyar Reumatológia. Vol. 1. Hungarian. 2011 [Diagnostic and therapeutic guidelines for the age-related and glucocorticoid-induced osteoporosis –2011, Hungary]. 8-33.
34. Goncalves M.J., Rodrigues A.M., Canhao H., Fonseca J.E. Osteoporosis: From bone biology to individual treatment decision. Acta Med. Port. 2013. 26. 445-55. PMID: 24016655.
35. Pérez Edo L., Alonso Ruiz A., Roig Vilaseca D. et al. Spanish Society of Rheumatology. 2011 Up-date of the consensus statement of the Spanish Society of Rheumatology on osteoporosis. Reumatol. Clin. 2011. 7. 357-79. doi: 10.1016/j.reuma.2011.05.013.
36. Etxebarria-Foronda I., Caeiro-Rey J.R., Larrainzar-Garijo R. et al. SECOT-GEIOS en osteoporosis y fractura por fragilidad. Actualización. Rev. Esp. Cir. Ortop. Traumatol. 2015. 59. 373-93. doi: 10.1016/j.recot.2015.05.007.
37. Makras P., Paiopoulos G., Lyritis G.P. 2011 Guidelines for the Diagnosis and Treatment of Osteoporosis in Greece. J. Musculoskelet. Neuronal Interact. 2012. 12. 38-42. PMID: 22373950.
38. Arznei & Vernunft. Osteoporose. Knochenbruch-Krankheit. Pharmig, Verband der pharmazeutischen Industrie. Österreichs, 2010.
39. Body J.-J. Aromatase inhibitors-induced bone loss in early breast cancer. BoneKEy reports. 2012. 1. 201. doi: 10.1038/bonekey.2012.201.
40. Orimo H., Nakamura T., Hosoi T. et al. Japanese 2011 guidelines for prevention and treatment of osteoporosis — executive summary. Arch. Osteoporos. 2012. 7. 3-20. doi: 10.1007/s11657-012-0109-9.
41. Lippuner K., Johansson H., Borgström F. et al. Cost-effective intervention thresholds against osteoporotic fractures based on FRAX® in Switzerland. Osteoporos. Int. 2012. 23. 2579-89. doi: 10.1007/s00198-011-1869-6.
42. Koski A.M. Glukokortikoidin aiheuttaman osteoporoosin hoitokaavio. 2013. http://www.kaypahoito.fi/web/kh/suositukset/suositus?id=ima02292 [Accessed 22 November 2019].
43. Kim J.W., Jeon Y.J., Baek D.H., Kim T.N., Chang J.S. Percentage of the population at high risk of osteoporotic fracture in South Korea: analysis of the 2010 Fifth Korean National Health and Nutrition Examination survey data. Osteoporos. Int. 2014. 25. 1313-9. doi: 10.1007/s00198-013-2595-z.
44. Grossman J.M., Gordon R., Ranganath V.K. et al. American College of Rheumatology 2010 recommendations for the prevention and treatment of glucocorticoid-induced osteoporosis. Arthritis Care Res. (Hoboken). 2010. 62. 1515-26. doi: 10.1002/acr.20295.
45. Johansson H., Kanis J.A., Oden A., Johnell O., McCloskey E. BMD, clinical risk factors and their combination for hip fracture prevention. Osteoporos. Int. 2009. 20(10). 1675-82. doi: 10.1007/s00198-009-0845-x.
46. Leslie W.D., Majumdar S.R., Lix L.M. et al. Manitoba Bone Density Program. High fracture probability with FRAX® usually indicates densitometric osteoporosis: implications for clinical practice. Osteoporos. Int. 2011. 23(1). 391-97. doi: 10.1007/s00198-011-1592-3.
47. Kanis J.A., McCloskey E., Johansson H., Oden A., Leslie W.D. FRAX® with and without BMD. Calcif. Tiss. Int. 2012. 90(1). 1-13. doi: 10.1007/s00223-011-9544-7.
48. Leslie W.D., Lix L.M., Morin S. et al. Fracture risk assessment without bone density measurement in routine clinical practice. Osteoporos. Int. 2012. 23(1). 75-85. doi: 10.1007/s00198-011-1747-2.
49. Cauley J.A., Robbins J., Chen Z. et al. Women’s Health Initiative Investigators. Effects of estrogen plus progestin on risk of fracture and bone mineral density: the Women’s Health Initiative randomized trial. JAMA. 2003. 290(13). 1729-38. doi: 10.1001/jama.290.13.1729.
50. McCloskey E.V., Beneton M., Charlesworth D. et al. Clodronate reduces the incidence of fractures in community-dwelling elderly women unselected for osteoporosis: results of a double-blind, placebo-controlled randomized study. Journal of Bone and Mineral Research. 2007. 22(1). 135-41. doi: 10.1359/jbmr.061008.

/214-1.jpg)
/215-1.jpg)
/216-1.jpg)
/217-1.jpg)