Журнал «Боль. Суставы. Позвоночник» Том 12, №4, 2022
Вернуться к номеру
Саркопенія та ревматичні захворювання: чи існує зв’язок?
Авторы: Джус М.Б. (1), Кулик М.С. (1), Карасевська Т.А. (1), Мостбауер Г.В. (1), Івашківський О.І. (2), Потьомка Р.А. (2), Новицька Г.Л.(2)
(1) — Національний медичний університет імені О.О. Богомольця, м. Київ, Україна
(2) — Комунальне некомерційне підприємство «Олександрівська клінічна лікарня», м. Київ, Україна
Рубрики: Ревматология, Травматология и ортопедия
Разделы: Справочник специалиста
Версия для печати
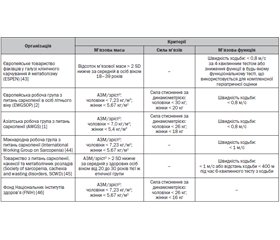
Саркопенія характеризується втратою маси скелетних м’язів, зниженням м’язової сили та/або зниженням фізичної працездатності і є однією з основних причин обмеження повсякденної діяльності в осіб літнього віку. Це пов’язано зі збільшенням частоти багатьох несприятливих наслідків, зокрема таких як падіння, м’язова слабкість, госпіталізація, інвалідність і смертність. Первинну саркопенію як складову процесу старіння і вторинну саркопенію внаслідок мальабсорбції, постільного режиму, голодування, гіпотиреозу, остеопорозу, імуноопосередкованих ревматичних захворювань об’єднує хронічний запальний процес різного ступеня вираженості. Саркопенія підтверджує одну з найбільш широко прийнятих теорій про те, що хронічне запалення низького ступеня є важливим у патогенезі багатьох захворювань. Тривалий час саркопенія розглядалась як вікасоційоване захворювання, проте останнім часом повідомляється про її поширеність серед молодих людей з автоімунними захворюваннями. Зокрема, детально вивчено зв’язок між саркопенією та ревматичним захворюванням, таким як ревматоїдний артрит. Хоча патогенез саркопенії при автоімунних захворюваннях остаточно не з’ясований, вважають, що хронічний запальний процес сприяє втраті м’язової маси й сили та є різним залежно від основного захворювання. Визначення саркопенії відрізняється за даними досліджень, що ускладнює та обмежує прямі порівняння. Тому в цьому огляді ми розглядаємо різні діагностичні критерії саркопенії, акцентуючи увагу на її поширеності серед пацієнтів з ревматичними захворюваннями, включно з ревматоїдним артритом, ювенільним ідіопатичним артритом, аксіальним спондилітом, псоріатичним артритом та системною склеродермією. Нами розроблена структурована стратегія пошуку публікацій англійською мовою в PubMed з використанням пошукового терміна «саркопенія» у поєднанні із такими ключовими словами: «запалення», «діагноз», «критерії», «м’язова маса», «сила», «наслідки», «інвалідність», «смертність», «патофізіологія», «ревматоїдний артрит», «ювенільний артрит», «аксіальний спондиліт», «псоріатичний артрит», «системний склероз». Ми зосередилися на клінічних дослідженнях, метааналізах і оглядових статях. Були відібрані статті, опубліковані після 2000 р., хоча ми не виключили основні внески, опубліковані раніше. Пошук було завершено 8 жовтня 2022 р.
Sarcopenia is characterized by a loss of skeletal muscle mass, a decrease in muscle strength and/or physical performance, and is one of the main causes for limiting daily activities in the elderly. This is associated with an increased incidence of many adverse events such as dysfunction, falls, frailty, hospitalization, disability, and mortality. Primary (considered as a part of the aging process) and secondary sarcopenia (due to malabsorption, immobility/bed rest, starvation, hypothyroidism, osteoporosis, immune-mediated rheumatic diseases) are united by a chronic inflammatory process of different degrees. Sarcopenia supports one of the most widely accepted theories that low-grade chronic inflammation is important in the pathogenesis of many diseases. For a long time, sarcopenia was considered an age-related disease, but recently it has been reported to be more common in young subjects with autoimmune diseases. In particular, the relationship between sarcopenia and rheumatic diseases such as rheumatoid arthritis has been studied in detail. Although the pathogenesis of sarcopenia in autoimmune diseases is not fully understood, it is believed that a chronic inflammatory process contributes to the development of loss of muscle mass and strength, and is different depending on the underlying disease. The definition of sarcopenia varies between studies, which complicates and limits direct comparisons. Therefore, in this review, we demonstrate various diagnostic criteria for sarcopenia, focusing on its prevalence in patients with rheumatic diseases, including rheumatoid arthritis, juvenile idiopathic arthritis, axial spondylitis, psoriatic arthritis, and systemic sclerosis. We developed a structured search strategy for English language publications in PubMed using the term “sarcopenia” in combination with the following keywords: “inflammation”, “diagnosis”, “criteria”, “muscle mass”, “strength”, “outcomes”, “disability”, “mortality”, “pathophysiology”, “rheumatoid arthritis”, “juvenile arthritis”, “axial spondylitis”, “psoriatic arthritis”, “systemic sclerosis”. We focused on clinical trials, meta-analyses and review articles. Articles published only after 2000 year were included, however, we did not include major contributions published before. The search was completed on October 8, 2022.
саркопенія; запалення; ревматичні захворювання; літературний огляд
sarcopenia; inflammation; rheumatic diseases; review
Для ознакомления с полным содержанием статьи необходимо оформить подписку на журнал.
- Chen L.K., Lee W.J., Peng L.N., Liu L.K., Arai H., Akishita M. Recent advances in sarcopenia research in Asia: 2016 update from the Asian Working Group for Sarcopenia. J. Am. Med. Dir. Assoc. 2016 Aug 1. 17(8). 767.e1-7. doi: 10.1016/j.jamda.2016.05.016.
- Cruz-Jentoft A.J., Landi F., Schneider S.M. et al. Prevalence of and interventions for sarcopenia in ageing adults: a systematic review. Report of the International Sarcopenia Initiative (EWGSOP and IWGS). Age Ageing. 2014 Nov. 43(6). 748-59. doi: 10.1093/ageing/afu115.
- Chen L.K., Liu L.K., Woo J. et al. Sarcopenia in Asia: consensus report of the Asian Working Group for Sarcopenia. J. Am. Med. Dir. Assoc. 2014 Feb. 15(2). 95-101. doi: 10.1016/j.jamda.2013.11.025.
- Chan R., Leung J., Woo J. A prospective cohort study to examine the association between dietary patterns and sarcopenia in Chinese community-dwelling older people in Hong Kong. J. Am. Med. Dir. Assoc. 2016 Apr 1. 17(4). 336-42. doi: 10.1016/j.jamda.2015.12.004.
- Beaudart C., Zaaria M., Pasleau F., Reginster J.Y., Bruyere O. Health outcomes of sarcopenia: a systematic review and meta-analysis. PLoS One. 2017 Jan 17. 12(1). e0169548. doi: 10.1371/journal.pone.0169548.
- Frost H.M. Bone’s mechanostat: a 2003 update. Anat. Rec. A Discov. Mol. Cell Evol. Biol. 2003 Dec. 275(2). 1081-101. doi: 10.1002/ar.a.10119.
- Kaji H. Interaction between muscle and bone. J. Bone Metab. 2014 Feb. 21(1). 29-40. doi: 10.11005/jbm.2014.21.1.29.
- Franceschi C., Bonafe M., Valensin S. et al. Inflamm-aging. An evolutionary perspective on immunosenescence. Ann. NY Acad. Sci. 2000 Jun. 908. 244-54. doi: 10.1111/j.1749-6632.2000.tb06651.x.
- Feng M., Peng H., Yao R. et al. Inhibition of cellular communication network factor 1 (CCN1)-driven senescence slows down cartilage inflammaging and osteoarthritis. Bone. 2020 Oct. 139. 115522. doi: 10.1016/j.bone.2020.115522.
- Chambers E.S., Akbar A.N. Can blocking inflammation enhance immunity during aging? J. Allergy Clin. Immunol. 2020 May. 145(5). 1323-31. doi: 10.1016/j.jaci.2020.03.016.
- Perretti M., D’Acquisto F. Novel aspects of annexin 1 and glucocorticoid biology. intersection with nitric oxide and the lipoxin receptor. Inflamm. Allergy Drug Targets. 2006 Apr. 5(2). 107-14. doi: 10.2174/187152806776383170.
- Wilson D., Jackson T., Sapey E., Lord J.M. Frailty and sarcopenia: The potential role of an aged immune system. Ageing Res. Rev. 2017 Jul. 36. 1-10. doi: 10.1016/j.arr.2017.01.006.
- Bano G., Trevisan C., Carraro S. et al. Inflammation and sarcopenia: A systematic review and meta-analysis. Maturitas. 2017 Feb. 96. 10-5. doi: 10.1016/j.maturitas.2016.11.006.
- Sanchez-Castellano C., Martin-Aragon S., Bermejo-Bescos P. et al. Biomarkers of sarcopenia in very old patients with hip fracture. J. Cachexia Sarcopenia Muscle. 2020 Apr. 11(2). 478-86. doi: 10.1002/jcsm.12508.
- Santoro A., Guidarelli G., Ostan R. et al. Gender-specific association of body composition with inflammatory and adipose-related markers in healthy elderly Europeans from the NU-AGE study. Eur. Radiol. 2019 Sep. 29(9). 4968-79. doi: 10.1007/s00330-018-5973-2.
- Dzhus M., Kulyk M., Karasevska T. POS1315. Prevalence of sarcopenia in young adults with juvenile idiopathic arthritis. Ann. Rheum. Dis. 2022. 81(suppl. 1, EULAR 2022 European Congress of Rheumatology; 2022 Jun 1-4. Copenhagen). 995. doi. 10.1136/annrheumdis-2022-eular.3742.
- Costamagna D., Costelli P., Sampaolesi M., Penna F. Role of inflammation in muscle homeostasis and myogenesis. Mediators Inflamm. 2015. 2015. 805172. doi: 10.1155/2015/805172.
- Livshits G., Kalinkovich A. Inflammaging as a common ground for the development and maintenance of sarcopenia, obesity, cardiomyopathy and dysbiosis. Ageing Res. Rev. 2019 Dec. 56. 100980. doi: 10.1016/j.arr.2019.100980.
- Zhao W.Y., Zhang Y., Hou L.S. et al. The association between systemic inflammatory markers and sarcopenia: Results from the West China Health and Aging Trend Study (WCHAT). Arch. Gerontol. Geriatr. 2021 Jan-Feb. 92. 104262. doi: 10.1016/j.archger.2020.104262.
- Schaap L.A., Pluijm S.M., Deeg D.J., Visser M. Inflammatory markers and loss of muscle mass (sarcopenia) and strength. Am. J. Med. 2006 Jun. 119(6). 526.e9-17. doi: 10.1016/j.amjmed.2005.10.049.
- Pan L., Xie W., Fu X. et al. Inflammation and sarcopenia: A focus on circulating inflammatory cytokines. Exp. Gerontol. 2021 Oct 15. 154. 111544. doi: 10.1016/j.exger.2021.111544.
- Bian A.L., Hu H.Y., Rong Y.D., Wang J., Wang J.X., Zhou X.Z. A study on relationship between elderly sarcopenia and inflammatory factors IL-6 and TNF-α. Eur. J. Med. Res. 2017 Jul 12. 22(1). 25. doi: 10.1186/s40001-017-0266-9.
- Stenholm S., Rantanen T., Heliovaara M., Koskinen S. The mediating role of C-reactive protein and handgrip strength between obesity and walking limitation. J. Am. Geriatr. Soc. 2008 Mar. 56(3). 462-9. doi: 10.1111/j.1532-5415.2007.01567.x.
- Velloso C.P. Regulation of muscle mass by growth hormone and IGF-I. Br. J. Pharmacol. 2008 Jun. 154(3). 557-68. doi: 10.1038/bjp.2008.153.
- Taillandier D., Polge C. Skeletal muscle atrogenes. From rodent models to human pathologies. Biochimie. 2019 Nov. 166. 251-69. doi: 10.1016/j.biochi.2019.07.014.
- Morgan S.A., Hassan-Smith Z.K., Doig C.L., Sherlock M., Stewart P.M., Lavery G.G. Glucocorticoids and 11β-HSD1 are major regulators of intramyocellular protein metabolism. J. Endocrinol. 2016 Jun. 229(3). 277-86. doi: 10.1530/JOE-16-0011.
- Whittemore L.A., Song K., Li X. et al. Inhibition of myostatin in adult mice increases skeletal muscle mass and strength. Biochem. Biophys. Res. Commun. 2003 Jan 24. 300(4). 965-71. doi: 10.1016/s0006-291x(02)02953-4.
- Ibrahim M.M. Subcutaneous and visceral adipose tissue. structural and functional differences. Obes. Rev. 2010 Jan. 11(1). 11-8. doi: 10.1111/j.1467-789X.2009.00623.x.
- Stefanyk L.E., Dyck D.J. The interaction between adipokines, diet and exercise on muscle insulin sensitivity. Curr. Opin. Clin. Nutr. Metab. Care. 2010 May. 13(3). 255-9. doi: 10.1097/MCO.0b013e328338236e.
- Taaffe D.R., Harris T.B., Ferrucci L., Rowe J., Seeman T.E. Cross-sectional and prospective relationships of interleukin-6 and C-reactive protein with physical performance in elderly persons: MacArthur studies of successful aging. J. Gerontol. A Biol. Sci. Med. Sci. 2000 Dec. 55(12). M709-15. doi: 10.1093/gerona/55.12.m709.
- Schrager M.A., Metter E.J., Simonsick E. et al. Sarcopenic obesity and inflammation in the InCHIANTI study. J. Appl. Physiol. (1985). 2007 Mar. 102(3). 919-25. doi: 10.1152/japplphysiol.00627.2006.
- Visser M., Pahor M., Taaffe D.R. et al. Relationship of interleukin-6 and tumor necrosis factor-alpha with muscle mass and muscle strength in elderly men and women: the Health ABC Study. J. Gerontol. A Biol. Sci. Med. Sci. 2002 May. 57(5). M326-32. doi: 10.1093/gerona/57.5.m326.
- Miller R.R., Shardell M.D., Hicks G.E. et al. Association between interleukin-6 and lower extremity function after hip fracture — the role of muscle mass and strength. J. Am. Geriatr. Soc. 2008 Jun. 56(6). 1050-6. doi: 10.1111/j.1532-5415.2008.01708.x.
- Sullivan D.H., Johnson L.E., Dennis R.A. et al. The Interrelationships among albumin, nutrient intake, and inflammation in elderly recuperative care patients. J. Nutr. Health Aging. 2011 Apr. 15(4). 311-5. doi: 10.1007/s12603-010-0297-1.
- Vavrova L., Rychlikova J., Mrackova M., Novakova O., Zak A., Novak F. Increased inflammatory markers with altered antioxidant status persist after clinical recovery from severe sepsis: a correlation with low HDL cholesterol and albumin. Clin. Exp. Med. 2016 Nov. 16(4). 557-69. doi: 10.1007/s10238-015-0390-1.
- Ikizler T.A. Nutrition, inflammation and chronic kidney disease. Curr. Opin. Nephrol. Hypertens. 2008 Mar. 17(2). 162-7. doi: 10.1097/MNH.0b013e3282f5dbce.
- Cheung W.W., Paik K.H., Mak R.H. Inflammation and cachexia in chronic kidney disease. Pediatr. Nephrol. 2010 Apr. 25(4). 711-24. doi: 10.1007/s00467-009-1427-z.
- Bartlett D.B., Firth C.M., Phillips A.C. et al. The age-related increase in low-grade systemic inflammation (Inflammaging) is not driven by cytomegalovirus infection. Aging Cell. 2012 Oct. 11(5). 912-5. doi: 10.1111/j.1474-9726.2012.00849.x.
- Serri O., St-Jacques P., Sartippour M., Renier G. Alterations of monocyte function in patients with growth hormone (GH) deficiency: effect of substitutive GH therapy. J. Clin. Endocrinol. Metab. 1999 Jan. 84(1). 58-63. doi: 10.1210/jcem.84.1.5374.
- Rajhans R., Nair H.B., Nair S.S. et al. Modulation of in situ estrogen synthesis by proline-, glutamic acid-, and leucine-rich protein-1: potential estrogen receptor autocrine signaling loop in breast cancer cells. Mol. Endocrinol. 2008 Mar. 22(3). 649-64. doi: 10.1210/me.2007-0350.
- Marzetti E., Calvani R., Cesari M. et al. Mitochondrial dysfunction and sarcopenia of aging: from signaling pathways to clinical trials. Int. J. Biochem. Cell Biol. 2013 Oct. 45(10). 2288-301. doi: 10.1016/j.biocel.2013.06.024.
- Sayer A.A., Cruz-Jentoft A. Sarcopenia definition, diagnosis and treatment: consensus is growing. Age Ageing. 2022 Oct 6. 51(10). afac220. doi: 10.1093/ageing/afac220.
- Cederholm T., Barazzoni R., Austin P. et al. ESPEN guidelines on definitions and terminology of clinical nutrition. Clin. Nutr. 2017 Feb. 36(1). 49-64. doi: 10.1016/j.clnu.2016.09.004.
- Fielding R.A., Vellas B., Evans W.J., Bhasin S., Morley J.E., Newman A.B., et al. Sarcopenia: an undiagnosed condition in older adults. Current consensus definition: prevalence, etiology, and consequences. International working group on sarcopenia. J. Am. Med. Dir. Assoc 2011. 12. 249-256. doi: 10.1016/j.jamda.2011.01.003
- Muscaritoli M., Anker S.D., Argiles J. et al. Consensus definition of sarcopenia, cachexia and pre-cachexia: joint document elaborated by Special Interest Groups (SIG) “cachexia-anorexia in chronic wasting diseases” and “nutrition in geriatrics”. Clin. Nutr. 2010. 29. 154-159. doi: 10.1016/j.clnu.2009.12.004
- Studenski S.A., Peters K.W., Alley D.E. et al. The FNIH sarcopenia project: rationale, study description, conference recommendations, and final estimates. J. Gerontol. A Biol. Sci. Med. Sci. 2014 May. 69(5). 547-58. doi: 10.1093/gerona/glu010.
- Morley J.E., Abbatecola A.M., Argiles J.M. et al. Sarcopenia with limited mobility: an international consensus. J. Am. Med. Dir. Assoc. 2011 Jul. 12(6). 403-9. doi: 10.1016/j.jamda.2011.04.014.
- Cruz-Jentoft A.J., Baeyens J.P., Bauer J.M. et al. Sarcopenia. European consensus on definition and diagnosis. Report of the European Working Group on Sarcopenia in Older People. Age Ageing. 2010 Jul. 39(4). 412-23. doi: 10.1093/ageing/afq034.
- Giles J.T., Bartlett S.J., Andersen R.E., Fontaine K.R., Bathon J.M. Association of body composition with disability in rheumatoid arthritis: impact of appendicular fat and lean tissue mass. Arthritis Rheum. 2008 Oct 15. 59(10). 1407-15. doi: 10.1002/art.24109.
- Dogan S.C., Hizmetli S., Hayta E., Kaptanoglu E., Erselcan T., Guler E. Sarcopenia in women with rheumatoid arthritis. Eur. J. Rheumatol. 2015 Jun. 2(2). 57-61. doi: 10.5152/eurjrheum.2015.0038.
- Mochizuki T., Yano K., Ikari K., Okazaki K. Sarcopenia-associated factors in Japanese patients with rheumatoid arthritis: A cross-sectional study. Geriatr. Gerontol. Int. 2019 Sep. 19(9). 907-12. doi: 10.1111/ggi.13747.
- Malm K., Bergman S., Andersson M.L., Bremander A., Larsson I. Quality of life in patients with established rheumatoid arthritis: A phenomenographic study. SAGE Open Med. 2017 Jun 7. 5. 2050312117713647. doi: 10.1177/2050312117713647.
- Guo Q., Wang Y., Xu D., Nossent J., Pavlos N.J., Xu J. Rheumatoid arthritis: pathological mechanisms and modern pharmacologic therapies. Bone Res. 2018 Apr 27. 6. 15. doi: 10.1038/s41413-018-0016-9.
- Chimenti M.S., Triggianese P., Conigliaro P., Candi E., Melino G., Perricone R. The interplay between inflammation and metabolism in rheumatoid arthritis. Cell Death Dis. 2015 Sep 17. 6(9). e1887. doi: 10.1038/cddis.2015.246.
- Morgan S.A., McCabe E.L., Gathercole L.L. et al. 11β-HSD1 is the major regulator of the tissue-specific effects of circulating glucocorticoid excess. Proc. Natl. Acad. Sci. USA. 2014 Jun 17. 111(24). E2482-91. doi: 10.1073/pnas.1323681111.
- Masuko K. Rheumatoid cachexia revisited: a metabolic co-morbidity in rheumatoid arthritis. Front. Nutr. 2014 Nov 24. 1. 20. doi: 10.3389/fnut.2014.00020.
- Baillet A., Vaillant M., Guinot M., Juvin R., Gau–din P. Efficacy of resistance exercises in rheumatoid arthritis: meta-analysis of randomized controlled trials. Rheumatology (Oxford). 2012 Mar. 51(3). 519-27. doi: 10.1093/rheumatology/ker330.
- Khoja S.S., Almeida G.J., Chester Wasko M., Terhorst L., Piva S.R. Association of light-intensity physical activity with lower cardiovascular disease risk burden in rheumatoid arthritis. Arthritis Care Res. (Hoboken). 2016 Apr. 68(4). 424-31. doi: 10.1002/acr.22711.
- Tournadre A., Vial G., Capel F., Soubrier M., Boirie Y. Sarcopenia. Joint Bone Spine. 2019 May. 86(3). 309-14. doi: 10.1016/j.jbspin.2018.08.001.
- Lemmey A.B., Marcora S.M., Chester K., Wilson S., Casanova F., Maddison P.J. Effects of high-intensity resistance training in patients with rheumatoid arthritis: a randomized controlled trial. Arthritis Rheum. 2009 Dec 15. 61(12). 1726-34. doi: 10.1002/art.24891.
- Saarinen J., Lehtonen K., Malkia E., Lahdenne P. Lower extremity isometric strength in children with juvenile idiopathic arthritis. Clin. Exp. Rheumatol. 2008 Sep-Oct. 26(5). 947-53. Режим доступу: немає.
- Sandstedt E., Fasth A., Eek M.N., Beckung E. Muscle strength, physical fitness and well-being in children and adolescents with juvenile idiopathic arthritis and the effect of an exercise programme: a randomized controlled trial. Pediatr. Rheumatol. Online J. 2013 Feb 22. 11(1). 7. doi: 10.1186/1546-0096-11-7.
- Brabnikova Maresova K., Jarosova K., Pavelka K., Stepan J.J. The association between lean mass and bone mineral content in the high disease activity group of adult patients with juvenile idiopathic arthritis. BMC Musculoskelet. Disord. 2014 Feb 21. 15. 51. doi: 10.1186/1471-2474-15-51.
- Lien G., Selvaag A.M., Flato B. et al. A two-year prospective controlled study of bone mass and bone turnover in children with early juvenile idiopathic arthritis. Arthritis Rheum. 2005 Mar. 52(3). 833-40. doi: 10.1002/art.20963.
- Caetano M.C., Sarni R.O., Terreri M.T. et al. Excess of adiposity in female children and adolescents with juvenile idiopathic arthritis. Clin. Rheumatol. 2012 Jun. 31(6). 967-71. doi: 10.1007/s10067-012-1947-y.
- Henderson C.J., Cawkwell G.D., Specker B.L. et al. Predictors of total body bone mineral density in non-corticosteroid-treated prepubertal children with juvenile rheumatoid arthritis. Arthritis Rheum. 1997 Nov. 40(11). 1967-75. doi: 10.1002/art.1780401108.
- Henderson C.J., Specker B.L., Sierra R.I., Campaigne B.N., Lovell D.J. Total-body bone mineral content in non-corticosteroid-treated postpubertal females with juvenile rheumatoid arthritis: frequency of osteopenia and contributing factors. Arthritis Rheum. 2000 Mar. 43(3). 531-40. doi: 10.1002/1529-0131(200003)43. 3 < 531. AID-ANR8>3.0.CO. 2-X.
- Dzhus M., Kulyk M. AB0746. The association between presarcopenia and bone mineral density in adult patients with juvenile idiopathic arthritis. Ann. Rheum. Dis. 2021. 80(suppl. 1, EULAR 2021 European Congress of Rheumatology. 2021 Jun 2-5). 1401-2. doi: 10.1136/annrheumdis-2021-eular.3641.
- Dzhus M., Kulyk M., Karasevska T. P646. Investigation of muscle mass in young adults with juvenile idiopathic arthritis. Aging Clin. Exp. Res. 2022. 34(suppl. 1, World Congress on Osteoporosis, Osteoarthritis and Musculoskeletal Diseases (WCO-IOF-ESCEO 2022)). S318-9. Режим доступу: немає.
- Bok D.H., Kim J., Kim T.H. Comparison of MRI-defined back muscles volume between patients with ankylosing spondylitis and control patients with chronic back pain: age and spinopelvic alignment matched study. Eur. Spine J. 2017 Feb. 26(2). 528-37. doi: 10.1007/s00586-016-4889-2.
- Zhang Y., Xu H., Hu X., Zhang C., Chu T., Zhou Y. Histopathological changes in supraspinous ligaments, ligamentum flava and paraspinal muscle tissues of patients with ankylosing spondylitis. Int. J. Rheum. Dis. 2016 Apr. 19(4). 420-9. doi: 10.1111/1756-185X.12305.
- Krajewska-Wlodarczyk M., Owczarczyk-Saczo–nek A., Placek W. Changes in body composition and bone mineral density in postmenopausal women with psoriatic arthritis. Reumatologia. 2017. 55(5). 215-21. doi: 10.5114/reum.2017.71627.
- Siegert E., March C., Otten L. et al. Prevalence of sarcopenia in systemic sclerosis: assessing body composition and functional disability in patients with systemic sclerosis. Nutrition. 2018 Nov. 55-56. 51-5. doi: 10.1016/j.nut.2018.03.046.
- Caimmi C., Caramaschi P., Venturini A. et al. Malnutrition and sarcopenia in a large cohort of patients with systemic sclerosis. Clin. Rheumatol. 2018 Apr. 37(4). 987-97. doi: 10.1007/s10067-017-3932-y.
- Paolino S., Goegan F., Cimmino M.A. et al. Advanced microvascular damage associated with occurence of sarcopenia in systemic sclerosis patients: results from a retrospective cohort study. Clin. Exp. Rheumatol. 2020 May-Jun. 38 Suppl. 125(3). 65-72.
- Marighela T.F., Genaro P. de S., Pinheiro M.M., Szejnfeld V.L., Kayser C. Risk factors for body composition abnormalities in systemic sclerosis. Clin. Rheumatol. 2013 Jul. 32(7). 1037-44. doi: 10.1007/s10067-013-2235-1.