Журнал «Медицина неотложных состояний» Том 20, №2, 2024
Вернуться к номеру
Вплив диналбуфіну себакату на інтенсивність післяопераційного болю після мінно-вибухової травми: пілотне дослідження
Авторы: Дмитрієв Д.
КНП «Вінницька обласна клінічна лікарня ім. М.І. Пирогова», Центр термічної травми та реконструктивної хірургії, м. Вінниця, Україна
Центр лікування та реабілітації хронічного болю «Прометей», м. Вінниця, Україна
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
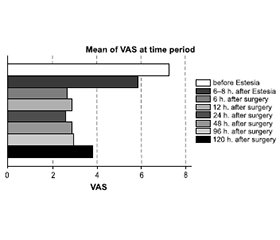
Актуальність. Мінно-вибухові поранення, часто пов’язані з травматичними й складними обставинами, створюють унікальні виклики у сфері хірургічних втручань і подальшого лікування болю. Саме тому основною метою цього дослідження було визначення безпеки й ефективності одноразової дози диналбуфіну себакату (лікарський засіб Естезія®, 150 мг/2 мл) як компонента мультимодальної аналгезії, застосованої внутрішньом’язово перед реконструктивними оперативними втручаннями з приводу мінно-вибухових уражень. Матеріали та методи. Проспективне відкрите нерандомізоване клінічне дослідження проведено за участі 15 пацієнтів з мінно-вибуховими травмами, яким як компонент мультимодальної анестезії післяопераційного болю було застосовано диналбуфіну себакат (Естезія®) 150 мг/2 мл. 15 пацієнтів отримали одноразову дозу диналбуфіну себакату 150 мг/2 мл внутрішньом’язово з використанням Z-техніки в сідничну ділянку за 12–24 год до оперативного втручання. Як інструмент оцінки вираженості больового синдрому була використана візуально-аналогова шкала (Visual Analogue Scale, VAS) з діапазоном від 0 до 10 балів (0 = відсутність болю, 10 = найгірший біль, який можна собі уявити). Для статистичного аналізу використовували програму StataCorp. 2023. Stata Statistical Software: Release 18. College Station, TX: StataCorp LLC. Для дослідження взаємозв’язку між показниками шкали оцінки тяжкості травми (Injury Severity Score, ISS) і VAS було використано simple linear regression analysis. Результати. Статистично значимого зв’язку між показниками ISS і VAS не було знайдено. Дослідження продемонструвало, що на 6-ту годину після оперативного втручання (ОВ) рівень болю значимо знизився порівняно з вираженістю болю через 6–8 годин після застосування лікарського засобу і статистично значимо не відрізнявся від показників наступних 4 діб: VAS 6 год після ОВ vs 12 год після ОВ — p = 0,2500; VAS 6 год після ОВ vs 24 год після ОВ — p = 1,0000; VAS 6 год після ОВ vs 48 год після ОВ — p = 0,4531; VAS 6 год після ОВ vs 96 год після ОВ — p = 0,2188. Водночас статистично значима різниця була виявлена між VAS 6 год після ОВ vs 120 год після ОВ — p = 0,0010. Висновки. Були продемонстровані ефективність і сприятливий профіль переносимості диналбуфіну себакату як компонента мультимодальної аналгезії в умовах післяопераційного знеболювання в пацієнтів після реконструктивних оперативних втручань, зумовлених мінно-вибуховими травмами.
Background. Mine-explosive injuries, often associated with traumatic and complex circumstances, pose unique challenges in the field of surgical interventions (SI) and subsequent pain management. That is why the main goal of this study was to determine the safety and effectiveness of a single dose of dinalbuphine sebacate (Esteziia®, 150 mg/2 ml) as a component of multimodal analgesia applied intramuscularly before reconstructive surgeries due to mine-explosive lesions. Materials and methods. A prospective, open, non-randomized clinical study was carried out with the participation of 15 patients with mine-explosive injuries, who were treated using dinalbuphine sebacate (Esteziia®) 150 mg/2 ml as a component of multimodal anesthesia for postoperative pain. All patients received a single dose of dinalbuphine sebacate 150 mg/2 ml intramuscularly using the Z-technique in the gluteal area 12–24 hours before surgery. The Visual Analogue Scale (VAS) with a range from 0 to 10 points (0 = no pain, 10 = the worst imaginable pain) was used as a tool for assessing the severity of the pain syndrome. The StataCorp 2023 program was used for statistical analysis. Stata Statistical Software: Release 18. College Station, TX: StataCorp LLC. Simple linear regression analysis was used to study the relationship between Injury Severity Score (ISS) and VAS. Results. No statistically significant relationship between ISS and VAS was found. The study showed that 6 h after SI, the level of pain significantly decreased in comparison with that 6–8 hours after the use of the drug and was not statistically significantly different from the indicators of the following four days: VAS 6 hours after SI vs. 12 hours after SI — p = 0.2500, VAS 6 hours after SI vs. 24 hours after SI — p = 1.0000, VAS 6 hours after SI vs. 48 hours after SI — p= 0.4531, VAS 6 hours after SI vs. 96 hours after SI — p= 0.2188. At the same time, a statistically significant difference was found between VAS 6 hours after SI vs. 120 hours after SI — p= 0.0010. Conclusions. The efficacy and favorable to-lerability of dinalbuphine sebacate as a component of multimodal analgesia in the setting of postoperative analgesia in patients after reconstructive surgical interventions caused by mine-explosive injuries was demonstrated.
мультимодальна аналгезія; хронічний біль; післяопераційний біль; диналбуфіну себакат; мінно-вибухова травма
multimodal analgesia; chronic pain; postoperative pain; dinalbuphine sebacate; mine-explosive injury
Вступ
Матеріали та методи
Результати та обговорення
Обговорення
/42.jpg)
Висновки
- Horoshko V., Kuchyn I. Effectiveness of pain treatment for patients with mine-blast wounds depending on the number of localizations in military mobile hospitals. Clinical and Preventive Medicine. 2023. 3. 39-44. https://doi.org/10.31612/2616-4868.3(25).2023.05.
- Kuchyn Iu.L., Horoshko V.R. Predictors of treatment failure among patients with gunshot wounds and post-traumatic stress disorder. BMC Anesthesiol. 2021. 21. 263. https://doi.org/10.1186/s12871-021-01482-8.
- Kuchyn Iu.L., Horoshko V.R. Pain syndrome in patients with gunshot wounds of the limbs and post-traumatic stress disorders. Emergency medicine. 2022. 17(7). 24-31. https://doi.org/10.22141/2224-0586.17.7.2021.244591.
- Kuchyn Iu.L., Horoshko V.R. Influence of the type of anesthesia during reconstructive surgical interventions on the final results of treatment of patients with gunshot wounds of the extremities and post-traumatic stress disorders. Current aspects of military medicine. 2021. 28(2). 92-104. https://doi.org/10.32751/2310-4910-2021-28-2-8.
- Kuchyn I., Horoshko V. Chronic pain in patients with gunshot wounds. BMC Anesthesiol. 2023. 47. https://doi.org/10.1186/s12871-023-02005-3.
- Moore E.E., Cogbill T.H., Jurkovich M.D. et al. Organ injury scaling: spleen and liver (1994 revision). J. Trauma. 1995. 38. 323.
- Wang A., Murphy J., Shteynman L., Daksla N., Gupta A., Bergese S. Novel Opioids in the Setting of Acute Postoperative Pain: A Narrative Review. Pharmaceuticals (Basel). 2023 Dec 25. 17(1). 29. doi: 10.3390/ph17010029. PMID: 38256863; PMCID: PMC10819619.
- Lee S.O., Huang L.P., Wong C.S. Preoperative Administration of Extended-Release Dinalbuphine Sebacate Compares with Morphine for Post-Laparoscopic Cholecystectomy Pain Management: A Rando-mized Study. J Pain Res. 2020 Sep 9. 13. 2247-2253. doi: 10.2147/JPR.S263315. PMID: 32982387; PMCID: PMC7490073.
- Lee Y.E., Wang S.Y., Chen J.H., Chen C.Y., Shiue Y.L., Soong T.C., Lam C.F. Efficacy and Safety of Parenteral Injection of an Extended Release κ-receptor Opioid Sebacoyl Dinalbuphine Ester for Acute and Chronic Pain After Laparoscopic Bariatric Surgery: a Randomized, Placebo-Controlled, Double-Blind Trial. Obes. Surg. 2023 Apr. 33(4). 1192-1201. doi: 10.1007/s11695-023-06502-9. Epub 2023 Feb 14. PMID: 36787017.
- Dmytriiev D. Assessment and treatment of postoperative pain in children. Anaesthesia, Pain & Intensive Care. 2018. 22(3). 392-400.
- Daverio M., von Borell F., Ramelet A.S., Sperotto F., Pokorna P., Brenner S. et al.; Analgosedation CONSORTIUM on behalf of the Pharmacology Section and the Nurse Science Section of the European Society of Paediatric and Neonatal Intensive Care. Pain and sedation management and monitoring in pediatric intensive care units across Europe: an ESPNIC survey. Crit. Care. 2022 Mar 31. 26(1). 88. doi: 10.1186/s13054-022-03957-7. Erratum in: Crit. Care. 2022 May 16. 26(1). 139. PMID: 35361254; PMCID: PMC8969245.
- Dobrovanov O., Dmytriiev D., Prochotsky A., Vidiscak M., Furkova K. Pain in COVID-19: Quis est culpa? Electron. J. Gen. Med. 2023. 20(1). em435. https://doi.org/10.29333/ejgm/12672.
- Ahmed H.M., Atterton B.P., Crowe G.G., Barratta J.L., Johnson M., Viscusi E. et al. Recommendations for effective documentation in regional anesthesia: an expert panel Delphi consensus project. Reg. Anesth. Pain. Med. 2022 May. 47(5). 301-308. doi: 10.1136/rapm-2021-103136. Epub 2022 Feb 22. PMID: 35193970; PMCID: PMC8961753.
- Dmytriiev D., Dmytriiev K., Stoliarchuk O., Semenenko A. Multiple organ dysfunction syndrome: what do we know about pain management? A narrative review. Anaesthesia, Pain & Intensive Care. 2019. 23(1). 84-91. [Google Scholar]
- Liu S.Y., Ho Y.H., Wong C.S. Multimodal Analgesia With Long-Acting Dinalbuphine Sebacate Plus Transversus Abdominis Plane Block for Perioperative Pain Management in Bariatric Surgery: A Case Report. Front. Pharmacol. 2021 May 28. 12. 683782. doi: 10.3389/fphar.2021.683782. PMID: 34122111; PMCID: PMC8193514.
- Tien Y.E., Huang W.C., Kuo H.Y., Tai L., Uang Y.S., Chern W.H., Huang J.D. Pharmacokinetics of dinalbuphine sebacate and nalbuphine in human after intramuscular injection of dinalbuphine sebacate in an extended-release formulation. Biopharm Drug Dispos. 2017 Nov. 38(8). 494-497. doi: 10.1002/bdd.2088. Epub 2017 Sep 14. PMID: 28741675.
- Lee Y.E., Fu C.Y., Shiue Y.L., Lu C.Y., Chen C.Y., Chen J.H., Chen J.L., Lam C.F. Efficacy and safety of an extended-release sebacoyl dinalbuphine ester for laparoscopic cholecystectomy: A randomized controlled trial. Medicine (Baltimore). 2023 Aug 4. 102(31). e34423. doi: 10.1097/MD.0000000000034423. PMID: 37543779; PMCID: PMC10403043.
- Lee S.O., Lu C.H., Man K.M., Cheng K.I., Wong C.S., Sun W.Z. Multimodal Analgesia With Extended-Release Dinalbuphine Sebacate for Perioperative Management: Expert Opinion and Consensus. Asian J. Anesthesiol. 2023 Sep 1. 61(3). 123-131. doi: 10.6859/aja.202309_61(3).0004. Epub 2023 Sep 1. PMID: 38320858.
- Chang T.K., Huang C.W., Su W.C., Tsai H.L., Ma C.J., Yeh Y.S. et al. Extended-Release Dinalbuphine Sebacate Versus Intravenous Patient-Controlled Analgesia with Fentanyl for Postoperative Moderate-to-Severe Pain: A Randomized Controlled Trial. Pain Ther. 2020 Dec. 9(2). 671-681. doi: 10.1007/s40122-020-00197-x. Epub 2020 Sep 29. PMID: 32990938; PMCID: PMC7648769.
- Zheng Z.H., Yeh T.T., Yeh C.C., Lin P.A., Wong C.S., Lee P.Y., Lu C.H. Multimodal Analgesia with Extended-Release Dinalbuphine Sebacate for Perioperative Pain Management in Upper Extremity Trauma Surgery: A Retrospective Comparative Study. Pain Ther. 2022 Jun. 11(2). 643-653. doi: 10.1007/s40122-022-00383-z. Epub 2022 Apr 15. PMID: 35426567; PMCID: PMC9098781.
- Pao L.H., Hsiong C.H., Hu O.Y., Wang J.J., Ho S.T. In vitro and in vivo evaluation of the metabolism and pharmacokinetics of sebacoyl dinalbuphine. Drug Metab. Dispos. 2005 Mar. 33(3). 395-402. doi: 10.1124/dmd.104.002451. Epub 2004 Dec 17. PMID: 15608131.
- Dmytriiev D., Dobrovanov O. Post-COVID pain syndrome. Anaesth. Pain Intensive Care. 2021. 25(4). 505-512. DOI: 10.35975/apic.v25i4.1582.
- Yeh C.Y., Jao S.W., Chen J.S., Fan C.W., Chen H.H., Hsieh P.S. et al. Sebacoyl Dinalbuphine Ester Extended-release Injection for Long-acting Analgesia: A Multicenter, Randomized, Double-Blind, And Placebo-controlled Study in Hemorrhoidectomy Patients. Clin. J. Pain. 2017 May. 33(5). 429-434. doi: 10.1097/AJP.0000000000000417. PMID: 27518486.

/41.jpg)
/42_2.jpg)