Международный эндокринологический журнал 3 (67) 2015
Вернуться к номеру
Результаты открытого многоцентрового нерандомизированного исследования по изучению эффективности и безопасности инсулинов: Инсуман Базал®, Инсуман Комб 25®, Инсуман Рапид® у пациентов с сахарным диабетом 2-го типа, которые прошли базовое обучение в школах диабета (SPIRIT)
Авторы: Ларин А.С., Юзвенко Т.Ю. (от группы исследователей) — Украинский НПЦ эндокринной хирургии, трансплантации эндокринных органов и тканей МЗ Украины, г. Киев
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
Целью данного исследования было определение уровня снижения гликированного гемоглобина (HbA1c) после 6 месяцев лечения инсулином Инсуман® пациентов с сахарным диабетом 2-го типа (СД-2), ранее не получавших терапию инсулином и не достигших гликемического контроля при приеме пероральных сахароснижающих препаратов (ПССП). Также изучалась эффективность обучения в школах самоконтроля СД, уточнялась средняя доза инсулина к окончанию исследования, частота гипогликемии и общая безопасность проводимого лечения.
Дизайн. Открытое многоцентровое нерандомизированное интервенционное исследование IV фазы длительностью 6 месяцев (Clinical Trials. gov: NCT01630369). Исследование проведено в 11 центрах Украины.
Популяция. Пациенты с СД-2, ранее не получавшие инсулин, мужчины и женщины > 18 лет с показателем HbA1c > 7,5 %, были распределены на три группы лечения на основании решения врача: n = 341 в группе 1 (Инсуман Базал®), n = 173 в группе 2 (Инсуман Комб 25®), n = 36 в группе 3 (Инсуман Рапид®).
Проводимое лечение. Пациенты получали один из трех видов инсулина Инсуман® в течение 24 недель в соответствии с группой распределения и титрационной схемой по протоколу. Исследование предполагало 4 визита, во время которых из медицинской документации собирались данные пациента: достижение целевого уровня HbA1c < 7,5 % к шестому месяцу, распределение пациентов в соответствии с динамикой HbA1c (снижение на 1 % и более) к шестому месяцу, Δ ГПН (глюкоза плазмы натощак) (до начала лечения — на 2–3-м визитах — шестом месяце). Между первым и вторым визитами все пациенты должны были пройти курс из пяти занятий в школе самоконтроля СД и заполнить тест, оценивающий уровень знаний.
Результаты. Лечение прошли 550 пациентов, которые были включены в анализ. Средний возраст пациентов составил 59,57 ± 9,53 года, мужчин было 231 (42 %), женщин — 319 (58 %). Общее количество пациентов, имевших макроваскулярные осложнения, в трех группах равнялось 419 (75,6 %), с микроваскулярными осложнениями — 525 (96,4 %). Статистически достоверная разница между тремя группами наблюдалась в стартовых показателях длительности СД, HbA1c и ГПН. Средняя длительность СД (годы) в группе 1 была 8,7 ± 5,0, в группе 2 — 7,7 ± 5,5 и в группе 3 — 9,9 ± 6,8. Средний показатель HbA1c (%) перед началом лечения в группе 1 был 10,4 ± 1,9, в группе 2 — 11,0 ± 1,9 и в группе 3 — 10,1 ± 1,5. Средний показатель ГПН перед началом лечения был 10,7 ± 2,2 ммоль/л в группе 1, 11,3 ± 2,7 ммоль/л в группе 2 и 10,4 ± 2,6 ммоль/л в группе 3. Было показано, что 43,9 % всех пролеченных пациентов достигли целевого значения HbA1c: 49,8 % в группе 1, 33,3 % в группе 2 и 32,3 % в группе 3. Наиболее значительное снижение показателя HbA1c к шестому месяцу лечения наблюдалось в группе 1 (Δ = –2,61 %) и в группе 2 (Δ = –2,81 %).
Общая оценка эффективности в группах (N пациентов со снижением показателя HbA1c > 1 %) n/N (%) составила 430/539 (79,7 %). Положительная динамика показателя Δ ГПН была статистически достоверной (p < 0,001) во всех группах. Повышения эффективности лечения у пациентов, успешно прошедших курс обучения в школах самоконтроля СД, не наблюдалось. У 16,5 % из 550 пациентов развились симптоматические гипогликемии: 14,9 % в группе 1, 19,6 % в группе 2 и 16,6 % в группе 3. В общей сложности 10,1 % пациентов отметили документированные эпизоды гипогликемии (≤ 3,9 ммоль/л) и 3,4 % — ночные гипогликемии. Случаев тяжелой гипогликемии отмечено не было. Одно серьезное побочное явление завершилось смертью пациента, в общей популяции было отмечено 8 побочных реакций в течение исследования.
Выводы. Лечение инсулинами Инсуман® пациентов с СД-2, не компенсированных на фоне приема ПССП, ассоциировалось с улучшением гликемического контроля без увеличения частоты тяжелых гипогликемий. Не отмечалось статистически значимого повышения эффективности терапии у пациентов, которые успешно завершили программу обучения в школе диабета, по сравнению с оценкой эффективности в целом. Состояние молодой исследуемой популяции пациентов с неадекватным контролем на исходном уровне и у которых уже развились сердечно-сосудистые осложнения, связанные с СД, в большинстве случаев улучшилось с точки зрения контроля гликемии, и при этом не было зарегистрировано эпизодов тяжелой гипогликемии. Это может быть связано с положительным влиянием обучения в школе диабета.
Метою даного дослідження було визначення рівня зниження глікованого гемоглобіну (HbA1c) після 6 місяців лікування інсуліном Інсуман® пацієнтів із цукровим діабетом 2-го типу (ЦД-2), які раніше не отримували терапію інсуліном і не досягли глікемічного контролю при прийомі пероральних цукрознижувальних препаратів (ПЦЗП). Також вивчалася ефективність навчання в школах самоконтролю ЦД, уточнювалася середня доза інсуліну до закінчення дослідження, частота гіпоглікемії і загальна безпека проведеного лікування.
Дизайн. Відкрите багатоцентрове нерандомізоване інтервенційне дослідження IV фази тривалістю 6 місяців (Clinical Trials. Gov: NCT01630369). Дослідження проведено в 11 центрах України.
Популяція. Пацієнти з ЦД-2, які раніше не отримували інсулін, чоловіки й жінки > 18 років із показником HbA1c > 7,5 %, були розподілені на три групи лікування на підставі рішення лікаря: n = 341 у групі 1 (Інсуман Базал®), n = 173 у групі 2 (Інсуман Комб 25®), n = 36 в групі 3 (Інсуман Рапід®).
Проведене лікування. Пацієнти отримували один із трьох видів інсуліну Інсуман® протягом 24 тижнів відповідно до групи розподілу і титраційної схеми по протоколу. Дослідження передбачало 4 візити, під час яких із медичної документації збиралися дані пацієнта: досягнення цільового рівня HbA1c < 7,5 % до шостого місяця, розподіл пацієнтів відповідно до динаміки HbA1c (зниження на 1 % і більше) до шостого місяця, Δ ГПН (глюкоза плазми натще) (до початку лікування — на 2–3-му візитах — шостому місяці). Між першим і другим візитами всі пацієнти повинні були пройти курс із п’яти занять у школі самоконтролю ЦД і заповнити тест, що оцінює рівень знань.
Результати. Лікування пройшли 550 пацієнтів, які були включені в аналіз. Середній вік пацієнтів становив 59,57 ± 9,53 року, чоловіків було 231 (42 %), жінок — 319 (58 %). Загальна кількість пацієнтів, які мали макроваскулярні ускладнення, у трьох групах дорівнювала 419 (75,6 %), з мікроваскулярними ускладненнями — 525 (96,4 %). Статистично достовірна різниця між трьома групами спостерігалася в стартових показниках тривалості ЦД, HbA1c і ГПН. Середня тривалість ЦД (роки) в групі 1 була 8,7 ± 5,0, у групі 2 — 7,7 ± 5,5 і в групі 3 — 9,9 ± 6,8. Середній показник HbA1c (%) перед початком лікування в групі 1 був 10,4 ± 1,9, у групі 2 — 11,0 ± 1,9 і в групі 3 — 10,1 ± 1,5. Середній показник ГПН перед початком лікування був 10,7 ± 2,2 ммоль/л у групі 1, 11,3 ± 2,7 ммоль/л у групі 2 і 10,4 ± 2,6 ммоль/л у групі 3. Було показано, що 43,9 % всіх пролікованих пацієнтів досягли цільового значення HbA1c: 49,8 % у групі 1, 33,3 % у групі 2 і 32,3 % у групі 3. Найбільш значне зниження показника HbA1c до шостого місяця лікування спостерігалося в групі 1 (Δ = –2,61 %) і в групі 2 (Δ = –2,81 %). Загальна оцінка ефективності в групах (N пацієнтів зі зниженням показника HbA1c > 1 %) n/N (%) становила 430/539 (79,7 %). Позитивна динаміка показника Δ ГПН була статистично достовірною (p < 0,001) в усіх групах. Підвищення ефективності лікування у пацієнтів, які успішно пройшли курс навчання в школах самоконтролю ЦД, не спостерігалося. У 16,5 % з 550 пацієнтів розвинулися симптоматичні гіпоглікемії: 14,9 % у групі 1, 19,6 % у групі 2 і 16,6 % у групі 3. Загалом 10,1 % пацієнтів відзначили документовані епізоди гіпоглікемії (≤ 3,9 ммоль/л) і 3,4 % — нічні гіпоглікемії. Випадків тяжкої гіпоглікемії відзначено не було. Одне серйозне побічне явище завершилося смертю пацієнта, у загальній популяції було відзначено 8 побічних реакцій протягом дослідження.
Висновки. Лікування інсулінами Інсуман® пацієнтів із ЦД-2, не компенсованих на фоні прийому ПЦЗП, асоціювалося з поліпшенням глікемічного контролю без збільшення частоти тяжких гіпоглікемій. Не відзначалося статистично значимого підвищення ефективності терапії в пацієнтів, які успішно завершили програму навчання в школі діабету, порівняно з оцінкою ефективності в цілому. Стан молодої досліджуваної популяції пацієнтів із неадекватним контролем на вихідному рівні і в яких вже розвинулися серцево-судинні ускладнення, пов’язані з ЦД, у більшості випадків покращився з точки зору контролю глікемії, і при цьому не було зареєстровано епізодів тяжкої гіпоглікемії. Це може бути пов’язано з позитивним впливом навчання в школі діабету.
The objective of this study was to evaluate the level of glycated hemoglobin (HbA1c) reduction after 6 months of treatment with Insuman® insulin in patients with diabetes mellitus type 2 (DM-2), who were not treated with insulin previously and did not achieve glycemic control with oral antidiabetic drugs (OADs). Also, we have studied the effectiveness of teaching in the schools of diabetes self-management, specified the average dose of insulin by the end of the study, the incidence of hypoglycemia and overall safety of the treatment.
Design. IV phase, open-label, multicenter, non-randomized interventional study with duration of 6 months (Clinical Trials. Gov: NCT01630369). The study was conducted in 11 centers in Ukraine.
Population. Patients with DM-2, who were not treated with insulin previously, men and women aged over 18 years, with an index HbA1c > 7.5 %, were divided into three treatment groups according do doctor’s decision: n = 341 in group 1 (Insuman Basal®), n = 173 in group 2 (Insuman Comb 25®), n = 36 in group 3 (Insuman Rapid®).
Treatment. Patients received one of three types of Insuman® insulin for 24 weeks, according to the group of distribution and titration scheme by protocol. Study suggested 4 visits, during which we have collected patient’s data from the medical records: achieving target HbA1c < 7.5 % by the sixth month, the distribution of patients according to HbA1c dynamics (a decrease of 1 % or more) to the sixth month, Δ FPG (fasting plasma glucose) (before treatment — during 2nd — 3rd visits — on sixth month). Between the first and second visit, all patients had to undergo a course of five lessons in the school of diabetes self-management and take a test assessing the level of knowledge.
Results. We have treated 550 patients included in the analysis. The average age of the patients was 59.57 ± 9.53 years, 231 patients were males (42 %), 319 — females (58 %). The total number of patients with macrovascular complications in three groups was equal to 419 (75.6 %), with microvascular complications — 525 (96.4 %). A statistically significant difference between three groups was observed in baseline parameters of DM duration, HbA1c and FPG. The average duration of DM (years) in group 1 was 8.7 ± 5.0, in group 2 — 7.7 ± 5.5, and in group 3 — 9.9 ± 6.8. The average HbA1c (%) level before treatment in group 1 was 10.4 ± 1.9, in group 2 — 11.0 ± 1.9, and in group 3 — 10.1 ± 1.5. Median FPG before treatment was 10.7 ± 2.2 mmol/l in group 1, 11.3 ± 2.7 mmol/l in group 2, and 10.4 ± 2.6 mmol/l in group 3. It was shown that 43.9 % of all treated patients achieved the target values of HbA1c: 49.8 % in group 1, 33.3 % in group 2, and 32.3 % in group 3. The most significant decrease in HbA1c level by the sixth month of treatment was observed in group 1 (Δ = –2.61 %) and in group 2 (Δ = –2.81 %). Overall assessment of the effectiveness in groups (N patients with a reduction in HbA1c > 1 %) n/N (%) was 430/539 (79.7 %). The positive dynamics of Δ FPG index was statistically significant (p < 0.001) in all groups. The improvement in the effectiveness of treatment in patients, who have successfully completed a training course at diabetes self-management schools, hasn’t been observed. In 16.5 % of 550 patients, symptomatic hypoglycemia developed: 14.9 % in group 1, 19.6 % in group 2, and 16.6 % in group 3. A total of 10.1 % of patients reported documented hypoglycemia episodes (≤ 3.9 mmol/l) and 3.4 % — nocturnal hypoglycemia. No cases of severe hypoglycemia were reported. One serious adverse event resulted in death of the patient, in the general population 8 adverse events were observed during the study.
Conclusions. Treatment with Insuman® insulins of patients with DM-2, who were not compensated while taking OADs, was associated with improved glycemic control without an increase in the incidence of severe hypoglycemia. There was no statistically significant increase in the effectiveness of therapy in patients, who have successfully completed a training program at diabetes school, compared with evaluation of overall efficiency. The state of young studied population of patients with inadequate control at baseline, and those who had developed cardiovascular complications associated with DM, improved in most cases in terms of glycemic control, and, at that, episodes of severe hypoglycemia were not detected. This may be due to the positive influence of training in diabetes school.
Статья опубликована на с. 67-81
Введение
После завершения UK Prospective Diabetes Study (UKPDS) стало очевидно, что компенсация углеводного обмена является одним из основных способов профилактики осложнений у пациентов с сахарным диабетом 2-го типа (СД-2) [1, 2]. На сегодняшний день принята концепция индивидуализации подхода к установлению целей терапии с учетом возраста пациента, наличия в анамнезе сосудистых осложнений, риска гипогликемии и ожидаемой продолжительности жизни. Целевой уровень гликированного гемоглобина (HbA1c), рекомендуемый Американской диабетической ассоциацией (АDА), а также Европейским обществом по изучению СД (EASD), составляет ≤ 7 % [3]. Рекомендации Всемирной организации здравоохранения (ВОЗ) и Международной диабетической федерации (IDF) более строгие: целевой уровень HbA1c должен быть ниже 6,5 % [5]. Национальный унифицированный клинический протокол по лечению СД-2 (2012) рекомендует следующие целевые параметры гликемического контроля: уровень НbА1с ≤ 7 %, уровень гликемии натощак (ГН) < 5,6 ммоль/л, через 2 часа после еды — < 10,0 ммоль/л [6].
Однако в исследовании UKPDS также было показано, что у 40 % больных к моменту постановки диагноза СД-2 уже имеется выраженное снижение секреторной функции бета-клеток, при этом ежегодно 5–10 % больных с впервые диагностированным СД-2 требуется терапия инсулином, а спустя 10–12 лет уже около 80 % пациентов нуждаются в постоянной инсулинотерапии. С течением времени у больных СД-2 ухудшается гликемический контроль, обусловленный нарастающим снижением остаточной секреции бета-клеток. Периферическая чувствительность к инсулину остается относительно сохранной, что определяет необходимость выбора оптимальной терапии на каждом этапе развития заболевания [2].
В последнее время врачи осознали необходимость проведения инсулинотерапии для ликвидации глюкозотоксичности и восстановления секреторной функции бета-клеток при умеренной гипергликемии. Такой же алгоритм прописан экспертами АDA в «Стандартах медицинской помощи при сахарном диабете» [4]. На первых этапах заболевания дисфункция бета-клеток носит обратимый характер и эндогенная секреция инсулина восстанавливается при снижении гликемии. Ранняя инсулинотерапия у больных СД-2 хотя и не является традиционной, но представляется одним из возможных вариантов медикаментозного лечения при значительной декомпенсации, минуя этап пероральных сахароснижающих препаратов (ПССП).
В исследовании UKPDS было показано, что адекватный контроль гликемии у больных СД-2 приводит к снижению риска развития диабетических осложнений [2]. Однако добиться жесткого контроля гликемии и поддерживать его сложно. Лечение обычно начинают с модификации образа жизни. Медикаментозная терапия, в том числе инсулином, становится необходимой при прогрессирующем снижении функции бета-клеток, которое приводит к ухудшению контроля гликемии [3–5]. Одним из главных препятствий к оптимальной инсулинотерапии является гипогликемия [7–10]. Боязнь гипогликемических реакций часто не позволяет пациентам и врачам проводить активное лечение и добиваться снижения уровней HbA1c до низких целевых значений [9, 10], рекомендуемых многими национальными организациями по изучению диабета [3–5]. Крупные обсервационные исследования показывают, что в клинической практике врачи обычно не добиваются оптимального контроля гликемии [13]. Препятствия к оптимальной инсулинотерапии включают в себя гипогликемию, прибавку массы тела, применение субоптимальных стартовых доз и неадекватное их титрование. Переход на инсулинотерапию требует от больного СД-2 внесения изменений в привычный образ жизни, особенно в режим приема пищи. Особую значимость приобретают самоконтроль уровня глюкозы в крови, а также знания об особенностях введения инсулина и питания при физических нагрузках и путешествиях, потреблении алкогольных напитков. Обучение пациентов — важнейший компонент терапии СД и неотъемлемая часть системы оказания помощи больным диабетом в большинстве стран мира [11]. Следует понимать, что цель образования пациентов с СД — это не только и не столько получение ими теоретических знаний о диабете, сколько обучение самоконтролю гликемии и приобретение практических навыков проведения инсулинотерапии и другой сахароснижающей терапии в условиях реальной жизни. Школы самоконтроля для пациентов с СД также способствуют формированию мотивации к здоровому образу жизни, знакомят с принципами диетотерапии, обучают методам профилактики осложнений и разъясняют необходимость их применения. Таким образом, обучение дает следующие преимущества для пациента с СД: эффективное управление заболеванием, предупреждение развития острых и хронических осложнений, уменьшение прогрессирования имеющихся осложнений, достижение стойкой компенсации углеводного обмена, экономическая выгода — предупреждение лечения поздних осложнений диабета, формирование стойкой мотивации пациента к достижению терапевтических целей, повышение комплайентности к проводимой терапии, более продуктивное общение с лечащим врачом [15]. Пациенты, которые прошли обучение в школах диабета и имели возможность чаще мониторировать уровень гликемии, были в 4 раза ближе к достижению целевых уровней HbA1c, чем необученные [15].
На сегодняшний момент число больных СД неуклонно возрастает: в 2013 году количество пациентов в Украине составляло 1 380 047, причем пациентов с СД-2 — 1 279 751 [13]. К тому же количество пациентов, требующих лечения инсулином, также увеличивается и на сегодняшний день составляет около 16 %. Инсулинотерапию при СД-2 зачастую применяют слишком поздно, рассматривая ее как последнюю возможность в лечении диабета. По данным исследования CREDIT, средний уровень HbA1c на момент начала инсулинотерапии у пациентов с СД-2 типа — 10,1 % [14]. На самом деле в ряде случаев инсулин должен использоваться очень рано. Для предупреждения развития осложнений СД применение инсулина следует начинать, если другие методы лечения не позволяют поддерживать уровень HbA1c ниже 7 % [5].
В связи с изложенным представляется актуальным изучение эффективности и переносимости лечения с применением человеческих инсулинов Инсуман® у больных СД-2, которые не достигли гликемического контроля на фоне приема ПССП, что отражает реальную клиническую практику и задачи терапии по достижению оптимального баланса между достижением целевого уровня гликемии и частотой гипогликемий у пациентов c СД-2.
Цель исследования. Первичная цель исследования включала в себя оценку эффективности инсулинов Инсуман Базал®, Инсуман Комб 25®, Инсуман Рапид® у пациентов с СД-2, у которых не удалось достичь компенсации в результате пероральной терапии, что определялось, исходя из уровня снижения HbA1c после 6 месяцев терапии. Вторичные задачи исследования состояли в оценке:
— эффективности и переносимости инсулинов Инсуман®;
— эффективности обучения в школах самоконтроля диабета;
— средней дозы инсулинов в конце исследования.
Материал и методы исследования
Дизайн. Данное исследование было открытым, многоцентровым, нерандомизированным, интервенционным, с фиксированной схемой визитов и длительностью 6 месяцев для оценки эффективности и безопасности лечения инсулинами в трех группах: Инсуман Базал®, Инсуман Комб 25®, Инсуман Рапид® (рис. 1).
Сбор клинических данных проводился до назначения инсулинов Инсуман® и в течение 6 месяцев лечения.
Критерии включения в исследование:
— пациенты с СД-2, некомпенсированные на фоне приема одного или двух ПССП;
— пациенты старше 18 лет;
— подписанное информированное согласие;
— уровень HbA1c > 7,5 %;
— пациент может самостоятельно заполнять дневник самоконтроля СД и корректировать дозу инсулина, мотивирован для обучения в школах СД;
— ожидается, что пациент будет оставаться на стабильной дозе ПССП в течение 6 месяцев лечения.
Критерии невключения в исследование:
— пациенты с СД 1-го типа;
— временная инсулинотерапия (гестационный диабет, хирургические вмешательства, рак поджелудочной железы, участие в другом клиническом исследовании);
— любые клинически значимые органные или системные заболевания, делающие невозможным интерпретацию и оценку результатов;
— пациентка планирует беременность сейчас или в ближайшие 6 месяцев;
— пациент участвует в другом клиническом исследовании в настоящее время или за последние 28 дней до визита 1;
— известно, что пациент в прошлом или в настоящее время употребляет наркотики.
Пациентам, подходящим по критериям включения/исключения и добровольно согласившимся принять участие в клиническом исследовании, во время визита 1 была назначена инсулинотерапия одним из следующих препаратов: Инсуман Базал®, или Инсуман Комб 25®, или Инсуман Рапид®. Применение инсулинов Инсуман® осуществлялось в соответствии с зарегистрированными показаниями. Выбор препарата для каждого пациента основывался на клиническом суждении врача-исследователя в соответствии с характеристикой пациента и течением СД. Каждый врач-исследователь должен был набрать 55 пациентов, из которых 33 должны были получать Инсуман Базал®, 16 — Инсуман Комб 25® и 6 — Инсуман Рапид®. В исследовании предусматривалось 4 визита, во время которых происходил сбор всех необходимых данных из медицинской документации пациентов. Ключевыми критериями, используемыми для оценки, были следующие: HbA1c, средняя доза инсулина в течение периода лечения (6 месяцев), количество задокументированных случаев симптоматической гипогликемии, всех зарегистрированных нежелательных явлений, количество правильных ответов по окончании школы сахарного диабета. В течение исследования пациенты должны были получать стабильную дозу ПССП, переход с одного инсулина на другой был невозможен. Доза назначенного препарата инсулина титровалась пациентом в соответствии с инструкциями, полученными от врача-исследователя и в школе самоконтроля диабета, на основании показателей гликемии. Врач-исследователь мог изменить дозу инсулина при необходимости на визите 2 и на визите 3, а также в неотложных случаях и случаях внепланового обращения за медицинской помощью.
При оценке безопасности были приняты такие определения. Документированный эпизод симптоматической гипогликемии — событие с типичными симптомами гипогликемии, которое сопровождается уровнем глюкозы плазмы крови ≤ 3,9 ммоль/л.
Ночная симптоматическая гипогликемия — событие, которое случается во время сна (после отхода ко сну после вечерней инъекции и до пробуждения утром (т.е. до утреннего определения уровня ГКН и до утренней инъекции) и связано с уровнем глюкозы в крови ниже 3,9 ммоль/л, но без симптомов.
Тяжелая документированная гипогликемия — все эпизоды, при которых показатель глюкозы плазмы крови ≤ 2,8 ммоль/л и неврологические нарушения являются достаточно тяжелыми для того, чтобы сделать невозможным самолечение, что, соответственно, может представлять риск нанесения вреда как для самого пациента, так и для окружающих. Необходимость посторонней помощи означает, что пациент не может сам себе оказать помощь. Если кто-то по доброй воле помог пациенту, когда в этом не было необходимости, такая ситуация не рассматривается как потребность пациента в посторонней помощи.
Результаты исследования
С момента начала исследования был произведен набор в общей сложности 552 пациентов с СД-2 с недостаточным контролем в результате проводимого предшествующего лечения в 12 украинских исследовательских центрах. Из 12 выбранных и утвержденных исследовательских центров 11 были активными и производили набор пациентов. Данные о двух пациентах были утеряны, и они были исключены из исследования, следовательно, в анализ данных были включены 550 пациентов. Распределение участников исследования в группы лечения было следующим: группа 1, Инсуман Базал® — 341 пациент; группа 2, Инсуман Комб 25® — 173 пациента; группа 3, Инсуман Рапид® — 36 пациентов. Средний возраст пациентов составил 59,57 ± 9,53 года, мужчин было 231 (42 %) и женщин 319 (58 %). Общее количество пациентов, имевших макроваскулярные осложнения, в трех группах равнялось 419 (75,6 %), с микроваскулярными осложнениями — 525 (96,4 %). Статистически достоверная разница между тремя группами наблюдалась в стартовых показателях длительности СД, HbA1c и ГПН (табл. 1, 2).
Микрососудистые осложнения в виде различной выраженности ретинопатий, микро- и макроальбуминурии, диабетической нейропатии, трофических поражений нижних конечностей встречались у 96,18 % пациентов в группе 1, 93,06 % в группе 2 и у 100 % в группе 3.
До включения в исследование пациенты получали терапию ПССП, однако достижения гликемического контроля на фоне приема препаратов не наблюдалось. Наиболее часто пациенты получали метформин и препараты производных сульфонилмочевины (табл. 3). С момента включения в исследование характер сопутствующей терапии ПССП должен был быть неизменным.
Была проведена оценка частоты гипогликемии на фоне предшествующей терапии инсулинами Инсуман® (визит 1). В табл. 4 приведено распределание частоты гипогликемий в группах, получавших разные виды инсулинов Инсуман®.
В целом до визита исходного уровня были зарегистрированы 8 случаев тяжелой гипогликемии (6 в группе 1 и 2 в группе 2, что составило 1,45 % от общего числа пациентов). Эти случаи были выявлены только в анамнезе до начала исследования.
Анализ сахароснижающей эффективности
Были изучены изменения в уровне глюкозы — ГПН (визит исходного уровня — визит через 6 месяцев): различие между визитом исходного уровня и визитом через 6 месяцев статистически значимое (р < 0,001) для всех групп пациентов. Максимальное снижение наблюдалось преимущественно на первом месяце терапии (в период между визитом исходного уровня и двумя визитами) и было незначительно ниже в течение визитов 2–4 (через 6 месяцев) (табл. 5). Различие в снижении уровня глюкозы в крови по результатам оценки величины эффекта между группами было незначительным (статистически незначимо, р = 0,082). Величина эффекта по результатам оценки снижения уровня глюкозы незначительно ниже в группе пациентов, которым проводилось лечение инсулином Инсуман Рапид®. Это можно объяснить большей вариабельностью изменений показателей в данной группе. Величина эффекта по результатам оценки динамики уровней глюкозы была больше (величина эффекта = 2,53–2,61) и меньше для динамики HbA1c (величина эффекта =1,01–1,53). Это было связано с большей инерцией изменения уровня HbA1c и зависимостью от изменений показателя HbA1c за последние 2–3 недели.
Эффективность по результатам оценки динамики уровня HbA1с в группах
/73/73.jpg)
Различие между группами в целевом уровне HbA1с < 7,5 % было статистически значимым (р = 0,0016).
Максимальная эффективность для данного показателя была обнаружена у пациентов, получающих лечение инсулином Инсуман Базал®, — 49,85 %. Отмечалось статистически значимое различие в снижении уровня HbA1c по сравнению с исходным уровнем и через 6 месяцев терапии (р < 0,05). Различия в группах стратификации на исходном уровне определялись с учетом тяжести и продолжительности сахарного диабета и индивидуального подбора препарата и дозировки. Различие между группами в связи с особенностями их формирования уменьшалось к концу исследования. Максимальное снижение уровня HbA1c наблюдалось в группах пациентов, получавших лечение инсулином Инсуман Базал® (Δ = –2,61) и Инсуман Комб 25® (Δ = –2,81). В группе пациентов, получавших лечение инсулином Инсуман Рапид®, были выявлены меньшие изменения. Это можно объяснить более тяжелым состоянием пациентов с СД, отобранных для участия в этой группе.
Показатель «Величина эффекта» использовался для сравнительной оценки изменений уровня HbA1c с учетом средних значений уровней HbA1c и вариабельности у отдельных пациентов. Показатели величины эффекта рассчитывались с использованием среднего значения и стандартного отклонения, когда вводимые параметры выборок были равными. В соответствии с классификацией величина эффекта, превышающая 0,5, расценивалась как высокая. Величина эффекта (r) в группах была следующей: группа 1 — 1,51, группа 2 — 1,53, группа 3 — 1,01. Оценка, которая основывалась на величине эффекта, показала, что снижение уровня HbA1c было меньше в группе пациентов, применявших Инсуман Рапид®. Это можно объяснить большей вариабельностью изменений и меньшим числом наблюдений.
Общая оценка эффективности в группах (количество пациентов со снижением уровня HbA1c > 1 %, n/N (%)) составляла 430/539 (79,78 %). Различия между группами по частоте снижения HbA1c > 1 % не являются статистически значимыми.
Эффективность школ диабета
Все пациенты, включенные в исследование, прошли курс обучения в школе диабета. Курс состоял из пяти занятий, проводившихся специально обученными медсестрами в соответствии с рекомендациями Ассоциации диабетологов Украины с рассмотрением следующих тем: необходимость в достижении контроля гликемии, использование инъекционных устройств для введения инсулина, использование глюкометра, построение профиля гликемии, заполнение дневника пациента. Курс проходил в период между первым и вторым визитом. В течение этого курса пациенты получали обучающие материалы и дневник пациента для регистрации следующей информации: дата, название и дозы инсулина, измеренный уровень глюкозы в крови, название и доза ПССП, случаи гипогликемии и нежелательные явления. Основная цель школы диабета заключалась в обучении пациента достижению максимального контроля сахарного диабета путем коррекции дозы инсулина с минимальным риском развития гипогликемии. В начале обучения в школе диабета и в конце пациенты заполняли анкету, отвечая на вопросы, связанные с самоконтролем сахарного диабета. Анализ эффективности школ диабета представлен в табл. 9, 10.
Данные свидетельствуют о статистически значимом увеличении общего количества правильных ответов, данных пациентами всех групп после завершения обучающего курса в школе диабета.
Различие между группами было статистически значимым (x2 = 12,01; р = 0,017). Максимальная эффективность школы диабета (в соответствии с повышением процента правильных ответов) отмечалась в группе пациентов, получавших лечение инсулином Инсуман Рапид®, — 86,11 %. Минимальная эффективность наблюдалась в группе пациентов, получавших лечение инсулином Инсуман Комб 25®, — 64,16 % пациентов. Была изучена зависимость изменений в уровне HbA1c более чем на 1 % и эффективность школы диабета (табл. 11).
Анализ включал в себя данные о пациентах с имеющимися данными о динамике уровня HbA1c > 1 % и уровне оценки школы диабета в начале и в конце исследования. В анализ не включали пациентов, в отношении которых не было в наличии полных данных.
Анализ динамики доз проводимой сахароснижающей терапии
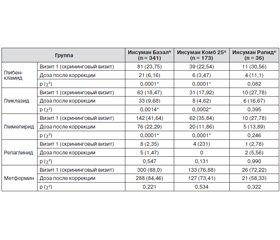
Был проведен анализ динамики доз на фоне проводимой терапии с учетом приема ПССП и инсулинов Инсуман®. Полученые результаты отражены в табл. 12–14. Частота назначения ПССП была статистически значимо сниженной до назначения инсулинов в группах пациентов, которые применяли Инсуман Базал® и Инсуман Комб 25®. В группе пациентов, применявших инсулин Инсуман Рапид®, различие не было статистически значимым в связи с небольшим количеством наблюдений. У пациентов, у которых терапия ПССП не прекращалась, в большинстве случаев снижали дозу.
Суточная доза инсулина увеличилась в период между визитом исходного уровня и визитом через 6 месяцев. Различие было статистически значимым в группах пациентов, применявших Инсуман Базал® и Инсуман Комб 25® (р < 0,05). В соответствии с протоколом не разрешался переход с одного вида инсулина на другой. Изменения в дозах инсулина в течение исследования отражены в табл. 15.
Отмечалось статистически значимое различие в дозах инсулина между пациентами, у которых было достигнуто и у которых не было достигнуто снижение уровня HbA1c > 1 %.
Данные по безопасности
В соответствии с Протоколом гипогликемия представляет собой патологическое состояние, характеризующееся снижением уровня глюкозы в крови ниже 3,9 ммоль/л (что документально подтверждено) или, в случае тяжелой гипогликемии, ниже 2,8 ммоль/л. Сбор информации о частоте и характере гипогликемии в ходе исследования между визитами производился в следующие периоды времени: визит 1 (исходный уровень) — визит 2: 30 ± 7 дней; визит 1 — визит 3: 90 ± 7 дней; визит 1 — визит 4 (через 6 месяцев): 180 ± 7 дней. Частота развития эпизодов задокументированной ночной гипогликемии и симптоматической гипогликемии отражена в табл. 16–17.
В течение периода исследования не было документально зарегистрировано случаев тяжелой гипогликемии.
Абсолютное число эпизодов гипогликемии следует оценивать, принимая во внимание продолжительность периода регистрации (интервал между визитами). В течение периода лечения среди всех 550 включенных в исследование пациентов количество всех типов симптоматической гипогликемии равнялось 91, при этом отмечалось 56 эпизодов задокументированной гипогликемии и 19 эпизодов ночной гипогликемии. Не было зарегистрировано случаев тяжелой гипогликемии. На момент визита 1 (гипогликемия в анамнезе в течение одного месяца до визита исходного уровня) симптоматическая гипогликемия отмечалась у 29 пациентов.
Проведен детальный анализ случаев гипогликемии по показателю «Случаи на 1000 пациенто-дней». Показатель «пациенто-время» представляет собой оценку фактического времени подверженности риску в период (дни) исследования. За отдельными пациентами проводится дальнейшее наблюдение в течение различных периодов времени, поскольку одни пациенты остаются без признаков заболевания дольше, чем другие. Зная количество новых случаев гипогликемии и пациенто-время подверженности риску в рамках исследования, мы можем вычислить частоту развития симптоматической гипогликемии или то, как быстро у пациентов развивается симптоматическая гипогликемия. В период до начала исследования в группе 1 было зарегистрировано 0,0017 случая симптоматической гипогликемии на пациента в сутки, или 1,704 случая на 1000 пациенто-дней. За период исследования риск развития симптоматической гипогликемии в этой группе пациентов снизился: на момент визита 2 он составлял 1,401 случая на 1000 пациенто-дней, при этом различие в уровне по сравнению с визитом исходного уровня составляло –0,303 случая на 1000 пациенто-дней. Для визита 3 это составляло 0,803 случая на 1000 пациенто-дней (сниженный уровень по сравнению с визитом исходного уровня = –0,901 случая на 1000 пациенто-дней, р = 0,027). Что касается визита через 6 месяцев, уровень на 1000 пациенто-дней составлял 0,572 (со сниженным уровнем по сравнению с визитом исходного уровня = –1,133 случая на 1000 пациенто-дней, р = 0,0008). Таким образом, в группе пациентов, применявших Инсуман Базал®, в период между визитом 1 (на исходном уровне) и 4 (через 6 месяцев) было выявлено статистически значимое снижение числа случаев гипогликемии с 1,704 до 0,572 на 1000 пациенто-дней (р = 0,0008).
В группе 2 среди пациентов, применявших Инсуман Комб 25®, в период между визитом 1 (визитом исходного уровня) и 4 (через 6 месяцев) был обнаружено уменьшение количества случаев симптоматической гипогликемии с 1,578 до 1,274 на 1000 пациенто-дней (р = 0,614). В группе пациентов, применявших Инсуман Рапид®, на момент визитов 2, 3, 4 риск гипогликемии снизился почти в 3 раза: с 3,922 случая на 1000 пациенто-дней до 0,995 и 1,025 случая на 1000 пациенто-дней (р = 0,058) соответственно. Учитывая небольшое количество наблюдаемых случаев в этой группе пациентов, невозможно подтвердить эту динамику как статистически значимое различие (величина p в диапазоне от 0,185 до 0,058). Общие оценки для трех групп пациентов (применявших Инсуман Базал®, Инсуман Комб 25®, Инсуман Рапид®) указывали на статистически значимое снижение частоты развития задокументированной симптоматической гипогликемии с 1,805 случая на 1000 пациенто-дней (визит 1) до 0,898 случая на 1000 пациенто-дней (визит через 6 месяцев), р = 0,0031.
Одно серьезное нежелательное явление привело к смерти пациента. В результате последующего наблюдения за этим случаем было выявлено, что причиной летального исхода была гипертензивная энцефалопатия, которая расценивалась компанией и исследователем как серьезное нежелательное явление без наличия связи с применением исследуемого препарата. Основываясь на критериях оценки, можно сделать заключение об отсутствии какой-либо связи между нежелательным явлением и применением исследуемого препарата. В этом исследовании не было зарегистрировано каких-либо других серьезных нежелательных явлений. В целом исследователи сообщали о восьми нежелательных явлениях в течение периода исследования (увеличение массы тела, зуд в месте инъекции, уплотнение в месте инъекции, повышение температуры в связи с вирусной инфекцией, мышечный тремор, головокружение, гипергидроз, гипергликемия в связи с пропущенной инъекцией). Все они расценивались исследователями как несерьезные и не требующие применения определенных мер.
Обсуждение
Проводился анализ данных 550 пациентов с СД-2, подходящих для исследования, которым были назначены Инсуман Базал®, Инсуман Комб 25® или Инсуман Рапид® в результате ранее существовавшего неадекватного контроля СД. Инсуман Базал®, Инсуман Комб 25® или Инсуман Рапид® назначались и использовались в соответствии с утвержденным показанием, международными и национальными руководствами по инсулинотерапии у пациентов с СД-2. Большинство пациентов имели различные макрососудистые заболевания, частота которых варьировала от 72,22 до 79,77 % случаев в соответствии с группой лечения. В период лечения отмечалось статистически значимое снижение уровня HbA1с (р < 0,0001) во всех группах. Но ΔHbA1с между исходным уровнем и окончанием исследования было статистически значимо более высоким среди пациентов, применявших Инсуман Комб 25® (–2,81 %), по сравнению с показателем в группе пациентов, применявших инсулин Инсуман Базал® (–2,61 %) или Инсуман Рапид® (–1,75 %).
Общая оценка эффективности в группах пациентов (количество пациентов со снижением уровня HbA1c > 1 %) составляла 430/539 (79,78 %). Различия между группами по частоте снижения уровня HbA1c > 1 % не были статистически значимыми: Инсуман Базал® — 271 (79,94 %), Инсуман Комб 25® — 135 (81,33 %), Инсуман Рапид® — 24 (70,59 %). В конце исследования количество пациентов в каждой группе, достигших целевого уровня HbA1с (< 7,5 %), было следующим: Инсуман Базал® — 169 пациентов (49,85 %), Инсуман Комб 25® — 57 пациентов (33,34 %) и Инсуман Рапид® — 11 пациентов (32,35 %). Различие между группами было статистически значимым (р = 0,0016). Максимальная эффективность по этому критерию наблюдалась в группе пациентов, применявших инсулин Инсуман Базал®. Сравнительный анализ суточной дозы инсулина во всех группах показал, что средняя суточная доза в группе пациентов, получавших лечение инсулином Инсуман Базал®, составляла 36,65 ± 16,36 МЕ, в группе пациентов, применявших Инсуман Комб 25®, — 40,41 ± 14,0 МЕ и в группе пациентов, применявших Инсуман Рапид®, — 30,14 ± 11,74 МЕ. Изменения доз инсулинов Инсуман Базал® и Инсуман Комб 25® были статистически значимыми. Максимальное увеличение доз наблюдалось на момент визита 2. Дозы Инсумана Рапид® не изменились статистически значимо, но наблюдалась тенденция к незначительному повышению. Средняя суточная доза инсулина увеличилась в течение периода исследования во всех группах пациентов, получавших различное лечение, в диапазоне от 11,7 до 20,1 %. Средняя суточная доза инсулина была выше у пациентов, которые достигли снижения уровня НbA1c > 1 %. Почти все пациенты во всех группах принимали различные перечисленные ПССП. Различие в принимаемых ПССП и дозах между группами не было статистически значимым для всех препаратов (р > 0,05). Исследуемые группы были сопоставимы по дозам ПССП — различия не были статистически значимыми для всех препаратов (р > 0,05). Базовая схема лечения ПССП была изменена у 63,82 % пациентов до назначения инсулинов во время визита 1. Наибольшая частота этих изменений наблюдалась в группе пациентов, которым был назначен Инсуман Комб 25®: 173 (73,41 %). Статистически значимо более низкая частота изменений до приема ПССП отмечалась в группе пациентов, применявших Инсуман Базал®: 201 (58,94 %). Различия между группами были статистически значимыми (р = 0,007). Лечение ПССП в анамнезе пациентов различных групп отмечалось у 95,95–98,24 %. На момент назначения инсулина применение ПССП было в некоторых случаях отменено. Во всех остальных случаях дозы ПССП, которые должны назначаться в комбинации с инсулинами, были снижены. Изменение (коррекция) средней суточной дозы глибенкламида в период между визитом исходного уровня и визитом в конце исследования не было статистически значимым (р > 0,05). Но частота приема глибенкламида статистически значимо снизилась: 131 (23,8 %) пациент, которые получали лечение глибенкламидом на момент скринингового визита (0), и только 31 (5,6 %) — после коррекции терапии до назначения инсулинов (p < 0,0001). В группах пациентов, получающих инсулинотерапию различными препаратами инсулина Инсуман®, не было статистически значимого различия по следующим параметрам: возраст, пол, длительность и тяжесть СД-2, данные анамнеза. Изменения (коррекция) средних суточных доз гликлазида статистически значимо уменьшились с 102,1 до 81,5 (р = 0,003). Эти изменения формируются группами пациентов, получавших лечение инсулином Инсуман Базал® (–22,8 мг, р = 0,007). Уменьшение дозы в других группах пациентов составляло –19,3 мг (Комб 25®) и –18,4 мг (Рапид®), но различия не были статистически значимыми (р > 0,05). Частота применения гликлазида снизилась с 104 (18,9 %) на момент визита 0 до 47 (8,5 %) на момент визита 1 (р < 0,0001). Средняя суточная доза глимепирида снизилась в среднем на 0,6 мг (р = 0,009). Сообщалось о статистически значимом снижении суточной дозы глимепирида у пациентов, которым были назначены Инсуман Базал® (–0,6 мг; р = 0,042) и Инсуман Комб 25® (–1,3 мг; р = 0,003). Также отмечалось снижение частоты применения глимепирида с 214 (38,9 %) на момент визита 0 до 101 (18,4 %) на момент визита 1 (р < 0,0001). Средняя суточная доза метформина в среднем снижалась на 245,2 мг (р < 0,0001). Во всех группах пациентов было обнаружено статистически значимое снижение суточной дозы метформина. Частота терапии метформином снизилась с 459 (83,5 %) на момент визита 0 до 436 (79,3 %) на момент визита 1 (р = 0,075). Изменения средних суточных доз репаглинида до назначения инсулинов не были статистически значимыми (р > 0,05). Только 14 пациентов получали лечение репаглинидом на момент скринингового визита, и после коррекции ПССП во время визита 1 репаглинид был назначен 7 пациентам.
Эффективность лечения, определяемая по результатам оценки снижения уровня HbA1c более чем на 1 %, в группе пациентов, применявших Инсуман Базал®, составляла 79,94 %; в группе пациентов, применявших Инсуман Комб 25®, — 81,33 %, а в группе пациентов, применявших Инсуман Рапид®, — 70,59 %. Уровень HbA1c ниже 7,5 % был достигнут у 49,85 % пациентов в группе 1, у 33,54 % пациентов в группе 2 и у 32,35 % пациентов в группе 3. В результате посещения школы диабета количество правильных ответов увеличилось во всех группах. Не отмечалось различий в частоте снижения уровня HbA1c в группе пациентов с увеличением количества правильных ответов по сравнению с общей популяцией пациентов. Результаты анализа данных о случаях гипогликемии, возникших во время исследования, свидетельствовали об отсутствии значимой связи с лечебной группой и отсутствии связи с визитом. О симптоматической гипогликемии сообщалось во время визита 1 — 1,6 % пациентов, во время визита 2 — 0,9 %, во время визита 3 — 0,7 % и во время визита 4 — 1,6 % пациентов. Не отмечалось статистически значимых различий в группах лечения (р > 0,05). Эпизоды гипогликемии, наблюдаемые в течение исследования, были сходными во всех группах пациентов, но частота возникновения таких случаев снизилась к концу исследования.
Выводы
Исследование позволило лучше изучить эффективность различных препаратов инсулина Инсуман® в украинской популяции пациентов с СД-2. 3 группы пациентов, получавших инсулинотерапию впервые различными препаратами инсулина Инсуман®, были статистически однородны по параметрам: возраст, пол, длительность и тяжесть СД-2, предшествующая терапия.
Все препараты инсулина Инсуман®, применяемые в течение 6 месяцев, позволяют достичь лучшей компенсации у пациентов с сахарным диабетом 2-го типа (что определяется по уровню HbA1с, ΔHbA1с) по сравнению с ранее проводившимся лечением.
В целом при применении инсулина Инсуман® уровень HbA1с снизился на 1,0 % и более у 79,9 % пациентов во всех группах в течение периода лечения.
У 43,97 % всех пациентов удалось достичь целевого уровня HbA1с (< 7,5 %) к концу 6-месячного периода терапии. Более высокий процент пациентов, у которых был достигнут этот целевой уровень, отмечался в группе больных, применявших инсулин Инсуман Базал® (49,85 %).
Не отмечалось статистически значимого повышения эффективности терапии у пациентов, которые успешно завершили программу обучения в школе диабета, по сравнению с оценкой эффективности в целом. Состояние молодой исследуемой популяции пациентов с неадекватным контролем на исходном уровне и у которых уже развились сердечно-сосудистые осложнения, связанные с сахарным диабетом, в большинстве случаев улучшилось с точки зрения контроля гликемии, и при этом не было зарегистрировано каких-либо серьезных эпизодов гипогликемии. Это может быть связано с положительным влиянием обучающей программы в школе диабета.
В качестве ограничений исследования следует отметить описательный метод анализа данных (в связи с обсервационным дизайном исследования). Таким образом, результаты исследования носят только эксплоративный характер.
1. UKPDS: Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33): UK Prospective Diabetes Study (UKPDS) Group // Lancet. — 1998. — 352. — 837–853.
2. Turner R., Cull C., Frighi V., Holmann R. Glycemic control with diet, sulfonylurea, metformin, or insulin in patients with type 2 diabetes mellitus: progressive requirement for multiple therapies (UKPDS 49): UK Prospective Diabetes Study (UKPDS) Group // JAMA. — 1999. — 281. — 2005–2012.
3. Inzucci S.E., Bergenstal R.M., Buse I.B. et al. Management of hyperglycemia in type 2 diabetes, 2015: a patient-centered approach: update to a position statement of the American Diabetes Association and the European Association for the Study of Diabetes // Diabetes Care. — 2015. — Vol. 38. — P. 140–149.
4. ADA/EASD Position Statement // Diabetes Care. — 2007. — Vol. 30 (Suppl. 1).
5. INTERNATIONAL DIABETES FEDERATION, Clinical Guidelines Task Force Global Guideline for Type 2 Diabetes, 2012.
6. Уніфікований клінічний протокол первинної та вторинної (спеціалізованої) медичної допомоги. Цукровий діабет 2-го типу: Наказ МОЗ від 21.12.2012 № 1118.
7. Полторак В.В., Красова Н.С., Горшунская М.Ю. Гликемическая память как патогенетическое основание для формирования алгоритма современной антидиабетической терапии // Міжнародний ендокринологічний журнал. — 2014. — № 3. — С. 15–21.
8. Cryer P., Childs B.P. Negotiating the barrier of hypoglycemia in diabetes // Diabetes Spectrum. — 2002. — 15. — 20–27.
10. Cryer P. Hypoglycemia is the limiting factor in the management of diabetes // Diabetes Metab. Res. Rev. — 1999. — Vol. 15. — Р. 42–46.
11. Полторак В.В., Красова Н.С., Горшунская М.Ю. Комбинированная терапия «метформин + глимепирид» у больных сахарным диабетом 2-го типа (молекулярные механизмы оптимизации реабилитирующего действия) // Мiжнародний ендокринологiчний журнал. — 2015. — № 1. — P. 87–97.
12. Тронько М.Д., Полторак В.В., Соколова Л.К. Дослідження ORIGIN (передумови, результати) // Міжнародний ендокринологічний журнал. — 2013. — № 1 (49). — С. 15–22.
13. Довідник основних показників діяльності ендокринологічної служби України за 2013 рік // Ендокринологія. — 2014. — Додаток 1, том 19, № 1. — С. 3–40.
14. Полторак В.В. и соавт. CREDIT. Долгосрочное международное неинтервенционное исследование у пациентов с диабетом 2-го типа, находящихся на инсулинотерапии. Анализ исходных данных украинской популяции // Проблеми ендокринної патології. — 2010. — № 4. — С. 94–108.
15. Маньковский Б.Н. Актуальные вопросы диабетологии в Украине // Здоровье Украины. — 2011. — № 36. — С. 7–9.

/70/70.jpg)
/71/71.jpg)
/72/72.jpg)
/73/73_2.jpg)
/74/74.jpg)
/75/75.jpg)
/76/76.jpg)
/77/77.jpg)